5水平冰冻混合人血清葡萄糖候选标准物质的制备研究
刘 欧,徐国宾,闪全忠,夏昌宇,李海霞,刘 岩,王兰珍,齐丽丽,何振坤
(1.清华大学第一附属医院 检验科,北京 100016;2.北京大学第一医院 检验科,北京 100034;3.北京利德曼生化技术有限公司;4.中生北控生物科技股份有限公司)
5水平冰冻混合人血清葡萄糖候选标准物质的制备研究
刘 欧1,徐国宾2*,闪全忠1,夏昌宇2,李海霞2,刘 岩2,王兰珍3,齐丽丽4,何振坤4
(1.清华大学第一附属医院 检验科,北京 100016;2.北京大学第一医院 检验科,北京 100034;3.北京利德曼生化技术有限公司;4.中生北控生物科技股份有限公司)
目的研制5水平冰冻混合人血清葡萄糖标准物质,为葡萄糖常规方法的准确度验证,提供稳定和互通性良好的真实值控制品。方法收集足量正常体检人群无肉眼溶血、脂血和黄疸的血清标本,依次采用Sartorius公司的0.8、0.45、0.2μ m过滤微膜过滤除菌后分装于冻存管中。按《标准物质/标准样品生产者能力认可准则》[1]的要求,对冰冻混合人血清进行均匀性研究,短期稳定性(室温、4℃、-20℃)和长期稳定性(-80℃)研究,定值结果用“靶值±不确定度”表示,2家候选葡萄糖参考实验室测定结果均值作为靶值,不确定度包括测定变异和测定系统偏差、瓶间差及稳定性所带来的不确定度。并对冰冻混合人血清在6种进口配套检测系统中的互通性进行观察。结果共制备5水平冰冻混合人血清(C1、C2、C3、C4、C5)。C4水平血清瓶间标准偏差为 0.018 mmol/L,其余 4水平瓶间偏差为零,经单因素方差分析后P值全部大于0.05。稳定性研究经线性回归方差分析P值全部大于0.05。2家候选葡萄糖参考实验室测定结果的均值为3.08、5.92、13.60、9.31、18.71 mmol/L,不确定度相应为 0.09、0.17、0.36、0.23、0.55 mmol/L。 5水平冰冻混合人血清的坐标点全部位于40份人血清标本的直线回归95%可信区间范围内,该5水平冰冻混合人血清与血清的反应性相同。结论5水平冰冻混合人血清均匀性、稳定性、互通性良好,定值准确。
葡萄糖;均匀性;稳定性;互通性
(Chin J Lab Diagn,2010,14:1009)
血清葡萄糖的准确测定对于糖尿病的诊断、治疗及预后评估具有重要意义,自上世纪八十年代,国际上开始统一糖尿病的诊治标准[1]。但葡萄糖的常规测定方法不统一,包括己糖激酶法、葡萄糖氧化酶法、电极法和干化学法4种,常规检测系统有试剂、校正品、仪器配套的全封闭检测系统;有仅试剂、校正品配套的检测系统;有试剂、校正品、仪器均不配套的检测系统,在此种情况下常规检测结果的可比性和准确性受到关注。采用以参考方法定值并具有互通性的标准物质是验证常规检测系统测定结果准确性及常规检测系统间结果可比性的最佳途径。国际上有证血清葡萄糖标准物质有美国国家标准品和技术研究院(NIST)的SRM965a、墨西哥蒙特雷国家中心(CENAM)的263a和日本临床化学参考物质研究所(ReCCS)的JCCRM521,这些国际血清质有证参考物质主要用于参考实验室参考方法准确性验证,目前还没有适合用于常规方法验证的标准物质。本研究制备5水平冰冻混合人血清定值葡萄糖标准物质,用于常规方法正确度验证,可以提高常规方法标准化进程。
1 材料与方法
1.1 标准物质的制备
于无溶血、黄疸和乳糜血的体检人群混合血清中,加入Sigma公司的 D葡萄糖(G8270-100G,≥99.5%),制成5个浓度水平的血清池,分别经过0.8、0.45、0.2 μ m 过滤膜过滤 ,在生物安全柜中 ,湿度不低于70%的条件下,分装于冻存管(Nunc公司产品,规格 1.8 mL)中,0.6 mL/支,每个水平分装700支,-80℃保存。
1.2 均匀性检验
按中国合格评定国家认可委员会2007年8月1日发布并实施的《标准物质/标准样品生产者能力认可准则》[1]的要求,采用系统抽样,5个浓度共抽取70支。采用Beckman公司的氧电极法进行测定,每支测3次,全部测定于当天完成。计算各水平瓶间标准偏差(Sbb)并进行差异显著性检验。
1.3 稳定性观察
将分装好的冻存管分别置室温(23℃,湿度50%)、4℃、-20℃、-80℃保存并定期检测,测定时采用复测,取均值计算。-80℃为冰冻混合人血清的保存条件,进行长期稳定性的观察,采用血清葡萄糖己糖激酶参考测量方法[2]测定。而室温、4℃、-20℃为运输过程中可能遭遇到的条件,仅进行短期稳定性研究,这三种温度分别观察3天、14天和28天,采用罗氏公司的己糖激酶法测定。求出各温度条件下各水平葡萄糖含量与时间关系的直线回归方程。
1.4 定值
北京大学第一医院检验科候选葡萄糖参考实验室(BDYYJYK)和北京利德曼生化技术有限公司候选葡萄糖参考实验室(LDMGS),两家实验室均采用己糖激酶参考测量方法[2],分别通过测定NIST的4个浓度的有证标准参考物质SRM965a和参加由IFCC委托德国临床化学协会(DGKL)组织的参考实验室间血糖RELA比对来验证参考方法的准确性。定值结果采用“靶值(x)±不确定度(U)”表示,每个实验室为5水平冰冻混合人血清赋值,每份标本连续测定3天,每天测定2次,剔除离群值后取平均值作为靶值;不确定度的贡献来自于测定变异(SD)及己糖激酶参考测量法与质谱法的系统偏差(system bias)、各水平标准物质的Sbb、长期保存稳定性所带来的不确定度(U10)共四方面。
1.5 互通性研究
1.5.1 比对血清标本的收集与处理
收集新鲜足量无溶血、脂血和黄疸的血清,葡萄糖浓度范围在1.9-22.0 mmol/L的标本40份,每份标本仅由1至2个病人的血清混合后获得,分装后-80℃保存。
1.5.2 校正品和质控品的收集与处理
收集罗氏公司的多项校正品及其高低值质控品、贝克曼-库尔特公司的3水平液体质控品和多项液体校正液、中生公司葡萄糖水溶液的校正液和朗道公司2水平质控品,共10份。按厂家推荐要求使用,分装后-80℃保存。
1.5.3 检测系统
常规检测系统采用6种配套检测系统(依厂家和方法笔画排序)分别是:贝克曼-库尔特公司的己糖激酶法(HK)和氧电极法、罗氏公司的己糖激酶法和葡萄糖氧化酶法(GOD)、强生公司的干化学法和德灵公司的己糖激酶法检测系统,参考测量方法为血清葡萄糖己糖激酶法。
1.5.4 互通性观察
将40份血清标本、10份校正品和质控品及5水平混合冰冻人血清,共55份标本同时采用6种常规测定系统及葡萄糖参考测量法测定,每份标本在每种测定系统上测定2次,取均值计算,以参考方法测定结果为对照,6种常规检测系统测定结果分别与之进行40份血清标本的直线相关与回归分析,并在回归图上画出95%可信区间,观察5水平冰冻混合人血清的坐标点是否位于95%可信区间范围内,如在则表明5水平冰冻混合人血清葡萄糖在该检测系统的反应性与血清相似具有互通性[3],并依照此法分析10份校正品和质控品的互通性。
1.6 统计学分析
采用SPSS 13.0进行统计学分析。均匀性检验采用单因素方差分析,Sbb为瓶间均方(MS瓶间)与瓶内均方(MS瓶内)之差除以测定次数(n)的商的平方根。稳定性检验采用直线回归分析,求出按时间(x)推算葡萄糖含量(y)的直线回归方程中的截距(a)和斜率(b),在-80℃研究中求出与斜率相关的不确定度(Sb),同时对方程进行线性回归方差分析以评估是否稳定。对定值原始数据作箱须图(Box-Whisker plot)剔除离群值。互通性采用直线相关与回归分析。P<0.05为差异有统计学意义。
2 结果
2.1 均匀性检验结果
C4水平MS瓶间和MS瓶内分别为0.004和0.003,计算Sbb等于 0.018 mmoL/L,其余4水平MS瓶间≤MS瓶内,Sbb等于0,经单因素方差分析P值全部大于0.05,5水平冰冻混合人血清全部具有良好的均匀性。
2.2 稳定性检验结果
-80℃储存条件采用参考方法测定,其余温度储存条件采用罗氏己糖激酶法测定,按每项测定结果均值计算方程,经线性回归方差分析P值全部大于0.05(结果见表1)。5个水平冰冻混合人血清葡萄糖含量在室温、4℃、-20℃分别至少稳定3天、14天、28天;-80℃至少稳定10个月,现在继续观察中。
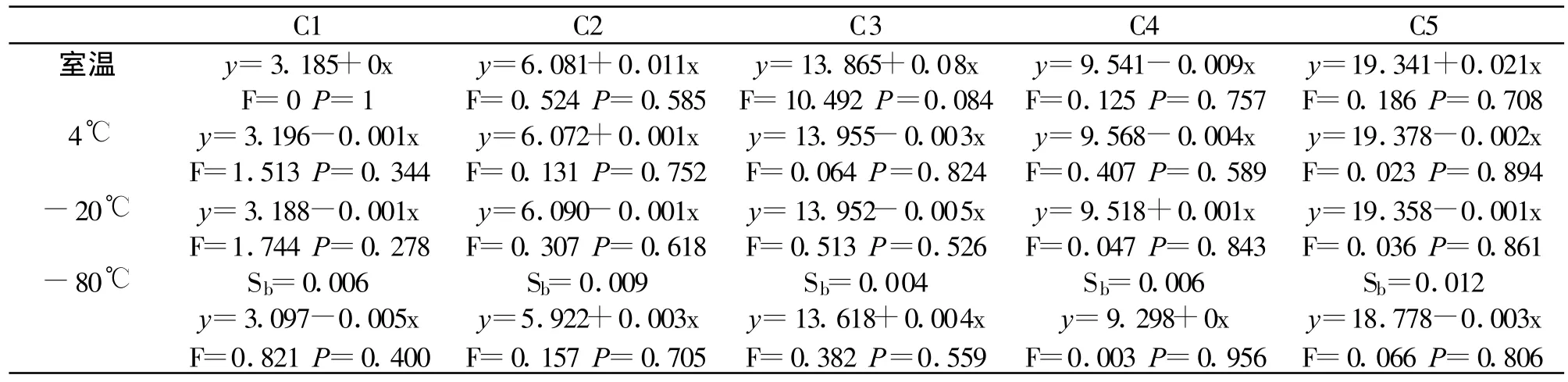
表1 5水平冰冻混合人血清在不同条件下的稳定性
2.3 定值
2.3.1 葡萄糖参考方法准确性验证
2家实验室为SRM965a(NIST出品,采用同位素稀释气相色谱质谱法定值)测定结果显示,酶法较定值偏低,平均偏差约为0.3%-2.6%,与1987年Pelletier和Arratoon[4]的报道相同,即测定血清标本时HK参考方法较质谱法偏低(-2.5%);同时参加2008年的参考实验室间血糖RELA比对,进一步验证了参考方法的准确性(数据可从http://www.dgklrfb.de:81获得)。
2.3.2 采用HK参考方法为5水平冰冻混合人血清定值
测定系统偏差以2家实验室测定SRM965a的结果为依据,稳定性所带来的不确定度(U稳定)=Sb×时间,10个月稳定性的不确定度为(U10个月)=Sb×10(结果见表2)。
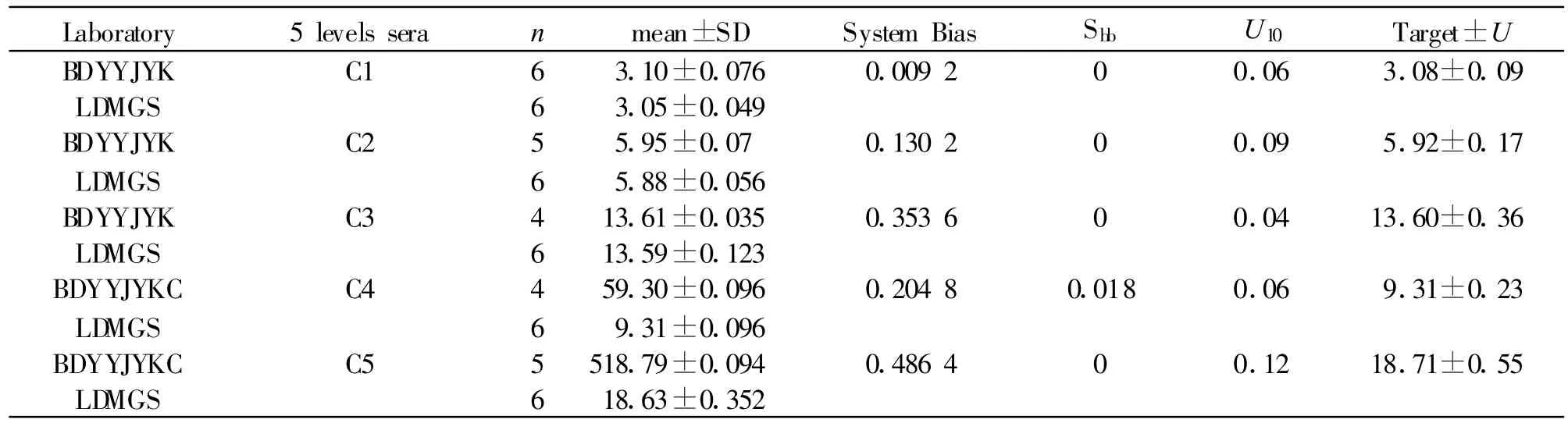
表2 两家实验室为5个水平血清葡萄糖标准物质的定值结果(单位mmol/L)
2.4 互通性
图1中图A-D分别为参考方法与4种常规方法40份血清测定结果的回归直线图,以参考方法为x轴,常规方法为y轴,图A-D分别代表贝克曼氧电极法、罗氏GOD法、德灵HK法和强生干化学法,贝克曼氧HK法和罗氏HK法与德灵HK法结果一致。5水平冰冻混合人血清葡萄糖测定结果的坐标点全部在回归直线95%可信区间范围内。5水平冰冻混合人血清在6种常规检测系统中全部具有良好的互通性。10份校正品和质控品较候选标准物质的互通性差,主要表现在干化学法上的互通性(见图1中图D),贝克曼库尔特公司出品的高值质控品BQ3尤其显著,其与BQ1和BQ2同为液体质控品,但其靶值显著高于后两者,可能其中的抗冻物质在反应过程中影响了互通性。中生公司水溶液校正品除在干化学法上互通性差外,在其它检测系统上互通性较好。其它血清基质的质控品和校正品互通性相对较好,罗氏公司PNU和朗道公司质控品2在6个测定系统上均有较好的互通性。
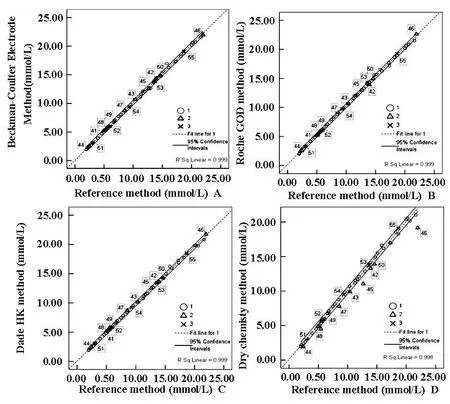
图1 图A-D分别表示参考方法与4种常规方法40份人血清测定结果回归直线的95%可信区间
3 讨论
由于常规检测系统自动化分析的普及,测定精密度大大提高,已足够满足临床要求。但常规系统的正确度还需要评估。应具备一种有靶值的物质用于常规系统间的评估,这种物质首先应具备互通性,最容易获得的当然是水溶液。我们观察了在临床上应用最广泛的10份校正品和质控品,其中包括水溶液的和血清质的。水作为基质与血清的反应性不同,这一点在试验中得到证实,主要表现在干化学方法上的差异;而血清质的校正品和质控品由于添加了一些成分,在高值时也会影响其互通性。
新鲜血清池无疑将成为最佳选择,但因葡萄糖为细菌代谢原料,为保证血清池无菌,又不能向其中添加任何抗生素和防腐剂,我们分别经过0.8、0.45、0.2 μ m过滤膜过滤以除菌。通过短期稳定性观察,5水平冰冻混合人血清在室温、4℃、-20℃葡萄糖含量至少分别稳定3天、14天和28天,以足够满足在运输过程中可能遇到的情况,-80℃为长期保存条件,至今至少稳定10个月。葡萄糖的溶解度高,在血清中很容易达到均匀状态,但在分装过程中血清池水分挥发会影响其浓度变化,因此我们在生物安全柜中,湿度不低于70%的条件下分装,及时盖盖,通过采用系统抽样做均一性检验,5水平冰冻混合人血清全部具有良好的均匀性。混合血清虽未向其中添加任何成分,但经过过滤,我们进行了互通性研究,从结果中可看出,经过滤后的混合血清葡萄糖在各检测系统上的测定与血清的反应性完全相同。
定值结果中已将对不确定度有贡献的因素进行较全面计算,短期稳定性的不确定度没有考虑,如在运输过程中没有超出本次研究的时间范围,则对定值结果没有影响,否则应考虑短期稳定性对结果的影响。
5水平冰冻混合人血清的稳定性、均匀性等基本性质完全达到《标准物质/标准样品生产者能力认可准则》[5]的要求,并具备与血清完全相同的反应性,定值结果准确。可用于常规检测系统精度的评价以发现并解决在临床测定系统中存在的问题,使葡萄糖统一的诊治标准在临床达到科学合理的应用,也为日后葡萄糖诊治节点的改变提供科学的依据。
[1]中国合格评定国家认可委员会.《标准物质/标准样品生产者能力认可准则》.北京:CNAS,2007.
[2]Neese JW,Duncan P,Bayse D,et al.Stewart C.Development and evaluation of a hexokinase/glucose-6-phosphate dehydrogenase procedure for use as a national glucose reference method.HEW Publication No.(CDC)77-8330:the United States Centers for Disease Control,1976.
[3]焦莉莉,李海霞,徐国宾,等.3种血浆 TCO2测定法分析性能与NaHCO3水质标准液互通性评估[J].临床检验杂志,2009,27(3):174.
[4]Pelletier O,Arratoon C.Precision of glucose measurement in control sera by ID/MS:proposed definitive method compared with a reference mothed[J].Clin Chem,1987,33(8):1397.
[5]叶任高,陆再英,谢 毅,等.内科学[M].第6版.北京:人民卫生出版社,2006:797-798.
The study of 5 levels serumglucose standard reference materials
LIU Ou,XUGuo-bin,SHAN Quan-zhong,et al.(Department of laboratory medicine,TsingHua University First Hospital,Beijing100016,China)
ObjectiveTo prepare 5 levels serum glucose standard reference materials,in order to provide material to evaluate glucose routine analyzed systems.MethodsFresh sera without hemolysis,lipemia and choloplania were collected.Serum pools were filtered with 0.8,0.45 and 0.2 μ m filtrationmembrane of Sartorius company andwere sub-packed in frozen tubes.According to《 Accreditation Criteria for the Competence of Reference MaterialProducers》,the uniformity of the poolswere examined,Stability study includes short-term(room temperture、4℃、-20℃)and long-term(-80℃)stability.Resultswere expressed as“target value ±uncertainty”,mean value of 2 glucose reference laboratories was used as target value,the uncertainty includes determination of vatiation and uncertainty brought by measurement system bias,Sbb,long-term stability.We observed commutability of serum on 6 routine analyzed systems.ResultsThe 5 levels serum have been obtained(C1,C2,C3,C4 and C5).Sbbof level C4 is0.018mmol/L and others are zero,P value of all levels are greater than0.05.P value of linear regression analysis of variance are greater than0.05.Mean value of 2 glucose reference laboratories are 3.08,5.92,13.60,9.31 and 18.71 mmol/L.Uncertainty are 0.09,0.17,0.36,0.23 and 0.55 mmol/L respectively.Coordinate dots of 5 levels serum are all within 95%confidence interval range of 40 serums regression line.They have the same speciality as serum.ConclusionThe uniformity,stability and commutability of 5 levels serum all meet the requirements,the target values are assigned accurately.
Glucose;Uniformity;Stability;Commutability
R446
A
1007-4287(2010)07-1009-04
“十一五”国家科技支撑计划资金资助(2007BA105B09),国家高技术研究发展计划(863计划)资金资助(2006AA020909)
*通讯作者
2010-03-02)

