抗乙型脑炎病毒E蛋白单克隆抗体5D4重链可变区基因的克隆及序列分析
赵付荣,杜 鹃,王 斌,陈娜莎,华荣虹,步志高
(1.中国农业科学院哈尔滨兽医研究所兽医生物技术国家重点实验室,黑龙江 哈尔滨 150001;2.华南农业大学兽医学院,广东 广州 510642;3.黑龙江大学生命科学学院,黑龙江 哈尔滨 150020)
流行性乙型脑炎(JE)简称乙脑,是由乙型脑炎病毒引起的一种重要蚊媒性人兽共患传染病。多种动物易感,蚊是JEV的主要传播媒介,猪是该病毒在自然界中最重要的贮存与增殖宿主,母猪感染可引起繁殖障碍,给养猪业造成巨大的经济损失。JEV主要在亚洲流行,而最近发现在南半球也有报道,这说明流行性乙型脑炎可能在世界范围内威胁着人类健康[1]。
JEV属黄病毒科黄病毒属,为单股正链、有囊膜的RNA病毒。病毒粒子包含3种结构蛋白(C、prM/M、E)。其中表面囊膜蛋白E蛋白是该病毒表面的一种重要的结构蛋白,在介导病毒的吸附、融合,决定病毒的血凝活性、细胞趋向性、病毒毒力和诱导宿主保护性免疫反应中起重要作用。
对乙型脑炎无特效治疗方法,接种疫苗是控制该病流行的有效措施。但是感染发病后再注射疫苗时,因抗体产生较慢,严重患者影响治疗效果,主张在注射疫苗的同时注射抗乙脑病毒免疫血清或单克隆抗体。但目前所能获得的上述制剂均来自动物,进入人体后易引起过敏反应[2],而人的制剂又相当难获得。本实验室在通过原核表达JEV E蛋白的基础上,制备了抗乙脑病毒 E蛋白的单克隆抗体5D4,通过一系列鉴定,能够特异性的识别JEV E蛋白[3]。本试验采用基因工程技术,从分泌抗JEV E蛋白的杂交瘤细胞中提取RNA,通过RT-PCR扩增抗体重链可变区基因VH,经克隆及测序分析VH基因,旨在为构建抗JEV基因工程抗体奠定基础。
1 材料与方法
1.1 细胞、质粒及菌株 分泌抗JEV抗体的杂交瘤细胞株5D4,大肠杆菌(E.coli)JM109菌株由兽医生物技术重点实验室保存。质粒pMD18-T Vector为TaKaPa公司产品,
1.2 主要试剂 Trizol试剂为Gibco公司产品,AMV 反转录酶、rRNasin Ribonuclease Inhibitor、为Promega公司产品,Taq DNA聚合酶、Ligation SolutionⅠ为TaKaRa公司产品,质粒抽提试剂盒为华舜生物工程有限公司产品。
1.3 方法
1.3.1 杂交瘤细胞总RNA的提取 从液氮罐中取出冻存的单抗杂交瘤细胞株5D4,复苏后用含20%犊牛血清的RPMI-1640培养至细胞总数约为2×107。1000 r/min离心10 min后,收集细胞,重悬沉淀于250μL pH 值7.2的无菌PBS中,并按RNA提取试剂盒(QIAGEN)提供的方法提取细胞总RNA,-20℃保存或直接用于反转录。
1.3.2 逆转录合成cDNA第一条链 按照AMV反转录酶说明书进行反转录:细胞 RNA提取液20μL,rRNasin Ribonuclease Inhibitor 2μL,dNTP(10 mmol/μ L)4μL,下游引物(50pmol/μ L)2μL,5×AMV 酶缓冲液8μL,AMV 反转录酶 4μL混匀后,室温放置10 min后移入42℃恒温槽中,水浴1 h取出,在冰上冰浴2 min。反转录产物可以直接进行PCR反应或-20℃贮存备用。
1.3.3 VH基因的扩增 根据抗体可变区基因序列的保守性,合成了针对重链可变区的通用引物[13-14],引物序列为:VHFor:5′-SAGGTSCAGCTGMAGGAGTCWGG-3′,VHBack:5′-TGAGGAGACGGTGACCATGGTCCC-3′[注:W=A/T;S=G/C;M=A/C;R=A/G]。以合成的cDNA为模板进行PCR扩增,反应条件:95℃5 min,94℃1 min,53℃1 min,72℃2.5 min,循环35次,72℃延伸10 min。PCR扩增产物以回收试剂盒回收。
1.3.4 VH基因的克隆 将回收的VH基因与T载体连接,连接产物转化大肠杆菌JM109,37℃培养过夜,随机挑取生长良好的单个菌落进行PCR鉴定。阳性克隆进行序列测定。
1.3.5 克隆的VH和VL基因序列分析 测得的基因序列,在NCBI网站上用BLAST程序进行检索,与获得的抗体VH基因序列进行同源性分析,V区基因的胚系分析可通过登录英国的生物信息学研究所的站点(http://www.ebi.ac.uk/imgt/),进入IMGT/V-QUEST网页,将VH基因序列输入对话框进行胚系基因片段的分析。
2 结果与分析
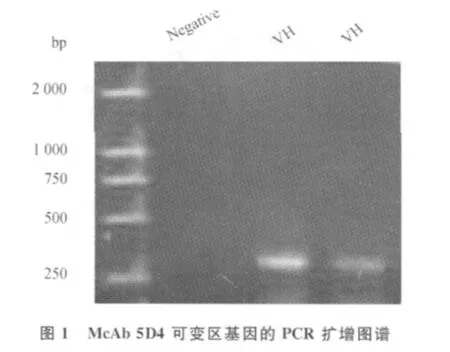
2.1 5D4的VH和VL基因的扩增及鉴定 分别用轻、重链特异性5′端和 3′端引物,对重链可变区基因进行PCR扩增。各取PCR产物5μL,以1.5%Agarose凝胶电泳,显示330 bp位置可见清晰的特异性扩增VH 条带(图1)。
2.2 5D4的VH在pMD18-T Vector质粒的克隆与鉴定 以pMD18-T-VH表示插入了5D4 VH重组质粒。以5D4 pMD18-T-VH的连接产物,转化E.coli JM109,在含Amp+的LB平板上培养,分别从中随机挑取单克隆进行培养,提取质粒DNA得到重组质粒5D4pMD18-T-VH通过提质粒进行PCR鉴定。得到330 bp左右的VH片段(图2),表明5D4的VH基因在质粒中克隆成功。

2.3 5D4的VH和VL核苷酸序列的测定及分析通过BLAST在GenBank数据库中对获得的抗体VH基因序列进行同源性分析,结果显示基因与序列 号 AY853694(gi:57169132)、AY208318(gi:37784217)同源性达94%,通过英国的生物信息学研究所在线程序进行胚系基因片段的分析,经分析为小鼠免疫球蛋白基因,其VH属于IgHVⅠ家族,D段无结果,J段来自IgHVⅡ家族。该抗体VH基因序列与对应的氨基酸序列如图3所示。
3 讨论

相关文献表明,抗体可变区基因扩增的关键是杂交瘤细胞生长状态与引物设计[4-5],由于扩增的抗体可变区基因是未知序列,所以引物的设计显得尤为重要,首先考虑到引物的通用性,本文根据抗体可变区基因序列的保守性,合成了一对针对重链可变区的通用引物,试验结果显示,扩增到328 bp的重链可变区基因,经序列测定后,发现该基因为小鼠免疫球蛋白基因。
与鼠源单克隆抗体比较基因工程抗体的具有操作简便、表达量大、成本低廉的特点[6],用克隆的V区基因可产生与抗原特异性结合的抗体片段[7],利用基因突变技术改变抗体的某些结构可提高抗体的亲和力,比如单链抗体,嵌合抗体等,可延长其半衰期[8]。随着分子生物学和免疫学技术的不断发展,基因工程抗体势必将会对人类的生产、生活起到更大的促进作用。
本试验通过RT-PCR技术成功扩增了抗JEV E蛋白单抗5D4重链可变区基因,并对该基因进行了序列分析,结果显示,该基因与小鼠免疫球蛋白基因相符。我们正在开展5D4基因工程抗体的研究,该基因克隆与序列分析为此研究奠定了良好的基础。
[1]van Den Hurk A F,Montgomery B L,Northill J A,et al.Short report:the first isolation of Japanese encephalitis virus from mosquitoes collected from mainland Australia[J].Am J T rop Med Hyg,2006,75(1):21-25.
[2]Larrick J W.Potential of monoclonal antibodies as pharmacological agents[J].Pharm Rev,1989,41:539-557.
[3]赵付荣,华荣虹,王斌,等.流行性乙型脑炎病毒E蛋白单克隆抗体的制备与鉴定[J].中国兽医杂志,2010,46(1):3-5.
[4]Martsev S P,Chumanevich A A,Vlasov A P,et al.Antiferritin single-chain Fv fragment is a functional protein with properties of a partially structure state:comparison with the completely folded V(L)domain[J].Biochemistry,2000,39(27):8047-8057.
[5]Asano R,Takemura S,Tsumoto K,et al.Functional construction of the anti-mucin core protein(M UC1)antibody MUSE11 variable regions in a bacterial ex pression system[J].J Biochem,2000,127(4):673-679.
[6]Winter G,Milistein C.Man-made antibodies[J].Nature,1991,349(6307):293-299.
[7]Benhar I,Pastan I.Identification of residues that stabilize the single-chain Fv of monoclonal antibodies B3[J].J Biol Chem,1995,270:23373-23380.
[8]Mats O,Henrik O,Michael M,et al.Light chain shuffling of a high affinity antibody results in a drift in epitope recog nition[J].Molecular Immunology,1996,33(1):47-56.

