我院108例抗肿瘤药致不良反应报告分析
蔡和平,王 卓,黄 瑾,徐慧欣,杨 黎(第二军医大学长海医院药学部,上海市 200433)
据世界卫生组织报告,全世界因癌症死亡的人数达600万,占总死亡人数的12%;在我国,肿瘤死亡率在主要疾病排名中列居第2位,死亡率为8.58万/10万,占死亡总人数的21.58%,肿瘤已成为我国高死亡的病种之一[1]。抗肿瘤药虽不断问世,但是绝大多数抗肿瘤药在抑制或杀伤肿瘤细胞的同时,对正常组织、器官不可避免地产生损害或毒性作用,给患者带来痛苦,甚至导致死亡。我院2004~2009年药品不良反应(ADR)报告资料显示,抗肿瘤药造成ADR的发生率均居前3位。为此,本文通过对上述6年所收集的108例抗肿瘤药致ADR报告深入分析,探讨临床药师对此类药物使用者进行药学监护的要点和重要性。
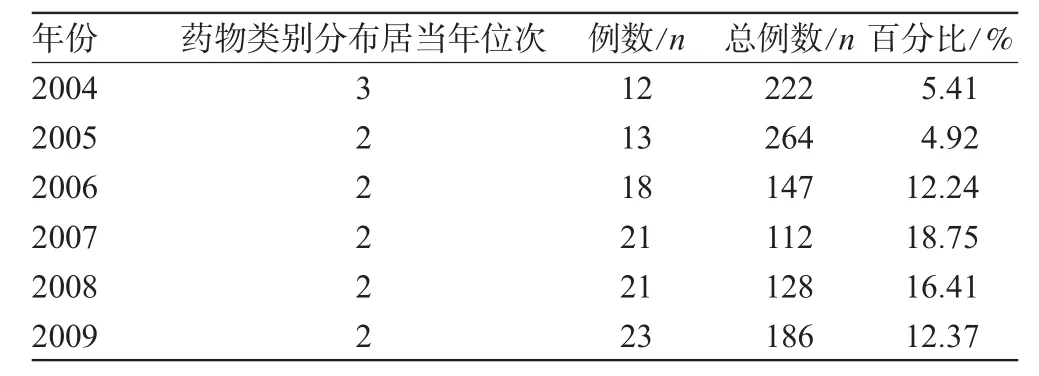
表1 抗肿瘤药致ADR年度类别分布位次、例数及构成比Tab 1 Distribution position,case number of antineoplastics-inducedADR and their constituent ratio
1 资料来源与方法
对我院2004~2009年上报的108例抗肿瘤药致ADR报告进行分类频数统计与分析评价。其中,抗肿瘤药致ADR年度类别分布位次、例数及构成比见表1。
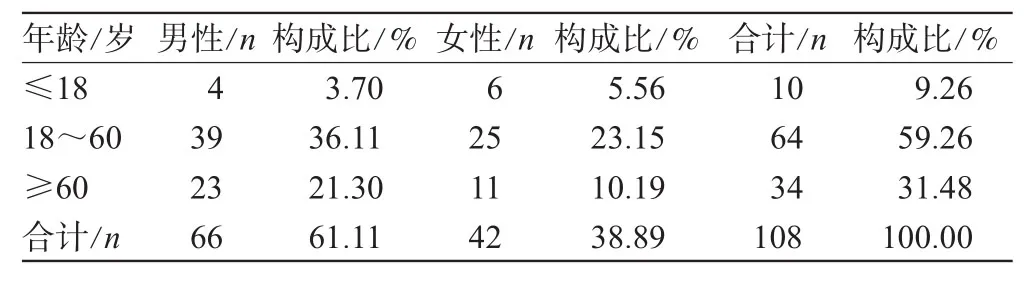
表2 抗肿瘤药致ADR发生的年龄与性别分布Tab 2 Distribution of patients’age and gender in ADR cases induced by antineoplastics
2 结果
2.1 性别与年龄分布
108例抗肿瘤药致ADR报告中,男性病例居多,共66例,占61.11%;18~60岁所占比例最大,占59.26%,其中男性占多数,有39例,占36.11%。抗肿瘤药致ADR发生的年龄与性别分布见表2。
2.2 ADR发生时间
用药当日发生ADR 64例,占59.26%,男性39例,占60.94%,女性25例,占39.06%,其中在药物滴注过程中发生ADR 32例,占50.00%。用药后1 d出现ADR 13例,占12.04%;其他时间发生ADR的有31例,占28.70%。
2.3 致ADR发生的抗肿瘤药类别、具体药品及例数
致ADR发生的抗肿瘤药类别、具体药品及例数见表3。

表3 致ADR发生的抗肿瘤药类别、具体药品及例数Tab 3 Category and case number of antineoplastics inducingADR and drugs involved inADR
2.4 抗肿瘤药致ADR发生的具体药品、例数、构成比、临床表现及ADR出现时间
抗肿瘤药致ADR发生的具体药品、例数、构成比、临床表现及ADR出现时间见表4。

表4 抗肿瘤药致ADR发生的具体药品、例数、构成比、临床表现及ADR出现时间Tab 4 Specific drugs involved in ADR and case number,constituent ratio,clinical manifestation and occurrence time of ADR cases induced by antineoplastics
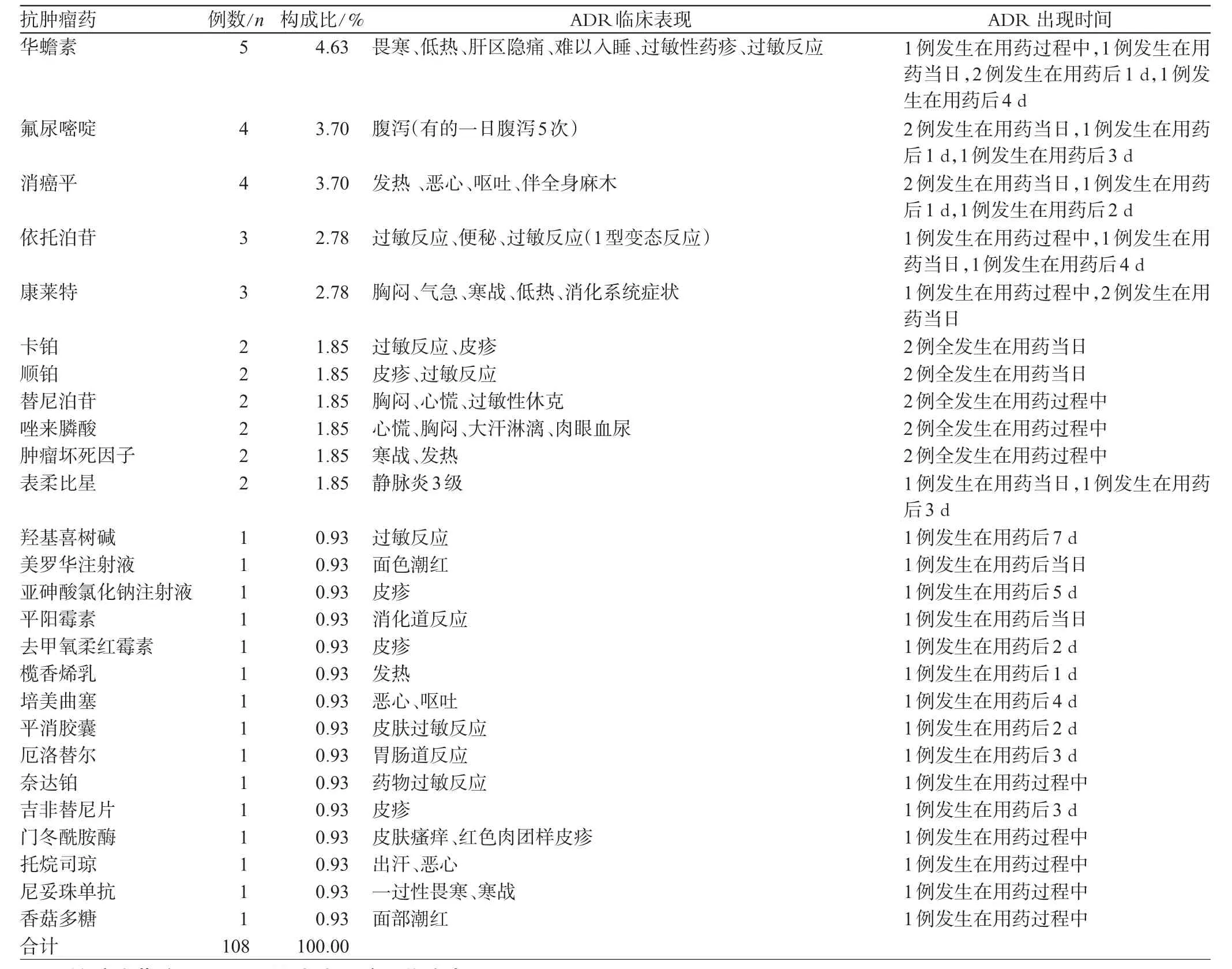
续表4
2.5 抗肿瘤药致ADR累及器官或系统及临床表现
抗肿瘤药致ADR累及器官或系统及临床表现见表5(由于同一例ADR可累及多个器官或系统,故统计例数大于实际例数)。
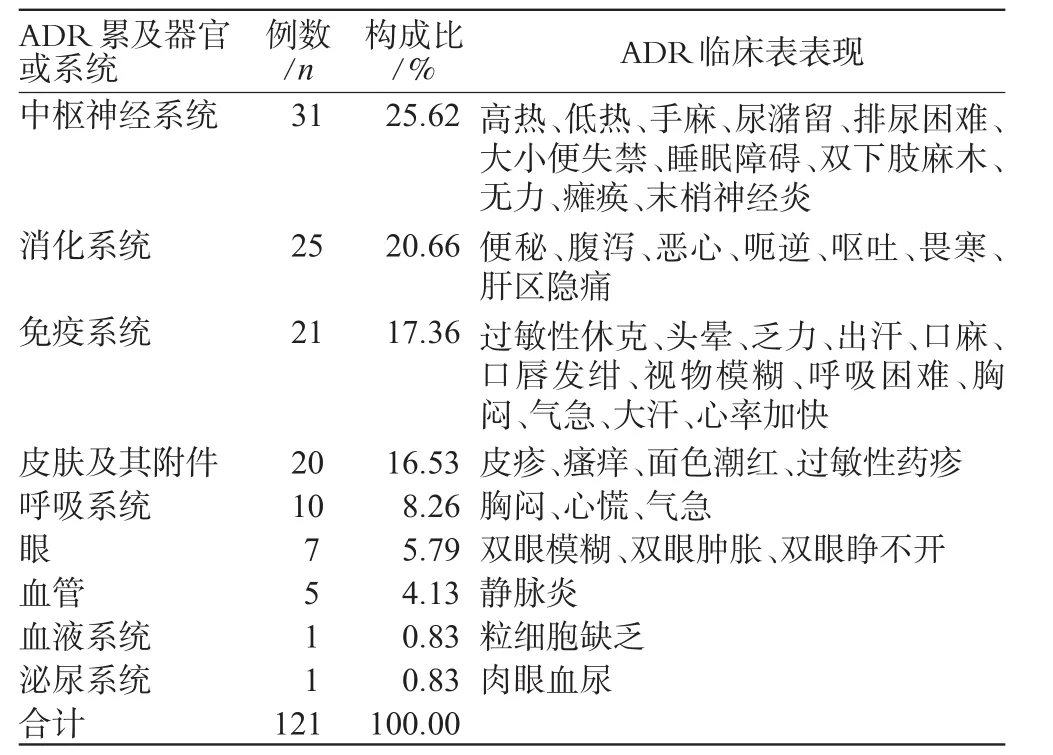
表5 抗肿瘤药致ADR累及器官或系统及临床表现Tab 5 Organs or systems involved in antineoplastics and clinical manifestations
3 讨论[2,3]
3.1 重点关注肿瘤患者的用药人群
从表2可以看出,男性的抗肿瘤药ADR发生率较高,占61.11%,18~60岁的青中年发生率较多,占59.26%,而且其中男性居多。由“2.2”项可以看出,用药当日发生ADR中男性的发生率也较高,占60.94%。这表明男性和中青年肿瘤患者ADR发生率较高。
3.2 重点关注抗肿瘤药致ADR发生时间
由“2.2”项可以看出,用药当日发生ADR比例最大,可见用药当日是出现ADR的高峰时间,其中用药过程中发生ADR占50.00%,如抗肿瘤药紫杉醇过敏反应,9例(100%)均发生在用药过程中,而且几乎发生在用药后约10 min,所以在用上述抗肿瘤药过程中及用药后1 d临床药师均应高度监护。
3.3 重点关注的抗肿瘤药
从表3可以看出,其它抗肿瘤药及辅助治疗药ADR发生率最高,主要以铂类比例最大;其次是抗代谢药。从表4可以看出,发生ADR的抗肿瘤药前5位分别为奥沙利铂(12.96%)、甲氨蝶呤(11.11%)、紫杉醇(8.33%)、多西他赛(5.56%)、吉西他滨(5.56%)。这些抗肿瘤药是临床常用化疗药,其中奥沙利铂常用于消化道肿瘤,甲氨蝶呤常用于白血病治疗,紫杉醇、多西他赛、吉西他滨常用于肺癌的化疗。消化道肿瘤、血液病与肺癌目前患病率较高,这些都是临床药师需关注的重点。
3.4 重点关注抗肿瘤药致ADR累及器官或系统及表现
从表4可以看出,中枢神经系统症状发生率最高,主要的临床表现为发热、双下肢麻木、无力等。抗肿瘤药进入人体后易引起发热,这可能与抗肿瘤药激活内源性致热原,使其释放进入血液有关[2];双下肢无力、瘫痪主要是因2007年不合格(混入另一种抗肿瘤药长春新碱)的甲氨蝶呤导致的,该事件已受到国家食品药品监督管理局的重视和查处。其次为消化道症状,大多数抗肿瘤药可刺激胃肠道黏膜上皮细胞,抑制其生长,引起不同程度、不同类型的胃肠道反应[2]。所以临床药师在临床上对化疗患者应重点关注患者用药后的反应及有无器官损害的早期症状。
3.5 临床药师在预防抗肿瘤药致ADR中的重要性
绝大多数抗肿瘤药在抑制或杀伤肿瘤细胞的同时,对正常组织、器官不可避免地产生损害或毒性作用。但是通过临床药师参与可以有针对性地预防抗肿瘤药致ADR的发生,或是及时采取适当措施减轻ADR造成的损害和影响。笔者作为呼吸科临床药师,曾在临床观察过1例紫杉醇引起过敏性反应的病例,其在输注过程中发生了严重的过敏性休克,因严密监测,临床医师给予及时抢救,患者才脱离危险。笔者后检索相关资料得知,紫杉醇注射液的过敏反应是由于制剂赋形剂聚氧乙烯蓖麻油引起的,几乎都发生于用药后最初10 min内。故在开始用药15 min内,输液速度应控制在10~15滴·min-1并严密观察,如无异常反应再将输液速度调至40~60滴·min-1,于3~4 h输完,这样可以减少过敏性反应的发生。同时临床药师提醒并协助医师在使用该药前依据说明书给予规范的预防药物及处理方案。此后所在病区紫杉醇引发的过敏反应越来越少。可见,临床药师有针对性地监护使用特定抗肿瘤药的患者,在预防ADR中可以起到有效的作用。
[1]刘世莲.抗肿瘤相关药物的不良反应报告分析[J].中国保健营养:临床医学学刊,2008,17(9):5.
[2]Liu SL.Analysis of adverse drug reactions induced by anti-tumor relevant drug[J].Clinical Journal,2008,17(18):5.
[3]李泽辉,王晓丹,李宝笙.95例抗肿瘤药物的不良反应报告分析[J].中国药物警戒,2008,5(2):104.

