高锑低银铅阳极泥控电氯化浸出
陈进中 ,杨天足
(1. 中南大学 冶金科学与工程学院,湖南 长沙,410083;2. 广西华锡集团股份有限公司,广西 柳州,545006)
由脆硫铅锑精矿冶炼成的粗铅经电解精炼后所产生的阳极泥成分较复杂,是一种典型的高锑低银类铅阳极泥。这类阳极泥普遍采用火法处理,其工艺落后,银回收率低,能耗高,环境污染严重。为此,丘克强等[1-4]提出采用真空还原法实现锑的分离。湿法处理铅阳极泥是近年来发展起来的一种新技术,通常湿法处理铅阳极泥是以浸出过程来实现贵、贱金属的分离,而浸出过程中采用何种氧化剂对贵、贱金属的分离和贱金属的进一步处理均有较大影响。聂晓军等[5]采用低温空气预氧化然后加氯酸钠作氧化剂进行氯化浸出高锑低银类铅阳极泥,氯化浸出虽能分离贵、贱金属,但浸出液中含有碱金属钠离子,不利于贱金属进一步处理。唐谟堂等[6]采用SbCl5作为氧化剂对高锑低银类铅阳极泥进行氯化浸出,氯化浸出过程也能分离贵、贱金属,虽未带入碱金属离子,但铅阳极泥中高含量的金属锑存在需要大量的氧化剂 SbCl5。控制电位氯化浸出是湿法冶金的一种有效手段,应用控制电位氯化浸出可有效地分离贵、贱金属和提取贵金属[7]。张关录[8]采用控制电位氯化浸出含贵金属铜镍合金,有效地分离贵、贱金属。林宏义等[9-10]提出了“盐酸介质控制电位氯化浸出—浸出液还原—蒸馏脱砷”处理铅阳极泥新工艺新流程,有效地分离贵、贱金属,贵、贱金属回收率都在99%以上。谢斌等[11]采用制电位氯化浸出铅阳极泥,对低砷铅阳极泥能顺利实现贵贱金属分离,而对高砷铅阳极泥则贵金属的损失较大,其损失量随铅阳极泥中砷的含量增加而增加。他们均注重控制电位氯化浸出分离贵、贱金属效果,而对有关影响因素对氯化浸出过程中溶液电位变化规律研究较少。为此,本文作者采用控制电位氯化浸出高锑低银类铅阳极泥,研究氯化浸出过程中溶液电位随时间变化规律,温度、Sb3+浓度对溶液电位的影响以及不同溶液电位下浸出渣的物相,探讨氯化浸出过程中铅、银的行为。
1 试验研究方法
1.1 试验原料
铅阳极泥试样取自广西华锡集团某冶炼厂,其成分分析结果如表1所示。由表1可知,锑含量为70.52%,属于高锑低银类铅阳极泥。
物相分析结果表明:锑主要为单质锑;银与少量锑形成金属间化合物;铜与砷形成金属间化合物,银、铜、砷无单质存在;阳极泥中铅主要以金属铅和氧化铅的形式存在。铋与铅、锑形成金属间化合物或金属氧化物。另外,铅阳极泥有自然氧化的特性,随着放置时间的增长,铅阳极泥中的铅、锑、铋等元素有部分以氧化物的形态存在。

表1 铅阳极泥各元素含量Table 1 Composition of lead anode slime w/%
1.2 研究过程
非氧化浸出是将一定量铅阳极泥加入到 6 mol/L的盐酸溶液中浸出2 h,控制温度为80 ℃,过滤,分析滤液中金属离子的浓度和滤渣中氯化铅的含量,从而计算铅阳极泥的消耗酸度。
控电氯化浸出试验是将300 g铅阳极泥加入到一定浓度的盐酸溶液中在一定温度下先浸出1 h,然后,以一定的流速通入氯气,同时测量溶液的电位。当溶液电位达到一定值时,停止通氯,稍后即过滤,用 2 mol/L盐酸溶液洗涤滤渣,干燥后分析其物相。
浸出过程中Sb3+质量浓度对溶液电位的影响试验是:将300 g铅阳极泥经非氧化浸出所得的浸出渣加入到不同Sb3+质量浓度的盐酸溶液中,在一定温度下以一定的流速通入氯气,同时测量溶液的电位。
溶液电位的测量是:在氯化浸出反应器内插入测定电位的铂电极(指示电极)和甘汞电极(参比电极),以铂电极对饱和甘汞电极测得控制电位。
Sb3+的测定采用硫酸铈滴定法,Bi3+和Pb2+的测定采用EDTA滴定法,Cu2+的测定采用碘量法滴定,Ag+的测定采用硫氰酸氨滴定法。采用 Thermo ARL X’TRA型X线衍射仪进行物相分析,射线源为Cu Kα,管电压为40 kV,电流为100 mA,扫描速率为5 (°)/min。
2 结果与讨论
2.1 浸出酸度的确定
在铅阳极泥浸出过程中,既要考虑金属锑的氧化过程,又要考虑SbCl3的氯络合平衡和水解平衡。
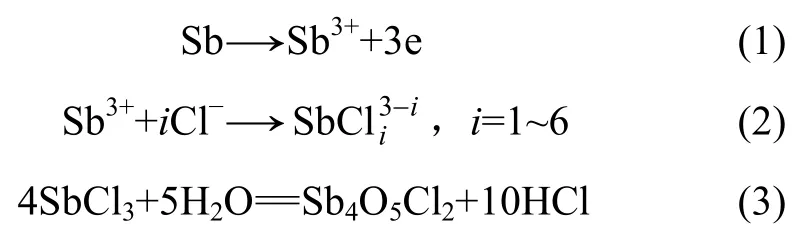
根据氯络合平衡和水解平衡而得到的三氯化锑水解体系基本热力学模型[6]可以确定 300 g铅阳极泥氯化浸出体系的极限酸度为2.25 mol/L。通过非氧化浸出实验,可测得这种阳极泥的消耗酸度为2.47 mol/L。故浸出体系的总酸度应该是极限酸度和消耗酸度之和,即4.72 mol/L。
图 1所示为浸出过程中溶液电位随时间变化曲线。从图1可以看出,即在浸出过程中,溶液的电位变化有3个阶段:第1阶段即AB段,是起始阶段,溶液的电位缓慢上升;第2阶段即BC段,是水平平台,溶液的电位变化不大;第3阶段即CD段,溶液的电位急剧上升。在第1阶段,溶液电位缓慢上升是由于氯气以一定流速通入溶液中,氯气溶入溶液可能发生如下反应:
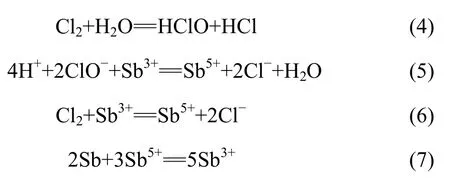
在开始阶段,虽然溶液中有HClO,ClO-,Cl2和Sb5+等组分存在,但反应(4)~(7)的反应速度较快,所以,溶液电位上升缓慢;在第2阶段,由于反应(4)~(7)这些反应达到动态平衡,即原料阳极泥中以单质金属锑形态大量存在,以本试验的流速通入溶液的氯气只能氧化阳极泥中的金属锑,以致溶液的电位变化不大;在第3阶段,阳极泥中单质金属锑大多数已被氧化,通入溶液的氯气使溶液中HClO,ClO-,Cl2和Sb5+等组分的含量急剧增加,所以,溶液电位快速上升。
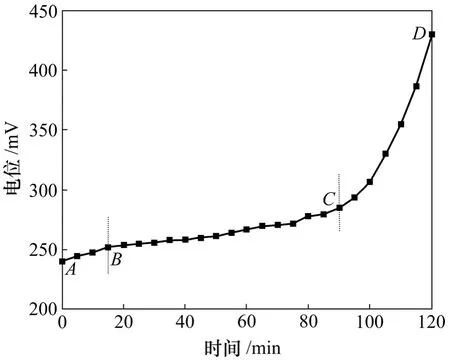
图1 浸出过程中溶液电位随时间变化曲线Fig.1 Solution potential—time curve during leaching process
2.3 Sb3+质量浓度对溶液电位的影响
图2 所示为浸出过程中Sb3+质量浓度对溶液电位的影响曲线。从图2可以看出:随着溶液中Sb3+质量浓度的升高,溶液电位随时间变化曲线的第2阶段水平平台逐渐缩短,30 g/L Sb3+溶液的电位随时间变化曲线的第2阶段水平平台延时80 min,60 g/L Sb3+的溶液其水平平台延时55 min,而90 g/L Sb3+的溶液其水平平台延时则降至40 min。这可能是由于氯气以一定流速通入溶液中去氧化阳极泥的金属锑,溶液中Sb3+主要起到催化作用,溶液中 Sb3+质量浓度越高则氯化浸出时间越短;溶液中Sb3+质量浓度越低,则氯化浸出时间越长。
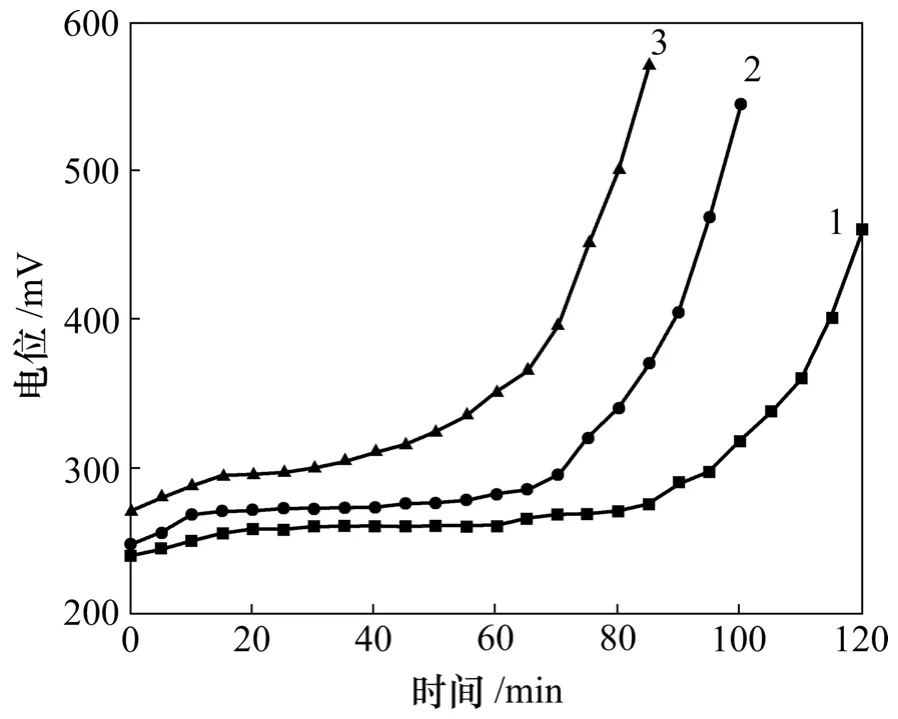
图2 浸出过程中Sb3+质量浓度对溶液电位的影响Fig.2 Influence of Sb3+ concentration on solution potential during leaching process
另一方面,随着溶液中Sb3+质量浓度的升高,溶液电位也相应较高,而且溶液电位随时间变化曲线的第 2阶段水平平台的坡度逐渐增大。这一现象符合Nerst方程:
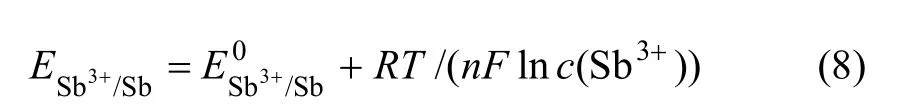
式中:E为测量电极电位,V;E0为标准电极电位,V;R为理想气体常数;T为热力学温度,K;n为电子数;F为法拉第常数;c(Sb3+)为Sb3+的有效浓度,mol/L。由式(8)可知,溶液中Sb3+浓度高,溶液电位也相应较高。随着溶液中Sb3+浓度的升高,溶液电位随时间变化曲线的第2阶段水平平台的坡度逐渐增大,可能是此时的溶液还存在Sb5+,溶液的电位还受其影响,即:
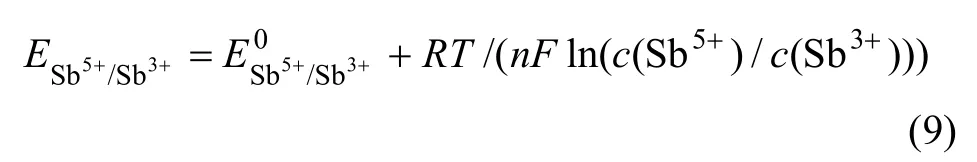
式中:c(Sb5+)为 Sb5+的有效浓度,mol/L。以一定的流速通入溶液中的氯气,使溶液中的 Sb3+氧化为Sb5+,Sb5+再将阳极泥中的金属锑氧化成Sb3+。当起始Sb3+浓度较高时,随着氯化浸出过程的进行,溶液中Sb5+浓度较高,所以,溶液电位随时间变化曲线的第2阶段水平平台的坡度较大。
2.3 温度对溶液电位的影响
图3所示为浸出过程中温度对溶液电位的影响曲线。从图3可以看出:随着溶液中温度的升高,溶液电位随时间变化曲线的第2阶段水平平台逐渐缩短;40 ℃时,溶液电位随时间变化曲线的第2阶段水平平台延时100 min;60 ℃时,其水平平台延时75 min,而80 ℃时,其水平平台延时则降至40 min。这说明温度对浸出过程中的影响较大。这主要是反应受动力学控制。
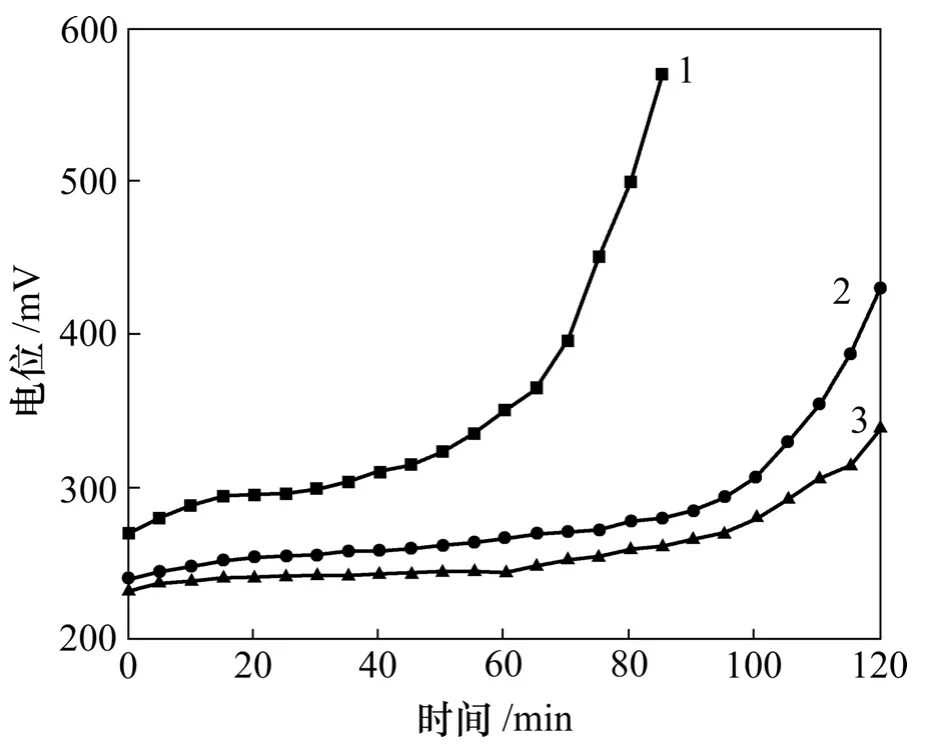
图3 浸出过程中温度对溶液电位的影响Fig.3 Influence of temperature on solution potential during leaching process
2.4 不同溶液电位下浸出渣的物相
图4所示为80 ℃时不同溶液电位下浸出渣的X线衍射图谱。从图4可以看出:溶液电位控制在430 mV以时,浸出渣中主要以PbCl2和AgCl存在,难以发现贱金属锑、铋和铜有单一的峰,说明在这样的电位下浸出贱金属锑、铋和铜的浸出率很高;随着溶液电位的升高,浸出渣中PbCl2和AgCl的含量逐渐增加;而控制溶液电位低于430 mV时,则浸出渣中除PbCl2和 AgCl物相外,还存在金属锑单一物相。从实验现象也可发现:当通氯气氯化浸出过程进行到溶液表观电位为425 mV时即停止通氯气,溶液表观电位随之下降。这也说明浸出渣中还存在金属锑,将溶液中生成的Sb5+又还原成Sb3+,溶液电位也随之降低。
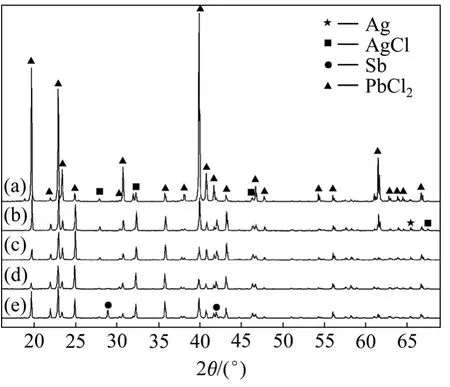
图4 不同溶液电位下浸出渣的XRD图谱Fig.4 XRD patterns of leaching residue at different solution potentials
2.5 溶液电位对金属浸出率的影响
图 5所示为不同溶液电位下金属浸出率的变化图。从图5可以看出:随着溶液电位的升高,金属锑、铋和铜的浸出率先缓慢升高,到一定溶液电位,金属锑、铋和铜的浸出率分别快速升高,可达到99%以上。这主要是由于在一定溶液电位下可将以金属或金属间化合物形态存在的完全氧化而进入溶液。

图5 不同溶液电位下金属浸出率的变化Fig.5 Leaching ratio of metals at different solution potentials
从图5还可以看出:随着溶液电位的升高,金属铅和银的浸出率逐渐降低;当溶液电位为430 mV时,金属铅和银的浸出率分别为 3.10%和 2.34%。这一结果与文献[12]中的测试结果相吻合,而与文献[13]中的研究结果正好相反。究其原因,这主要是浸出条件不同所致。刘伟峰[13]在试验过程中采用液固比为7.5∶1,酸度为3.5 mol/L且加有氯化钠溶液,使体系的总金属离子浓度较低,氯离子浓度较高,从而导致 PbCl2的溶解度增加。
随着溶液电位的升高,铅阳极泥中的金属银和铅逐渐被氧化进入溶液或以 AgCl(s)和 PbCl2(s)的形式沉淀于浸出渣中,铅阳极泥中的铅在较低的溶液电位下即被氧化,而铅阳极泥中的金属银则要求较高的溶液电位才能被氧化,从图4也可以看出:当溶液电位为380 mV时,浸出渣中已不存在金属铅这一物相;而当溶液电位为550 mV时,浸出渣中还能发现金属银这一物相。
铅阳极泥中的金属银和铅逐渐被氧化后是进入溶液还是以AgCl(s)和PbCl2(s)的形式沉淀于浸出渣中,主要取决于溶液的温度[14]、溶液中氯离子浓度和Sb3+浓度[15]等影响因素,这也是决定AgCl(s)和PbCl2(s)溶解度的影响因素。当溶液中氯离子浓度较低时金属银和铅逐渐被氧化后大部分是以 AgCl(s)和 PbCl2(s)的形式沉淀于浸出渣中;随着溶液中氯离子浓度增加,AgCl(s)和PbCl2(s)溶解度也增大,部分以络合物的形态进入溶液,最后全部溶解。而当溶液中Sb3+浓度较小时,AgCl(s)和PbCl2(s)溶解度大,随着溶液中Sb3+浓度增加,AgCl(s)和PbCl2(s)溶解度减小;当溶液温度较低时,AgCl(s)和PbCl2(s)溶解度小,随着溶液温度升高,AgCl(s)和PbCl2(s)溶解度逐渐增大。
在本试验研究条件下,阳极泥中的金属银和铅被氧化后大部分是以 AgCl(s)和 PbCl2(s)的形式沉淀于浸出渣中,有少部分以络合物的形态进入溶液。为提高银和铅的回收率,应提高溶液中Sb3+浓度,降低溶液中氯离子浓度,同时,适当降低浸出过程的温度。
3 结论
(1) 浸出过程中溶液的电位变化有3个阶段:第1阶段,溶液的电位缓慢上升;第2阶段是水平平台,溶液的电位变化不大;第3阶段,溶液的电位急剧上升。随着溶液中Sb3+浓度的升高,溶液电位随时间变化曲线的水平平台逐渐缩短;随着溶液中温度升高,曲线的水平平台也逐渐缩短。
(2) 溶液电位决定浸出渣的物相,控制溶液电位在430 mV以上,浸出渣中主要以PbCl2和AgCl存在,无单一贱金属的峰发现,而控制溶液电位在 380 mV以下,浸出渣中还有金属锑单一物相。
(3) 在溶液电位为430 mV时,金属锑、铋和铜的浸出率均达到 99%以上,铅和银的浸出率分别为3.10%和2.34%。阳极泥中的金属银和铅被氧化后大部分是以AgCl(s)和PbCl2(s)的形式沉淀于浸出渣中,有少部分以络合物的形态进入溶液,还有部分银以金属态存在于浸出渣中。
[1] 丘克强, 杨学林, 张露露. 高锑铅阳极泥处理新工艺试验研究[J]. 黄金, 2003, 24(11): 37-39.QIU Ke-qiang, YANG Xue-lin, ZHANG Lu-lu. The new treatment technology of antimony-rich lead anode slime[J].Gold,2003, 24(11): 37-39.
[2] 杨学林, 丘克强, 张露露, 等. 利用高锑铅阳极泥制备三氧化二锑的工艺研究[J]. 现代化工, 2004, 24(2): 44-46.YANG Xue-lin, QIU Ke-qiang, ZHANG Lu-lu, et al. Preparation of antimony trioxide from antimony-rich lead anode slime[J].Modern Chemical Industry, 2004, 24(2): 44-46.
[3] 张露露, 杨学林, 丘克强. 高锑铅阳极泥真空还原除锑研究[J]. 化工进展, 2004, 23(8): 869-873.ZHANG Lu-lu, YANG Xue-lin, QIU Ke-qiang. Research on antimony removal from antimony-rich lead anode slime by vacuum reduction[J]. Chemical Industry and Engineering Progress, 2004, 23(8): 869-873.
[4] 杨学林. 高锑铅阳极泥处理新工艺[D]. 长沙: 中南大学冶金科学与工程学院, 2004: 30-56.YANG Xue-lin. The new treatment technology of antimony-rich lead anode slime[D]. Changsha: School of Metallurgical Science and Engineering, Central South University, 2004: 30-56.
[5] 聂晓军, 陈庆邦, 刘如意. 高锑低银铅阳极泥湿法提银及综合回收的研究[J]. 广东工学院学报, 1996, 13(4): 51-57.NIE Xiao-jun, CHEN Qing-bang, LIU Ru-yi. Studies on hydrometallurgical recovery of silver and other metals from high-antinomy and low-silver lead anode slimes[J]. Journal of Guangdong University of Technology, 1996, 13(4): 51-57.
[6] 唐谟堂, 唐朝波, 杨声海, 等. 用 AC法处理高锑低银类铅阳极泥—— 氯化浸出和干馏的扩大试验[J]. 中南工业大学学报:自然科学版, 2002, 33(4): 360-363.TANG Mo-tang, TANG Zhao-bo, YANG Sheng-hai, et al. AC process for treating lead electrolysis refining anodicslime bearing high antimony and lower sliver: Enlarge experiments of chlorination-leaching and dry-distillation[J]. Journal of Central South University of Technology: Natural Science, 2002, 33(4):360-363.
[7] 夏星, 杨天足, 刘伟峰. 贵锑选择性氯化浸出富集金过程中铅的行为研究[J]. 贵金属, 2008, 29(1): 5-10.XIA Xing, YANG Tian-zu, LIU Wei-feng. Study on the behavior of lead in the process of selective chlorination leaching of precious metals from base metals in gold-antimony alloy[J].Precious Metals, 2008, 29(1): 5-10.
[8] 张关录. Cu-Ni合金氯化浸出富集贵金属[J]. 贵金属, 2000,21(2): 20-25.ZHANG Guan-lu. Concentration of precious metals from copper-nikel alloy by chlorination leaching[J]. Precious Metals,2000, 21(2): 20-25.
[9] 林宏义. 铅阳极泥湿法处理新工艺研究[D]. 长沙: 中南大学冶金科学与工程学院, 2004: 11-33.LIN Hong-yi. The new hydrometallurgical process of lead anode slime[D]. Changsha: School of Metallurgical Science and Engineering, Central South University, 2004: 11-33.
[10] 左新田. 铅阳极泥处理新工艺及超细银粉的制备[D]. 长沙:中南大学冶金科学与工程学院, 2004: 13-30.ZUO Xin-tian. The new treatment process of lead anode slime and preparation of ultra-fine power[D]. Changsha: School of Metallurgical Science and Engineering, Central South University,2004: 13-30.
[11] 谢斌, 胡绪铭. 高砷铅泥控制电位氯化浸出金银[J]. 贵金属,1995, 16(1): 6-11.XIE Bin, HU Xu-ming. Study of a process of leaching high arsenic lead anode slime using chloridization under controlled electronic potential[J]. Precious Metals, 1995, 16(1): 6-11.
[12] 刘云霞. PbCl2在不同盐酸浓度、Sb3+浓度和温度条件下溶解度的研究[J]. 稀有金属, 2000, 24(4): 270-272.LIU Yun-xia. Study on PbCl2solubility under different conditions of HCl concentration, Sb3+concentration and temperature[J]. Chinese Journal of Rare Metals, 2000, 24(4):270-272.
[13] 刘伟峰. 控电位选择性氯化分离贵锑中贵贱金属的工艺研究[D]. 长沙: 中南大学冶金科学与工程学院, 2005.LIU Wei-feng. Study on the process of selective chlorination leaching of precious metals from base metals in gold-antimony alloy[D]. Changsha: School of Metallurgical Science and Engineering, Central South University, 2005.
[14] CHEN Jin-zhong, CAO Hua-zhen, LI Bo. Thermodynamic analysis of separating lead and antimony in chloride system[J].Transactions of Nonferrous Metals Society of China, 2009, 19(3):730-734.
[15] 陈进中, 曹华珍, 郑国渠. 高锑低银类铅阳极泥制备五氯化锑新工艺[J]. 中国有色金属学报, 2008, 18(11): 2094-2099.CHEN Jin-zhong, CAO Hua-zhen, ZHENG Guo-qu. Novel technology for preparation of SbCl5from lead anode slime with high antimony and low silver content[J]. The Chinese Journal of Nonferrous Metals, 2008, 18(11): 2094-2099.
[16] 支波. 高锑铅阳极泥制备五氯化锑及其水解过程的研究[D].杭州: 浙江工业大学化学工程与材料学院, 2006: 25-42.ZHI Bo. The preparation of antimony pentachloride from antimony-rich lead anode slime and its process of hydrolysis[D].Hangzhou: College of Chemical Engineering and Materials,Zhejiang University of Technology, 2006: 25-42.

