凝固点降低测定物质摩尔质量实验装置的改进
白云山李世荣 安洁 罗五魁
(陕西师范大学化学与材料科学学院 陕西西安710062)
凝固点降低测定物质摩尔质量实验装置的改进
白云山*李世荣 安洁 罗五魁
(陕西师范大学化学与材料科学学院 陕西西安710062)
介绍一种改进的凝固点降低法测定物质摩尔质量的实验装置,通过调节合适的阻凝温度与散热补偿电流,对样品凝固点的测定精度可以达到±0.003℃,对样品摩尔质量的测定误差可控制在0.5%左右。
凝固点降低法是测定物质摩尔质量的经典方法之一,亦是物理化学实验的基本实验之一。
传统的凝固点测定装置如图1所示,该装置存在的问题主要有:(1)操作复杂,要求实验者同时进行恒温槽温度控制、样品及恒温槽搅拌、温度读取等操作,容易顾此失彼。(2)样品起晶困难,往往造成过冷程度过大,引入负偏差。(3)以手掌为热源对样品进行加热,样品升温程度难以控制,延长了实验时间。(4)系统不封闭,空气中的水蒸气往往会对测量产生干扰,在高温高湿天气很难取得满意结果。(5)在该装置中,当样品达到固液两相平衡时,系统散热仍在进行,体系所能到达的是动态平衡而非静态平衡,从而导致温度测量结果偏低。另外,由于搅拌速度慢,样品均匀程度低,使温度测量结果波动较大。
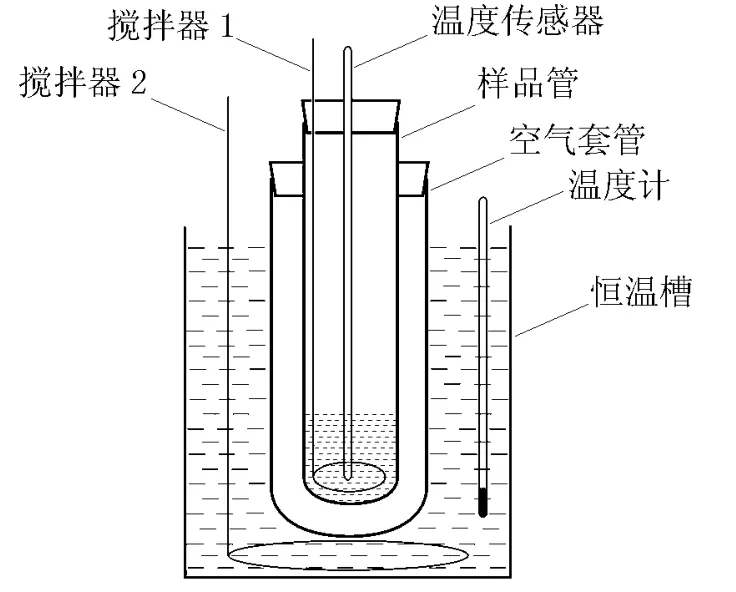
图1 传统凝固点测定装置示意图
近年来,对该实验的改进主要集中在以下几个方面:
(1)使用数字贝克曼温度计取代玻璃贝克曼温度计[1-2],简化了读数方式。(2)将恒温槽改为电制冷[3-4],取代手工加入冰块的制冷方式,大大提高了控温精度,特别是为取得低于0℃的水浴降低了成本,提供了方便,亦将该实验由环己烷(苯)-萘体系改为水-尿素(蔗糖)体系创造了条件。(3)将上下拉动的搅拌方式改为磁力搅拌[5],使测量体系实现了封闭,减小了环境中的水蒸气和样品的挥发对测定的干扰。事实上,磁力搅拌要达到与上下拉动搅拌相同的效果必须提高搅拌速率,而搅拌速率的提高使体系散热加快,导致测量结果偏低程度加剧。同时提高搅拌速率加重了样品首先在气液界面处结晶析出的问题,使测量终点难于观察。(4)改进样品的起晶方式[6-8],以减少体系过冷程度从而减小误差。但若采用加入晶种的方式,会导致溶液浓度发生较大的变化,降低平行测定结果之间的精度。
以上改进由于未从根本上改变体系所达到的固液平衡是动态平衡而非静态平衡的本质,所以很难从根本上解决该实验费时、费力且测不准的问题。基于此,我们设计了新型凝固点测量系统,在实际应用中取得了良好的效果。
1 实验装置的改进
改进的实验装置如图2所示,与传统的凝固点测定装置比较,其改进主要有:
(1)将由样品管和空气套管组成的两层玻璃仪器,改为由样品管、加热套管和空气套管组成的3层玻璃套管。加热套管是将加热用电阻丝缠绕在玻璃管上构成,从加热线圈上引出的3根导线使加热线圈分别构成上下两个独立的加热单元,分别称为加热线圈1和加热线圈2。加热线圈1有两个作用,一是对样品进行加热,可有效控制样品温度的上升幅度;二是当体系达到固液两相平衡时对样品的散热进行补偿(通过对线圈施加一定电流,即散热补偿电流实现),使系统达到固液平衡时更趋近于静态平衡,从而使测量结果更加准确。加热线圈2主要用于防止样品在容器壁及气液界面上结晶析出,通过温度传感器2与控温仪设置一定的温度(称为阻凝温度)配合使容器壁及样品上方空气的温度不低于设定值。
(2)实验前将数字贝克曼温度计电源打开预热4h,可得到稳定精确的测量结果,使平行测量结果之间偏差达到±0.003℃要求。
(3)直接使用冰水浴,并采用磁力搅拌,提高了实验的可操作性。
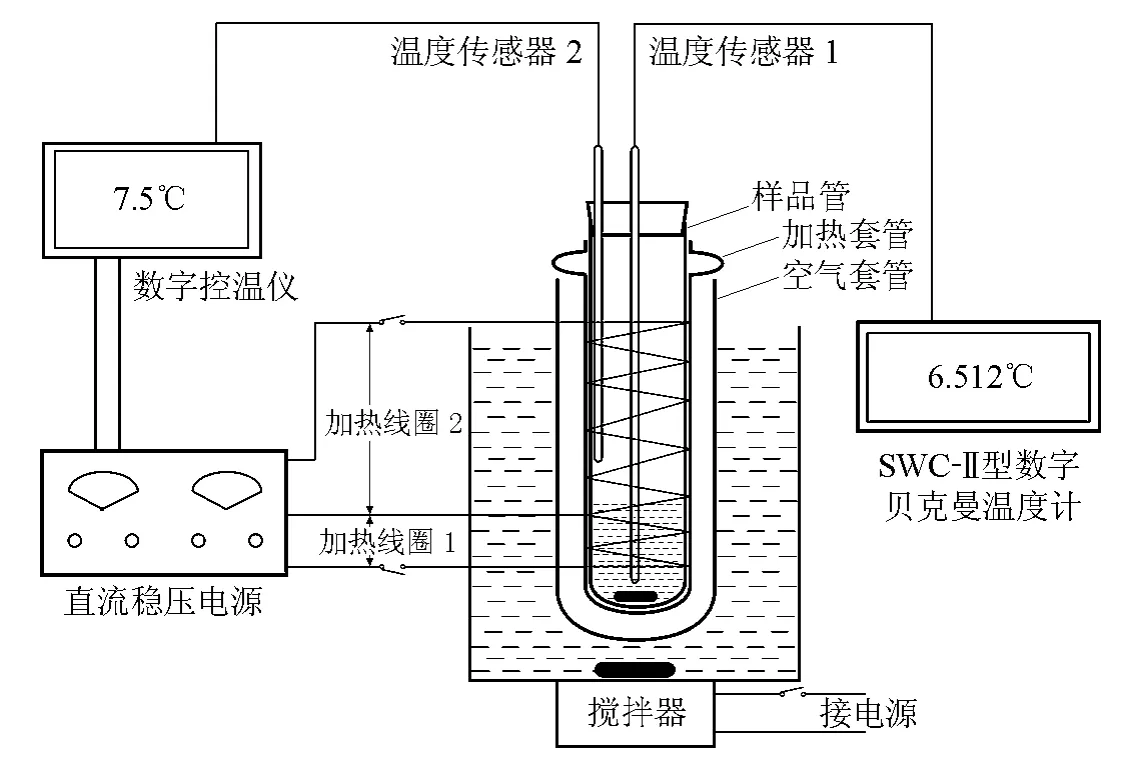
图2 改进后的实验装置图
2 实验部分
2.1 仪器与试剂
分析天平(北京赛多利斯仪器系统有限公司),改进的凝固点测量装置(自制);环己烷(分析纯,国药集团化学试剂有限公司,经蒸馏提纯,分子筛脱水),萘(分析纯,国药集团化学试剂有限公司)。
2.2 实验方法
首先在水浴中加冰获得冰水浴,然后用量筒量取30mL环己烷于干燥的样品管中,在分析天平上称重为23.3543g。调节样品套管的位置,使上下两个搅拌子处于同轴线上。打开控温仪开关,设定并控制阻凝温度为7.5℃,观察样品的降温过程,当样品中出现结晶,温度开始回升时,打开加热线圈1的电源开关,调节加热电压为1.5V,当样品温度回升至最高点时,记录该温度值作为溶剂的凝固点。记录完毕,调节加热线圈1的电压为5V,使样品温度回升0.5~1℃后,关闭加热线圈1的电源开关,使系统降温并按上述方法进行测量。平行测量3次后在样品管中加入经压片称量的0.1680g萘,用同样方法测定溶液的凝固点。
3 结果与讨论
萘摩尔质量的测定结果如表1所示。

表1 环己烷体系凝固点测定数据
用改进装置测定萘摩尔质量的实验操作比传统测定操作简单易行,具有反复测量重现性好的特点。同时,该装置对溶剂及溶液凝固点的测定进行了散热补偿,提高了实验测量精度,使凝固点的测量精度达到了±0.003℃。在实际操作中,通过选择合适的散热补偿电流,可将样品摩尔质量的测定误差稳定控制在0.5%左右。
[1] 陆兆仁,张铮扬,沈亚平.实验室研究与探索,2003,22(2):65
[2] Charles S,Judy S,Ronald J.JChem Educ,1982,59:682
[3] 袁红安,张逢星,赵小侠,等.化学分析计量,2006,15(3):49
[4] 陈缵光,张敏生.大学化学,1997,12(4):38
[5] 钱保华.大学化学,2006,21(1):47
[6] 北京大学化学系物理化学教研室.物理化学实验.第3版.北京:北京大学出版社,1995
[7] 荣华,佟拉嘎,徐中波.大学化学,2007,22(5):40
[8] 魏亚杰,姚广伟,李向东,等.大学化学,2001,16(6):40

