沸石分子筛吸附和扩散:研究现状、存在问题和展望
朱伟东, 钟依均, 张富民,肖 强, 许春慧, 郝仕油, 代 伟
(浙江师范大学 物理化学研究所,先进催化材料省部共建教育部重点实验室,浙江 金华 321004)
1 研究背景
沸石分子筛是一类具有骨架结构的微孔晶体材料,由于其特有的规则孔道结构(择形选择性,shape-selectivity)、强酸性和高水热稳定性,在催化、分离等化学工业和石油化工领域具有广泛的应用.因为天然沸石分子筛不能满足工业生产的大规模需求,沸石分子筛的人工合成一直以来都受到广泛的关注,科学家不断地合成出具有新型结构、优异催化或吸附性能的沸石分子筛[1].另外,沸石分子筛催化的研究范围也不断地被扩大,在烃类转化、选择氧化、环境催化等多方面都有涉及[2-3].近年来,随着科学仪器的发展改进,人们对沸石分子筛的吸附和扩散研究不断地深入.同时,随着计算机技术的进步,相关分子模拟(molecular simulation)技术及理论方面的研究也得到了长足发展[4-5].
吸附和扩散(adsorption and diffusion)现象不仅在科学上引起人们的高度关注,而且在工业中具有广泛的应用[6].根据吸附质分子尺寸和形状的不同,沸石分子筛(膜)能够选择性地吸附特定分子,与传统的精馏分离工艺相比,采用沸石分子筛(膜)进行分离的能耗明显降低.沸石分子筛的吸附扩散性能对于吸附分离至关重要,吸附质在孔道里的扩散速度往往是吸附分离的控制步骤.因此,对基于吸附的分离或纯化过程来说,精确的吸附平衡数据和扩散系数的获取对优化过程设计非常重要.
沸石分子筛的多相催化反应在现代大型石油化工和各种精细化工生产中起着举足轻重的作用.沸石分子筛的催化性能往往与分散在沸石分子筛晶体孔道内部的催化活性中心密切相关.沸石分子筛催化反应的宏观过程包括:1)反应物从流体主体扩散到沸石分子筛晶体的外表面(外扩散);2)反应物从沸石分子筛晶体外表面向孔道内部扩散(内扩散);3)在沸石分子筛晶体内部孔道的内表面上进行催化反应(化学反应);4)产物从沸石分子筛晶体内孔道扩散到外表面(内扩散);5)产物从沸石分子筛晶体外表面扩散到流体主体(外扩散).从优化过程设计、工业控制及开发或改良沸石分子筛催化剂等方面考虑,本征催化动力学的获取显得非常重要.沸石分子筛的择形选择性是用以描述只有大小、形状与沸石分子筛孔道相匹配的分子才能进入沸石分子筛孔道并被吸附或催化的现象.由于分子大小要与沸石分子筛孔道尺寸相当,从而使得分子在沸石分子筛孔道里的扩散速度较慢,限制了分子在沸石分子筛中的传质速率(即扩散限制),由此严重影响了沸石分子筛催化剂的活性、选择性等性能[7].因此,探讨吸附物种在纳米尺寸范围的扩散效应对沸石分子筛催化反应动力学的影响具有重要的学术价值.同时,这些研究将为沸石分子筛催化剂的设计、制备及使用条件提供重要的指导作用,可加深对催化过程中发生的复杂反应动力学行为的认识.
2 研究现状
2.1 吸附
表征单组分体系在沸石分子筛晶体中吸附的常规实验技术是体积法和重量法,在过去的数十年里,在系统灵敏度、操作范围和自动化程度等方面,这两种常规实验技术都得到了极大的提高[8].目前,应用这两种常规实验技术,可以精确地测定单组分物种在沸石分子筛晶体中的平衡吸附量.此外,随着计算机科学的不断发展,应用蒙特卡罗(Monte Carlo)法可以模拟和预测单组分物种在沸石分子筛晶体中的平衡吸附量,并能与实验测定值很好地吻合.最近,Smit和Maesen[5]在国际权威刊物《化学评论(Chemical Reviews)》上对分子模拟技术在研究沸石分子筛吸附、扩散及择形选择性等方面的应用作了全面回顾及评述.鉴于已报道的大量实验结果与分子模拟预测结果相一致,他们指出目前分子模拟技术可以代替“实验”用于精确地“测定”单组分物种在沸石分子筛晶体中的平衡吸附量.图1[9]比较了异丁烷(isobutane)在纯硅(疏水性)沸石分子筛silicalite-1上的实验等温线和分子模拟结果,可以看到两者具有一致性.文献[10]通过实验观察到直链和支链烷烃在silicalite-1上的吸附性质之间的差异,提出了“不同分子定位”的概念,并通过分子模拟对此予以证明[11].根据具有2个不同空间的体积填充过程,分子模拟对吸附给出了令人满意的解释,并且与实验结果一致.基于这样的事实,文献[12-13]进一步提出了一个用于描述烷烃类分子在沸石分子筛silicalite-1上等温吸附的双位朗缪尔(dual-site Langmuir,DSL)模型:
(1)
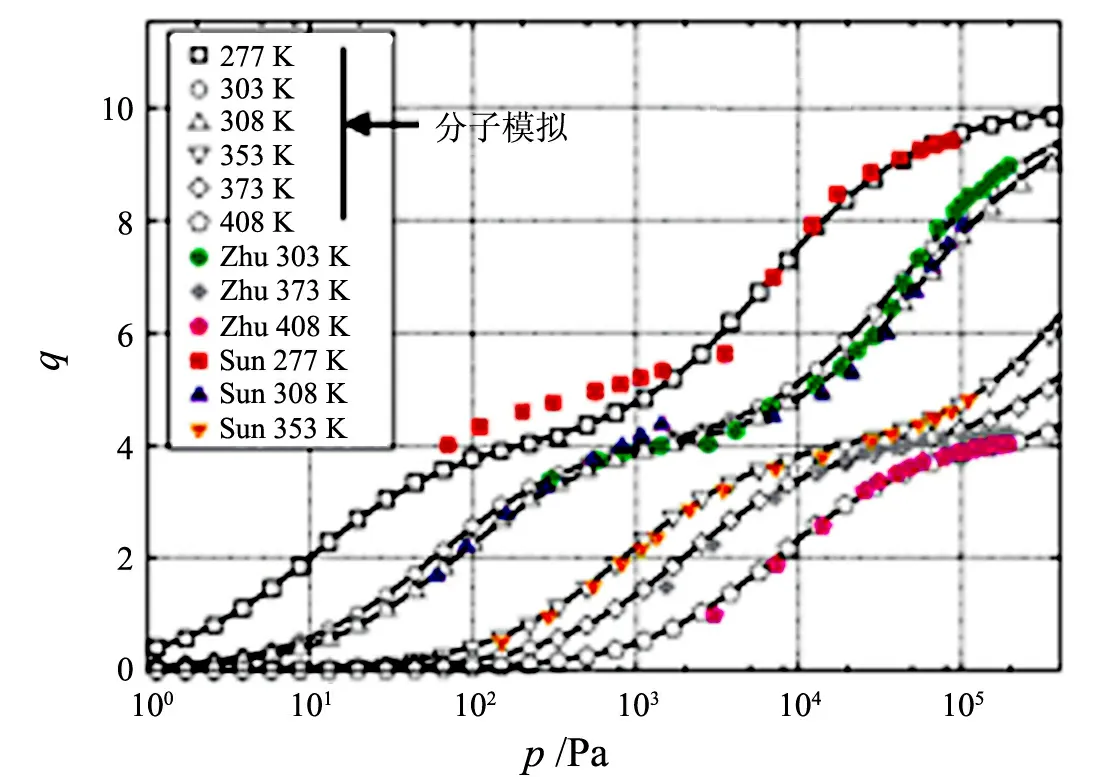
吸附量q的单位为单位晶胞分子数
如图2所示,DSL模型很好地描述了正丁烷和异丁烷在silicalite-1上的吸附行为.总之,无论是实验手段还是分子模拟技术,都能很好地测定和预测单组分物种在沸石分子筛晶体中的平衡吸附量[12-14].
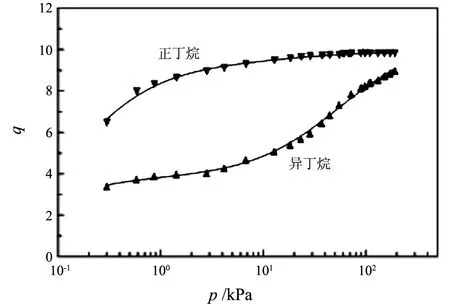
吸附量q的单位为单位晶胞分子数
沸石分子筛在催化反应和吸附分离的实际应用中,多组分体系的吸附行为常基于实验所测得的纯组分吸附等温线,通过选择合适的理论模型(如理想吸附溶液理论,ideal adsorbed solution theory,IAST[15])来预测混合体系的吸附行为[14].但这种预测有时会产生很大的偏差,甚至与实验结果呈相反的趋势.因此,应用合适的实验手段测量多组分体系在沸石分子筛中的平衡吸附量具有重要的理论研究意义和应用价值.然而,迄今为止,关于多组分体系在沸石分子筛中的平衡吸附量实验值的报道很少.这是由于没有一种实验手段可以直接确定吸附相物种的浓度,只能通过间接的实验方法测定多组分体系的平衡吸附量,导致数据处理繁复、极其耗时,且有时受分析手段的限制而无法实施[8].
然而,随着分子模拟技术和理论的不断发展,模拟和预测多组分体系在沸石分子筛晶体中的吸附成为可能,大量模拟结果已见报于近期《化学评论》[5].模拟结果显示,多组分体系在沸石分子筛中的吸附行为符合理想吸附溶液理论.如图3所示,正丁烷-异丁烷混合体系在沸石分子筛silicalite-1上的分子模拟吸附等温线与IAST预测完全吻合;对正丁烷的吸附分离因子随着气相总压力的增加而增大.与之相比,笔者利用穿透柱(breakthrough column)技术,结合Interscience Compact GC快速检测流出相中正丁烷和异丁烷的浓度,获得了该双组分体系在silicalite-1上的吸附等温线和分离因子,实验所测对正丁烷的选择性随着气相总压力的增加而减小.由于丁烷异构体的分子形状及大小不同,导致它们在silicalite-1晶体内的吸附定位不同:含支链的异丁烷分子倾向于吸附在直型孔道(straight channels)与Z字型孔道(zig-zag channels)相接的交叉孔道(intersections)里;而直链烷烃正丁烷倾向于吸附在直型和Z字型孔道里[12].由此,silicalite-1对丁烷异构体呈现吸附异性,然而经典的IAST无法描述该双组分体系在silicalite-1上的吸附行为.
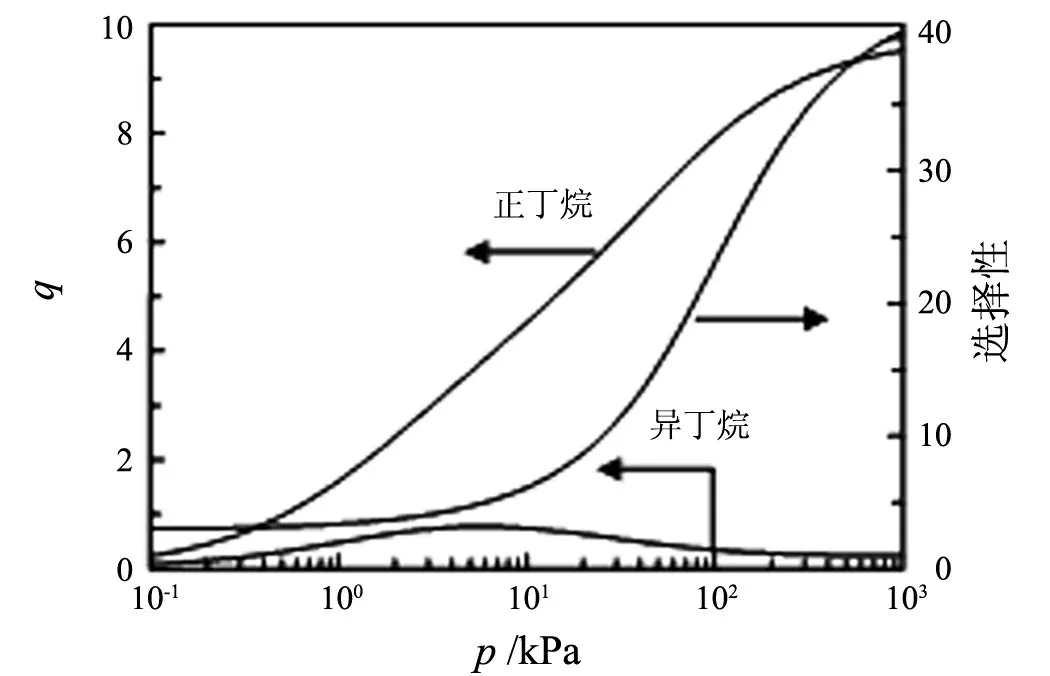
吸附量q的单位为单位晶胞分子数
2.2 扩散
研究分子在沸石分子筛中的扩散机理一直被视为一项富有挑战性的工作.迄今,已有多种实验技术应用于测定探针分子在沸石分子筛微孔道内的扩散系数,各种测定沸石分子筛内扩散系数(intracrystalline diffusivity)的实验技术、实验原理及它们的优缺点见表1.
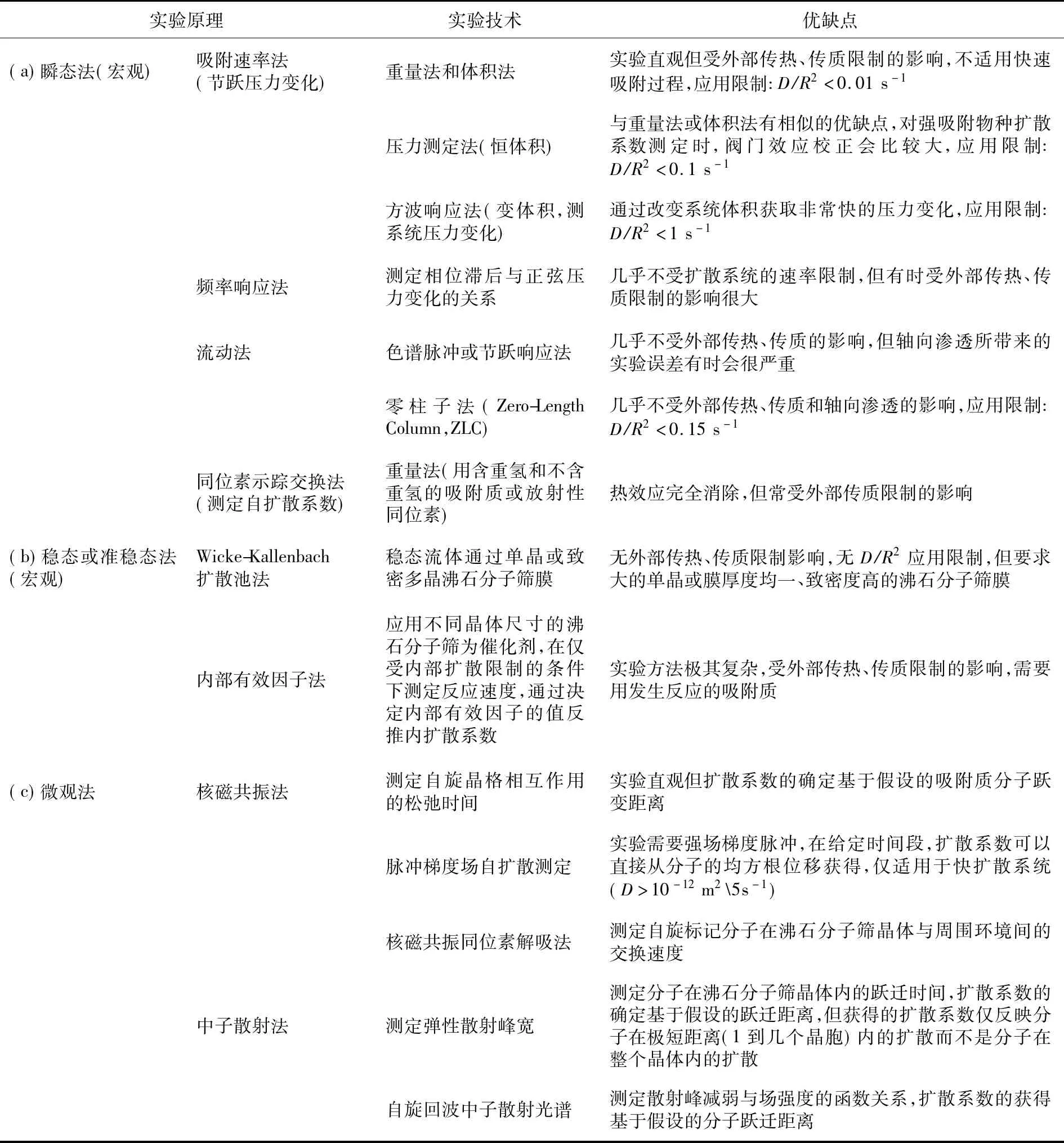
表1 测定沸石分子筛内扩散系数的实验方法
宏观方法确定沸石分子筛晶体内扩散系数都是建立在测定探针分子从晶体外表面进入并通过晶体的流量的基础上,在明确的边界条件下,运用Fick第一定律推算内扩散系数,所测得的扩散系数叫传递扩散系数(transport diffusivity,Dt),或Fick扩散系数.
J=-Dt▽c.
(2)
式(2)中:J是流体流量;c指扩散物种的浓度.在宏观方法中,实验上给予系统一个浓度梯度,但从热力学的角度看,扩散的驱动力(driving force)是化学势梯度(chemical potential gradient).由此,式(2)可写成
▽μ=-DMS▽μ.
(3)
式(3)中:L是单组分Onsager输移系数;μ是化学势;DMS称校正(corrected)扩散系数或称Maxwell-Stefan扩散系数.为了建立Maxwell-Stefan扩散系数DMS与传递扩散系数Dt间的关系,定义热力学校正因子Γ为
(4)
由此,
▽μ=Γ▽c.
(5)
即通过热力学校正因子Γ,可以建立Dt与DMS间的关系
Dt=ΓDMS.
(6)
当吸附质在沸石分子筛中的浓度很低时,Γ值接近1,这时传递扩散系数等于Maxwell-Stefan扩散系数,否则,热力学校正因子需根据所测得的吸附平衡方程而获得
(7)
式(7)中:p是平衡压力;q是吸附量.对于Langmuir吸附方程
(8)
式(8)中,θ是吸附占有率(occupancy).显然传递扩散系数Dt随着吸附量的增加而增大.
由微观方法所测得的扩散系数称为自扩散系数(self-diffusivity,Ds),通过确定分子完成一次跃迁所需平均位移时间而计算得到.迄今,所有微观方法存在一个普遍缺点,即自扩散系数的确立是建立在假设的跃迁距离基础上.理论上,吸附相浓度较低时,自扩散系数等于Maxwell-Stefan扩散系数或校正传递扩散系数,即
Ds(0)=DMS.
(9)
此外,自扩散系数随着吸附相浓度的增加而减小,这与传递扩散系数与吸附相浓度间的关系呈相反的趋势:
Ds=Ds(0)(1-θ).
(10)
分别应用宏观方法和微观方法对同一体系进行实验测定,所测得的扩散系数会有很大的差异,不仅所测得扩散系数与吸附相浓度的变化呈相反趋势,而且由2种方法分别获得的低吸附相浓度时的扩散系数有数量级上的差异[16].图4是用不同方法测得的低吸附相浓度时丙烷在silicalite-1上的扩散系数.显而易见,常用的宏观技术,例如:ZLC,Wicke-Kallenbach和频率响应(frequency response)法,获得基本一致的实验值;而相比较,用脉冲梯度场核磁共振(pulsed field gradient NMR,PFG-NMR)法所测扩散系数要高2个数量级.这种差异迄今还没有一个完整的理论解释[16].
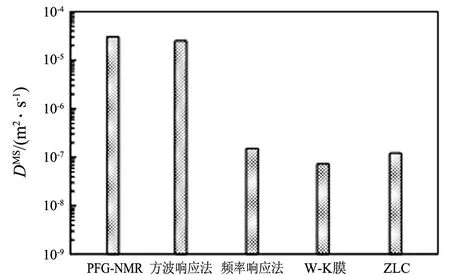
图4 微观和宏观实验技术在334 K和低吸附相浓度时测得丙烷在silicalite-1中的自扩散系数及校正传递扩散系数的比较[16]
近年来,分子模拟技术在预测沸石分子筛扩散系数方面得到了广泛应用,模拟所得扩散系数及它们与吸附相浓度间的关系与微观实验法所测结果基本一致[4-5].微观实验法和分子模拟技术在“分子水平”上研究探针分子在沸石分子筛微孔道内的扩散机理,极大地丰富了该领域的理论,但它们的“实验条件”与工业应用条件差异很大.相对而言,宏观法(例如:ZLC和Wicke-Kallenbach技术)的实验条件与沸石分子筛在工业应用时的条件更接近.事实上,到目前为止,在分离及催化过程设计中,所用沸石分子筛扩散系数大都来自宏观法测定.
多组分体系在沸石分子筛中的扩散,由于其复杂性,一直被视为化工传质领域的一大难题.迄今,国际上应用较为广泛的理论模型是由荷兰Amsterdam大学Krishna教授提出的广义Maxwell-Stefan方程(generalized Maxwell-Stefan,GMS)[17-18].在单组分扩散情况下,化学势差是驱动力;但对于混合物来说,还包括分子间作用力(“摩擦”或“交换”)
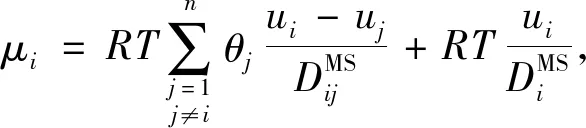
i=1,2,…,n.
(11)
如同单组分体系的情况下,化学势差可以用所有组分的吸附量表示为
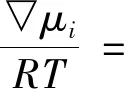
(12)
式(12)中,热力学校正因子为
i,j=1,2,…,n.
(13)
值得注意的是,由于不同分子的大小和几何形状的差异,使得其在沸石分子筛上具有不同的饱和吸附量,因此,式(13)包含组分i和j的饱和吸附量.考虑这种特性,GMS公式以流量和吸附量表示[19-20],即
▽
i=1,2,…,n.
(14)
以矢量-矩阵符号表示,式(14)转化为
(J)=-ρ[B′]-1[Γ](▽θ)=
-ρ[qsat][B]-1[Γ](▽θ).
(15)
矩阵元素:
(16)
[qsat]是饱和吸附量的一个对角矩阵.对双组分体系,流量的明确表达式为:
(17)
(18)
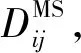
(19)
Maxwell-Stefan方程结合理想吸附溶液理论已应用于多组分体系在沸石分子筛中的传质研究,大部分研究工作基于分子模拟[4-5],而建立在实验工作基础上的研究论文报道甚少[20-22].最近,Krishna等[18]通过分子模拟指出:对于孔道型(channel type)沸石分子筛(例如MFI)应用GMS方程结合IAST时,必须考虑扩散物种间的相互作用,即Maxwell-Stefan交换扩散系数(exchange diffusivity);相反,对于笼子型(cavity type)沸石分子筛(例如DDR),扩散物种间的相互作用可以忽略.但这一分子模拟结果还未得到实验证实.
3 存在的科学问题
鉴于以上讨论,在沸石分子筛吸附和扩散研究领域,存在如下重要科学问题:
1)分子模拟结果显示,silicalite-1对烷烃异构体呈现吸附异性,但经典的理想溶液吸附理论仍能很好地描述该双组分吸附行为.用实验方法验证这一分子模拟结果势在必行.
2)微观实验方法或分子模拟技术测得或预测的自扩散系数随着吸附相浓度的增加而减少,这与经典扩散理论和宏观实验方法所观察到的结果呈相反趋势.而目前,宏观实验方法研究探针分子在沸石分子筛中的扩散的大部分工作局限于测定低吸附量时(线性处)的扩散系数,但在实际工业应用中,分子在沸石分子筛中的吸附量在非线性处.因此,实验研究探针分子在较高吸附相浓度时的扩散机理具有十分重要的科学意义和工业应用价值.
3)Smit和Maesen[5]指出,用微观实验方法或分子模拟技术测定或预测分子在多维孔道沸石分子筛(如silicalite-1)中的一个特定微孔道里的扩散系数,而用宏观方法则测定探针分子在整个晶体内的传递扩散系数,由此导致它们间的差异.那么能否利用宏观实验方法测定探针分子在一个特定的微孔道内的扩散系数?
4)应用Maxwell-Stefan方程研究多组分体系在沸石分子筛中的传质,需要结合由混合物吸附方程而得到的热力学校正因子Γij.如果实验证明理想吸附溶液理论不能描述混合物的吸附行为(例如丁烷异构体在silicalite-1上的吸附),则必须建立新的混合物吸附方程,方能更确切地阐述多组分体系在沸石分子筛中的扩散机理.
4 展 望
基于国内外在沸石分子筛吸附和扩散研究领域所共存的重要科学问题,本研究小组以烷烃异构体在silicalite-1及二氧化碳和甲烷在DDR型沸
石分子筛中的吸附和扩散为体系,将展开全面而深入的研究.选择silicalite-1和DDR沸石分子筛为研究体系,其理由是:1)无论是实验研究还是分子模拟,在沸石分子筛吸附和扩散研究领域,silicalite-1是迄今研究最多的一种沸石分子筛[5],但如前述,仍有大量的科学问题有待解决;2)基础研究已显示,silicalite-1在烷烃、二甲苯异构体的分离上有广阔的应用前景[20,23],而纯硅DDR型沸石分子筛能有效地分离CO2,在天然气净化领域有潜在的应用价值[22];3)同属MFI型的ZSM-5沸石分子筛在石油化工领域里是应用最广泛的催化剂之一[2-3];4)Silicalite-1属孔道型而DDR属笼子型沸石分子筛,它们代表了沸石分子筛的2种典型的结构类型.
本研究小组将合成高纯度silicalite-1和DDR型沸石分子筛晶体,且晶体形貌一致、大小均匀,研究丁烷和己烷异构体在silicalite-1晶体中的混合吸附及CO2和甲烷在DDR晶体中的混合吸附;合成晶轴有序的silicalite-1膜及膜厚度均一、致密度高的DDR膜;应用ZLC和Wicke-Kallenbach(膜)技术测定单组分体系的扩散系数,重点考察吸附相浓度与扩散系数间的关系;测定两组分混合体系通过silicalite-1和DDR沸石分子筛膜的流量,建立温度、压力与流量间的关系.
在此基础上,提出新的混合物吸附理论模型,用于描述烷烃异构体混合物(例如:正丁烷与异丁烷,正己烷与3-甲基戊烷)在silicalite-1(由于烷烃异构体的分子形状、大小不同,导致它们在silicalite-1孔道内的吸附定位不同)和CO2与甲烷混合物在DDR(吸附质分子间强相互作用)中的非理想吸附行为;基于实验所测单组分体系扩散系数,建立沸石分子筛传递扩散系数与吸附相浓度间的方程;从实验角度验证Maxwell-Stefan方程应用于研究多组分体系在沸石分子筛中的扩散机理的可靠性,在此基础上修正或发展新的模型;阐明利用微观和宏观实验方法对同一体系所测扩散系数差异的内在原因.
参考文献:
[1]徐如人,庞文琴.分子筛与多孔材料化学[M].北京:科学出版社,2004.
[2]Corma A.From microporous to mesoporous molecular sieve materials and their use in catalysis[J].Chem Rev,1997,97(6):2373-2419.
[3]Corma A,Carcia H.Lewis acids:From conventional homogeneous to green homogeneous and heterogeneous catalysis[J].Chem Rev,2003,103(11):4307-4365.
[4]Keil F J,Krishna R,Coppens M O.Modeling of diffusion in zeolites[J].Rev Chem Eng,2000,16(2):71-197.
[5]Smit B,Maesen T L M.Molecular simulations of zeolites:Adsorption,diffusion,and shape selectivity[J].Chem Rev,2008,108(10):4125-4184.
[6]Do D D.Adsorption analysis:equilibrium and kinetics[M].London:Imperial College Press,1998.
[7]Corma A,Fornes V,Pergher S B,et al.Delaminated zeolite precursors as selective acidic catalysts[J].Nature,1998,396:353-356.
[8]Talu O.Needs,status,techniques and problems with binary gas adsorption experiments[J].Adv Colloid Interface Sci,1998,77:227-269.
[9]Dubbeldam D,Calero S,Vlugt T J H,et al.Force field parametrization through fitting on inflection points in isotherms[J].Phys Rev Lett,2004,93(8):0883021-0883024.
[10]Zhu W,van de Graaf J M,van den Broeke L J P,et al.TEOM:A unique technique for measuring adsorption properties.Light alkanes in silicalite-1[J].Ind Eng Chem Res,1998,37(5):1934-1942.
[11]Vlugt T J H,Zhu W,Kapteijn F,et al.Adsorption of linear and branched alkanes in the zeolite silicalite-1[J].J Am Chem Soc,1998,120(22):5599-5600.
[12]Zhu W,Kapteijn F,Moulijn J A.Adsorption of light alkanes on silicalite-1:Reconciliation of experimental data and molecular simulations[J].Phys Chem Chem Phys,2000,2(9):1989-1995.
[13]Zhu W,Kapteijn F,van der Linden B,et al.Equilibrium adsorption of linear and branched C6alkanes in silicalite-1 studied by the tapered element oscillating microbalance[J].Phys Chem Chem Phys,2001,3(9):1755-1761.
[14]Vlugt T J H,Krishna R,Smit B.Molecular simulations of adsorption isotherms for linear and branched alkanes and their mixtures in silicalite[J].J Phys Chem B,1999,103(7):1102-1118.
[15]Myers A L,Prausnitz J M.Thermodynamics of mixed-gas adsorption[J].AIChE J,1965,11(1):121-127.
[16]Karger J,Ruthven D M.On the comparison between macroscopic and n.m.r. measurements of intracrystalline diffusion in zeolites[J].Zeolites,1989,9(4):267-281.
[17]Krishna R.A unified approach to the modelling of intraparticle diffusion in adsorption processes[J].Gas Sep Purif,1993,7(2):91-104.
[18]Krishna R,van Baten J M.Onsager coefficients for binary mixture diffusion in nanopores[J].Chem Eng Sci,2008,63(12):3120-3140.
[19]Kapteijn F,Moulijn J A,Krishna R.The generalized Maxwell-Stefan equations for zeolites:sorbate molecules with different saturation loadings[J].Chem Eng Sci,2000,55(15):2923-2930.
[20]Kapteijn F,Zhu W,Moulijn J A,et al.Zeolite membranes-modelling and application[M]//Cybulski A,Moulijn J A.Structured Catalysts and Reactors.2nd ed.Boca Raton:Taylor & Francis Group,2006:701-747.
[21]Zhu Weidong,Hrabanek P,Gora L,et al.Role of adsorption in the permeation of CH4and CO2through a silicalite-1 membrane[J].Ind Eng Chem Res,2006,45(2):767-776.
[22]Van den Bergh J,Zhu W,Gascon J,et al.Separation and permeation characteristics of a DD3R zeolite membrane[J].J Membr Sci,2008,316(1/2):35-45.
[23]Lai Zhiping,Bonilla G,Diaz I,et al.Microstructural optimization of a zeolite membrane for organic vapor separation[J].Science,2003,300(5618):456-460.

