HPLC-ELSD法测定不同厂家银杏叶提取物分散片剂中萜类内酯溶出度
周自桂, 苏 晋, 金 春, 徐 成, 秦 勇
(江苏弘惠医药有限公司研发部,江苏南京210008)
银杏叶分散片[1]是由银杏叶提取物制成的片剂,其活性成分为总黄酮醇苷和二萜内酯;银杏酮酯[2-4]为第五代银杏叶提取物,其活性成分也是总黄酮醇苷和萜类内酯,银杏酮酯分散片是以银杏酮酯为原料制成的片剂。这两类片剂均具有活血化瘀,通络舒脉的功效,临床用于治疗血瘀型胸痹及血瘀型轻度脑动脉硬化引起的眩晕、冠心病、心绞痛。但在临床疗效上,患者均反映银杏酮酯分散片疗效明显好于银杏叶分散片,且疗效稳定,而银杏叶分散片不同厂家之间疗效差异也很大。由于药物的溶出度直接影响药物在体内的吸收和利用,而国内现行的质量标准均以分散时限作为分散片的控制指标,但这并不能反映产品的内在质量,片剂虽然分散了,但其有效成分并不能马上溶出,对于那些水溶性差的成分更是难以溶出。有文献报道[5]通过测定片剂中的总黄酮醇苷的溶出度来评价与控制药品质量,这确实在质量控制上有了很大的提高。由于银杏叶提取物的另一类有效成分萜类内酯水溶性更低于黄酮醇苷,故本试验采用HPLCELSD法[6]测定不同厂家分散片中萜类内酯的溶出度,以期为评价与控制药品质量提供更充分的依据,保证药品疗效。
1 仪器、药品、试剂
仪器:ZRS-8智能溶出仪(天津天大天发科技有限公司)、Waters 515泵高效液相,Varian380-LC蒸发光散射检测器;对照品:白果内酯(批号110865-200404)、银杏内酯A(批号110862-200608)、银杏内酯B(批号110863-200508)、银杏内酯C(批号110864-200505),均购自中国药品生物制品检定所;试剂:乙腈(色谱纯)、水(超纯水)、其它试剂均为分析纯。供试药品:银杏酮酯分散片为江苏A厂产品,其余厂家的产品均为银杏叶分散片,具体规格见表1。
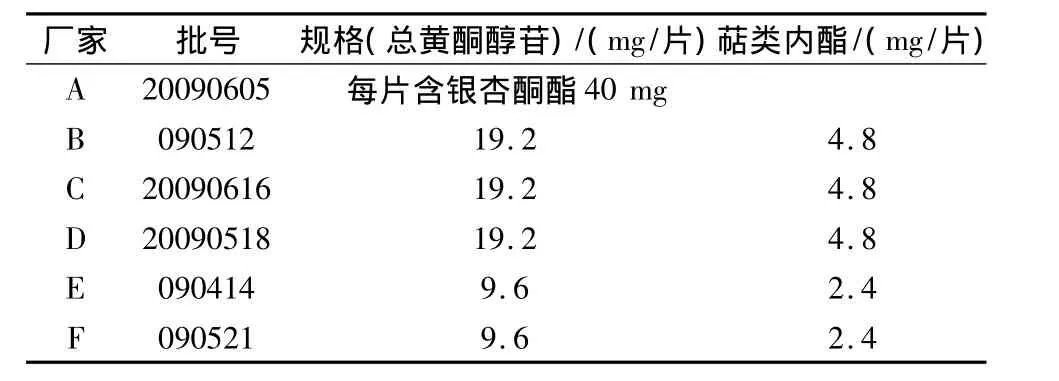
表1 各厂家分散片规格
2 方法与结果
2.1 色谱条件
Alltech C18色谱柱(4.6 mm × 150 mm,5 μm),流动相:水-乙腈-四氢呋喃(80 ∶8 ∶12);流速:1.0 mL/min;漂移管温度:105℃,氮气流速:2.70 mL/min。理论板数按银杏内酯A峰、银杏内酯B峰、银杏内酯C峰和白果内酯峰计算均不低于3 000。
2.2 对照品制备方法
取银杏内酯A、B、C和白果内酯对照品适量,加甲醇制成每1 mL含银杏内酯A 30 μg、银杏内酯B 15 μg、银杏内酯C 15 μg、白果内酯 50 μg 的混合溶液,即得。
2.3 供试品及自身对照溶液处理方法
2.3.1 供试品溶液
取溶出液7 mL,滤过,精密吸取5 mL,用醋酸甲酯振摇提取2次,每次10 mL,合并醋酸甲酯液,蒸干,残渣加甲醇1 mL使溶解置2 mL量瓶中,以流动相稀释至刻度,摇匀,滤过,即得。
2.3.2 自身对照溶液
取10片,研细,精密称取相当于1片的重量,置100 mL量瓶中,加0.1 mol/L的盐酸溶液至刻度,超声提取30 min,取溶液7 mL,滤过,照2.3.1项下供试品处理方法同法制备,即得。
2.4 阴性干扰试验
按处方比例称取空白辅料,置100 mL量瓶中,加0.1 mol/L的盐酸溶液至刻度,超声提取30 min,取溶液7 mL,滤过,照2.3.1项下供试品处理方法同法制成阴性样品溶液。取对照品溶液20 μL、供试品溶液、阴性样品溶液各10 μL,按上述色谱条件进样测定,记录色谱图(见图1),结果表明阴性样品对萜类内酯的测定无干扰。

图1 HPLC色谱图
2.5 标准曲线制备
精密吸取对照品溶液 2、5、10、15、20 μL 注入液相色谱仪,以对照品进样量的自然对数为横坐标,以峰面积的自然对数为纵坐标,绘制标准曲线,结果表明白果内酯在102.8~1028 ng、银杏内酯A在65.4~654 ng、银杏内酯B在32.8~328 ng、银杏内酯C在34.4~344 ng范围内线性关系良好,回归方程分别为:白果内酯:Y=1.062 3X+6.534 5,r=0.999 9、银杏内酯 A:Y=1.017 5X+6.456 1,r=0.999 8、银杏内酯B:Y=1.056 2X+6.054 8,r=0.999 6、银杏内酯C:Y=1.033 1X+6.882 3,r=0.999 8。
2.6 精密度试验
精密吸取对照品溶液20 μL注入液相色谱仪,连续进样5次,银杏内酯A、B、C和白果内酯峰面积的 RSD分别为0.9%、1.3%、1.1%、0.7%,表明本法精密度良好。
2.7 溶液稳定性试验
取上述供试品溶液(A 厂)室温放置,分别于 0、2、4、6、8 h精密吸取10 μL注入液相色谱仪,记录色谱图,峰面积的RSD为1.2%,表明本供试品溶液室温8 h内基本稳定。
2.8 加样回收率试验
精密称取已知含量的样品(A厂,批号090407,含银杏萜类内酯为5.761 mg/片,其中白果内酯2.578 mg/片、银杏内酯A 1.546 mg/片、银杏内酯B 0.987 mg/片、银杏内酯C 0.65 mg/片)约75 mg,共5份,分别精密加入混合对照品溶液(每1 mL 含白果内酯 514 μg、银杏内酯 A 327μg、银杏内酯 B 164μg、银杏内酯 C 172 μg)2 mL,置100 mL 量瓶中,加0.1 mol/L的盐酸溶液至刻度,超声提取30 min,照2.3项供试品处理方法同法制备,进样10 μL,用上述色谱条件测定,计算回收率,结果白果内酯、银杏内酯A、B、C的平均回收率分别为100.2%、98.3%、99.3%、98.5%,RSD分别为2.0%、2.1% 、2.6% 、2.4% 。
2.9 溶出度的测定
取6片,照溶出度测定法(中国药典2005年版二部附录ⅩC第三法),以0.1 mol/L的盐酸溶液100 mL为溶剂,(37 ±0.5)℃,转速为 100 r/min,分别于 3、10、20、30、45、60 min取溶液7 mL(同时补充等温介质7 mL)滤过,照2.3.1项同法制成供试品溶液并按上述色谱条件测定(注:溶出度低于50%时进20 μL,其它进10 μL),将峰面积取自然对数后代入标准曲线求出供试品浓度的自然对数,再转换成供试品的量。同时取同一厂家的样品10片,照2.3.2项制成自身对照溶液,同法测定,并以此做为百分之百的溶出量。再将供试品各时间点的溶出量与相应的百分之百溶出量比较,得出累积溶出百分率,绘制累积溶出曲线(图2),结果见表2。

表2 各厂家样品的累积溶出量(mg)与溶出率(%)
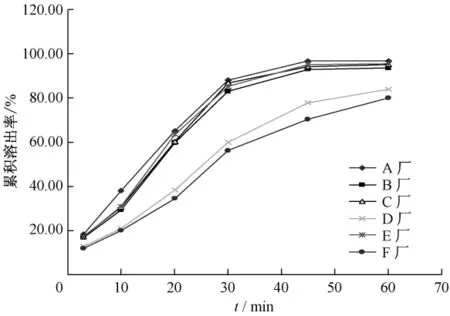
图2 各厂家样品的累积溶出曲线
2.10 溶出参数的计算[7]
将各厂家在各时间的累积溶出度输入计算机,按Weibull分布模型图 Excel 2003 计算溶出参数[6]T50、Td、m并做方差分析,结果见表3、表4。

表3 各厂家溶出度参数
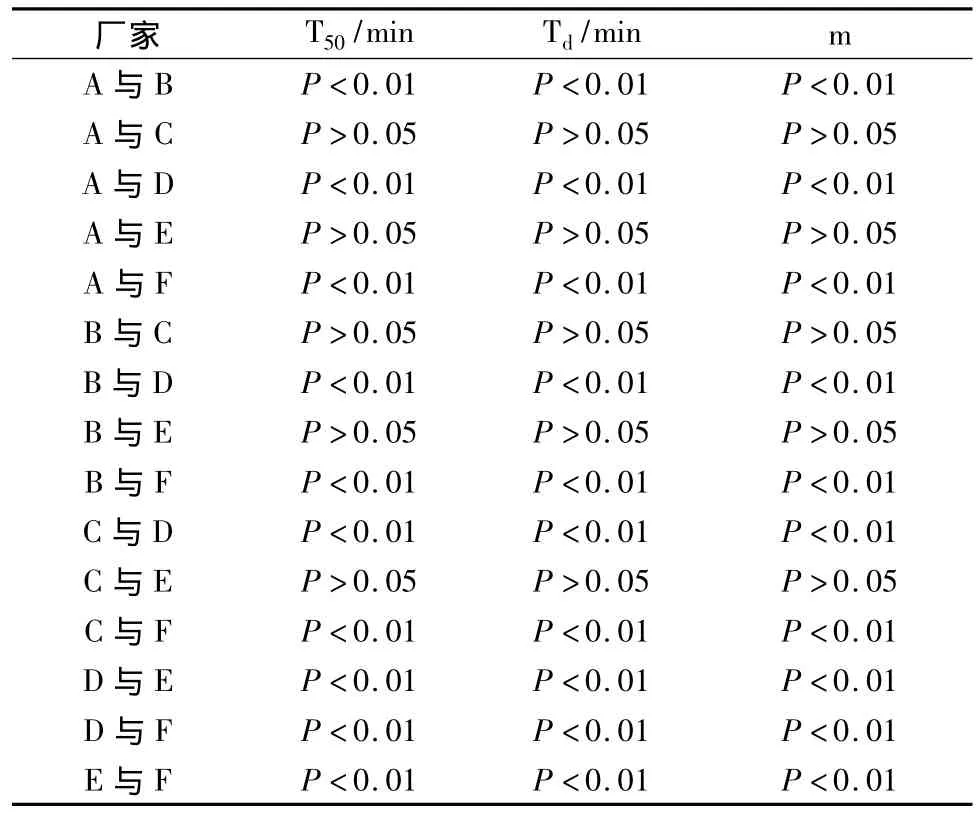
表4 厂家间的F检验
结果表明:A厂与B、D、F厂有显著性差异,B厂与D、F厂,C厂与D、F厂,D厂与E、F厂,E厂与F厂之间的溶出度均有显著性差异;而A厂与C、E厂,B、C、E 3厂之间的溶出度无显著性差异。
3 讨论
3.1 溶出方法的选择 由于分散片质量标准规定必须在3 min内崩解,不必担心片会漂浮而影响溶出,故直接选择浆法,比较了转速为50、75、100 r/min的溶出度,结果50、75 r/min均低于100 r/min,加快搅拌速度则加快扩散,有助于溶出,但过快的搅拌速度与人体内的蠕动不相符,故选择100 r/min。
3.2 溶出介质及体积的选择 分别以蒸馏水、0.1 mol/L盐酸、1.5% 十二烷基硫酸钠为溶出介质,测定同一厂家(A厂)的药品在45 min内的溶出度,结果溶出度蒸馏水(77.8%)低于0.1 mol/L盐酸(96.7%)与1.5%十二烷基硫酸钠(97.4%),而0.1 mol/L盐酸与1.5% 十二烷基硫酸钠无明显区别,故选择0.1 mol/L盐酸为溶出介质。由于本品内酯规格较小(4.8 mg/片与2.4mg/片),故选择介质体积为100 mL。
3.3 结果表明,各厂家样品的溶出行为有显著性差异,总体看来A厂的溶出要优于其它厂家,且内酯的含量也明显高于其它厂家,说明银杏酮酯做为第五代银杏叶提取物,其纯度确实高于普通的银杏叶提物,这也可能是患者反映的银杏酮酯类制剂疗效优于银杏叶提取物类制剂的因素之一吧。对相同规格的不同厂家,其T50大规格(4.8mg/片)样品D厂家约为其它厂的2倍,小规格(2.4 mg/片)样品的F也是E厂的2倍多,这表明各厂的产品质量有差异,这可能也是引起临床疗效不稳定的因素之一。
溶出度是评价制剂处方、生产工艺、制剂生物利用度的重要指标,而中药制剂由于成分及样品处理复杂,使得其建立有效可控的溶出度方法较为困难,中药分散片常以分散时限来控制产品质量,实际结果表明,虽然每个厂家的样品均在3 min内崩解了,但其溶出度却存在显著的差异,因为样品崩解、分散后还需经历成分的溶出,而对一些疏水性成分则更难溶出,因此测定疏水性成分萜类内酯的溶出能更好的反映药品的内在质量,且通过溶出度的检查,能更好的反映药品制备工艺的优劣,保证临床疗效的稳定有效。
[1]中国药典[S].一部.2005.
[2]国家食品药品监督管理局国家药品标准,WS-228(z-028)-2000,银杏酮酯[S].
[3]杨 光,刘晓军.重新评价银杏叶制剂的质量与功效[J].北京中医,1999,(3):60-62.
[4]谢德隆,高 崎,黄新生.中国银杏药品质量标准体系的建立[J],世界科学技术-中药现代化,2002,4(10):61-62.
[5]国家食品药品监督管理局国家药品标准,YBZ077432005,银杏酮酯分散片[S].
[6]陶 红,张 韬,单 义.RP-HPLC测定不同厂家银杏叶片剂中总黄酮醇苷溶出度[J].中成药,2009,31(8):1226-1229.
[7]胡祥珍,董 荩.Excel在测定药物制剂溶出度参数数据处理中的应用[J].解放军药学学报,2003,19(1):74-76.

