磷酸法制备甲酸的工艺研究
熊祥祖 李志保 魏世辕 张林锋 李文歆
(武汉工程大学磷化工工程中心,湖北武汉,430074)
磷酸法制备甲酸的工艺研究
熊祥祖 李志保 魏世辕 张林锋 李文歆
(武汉工程大学磷化工工程中心,湖北武汉,430074)
研究了磷酸与甲酸钠制取甲酸和磷酸钠盐的工艺过程。同时考察物料配比、温度、反应时间、焦磷酸量对甲酸收率影响,确定最适宜的工艺条件。实验结果表明:甲酸钠与磷酸物料配比为1:1.03、温度55℃、反应时间为240min、焦磷酸量193.73g时,甲酸收率达到90%,甲酸最终浓度可达到96%。
甲酸 焦磷酸 磷酸法 制备
我国是产磷大国,2004年全国实际生产黄磷超过了60万吨,每年大约要产生20亿立方米的尾气。量虽大,但利用率却不到35%。作为化工原料使用不到1.5%,特别是只生产黄磷的企业,基本上都是放空燃烧了;2004年直接或间接燃烧的黄磷尾气所排放的CO2的总量就有370多万吨[1]。在当前能源紧缺、环保要求越来越严格的形势下,国内黄磷生产正向充分利用资源和地域优势、进一步组建联合企业、建设经济生产规模、加大综合利用力度、降低生产成本、加速下游产品开发的方向发展。黄磷尾气的主要成分是CO,除去水分含量占90%左右。黄磷尾气的开发利用,已经成为众多黄磷生产企业的主要议题。人们已经开发出了回收CO制甲酸甲酯[2]、二甲醚[3]、甲醇[4]等成熟的技术。针对磷酸盐钠化工企业的产品结构特点,本文提出了用黄磷电炉尾气制取甲酸钠再与由黄磷企业自产的磷酸工艺相结合联产甲酸和磷酸钠盐。甲酸和磷酸钠既是商品,又可作为中间原料加工成其他下游产品。
回收CO与烧碱反应制取甲酸钠,单质磷氧化制P2O5,和用水吸收制磷酸的技术已经成熟。在研究过程中,发现其主要问题是:甲酸一元弱酸、沸点低并于水接近,同时易分解,导致甲酸的回收率低、浓度难以提高等突出问题,因此本文主要对甲酸钠通过磷酸法合成甲酸的工艺过程和条件进行探讨。通过实验得出:温度为55℃、物料配比为1:1.03、反应时间240min、焦磷酸量193.73g的条件下,可使甲酸的收率达到90%,甲酸浓度最高达到96%,是一条将黄磷尾气CO回收与磷酸生产工艺相结合、充分利用资源、减少尾气排放而增加企业效益的新技术。同时对黄磷生产企业产品结构不受影响,对延伸下游产品,优化资源配置开辟了一条新的途径。
1 实验部分
1.1 实验基本原理
由于正磷酸盐遇酸量不同可转化为磷酸、二氢盐或一氢盐。一氢盐与酸反应亦可转化为磷酸或二氢盐;二氢盐与强酸则有磷酸生成。磷酸酸式盐与不同量的碱可转化为正盐或含氢更少的盐,可知磷酸根只存在碱性环境中,而 HPO42-和 H2PO4-不能与强酸和强碱共存。磷酸与足量碱生成正盐,磷酸与碱中OH-的物质的摩尔量比为1:2时生成一氢盐,为1:1时生成二氢盐[5],由此可知,磷酸法制甲酸反应体系应保持弱酸性[6],磷酸含量应稍过量。有关反应如下:

为了提高甲酸浓度,在蒸馏过程中加入焦磷酸,使其与液相中的水反应生产磷酸,增加反应物磷酸的浓度,提高反应推动动力。反应方程如下:

在反应体系中生成磷酸使其p H值控制在<5,反应产物主要为磷酸二氢钠。
1.2 实验原料、装置及方法
实验原料:磷酸(分析纯),武汉市亚泰化工试剂有限公司;甲酸钠(分析纯),天津市科密欧化学试剂有限公司;焦磷酸(分析纯),国药集团化学试剂有限公司。
实验设备:高压反应釜型号为 GCF-1型,威海祥威化工机械厂。
实验方法:在实验确定温度下,固定甲酸钠量为68g,以一定比例按甲酸钠、磷酸的顺序依次加入高压反应釜内(主要起保持密闭作用,防止甲酸挥发)并开始反应。反应一定时间后,停止加热。在加热反应过程中从105℃开始有甲酸不停地挥发出来,反应釜内所存固体为磷酸钠盐。往蒸馏出的粗甲酸溶液中加入焦磷酸,在160℃再次蒸馏得到高浓度的甲酸。
2 实验结果与讨论
2.1 物料配比对甲酸收率的影响
在实验条件为:操作压力常压,初始温度55℃,反应时间240min,焦磷酸量193.73g,考察甲酸钠与磷酸的摩尔比(以下简称物料配比)对甲酸收率的影响(如图1)。
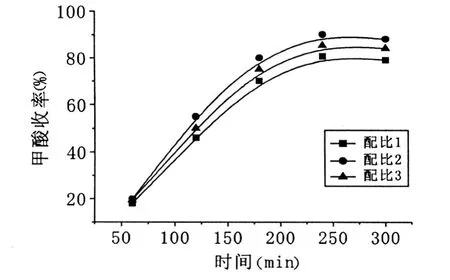
图1 物料配比、甲酸产率关系曲线
从图1可知,当反应时间240min,物料配比为1:1.05、1:1.03、1:1.01,甲酸收率分别为 85.3%、90%、80.6%。说明物料配比不是越高越好,选择适当的物料配比,才能使甲酸收率达到最佳。结合反应方程分析,提高物料配比即增大反应物甲酸钠的浓度,使反应平衡向生成甲酸方向移动,提高了甲酸收率和磷酸的利用率。但随着物料配比不断提高,溶液碱性增强,反应后生成物中混合磷酸一氢钠或磷酸三钠偏多,从而使甲酸收率下降。因此选取合适的物料配比是1:1.03。
2.2 温度对甲酸收率的影响
在实验条件为:操作压力常压,物料配比为1:1.03,反应时间240min,焦磷酸量193.73g,考察温度对甲酸收率的影响(如图2)。

图2 温度、甲酸产率关系曲线
从图2可以看出,温度从50℃升高到55℃甲酸收率呈上升趋势,高于55℃时,甲酸收率增大有所减缓,温度升高到60℃甲酸收率下降。从热力学角度分析,该反应是放热反应,低温有利于反应的进行。同时从动力学角度分析,提高温度能加快反应速率,反应达到平衡时间短有利于反应进行。因此选取55℃为适宜温度。
2.3 反应时间对甲酸收率的影响
在实验条件为:操作压力常压、温度55℃、物料配比为1:1.03、焦磷酸量193.73g,考察反应时间对甲酸收率的影响(如图3)。
由图3可以看出:随着反应时间的增加甲酸收率也随之提高。当反应时间由 120min增加到180min和240min,甲酸收率增加明显,由55%增大到75%和90%;当增加到300min时,甲酸收率增加到90.1%。根据热力学对反应平衡常数及动力学速率的计算,反应在5h时,已接近平衡,瞬时反应速率很小。考虑到能耗及实验数据等原因,选取反应时间为240min适宜。

图3 时间、甲酸产率关系曲线
2.4 焦磷酸量对甲酸产率影响
在实验条件为:操作压力常压、温度55℃、物料配比为1:1.03、反应时间240min,考察焦磷酸量对甲酸收率的影响(见表1)。
以上结果表明:当加入焦磷酸量193.73g时,甲酸收率达到90%,甲酸浓度可达到96%,焦磷酸与水生成的 H3PO4又可以作为反应物原料予以利用。

表1 焦磷酸对甲酸提纯实验数据
3 结论
(1)控制物料配比、反应温度、反应时间可以有效的提高甲酸收率。
(2)在本实验范围内确定的适宜反应条件:物料配比为1:1.03、温度为55℃、反应时间为240min、焦磷酸量193.73g。
(3)在适宜反应条件下,甲酸收率达到90%,经过处理甲酸浓度达到96%,达到工业品要求。
[1]左建国.关于黄磷尾气的利用[J].磷酸盐工业,2007,2:9~12.
[2]陈木梁,张晴章,江洪等.净化黄磷尾气合成甲酸甲酯研究[J].云南化工,2002,29(6):11~13.
[3]许松林,郑搜,徐世民.综合利用黄磷尾气生产二甲醚的可行性研究[J].化工技术经济,2003,21(4):33~35.
[4]宁平,王学谦,陈梁.黄磷尾气净化制甲醇[J].磷酸盐工业,2006(3):3~8.
[5]陈嘉甫,谭光熏.磷酸盐的生产与应用[M].四川:成都科技大学出版社,1989.36~41.
[6]陈五平.无机化工工艺学[M].北京:化学工业出版社,2001.121~122.
Study on Synthesize Fomic Acid by the Method of Phosphorus Acid
XiongXiangzu,LiZhibao,WeiShiyuan,ZhangLinfeng,LiWenxin
(Theresearchcentreofphosphoricchemicalengineering,WuhanInstituteofTechnology,Wuhan430074,China)
The preparation process of formic acid(FA)by the method of phosphorus acid in high-pressure reaction kettle was studied.At the same time,the influence of the ratio of phosphoric acid and sodium formate,temperature,reaction time,the addition of pyrophosphoric acid(PPi)on synthesize yield rate of formic acid ratio were observed and the best process conditions for synthesize formic acid.The result showed that the ultimately productive rate of formic acid reach 90%and concentration of formic acid reach 96%when the mixture ratio of sodium formate and phosphoric acid was 1:1.03,temperature was 55℃,reaction time was 240min,the addition of pyrophosphoric acid(PPi)was193.73g.
fomic acid;pyrophosphoric acid(PPi);the method of p hosphorus acid;preparation

