原发性干燥综合征继发血小板减少患者的临床特征及相关因素分析


【摘 要】目的:探讨原发性干燥综合征(pSS)继发血小板减少患者的临床特征及相关因素。
方法:回顾性分析2017年5月至2022年10月在荆门市人民医院风湿免疫科住院的58例pSS患者的资料,包括一般情况、临床表现、实验室指标(包括炎性指标和自身抗体等)及治疗,并将有无并发血小板减少进行分组比较。Logistic回归探索pSS发生血小板减少的相关因素。结果:pSS患者血小板减少的发生率为37.93%(22/58)。伴血小板减少组以关节痛、疲劳和乏力、出血为主要表现,常见的出血症状为皮肤出血、牙龈出血、鼻出血和小脑出血;红细胞沉降率升高的比例更高,与无血小板减少组比较,差异有统计学意义(P < 0.05);使用糖皮质激素和免疫抑制剂治疗的比例更高,与无血小板减少组比较,差异有统计学意义(P < 0.05)。Logistic回归分析显示,血小板减少的pSS患者较无血小板减少者关节痛
(OR = 0.106,95%CI =[0.022,0.526],P = 0.006)比例更高,糖皮质激素治疗(OR = 7.237,95%CI =[1.631,32.122],P = 0.009)的比例更高。结论:血小板减少是pSS患者常见的并发症。伴血小板减少的pSS患者临床表现多样,主要为关节痛、疲劳和乏力、出血,其中伴有关节痛可能是pSS继发血小板减少的危险因素。伴血小板减少组患者易合并红细胞沉降率升高,提示病情活动度较高。以糖皮质激素和免疫抑制剂治疗为主,使用糖皮质激素治疗比例更高,经积极治疗预后良好。
【关键词】 原发性干燥综合征;血小板减少;关节痛;疲劳和乏力;出血;糖皮质激素;免疫抑制剂
Analysis of Clinical Characteristics and Related Factors in Patients with Secondary Thrombocytopenia in Primary Sjögren's Syndrome
WANG Hong-quan,SU Jin-feng,PENG Chun-xiao,ZHOU Li-ping,ZHAN Jie,ZOU Liang,MEI Zhen-hua
【ABSTRACT】Objective:To explore the clinical characteristics and related factors of patients with secondary thrombocytopenia in primary Sjögren's syndrome(pSS).Methods:A retrospective analysis was conducted on the data of 58 pSS patients admitted to the Rheumatology and Immunology Department of Jingmen People's Hospital from May 2017 to October 2022,including general information,clinical manifestations,laboratory indicators(including inflammatory indicators and autoantibodies),and treatment.The presence or absence of concurrent thrombocytopenia was compared among groups.Logistic regression was used to explore the related factors of thrombocytopenia in pSS.Results:The incidence of thrombocytopenia in pSS patients was 37.93%(22/58).pSS patients with thrombocytopenia mainly presented with joint pain,fatigue and weakness,and bleeding.Common bleeding symptoms included skin bleeding,gum bleeding,nose bleeding,and cerebellar bleeding.The proportion of increased erythrocyte sedimentation rate was higher,and the difference was statistically significant
(P < 0.05).The proportion of patients treated with glucocorticoids and immunos-
uppressants was higher,and the difference was statistically significant compared with the group without thrombocytopenia(P < 0.05).Logistic regression analysis showed that pSS patients with thrombocytopenia had a higher proportion of joint pain(OR = 0.106,95% CI = [0.022,0.526],P = 0.006)and a higher proportion of glucocorticoid therapy(OR = 7.237,95% CI = [1.631,32.122],P = 0.009)compared to those without thrombocytopenia.Conclusion:Thrombocytopenia is a common complication in pSS patients.The clinical manifestations of pSS patients with accompanying thrombocytopenia are diverse,mainly including joint pain,fatigue and weakness,and bleeding.Among them,joint pain may be a risk factor for secondary thrombocytopenia in pSS.Such patients are prone to an increase in erythrocyte sedimentation rate,indicating a high degree of disease activity.Glucocorticoids and immunosuppressants are mainly used in the treatment,with a higher proportion of using glucocorticoids.After active treatment,the prognosis is good.
【Keywords】 primary Sjögren's syndrome;thrombocytopenia;joint pain;fatigue and weakness;bleeding;corticosteroids;immunosuppressants
原发性干燥综合征(primary Sjögren's syndrome,pSS)是一种好发于中老年女性,以淋巴细胞增殖及进行性外分泌腺体损伤为特征,且不合并其他结缔组织病(connective tissue disease,CTD)的慢性炎症性自身免疫病[1-3],全球患病率为0.03%~
2.7%[4],我国报道的患病率为0.33%~0.77%[2]。有研究表明,pSS住院患者多存在系统受累,血液系统损害发生的风险较高[5],其中以血小板减少的诊治尤为棘手[6]。我国近年一项研究表明,pSS患者血小板减少被确定为死亡的独立预测因素
(HR = 1.97,95% CI =[1.03,3.79],P = 0.041)和独立危险因素(HR = 1.93,95% CI = [1.01,3.72],P < 0.048),通常表明为较严重的血液系统受累,是一种疾病活动指数[7]。由于患者症状隐匿,往往不是以口干、眼干等典型干燥症状就诊[6],通常在常规实验室检查中被发现,诊治时间常被延误,部分患者病情顽固、难控制、且易复发[2],为风湿科治疗难点。目前,有研究探索了pSS继发血细胞减少的相关危险因素[1],仍缺少大样本、前瞻性研究。了解pSS继发血小板减少的相关因素,对早防治和预后评估、监测有一定指导意义。本研究对58例pSS患者的临床症状和实验室指标(包括炎性指标和自身抗体)等资料进行总结,回顾性分析pSS继发血小板减少患者的临床特征及相关因素,以期为病情评估、临床防治和相关研究提供参考。
1 资料与方法
1.1 资料来源 收集并整理2017年5月至2022年
10月在荆门市人民医院风湿免疫科住院并诊断为pSS的患者基本资料,包括性别、年龄及病程;临床表现包括口干、眼干、疲劳和乏力、关节痛、猖獗齿、腮腺炎、雷诺现象、全身疼痛、心悸、吞咽梗阻、周围神经病变、干眼症及肺间质病变;实验室指标和自身抗体包括血常规、红细胞沉降率(ESR)、C反应蛋白(CRP)、类风湿因子(RF)、补体C3、补体C4及免疫球蛋白A(IgA)、IgG、IgM和自身抗体[ANA、抗SSA抗体、抗SSB抗体、抗Ro52抗体、抗着丝点蛋白B(CENPB)抗体];骨髓穿刺检查;以及治疗药物,包括改善病情抗风湿药(DMARDs,如甲氨蝶呤、来氟米特、艾拉莫德、羟氯喹),靶向合成DMARDs(如枸椽酸托法替布),免疫抑制剂[如吗替麦考酚酯(MMF)],糖皮质激素,植物药(如白芍总苷)。本研究符合荆门市人民医院人体试验委员会制定的伦理学标准,并取得该伦理委员会的批准(批准号2023101212)。本研究为回顾性研究,知情同意豁免。
1.2 诊断标准 按照2023年中华医学会风湿病学分会发布的《原发性干燥综合征诊疗规范》中pSS诊断标准[2]。
1.3 纳入标准 ①符合上述诊断标准;②血小板计数 < 125×109·L-1,至少2次;③年龄≥18岁。
1.4 排除标准 ①合并其他CTD者,如类风湿关节炎、系统性红斑狼疮、系统性硬化症、抗磷脂综合征等;②继发于血液系统肿瘤或其他部位肿瘤化疗后患者;③伴有白细胞计数和红细胞计数减少,血红蛋白浓度降低者;④药物所致(如化疗药等)和既往存在血小板减少的患者。
1.5 统计学方法 采用SPSS 26.0软件进行统计分析。Shapiro-Wilk检验判断资料是否为正态分布,连续变量中符合正态分布者以表示,采用t检验;非正态分布者以中位数和四分位数间距
[M(P25,P75)]表示,采用Mann‑Whitney U检验;计数资料以例(%)表示,采用χ2检验或Fisher确切概率法。将P≤0.05的因素带入二元Logistic回归模型探索相关性。以P <; 0.05为差异有统计学意义。
2 结 果
2.1 一般资料 共纳入58例pSS患者,其中男4例,女54例;年龄35~83岁,平均(57.31±11.05)岁;病程1~192个月,平均(53.55±31.16)个月。其中并发血小板减少者22例(37.93%),根据是否并发血小板减少,分为血小板减少组和无血小板减少组。2组患者基本资料见表1。
2.2 血小板减少特点 22例血小板减少组pSS患者入院时血小板(73.4±36.7)×109·L-1,皮肤出血6例(27.27%)、牙龈出血5例(22.73%)、鼻出血2例(9.09%)、小脑出血1例(4.55%)。12例行骨髓穿刺检查,①骨髓细胞形态学:骨髓有核细胞增生均活跃,其中3例巨核细胞数量增多伴成熟障碍,1例巨核细胞未见(颗粒型和产板型巨核细胞),考虑为原发免疫性血小板减少症
(ITP);6例巨核细胞数量正常;2例巨核细胞数量减少。②骨髓活检:骨髓有核细胞增生活跃10例、减低2例,其中2例巨核细胞数量增多,考虑为ITP;8例巨核细胞数量正常;1例巨核细胞数量减少,1例巨核细胞未见。③骨髓流式细胞免疫分型(急慢性白血病、淋巴瘤及骨髓瘤和骨髓增生异常综合征全面CD系列40CD)均正常。
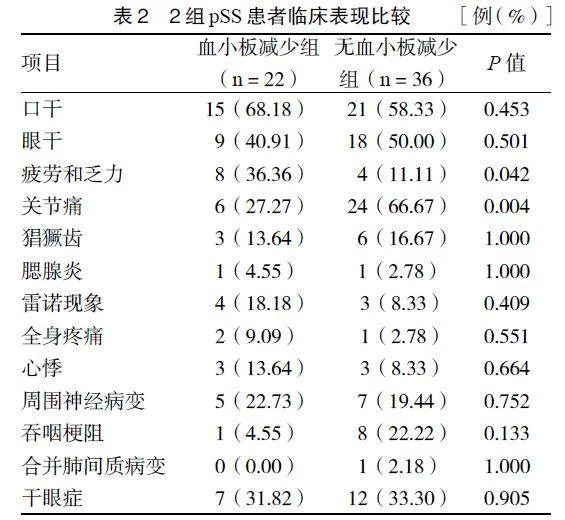
2.3 临床表现 血小板减少组患者中6例关节痛,8例疲劳和乏力,与无血小板减少组比较,差异有统计学意义(P < 0.05)。见表2。
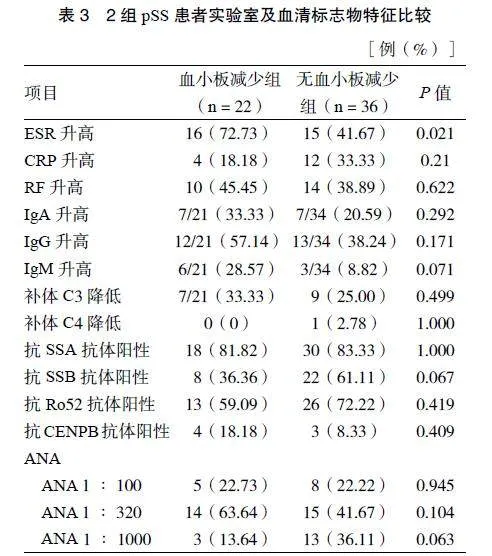
2.4 实验室指标及血清学标志物特征 16例血小板减少组患者ESR升高,与无血小板减少组比较,差异有统计学意义(P < 0.05)。而RF、CRP、IgA、IgG、IgM升高及补体C3、C4降低,抗SSA抗体、抗SSB抗体、抗Ro52抗体、抗着丝点抗体阳性和ANA滴度比较,2组差异无统计学意义(P ﹥ 0.05)。见表3。
2.5 治疗药物 血小板减少组16例患者给予糖皮质激素治疗,与无血小板减少组比较,差异有统计学意义(P < 0.001);10例患者给予MMF治疗,2组比较,差异有统计学意义(P < 0.05)。见表4。
2.6 pSS继发血小板减少的相关因素分析 单因素分析发现,与无血小板减少组比较,血小板减少组关节痛、疲劳和乏力的比例更高,ESR升高的比例更高,MMF和糖皮质激素治疗的比例更高。
将P≤0.05的因素带入Logistic回归模型发现,血小板减少组患者较无血小板减少组关节痛(OR = 0.106,95%CI =[0.022,0.526],P = 0.006)比例更高,糖皮质激素治疗(OR = 7.237,95%CI =[1.631,32.122],P = 0.009)的比例更高。
3 讨 论
本研究纳入58例pSS住院患者,发现37.93%(22/58)的患者继发血小板减少。既往有资料显示,在诊断pSS时已有7.8%的患者存在血小板减少[8]。
本研究中pSS继发血不板减少的比例较既往研究增高,可能与此次仅以住院患者和病例数相对较少有关。总体而言,此次发现pSS继发血小板减少的比例较高,值得临床重视。而且对于孤立性血小板减少者仍需要考虑潜在的系统性疾病或合并ITP[9],因部分患者血小板减少程度和出血症状与ITP无异,骨髓细胞形态学也多表现为巨核细胞增加或正常,易诊断为ITP[10],而忽略了继发CTD的可能。有回顾性研究显示,约12.03%的pSS患者继发ITP[11],也有报道在pSS中的发病率更
高[12]。本研究中,有12例患者行骨髓穿刺检查,其中3例骨髓细胞形态学示巨核细胞数量增多伴成熟障碍,1例巨核细胞未见;2例骨髓活检示巨核细胞数量增多,符合ITP,比例较高。因此骨髓穿刺检查对诊断和鉴别诊断及指导治疗仍具有重要意义,本研究并未对所有患者行骨髓穿刺检查,具有一定的局限性。
有研究表明,pSS 继发血小板减少通常与更高级别的持续性炎症状态相关,可能是pSS以全身炎症状态为特征的一部分[8],而且合并血小板减少的pSS患者疾病活动度更高(P = 0.013)[11],通常是一种疾病活动指数[13]。有报道,在以血小板减少为首发症状的CTD患者中ESR显著升高[10],但也报道ESR升高与pSS发生血小板减少无相关性(P = 0.888)[11]。本研究发现,血小板减少的pSS患者ESR升高比例更高,与无血小板减少组比较,差异有统计学意义(P < 0.05),但行Logistic回归分析显示,ESR升高并不是pSS继发血小板减少的危险因素。上述结果仍提示,ESR升高对pSS患者继发血小板减少可能存在一定的提示意义,但是需要充分考虑到ESR的相关混杂因素。
既往研究显示,并发血小板减少的pSS患者中有60.0%出现出血症状,0.4%颅内出血,6.0%严重出血[14],严重出血多发生在20.2%的儿童和9.6%的成人中,仍以鼻出血常见,其次是皮肤和黏膜出血[15]。一项回顾性研究显示,有65.71%(23/35)的患者出现出血症状,主要表现为四肢皮肤出血点和瘀斑,其次是牙龈出血[11]。本研究发现,血小板减少的pSS患者中有63.64%(14/22)出现出血症状,与报道较一致。其中27.27%皮肤出血、22.73%牙龈出血、9.09%鼻出血、4.55%小脑出血。有资料表明,在这类患者中,腺体外受累也较常见,通常伴有疲劳[12],约70.0%的患者疲劳和乏力明显[16],且与疾病活动相关,常提示病情可能较重[12],因症状无特异性而被忽视。另外,有约30.0%的患者伴有关节痛[7],但也有回顾性分析显示,与无血小板减少的pSS患者(97/248)相比,继发血小板减少的pSS患者(6/35)关节炎的患病率较低(39.11% vs 17.14%;P = 0.014)[11]。本研究显示,pSS继发血小板减少的患者有38.1%疲劳和乏力,27.3%关节痛,与无血小板减少组比较,差异有统计学意义(P < 0.05)。疲劳和乏力比既往报道低,关节痛与既往报道相符。进一步行Logistic回归分析显示,pSS继发血小板减少患者较无血小板减少者关节痛比例更高(P = 0.006),可能为继发血小板减少的危险因素,临床可进一步通过伴有关节痛预测pSS继发血小板减少的风险可能增加。但此次研究的不足在于为单中心研究,样本量较小,对关节痛的程度与继发血小板减少的关联性并未进行更深入研究,因此对继发血小板减少的预测因素和预后影响因素无法深入分析,仍具有一定的局限性,未来需要更多的大样本、前瞻性、多中心、随机对照研究进一步探索并深入分析pSS继发血小板减少的相关因素,特别是对关节痛的程度、疲劳、乏力与pSS继发血小板减少的关联等进行研究,为更好地实施临床诊疗和病情评估,降低复发率和出血等提供参考。
本研究发现,自身抗体如ANA滴度,抗SSA抗体和抗SSB抗体阳性,补体C3、补体C4降低,IgA、IgG、IgM升高在2组患者中差异无统计学意义(P ﹥ 0.05),这与相关报道较一致[7,11]。但也有报道,抗SSA抗体和抗Ro52抗体阳性是原发性血小板减少患者中最常见的自身抗体[17],这可能需要更进一步研究。
大剂量糖皮质激素和静脉注射人免疫球蛋白长期被作为继发血小板减少的一线治疗[13]。但激素的不良反应、对治疗反应的应答差异和高复发率仍是其严重缺点,而且仅约20.0%单用激素治疗的患者得到长期缓解[12]。有报道,ANA阳性的血小板减少患者较少使用免疫抑制剂(P = 0.049),在所使用的免疫抑制剂中以环孢素A为多[17]。近年,英国一项多中心随机对照试验显示,MMF对50.0%~80.0%的血小板减少患者有效且耐受性良好,但起效时间较长(2个月)[18]。研究表明,激素对免疫细胞(包括巨噬细胞、T细胞和B细胞)有广泛、非特异性抑制作用,限制并减少血小板破坏[14],可抑制自身抗体IgG的产生,稳定血小板和内皮细胞膜,减少血小板破坏,刺激骨髓造血[19],还可通过上调记忆B细胞上FcγRⅡb的表达水平升高血小板[14,20]。MMF对T细胞和B细胞具有调节作用,并可抑制T细胞效应,降低血小板的消耗、促进血小板生成[18,21]。BRADBURY等[12]的一项多中心、开放、随机、对照试验显示,在糖皮质激素作为一线治疗的免疫性血小板减少患者中联合MMF可提高疗效,降低难治性、复发性(包括对糖皮质激素耐药)血小板减少的风险,两者联合使用比仅用糖皮质激素方案更有效,且治疗无效率更低,疗效更好、更持久。但在随后12个月的随访中发现,与仅用激素相比,接受MMF治疗的患者疲劳程度较高,生活质量有所下降。但2组患者出血发生率相似且相对较少,无致命性出血发生。本研究中,血小板减少的pSS组主要使用糖皮质激素和MMF治疗,而且两者联合使用的比例更高,2组差异有统计学意义(P < 0.05),但是并没有观察到报道中类似表现。进一步的Logistic回归分析显示,血小板减少组糖皮质激素治疗的比例更高(P = 0.009),这可能与糖皮质激素可短期提升血小板计数及降低出血风险有关,可能为保护因素,有待今后进一步研究。
综上所述,血小板减少是pSS患者常见的严重并发症,继发血小板减少的pSS患者临床表现多样,主要为关节痛、疲劳和乏力、出血,其中伴有关节痛可能是pSS继发血小板减少的危险因素。该组患者更易合并ESR升高,提示病情活动度较高。且使用糖皮质激素及免疫抑制剂治疗比例较高,其中使用糖皮质激素治疗比例更高,可能为保护因素,这类患者经积极治疗预后良好。
参考文献
[1] 罗静,陈嘉琪,黄子玮,等.原发性干燥综合征继发血细胞减少和间质性肺病相关因素分析[J].中华风湿病学杂志,2021,25(6):393-397.
[2] 中华医学会风湿病学分会.原发性干燥综合征诊疗规范[J].中华内科杂志,2023,62(9):1059-1067.
[3] 吴斌.原发性干燥综合征疾病亚群和并发症的研究进展[J].风湿病与关节炎,2021,10(10):64-69.
[4] HAMMITT KM,NAEGELI AN,BROEK RWM,et al.
Patient burden of Sjögren's:a comprehensive literature review revealing the range and heterogeneity of measures used in assessments of severity[J].RMD Open,2017,3(2):e000443-e000452.
[5] 陈树,陈洁,常新,等.原发性干燥综合征合并血液系统受累的危险因素分析[J].实用临床医药杂志,2023,27(3):91-96,102.
[6] 董怡.原发性干燥综合征诊疗规范的必要性与重要性[J].中华内科杂志,2020,59(4):267-268.
[7] QIAN JY,HE CM,LI Y,et al.Ten-year survival analysis of patients with primary Sjögren's syndrome in China:a national prospective cohort study[J].Ther Adv Musculoskelet Dis,2021,13(1):1-11.
[8] ZHANG S,QU JG,WANG L,et al.Activation of toll-like receptor 7 signaling pathway in primary Sjögren's syndrome-associated thrombocytopenia[J].Front Immunol,2021,12(1):637659-637668.
[9] MILLER DD,KRENZER JA,KENKRE VP,et al.
Sequential Immune Thrombocytopenia(ITP)and Thrombotic Thrombocytopenic Purpura(TTP) in an elderly male patient with primary Sjögren's syndrome:when in doubt,use the PLASMIC score[J].Case Rep Med,2021,2021(1):6869342-6869346.
[10] 曹林娟,陈沙娜,乌兰图雅,等.以血小板减少为首发症状的结缔组织病与免疫性血小板减少性紫癜的鉴别诊断[J].实验检验医师杂志,2016,8(1):41-44.
[11] DAI F,YANG GM,RAO PS,et al.Clinical characteristics of secondary immune thrombocytopenia associated with primary Sjögren's syndrome[J].Front Med(Lausanne),2020,7(1):138-142.
[12] BRADBURY CA,PELL J,HILL Q,et al.Mycophenolate mofetil for first-line treatment of immune thrombocytopenia[J].N Engl J Med,2021,385(10):885-895.
[13] WANG T,HE X,RAN NY,et al.Immunological characteristics and effect of cyclosporin in patients with immune thrombocytopenia[J].J Clin Lab Anal,2021,35(9):e23922-e23931.
[14] AUDIA S,BONNOTTE B.Emerging therapies in immune thrombocytopenia[J].J Clin Med,2021,10(5):1004-1022.
[15] CONSOLINI R,COSTAGLIOLA G,SPATAFORA D.
The centenary of immune thrombocytopenia-part 2:
revising diagnostic and therapeutic approach[J].Front Pediatr,2017,5(1):179-189.
[16] VITALI C,MINNITI A,PIGNATARO F,et al.
Management of Sjögren's syndrome:present issues and future perspectives[J].Front Med (Lausanne),2021,8(1):676885-676897.
[17] LIU Y,CHEN SJ,YANG GM,et al.ANA-positive primary immune thrombocytopaenia:a different clinical entity with increased risk of connective tissue dise-
ases[J].Lupus Sci Med,2021,8(1):e000523-e000531.
[18] PELL J,GREENWOOD R,INGRAM J,et al.Trial protocol:a multicentre randomised trial of first-line treatment pathways for newly diagnosed immune thrombocytopenia:standard steroid treatment versus combined steroid and mycophenolate.The FLIGHT
trial[J].BMJ Open,2018,8(10):e024427-e024435.
[19] SONG JC,LIU SY,ZHU F,et al.Expert consensus on the diagnosis and treatment of thrombocytopenia in adult critical care patients in China[J].Mil Med Res,2020,7(1):15-33.
[20] CHEN HF,ZHOU SL,SU DL,et al.High-dose methylprednisolone pulse therapy upregulated FcγRⅡb expression on B cells in primary Sjögren's syndrome patients with thrombocytopenia[J].Clin Rheumatol,2013,32(12):1783-1790.
[21] CRICKX E,EBBO M,RIVIÈRE E,et al.Combining thrombopoietin receptor agonists with immunosupp-
ressive drugs in adult patients with multirefractory immune thrombocytopenia,an update on the French experience[J].Br J Haem,2023,202(4):883-889.
收稿日期:2024-03-11;修回日期:2024-04-26

