高血压病合并主动脉夹层急性期患者降压药物使用及血压控制情况探讨
黄炳玉
(福建省漳州市第二医院,福建 漳州 363100)
高血压病是一种常见的慢性疾病,当血压长期超过正常范围时,会对血管壁产生损伤,导致血管壁的弹性减弱。而主动脉夹层是一种主动脉内膜剥离的疾病,病因复杂,其中高血压是主要的危险因素之一[1]。然而,高血压病合并主动脉夹层患者的降压药物治疗方案及其临床效果的研究还较为有限。因此,本研究旨在探讨高血压病合并主动脉夹层患者的降压药物使用及血压控制情况,并提出相应的治疗建议,为临床治疗提供科学依据和参考。本研究将综合考虑降压药物的种类、剂量、疗程以及患者个体差异等因素,对高血压病合并主动脉夹层患者进行治疗方案的制定和血压控制的评估,旨在为临床治疗提供更为准确、可靠的治疗策略,现将获得的研究过程、成果及数据结果报告如下。
1 资料及方法
1.1 一般资料
选取2019年1月至2022年12月于我研究中心就诊的高血压病合并主动脉夹层患者,根据入组标准筛选研究对象80例,80例患者中,无高血压病史的40例患者为对照组,有高血压病史的40例患者为观察组,对两组患者分别采用降压药物治疗,并根据患者具体情况结合硝酸酯类药物及降压药物[α1受体阻滞剂(乌拉地尔)]治疗。对照组患者中男性25例,女性15例,年龄39~81岁,平均(64.10±4.10)岁。观察组患者中男性为26例,女性为14例,年龄39~80岁,平均(64.15±4.15)岁。纳入标准:(1)高血压病患者:血压≥140/90mmHg或正在服用降压药物;(2)确诊为主动脉夹层患者:通过超声心动图或CTA检查进行诊断;(3)年龄在18岁以上;(4)有足够的病史资料和相关检查报告可进行分析研究。排除标准:(1)合并其他心血管疾病,如心肌梗死、冠心病等;(2)活动性出血或病史中有消化道出血、脑出血;(3)重度肝功能不全;(4)孕妇或哺乳期妇女;(5)需要紧急手术的患者;(6)不能独立完成治疗的患者。本次研究患者的一般资料均衡可比,P>0.05。
1.2 方法
将纳入的患者根据血压水平、年龄、身体健康状况等因素进行综合分析和判断,选择硝酸酯类(硝酸甘油)及α1受体阻滞剂(乌拉地尔),或者硝酸甘油+β受体阻滞剂、乌拉地尔+β受体阻滞剂等适当降压药物进行治疗,具体内容如下。
(1)降压药物的选择:针对于高血压病合并主动脉夹层的患者,降压药物的使用需要根据患者的具体情况进行选择。常见的降压药物包括以下几种:硝酸酯类(硝酸甘油)及α1受体阻滞剂(乌拉地尔)必要时联合β受体阻滞、血管紧张素转换酶抑制剂(Angiotensin-Converting Enzyme Inhibitors)和血管紧张素II受体拮抗剂(Angiotensin II Receptor Blockers):主动脉夹层发生的相关机制可能跟高血压病息息相关,因此ACEI和ARB可以说是治疗高血压病合并主动脉夹层的首选药物。但是,使用这类药物需要注意肾功能,因为ACEI和ARB与肾功能有关,可能会影响肾功能。CCB:钙通道阻滞剂可通过拓宽血管和减低心脏的收缩力来降低血压。使用时需注意控制提高血压过程中可能出现的心率增加,我院目前主要常用硝酸酯类(硝酸甘油)及α1受体阻滞剂(乌拉地尔)。利尿剂:利尿剂能够促进尿液的排泄,从而降低血容量和血压。当然,利尿药可能会对肾功能造成一定的影响,需慎重使用。
(2)降压药物的剂量设定:药物剂量的设定是高血压病合并主动脉夹层患者降压药物使用的重要环节。常用的方法是基于患者的具体情况确定治疗的目标值,主动脉夹层目标血压一般控制在收缩压在100~120mmHg为宜,同时控制心室率在50~80次/分,从而设置初始剂量。同时,要根据患者的情况,逐步进行剂量调整。初始剂量:在开始治疗时,药物的剂量应不高于最小标准剂量的一半。这样可以避免药物的不良反应,如低血压、低钾症等等,而且能更好地掌握药物的反应情况。药物调整:根据患者的生理指标变化及治疗反应,逐渐加大药量并进行调整,以达到目标值。调整剂量需要逐渐进行,建议采取逐步加大剂量,避免急剧上升、反跳等情况的发生。
(3)降压药物的监测与不良反应的处理:患者应在正规的医疗机构进行监测,其中包括血压的监测、生理指标的监测(如血尿素氮、肌酐、血钾、心电图等)、药物反应的监测等。如发现不良反应和药物过敏应采取积极措施处理,如根据对症处理的需要,可使用对症辅助药物,如抗过敏药、充分纠正低血压、低钾症或肾损伤等。
1.3 观察指标
比较两组患者在住院期间的降压药物使用情况、出院时的血压情况及血压、心率达标情况。(根据《主动脉夹层诊断与治疗规范中国专家共识》推荐高血压病合并主动脉夹层急性期患者药物治疗目标为控制收缩压在100~120mmHg,心率60~80次/min)。
1.4 统计学分析
2 结果
2.1 两组患者住院期间的降压药物使用情况
观察组患者的硝酸酯类药物及三联降压药物的使用量均高于对照组(P<0.05),详见表1。
2.2 比较两组患者治疗前后的血压变化
离开抢救室时观察组患者的收缩压高于对照组(P<0.05),详见表2。
表2 高血压病合并主动脉夹层患者离开抢救室时的血压情况
2.3 高血压病合并主动脉夹层患者离开抢救室时的血压、心率达标情况
观察组患者的血压达标率低于对照组患者,(P<0.05),详见表3。
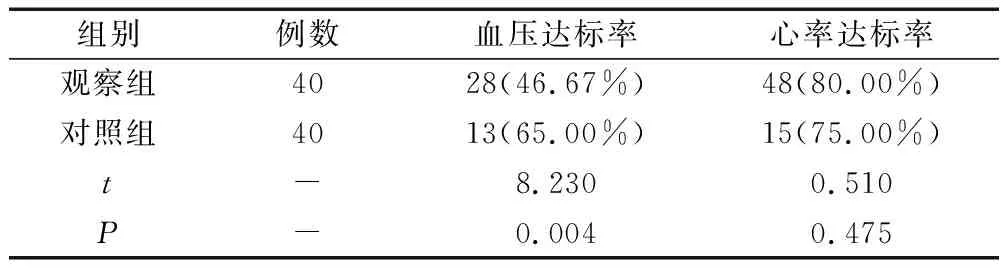
表3 高血压病合并主动脉夹层患者离开抢救室时的血压、心率达标情况[n(%)]
3 讨论
高血压病合并主动脉夹层是一种心血管疾病,指在高血压患者中,主动脉表层产生裂口,血液穿过夹层形成的虚假性腔道,是一种比较严重的并发症,该病具有发病率高、病情严重、诊治难度大等特点[2]。主动脉夹层可分为两种类型:Stanford分型和DeBakey分型。Stanford分型将主动脉夹层分为A型和B型,A型发生在主动脉起始部,B型发生在主动脉起始部以下[3]。高血压病合并主动脉夹层具有以下特点:(1)发病率:高血压合并主动脉夹层的发生率较低,但由于高血压患者数量众多,因此合并主动脉夹层的患者仍然相对较多。(2)发病机制:高血压导致的长期血压升高会对主动脉壁产生损伤,主动脉壁的弹性减弱,容易发生内膜剥离,从而形成主动脉夹层。(3)临床表现:高血压病合并主动脉夹层的症状与非合并病例类似,表现为突发胸痛、背痛、腹痛、呼吸困难、高血压危象等。有时还会出现神经系统缺血症状,如偏瘫、失语等。(4)诊断:诊断主动脉夹层的关键是通过影像学检查,如CT或MRI,来确定主动脉内膜是否剥离。此外,根据病情还需进行心电图、血液学和生化检查等。(5)治疗:高血压病合并主动脉夹层需要紧急治疗,治疗的目标是减轻剥离压力、控制血压和预防并发症。一般情况下,通过手术或介入治疗来修复主动脉夹层,并同时进行药物治疗来降低血压和防止再发。总之,高血压病合并主动脉夹层是一种较为严重的疾病,需要及时治疗,早期诊断和干预非常重要。高血压患者应定期检查血压,进行心脏超声和其他相关检查,以及遵循医生的治疗建议,以降低发生主动脉夹层的风险。在高血压病合并主动脉夹层的治疗中,降压药物是不可或缺的治疗手段。对于高血压病合并主动脉夹层患者,合理、个体化的降压药物治疗方案,主动脉夹层患者急性期首先是以控制血压和疼痛为主的急救治疗。发病急性期有效平稳的控制血压,从而减少夹层的进一步撕裂的同时预防其他高血压危象发生和破裂风险,提高患者的预后,为后续手术干预赢得时间,提高术后生存质量及远期生存率。针对不同的情况,有不同的降压药物及血压控制方案,常用的降压药物包括硝酸酯类药物及α1受体阻滞剂(乌拉地尔)及β受体拮抗剂、钙通道阻滞剂、ACEI、ARB等[4],急性期血压过低亦致全身缺血、多脏器功能障碍发生,此种情况则需适当升压维持基本全身灌注,常用药物如多巴胺等。高血压病合并主动脉夹层的病因尚不明确,可以是机械性压力、血流剪切力、片层区域的变形、损伤和代谢障碍等多种因素共同作用的结果[5]。高血压病患者常常存在动脉硬化、血管内皮细胞屏障和纤溶系统的功能障碍等,这些因素导致在主动脉内壁产生撕裂,形成夹层,随着时间的推移[6],夹层会发展扩展,导致破裂,引起主动脉瘤或动脉瘤破裂等严重并发症。高血压病合并主动脉夹层的临床表现复杂多样,常见的症状包括胸痛、胸闷、呼吸困难、心悸、下肢水肿等[7]。由于病情复杂,缺乏特异性,容易被误诊,尤其是容易与心肌梗死、冠心病、肺栓塞等疾病相混淆。因此,需要结合患者的病史、临床表现以及影像学检查等多个方面的信息来确诊。高血压病合并主动脉夹层的诊断可通过CT、MRI、超声心动图等影像学检查手段进行,但需要注意的是,对于一些轻度的病例,常规的影像学检查难以发现夹层的存在,因此需要结合血流动力学检查和生理检查等综合诊断手段才能确诊。
高血压病合并主动脉夹层的治疗需要综合考虑病变的位置、程度、大小、性质等因素[8]。高血压病合并主动脉夹层的治疗需要根据患者的具体情况进行针对性的治疗,对于病情较轻的患者,可以通过休息、控制血压、血液稀释剂等措施进行保守治疗。而对于病情较重的患者,可能需要进行手术治疗,以避免血管破裂引起的严重后果,如主动脉瘤、大出血等危险情况。目前主要通过药物治疗和手术治疗来控制病情,药物治疗是缓解症状的主要手段,包括硝酸酯类(硝酸甘油)、α1受体阻滞剂(乌拉地尔)、钙通道阻滞剂、ACEI/ARB、β受体阻滞剂等[9];而手术治疗则是治愈及缓解病情的主要手段,包括内科手术和外科手术,针对病情和患者情况量身定制治疗方案[10]。高血压病合并主动脉夹层是一种较为常见的疾病,其病情更加复杂,导致治疗难度增加[11],因此探讨各种降压药物对该患者的治疗效果是非常有必要的。目前常用的降压药物主要包括硝酸酯类(硝酸甘油)及α1受体阻滞剂(乌拉地尔)、金属离子拮抗剂(包括钙通道阻滞剂和ACEI/ARB)、β受体阻滞剂等,针对这些降压药物对高血压病合并主动脉夹层患者的治疗效果进行分析得同以下结论。
(1)α1受体阻滞剂(乌拉地尔)):α1受体阻滞剂是一类药物,通过阻断α1肾上腺素受体的活性,产生双重降压效果。外周降压效应:α1受体阻滞剂作用于血管平滑肌的α1受体,阻断了肾上腺素对这些受体的结合,从而导致血管平滑肌的松弛和外周阻力的降低。这种作用使得血压下降,从而减少心脏的负荷和血管的硬化。中枢降压效应:在中枢神经系统中,α1受体阻滞剂作用于脑干和延髓中的α1受体,抑制了血管收缩效应。这可以导致迷走神经活性增加,降低心输出量和交感神经活性,抑制体液激素的释放,进一步降低血压。通过产生双重降压效应,α1受体阻滞剂成为治疗高血压疾病的一线药物之一。该类药物可以降低收缩压和舒张压,减少心血管事件的发生率,并且对心率和心脏血液供应的改善也具有积极作用。
(2)硝酸酯类(硝酸甘油:降低血管平滑肌张力,对静脉容量血管的这种作用比动脉血管显著,减少静脉回心血量而降低心脏充盈压力。心脏充盈压力的下降可减少左室舒张末期容积和前负荷,从而显著降低心肌耗氧量。硝酸甘油尚可降低全身血管阻力、肺血管和动脉血管压力,从而降低后负荷。硝酸甘油使血流沿心外膜到心内膜的侧枝血管床重新分布,从而改善心肌供氧[12]。
(3)β受体阻滞剂:β受体阻滞剂通过竞争性抑制β1受体,减少肾上腺素和去甲肾上腺素的作用[13],从而降低心率,降低心输出量,降低血压[14]。β受体阻滞剂主要适用于心率较高的高血压患者,在处理高血压病合并主动脉夹层患者时,一些研究认为β受体阻滞剂对于主动脉瘤的扩张有一定的影响。
各种降压药物在对高血压病合并主动脉夹层患者的治疗中均具有一定的效果,应根据患者个体情况而定,采用合理的联合用药方案进行治疗。当然,在治疗的过程中,需严格注意药物的剂量和用药时间,尽可能的减少药物的不良反应,进行有效的血压控制和改善患者的心血管功能,从而提高患者的生活质量和预后。同时需要结合患者的情况,制定合理的饮食和运动方案,以及遵循良好的生活方式,积极预防并发症的发生,为患者提供更加全面的治疗[15]。本研究结果显示,观察组患者的硝酸酯类药物及三联降压药物使用情况均高于对照组(P<0.05);离开抢救室时观察组患者的收缩压高于对照组(P<0.05);观察组患者的血压达标率低于对照组患者(P<0.05),表明β受体阻滞剂能够降低主动脉夹层患者的心率和血压,减缓心肌缺血,改善心脏功能,单一降压药物可能无法控制血压和夹层的进展,在此情况下,联合使用多种降压药物则可以提高控制血压和夹层的效果。
综上所述,高血压病患者若平均血压越高,控制血压就越困难,一般需要使用两种以上静脉降压药物进行治疗。在ICU中,联合用药越多,停留时间会越长,出院时达标的比例会越低,同时出院后口服的降压药种类也会增加。临床医生需要密切监测高血压病患者的血压,必要时联合用药,加快降低血压使之达到目标值,以降低主动脉破裂等并发症发生的风险。

