龙泽熊胆胶囊中水防风掺伪的检测方法研究
刘珍,陆佳,张万青,苏章轩,吴群悦,刘潇潇(广东省药品检验所,广东 广州 510663)
龙泽熊胆胶囊原名熊胆丸,为非处方药(OTC)甲类药品,系由龙胆、防风、熊胆粉等17味药组成的中药复方制剂,具有清热散风,止痛退翳的功效,用于风热或肝经湿热引起的目赤肿痛、羞明多泪[1]。目前该品种全国有生产企业10家,其现行质量标准收载于《中国药典》2020年版一部,该标准对组方中的6味药进行了控制,包括当归、栀子、防风、黄连、熊胆粉的薄层色谱鉴别,以及以龙胆苦苷为指标的龙胆含量测定。鉴于该处方药味多,药效物质基础复杂,其质量标准有待进一步提升。处方中防风为常用大宗中药饮片,来源于伞形科植物防风Saposhnikovia divaricata(Turcz.)Schischk.的干燥根[1],其始载于《神农本草经》,具有祛风解表、胜湿止痛的功效,多分布于内蒙古、黑龙江、吉林等省[2],其质量标准收载于《中国药典》2020年版一部。防风地方习用品种较多,如水防风、陕防风、川防风等[3-5]。2019年国家中药材饮片抽检专项中发现,目前市场上存在水防风掺混入防风饮片的现象[6]。水防风为伞形科岩风属植物宽萼岩风Libonotis laticalycinaShan et sheh.的干燥根,多分布于河南荥阳、山西运城等地区[6-7],其质量标准收载于《河南省中药材标准》1991年版[7]。防风和水防风两者基原不同,功效亦存在差异。水防风的挥发油含量同正品防风比较差异很大,解热作用略逊于正品防风,而镇痛作用较强,但毒性较正品大[8-9]。水防风掺伪防风投料,其安全性和有效性均未得到充分评估和验证,不但影响制剂质量,更可能直接影响其临床疗效[10-12]。防风与水防风的色原酮类化学成分相似,均含有升麻素苷、5-O-甲基维斯阿米醇苷等。防风现行质量标准中,以上述两种化学成分为指标进行定性和定量[1],无法有效地鉴别防风与水防风[13-15]。本课题组开展了水防风中Xanthalin分离鉴定,分别以薄层色谱法(TLC)、高效液相色谱-紫外检测法(HPLC-UV)对59批次防风和12批次水防风药材进行鉴别,证明Xanthalin为区别于防风的专属性化学成分[16]。在此基础上,进一步开展龙泽熊胆胶囊水防风掺伪的特征成分Xanthalin的检测研究,以TLC、HPLC和超高效液相色谱串联三重四级杆质谱法(UPLC-MS/MS)等方法,研究建立含防风制剂龙泽熊胆胶囊中水防风掺伪投料的质量控制方法,以期实现对该制剂中是否存在水防风掺伪或代替防风投料的检测与甄别。
1 材料与试药
1.1 仪器TLC Visualizer 3薄层数码成像系统(瑞士卡玛公司);LC-20AT高效液相色谱仪,包括柱温箱CTO-M20AC、自动进样器SIL-20AC、紫外检测器SPD-20A(日本岛津公司);XevoTMTQ-S型三重四级杆质谱联用仪(美国Waters公司);Milli-Q Academic型超纯水系统(美国Millipore公司);M8800H-C超声波清洗器(美国必能信公司);CP224S万分之一电子天平、CP225D十万分之一电子天平(德国Sartorius公司)。
1.2 试药水防风对照药材(批号:121349-202002)、防风对照药材(批号:120947-201810),中国食品药品检定研究院;Xanthalin对照品(自制,高效液相色谱法标定纯度大于98%)。硅胶G预制板(德国Merck公司、青岛海洋化工厂分厂);柱层析硅胶(青岛海洋化工厂分厂)。甲醇、乙腈(色谱纯,德国Merck公司);乙腈、甲酸(质谱级,美国Fisher chemeical公司);水为超纯水;其余试剂均为分析纯。
龙泽熊胆胶囊样品107批次(市售),由10家企业(A~J)生产。水防风药材9批次,均于产地山西收集(编号:SX01~SX09),经广东省药品检验所中药材(饮片)室林锦锋主任中药师鉴定,为伞形科岩风属植物宽萼岩风Libonotis laticalycinaShan et sheh.的干燥根。龙泽熊胆胶囊标准制剂3批次,由广东省药品检验所按龙泽熊胆胶囊的处方和工艺模拟制备,投料饮片均符合《中国药典》2020年版一部品种标准项下有关的规定。缺防风阴性样品1批次,由广东省药品检验所按龙泽熊胆胶囊的处方(缺防风)和工艺模拟制备。按不同掺入比例(防风中分别掺入5%、10%、20%、30%、50%、100%水防风)的龙泽熊胆胶囊样品,由广东省药品检验所按处方和工艺模拟制备。
2 方法与结果
2.1 薄层色谱法
2.1.1色谱条件 照《中国药典》2020年版四部薄层色谱法(通则0502)试验,吸取供试品溶液10μL,对照品溶液2μL,分别点于同一硅胶G薄层色谱板上,以环己烷-乙酸乙酯(8∶3.5)为展开剂展开,取出,晾干,置紫外光灯(365 nm)下检视。
2.1.2对照品溶液制备 取Xanthalin对照品适量,加甲醇制成每1 mL含0.5mg的溶液即得。
2.1.3对照药材溶液制备 取防风对照药材、水防风对照药材各0.5 g,分别加甲醇5 mL,超声处理30 min,滤过,取上清液,作为对照药材溶液。
2.1.4供试品溶液制备 取龙泽熊胆胶囊内容物2.5 g,加乙醇50 mL,加热回流30 min,放冷,滤过,滤液蒸干,残渣加氨试液10 mL使溶解,用水饱和的正丁醇振摇提取3次(20、20、10 mL)。合并正丁醇液,用正丁醇饱和的水20 mL洗涤,取正丁醇液,蒸干。残渣加乙醇4 mL使溶解,加在中性氧化铝柱上(100~200目,3 g,内径为1~1.5 cm),用乙醇100mL洗脱,收集洗脱液,蒸干。残渣加甲醇2mL使溶解,即得。
2.1.5标准制剂溶液制备 取龙泽熊胆胶囊标准制剂适量(相当于本品内容物2.5 g),按“2.1.4”项下的方法制成标准制剂溶液。
2.1.6缺防风阴性样品溶液制备 取缺防风阴性1 2样 品 3 10 g(相当于本品内容物2.5 g),按“2.1.4”项下的方法制成缺防风制剂溶液。
2.1.7掺入不同比例水防风样品溶液制备 分别取掺入5%、10%、20%、30%、50%、100%水防风的龙泽熊胆胶囊样品约7.74~11.35 g(相当于本品内容物2.5 g),精密称定,按“2.1.4”项下的方法制成掺入不同比例水防风样品溶液。
2.1.8方法学考察 (1)专属性考察:按“2.1.1”项下的色谱条件进行试验,标准制剂溶液、缺防风阴性样品溶液、防风对照药材溶液、龙泽熊胆胶囊样品(A、B、C、D企业)溶液,在与对照品溶液色谱相应的位置上,不显相同颜色的荧光主斑点;水防风对照药材溶液、8批次龙泽熊胆胶囊样品(G企业)溶液,在与对照品溶液色谱相应的位置上,显相同颜色的荧光主斑点,表明方法专属性好(见图1)。

注:1~3:龙泽熊胆胶囊标准制剂;5、16:Xanthalin对照品;22:缺防风阴性样品;7、17.防风对照药材;8、18:水防风对照药材;4、6、9、10:分别为A企业、B企业、C企业、D企业的龙泽熊胆胶囊样品;11~15、19~21:8批次G企业的龙泽熊胆胶囊样品图1 水防风薄层色谱检查方法专属性试验图谱Figure 1 TLCchromatogramsofspecifictestofLibanotislaticalycinainLongzeXiongdanCapsules
(2)重复性试验:取同一批次龙泽熊胆胶囊样品(G企业)6份,精密称定,按“2.1.4”项下的方法制备供试品溶液,按“2.1.1”项下的色谱条件展开、检视,在与对照品溶液色谱相应的位置上,均显相同颜色的荧光主斑点,表明方法重复性好。
(3)耐用性试验:经不同品牌的预制硅胶G薄层板、低温(8 ℃)和室温(25 ℃)条件,低湿(32%)和高湿(88%)的不同条件验证,主斑点的比移值(Rf)值均适中,且分离效果均较好,认为温度和湿度对该薄层鉴别方法无明显影响。表明方法耐用性佳。
(4)限度确定: 分别取“2.1.7” 项下掺入5%、10%、20%、30%、50%、100%水防风样品溶液。按“2.2.1”项下的色谱条件展开、检视,供试品色谱中,掺入10%、20%、30%、50%、100%水防风样品均能检出水防风的特征斑点。故TLC法检测限拟定为制剂中掺伪10%水防风,即每1 g龙泽熊胆胶囊中掺入水防风24 mg即可检出。
2.2 高效液相色谱法
2.2.1色谱条件 色谱柱:SHIMADZU InertSustain®C18(250 mm×4.6 mm,5μm);乙腈-水(58∶42)为流动相,等度洗脱;流速:1.0 mL·min-1;柱温:30℃;检测波长:324 nm;进样量:10μL。
2.2.2对照品溶液制备 取Xanthalin对照品适量,精密称定,加甲醇制成每1mL含3μg的溶液,即得。
2.2.3供试品溶液制备 取龙泽熊胆胶囊内容物适量,混匀,取约2.5 g,精密称定,加乙醇50 m L,加热回流30 min,放冷,滤过,滤液蒸干。残渣加氨试液10 mL使溶解,用水饱和的正丁醇振摇提取3次(20,20,10 mL)。合并正丁醇液,用正丁醇饱和的水20mL洗涤,取正丁醇液,蒸干。残渣加乙醇4mL使溶解,加在中性氧化铝柱上(100~200目,3 g,内径为1~1.5 cm)。用乙醇100 mL洗脱,收集洗脱液,蒸干。残渣加甲醇适量使溶解,并分次转移至10 mL量瓶中。用甲醇稀释至刻度,摇匀,即得。
2.2.4标准制剂溶液制备 取龙泽熊胆胶囊标准制剂适量(相当于本品内容物2.5 g),精密称定,按“2.2.3”项下的方法制成溶液。
2.2.5缺防风阴性样品溶液制备 取缺防风阴性样品10 g(相当于本品内容物2.5g),精密称定,按“2.2.3”项下的方法制成溶液。
2.2.6掺入100%水防风样品溶液制备 取掺入100%水防风的样品适量(相当于本品内容物2.5g,含水防风0.6 g的量),精密称定,按“2.2.3”项下的方法制成溶液。
2.2.7掺入不同比例水防风样品溶液制备 分别取按不同掺入比例(防风中分别掺入5%、10%、20%、30%、50%、100%水防风)制备的泽熊胆胶囊样品约7.74~11.35 g(相当于本品内容物2.5 g),精密称定,按“2.2.3”项下的方法制成掺入不同比例水防风样品溶液。
2.2.8方法学考察 (1)专属性考察:以Xanthalin色谱峰为指标,按“2.2.1”项下的色谱条件,对上述溶液进行检测。结果龙泽熊胆胶囊样品(B企业)、标准制剂、缺防风阴性样品色谱中,在与Xanthalin对照品色谱峰保留时间处未呈现相同的色谱峰;龙泽熊胆胶囊样品(G企业)、掺入100%水防风样品,均检出与Xanthalin对照品保留时间相同的色谱峰(见图2)。采用二极管阵列检测器检测,比较相应色谱峰在200~400 nm波长范围的紫外-可见吸收光谱。结果龙泽熊胆胶囊样品(G企业)、掺入100%水防风样品与Xanthalin对照品的光谱扫描图谱相同,在324 nm处有最大吸收(见图3)。综上所述,表明方法专属性好。

注:A.Xanthalin对照品;B.龙泽熊胆胶囊样品(G企业);C.自制掺入100%水防风样品;D.龙泽熊胆胶囊样品(B企业);E.缺防风阴性样品;F.自制标准制剂。Ⅰ.Xanthalin色谱峰图2 龙泽熊胆胶囊中水防风掺伪的高效液相色谱图Figure 2 HPLC chromatograms of Libanotis laticalycina adulterated in Longze Xiongdan Capsules

图3 Xantha lin特征峰的紫外吸收光谱图Figure 3 Characteristic peaks in UV spectrum of xanthalin
(2)精密度试验:取Xanthalin对照品溶液,按“2.2.1”项下的色谱条件,连续进样6次,记录色谱峰面积,计算得峰面积的RSD为3.2%(n=6),表明仪器精密度好。
(3)稳定性试验:取同一龙泽熊胆胶囊样品(G企业)溶液,按“2.2.1”项下的色谱条件,分别于0、2、5、8、12、24 h注入液相色谱仪进行测定,记录Xanthalin色谱峰的峰面积,计算得峰面积的RSD为1.7%(n=6),表明样品溶液在24 h内稳定。
(4)重复性试验:取同一龙泽熊胆胶囊样品(G企业)6份,精密称定,按“2.2.3”项下的方法制成供试品溶液,按“2.2.1”项下的色谱条件,分别注入液相色谱仪检测,记录Xanthalin色谱峰的峰面积,计算得峰面积的RSD为3.3%(n=6),表明方法重复性良好。
(5)耐用性试验:分别采用不同品牌色谱柱:SHIMADZU InertSustain®C18(250mm×4.6mm,5μm)、SHISEIDOCAPCELLPAKC18MGⅡ(200mm×4.6mm,5μm)、Kromasil100-5-C18(250mm×4.6mm,5μm),考察液相方法的可行性和适用性。取龙泽熊胆胶囊样品(G企业)溶液,按“2.2.1”项下的色谱条件,分别注入液相色谱仪,记录图谱,不同品牌色谱柱均能满足分离要求,峰形佳,计算得峰面积的RSD为2.5%(n=3),表明方法耐用性好。
(6)线性试验:分别取“2.2.7”项下的水防风不同掺入比例(防风中分别掺入5%、10%、20%、30%、50%、100%水防风)制备的龙泽熊胆胶囊样品溶液。按“2.2.1”项下的色谱条件,注入液相色谱仪,记录Xanthalin色谱峰的峰面积。以峰面积值为纵坐标,水防风的掺入量为横坐标,绘制标准曲线,计算得回归方程为Y=73 525X-443.13,r=0.999 6,表明掺入量在5%~100%范围内,水防风掺入量与色谱峰面积的线性关系良好。
(7)限度确定:将掺入10%水防风的样品溶液,按“2.2.1”项下的色谱条件,注入液相色谱仪进行检测,测得Xanthalin色谱峰的S/N=4。故拟定该方法检测限,龙泽熊胆胶囊中防风掺伪10%水防风,即每1 g龙泽熊胆胶囊掺入水防风24mg即可检出。
取不同批次的水防风药材(编号:SX01~SX09),按照水防风掺伪10%的比例制备9份龙泽熊胆胶囊样品,按“2.2.3”项下的方法制成供试品溶液,按“2.2.1”项下的色谱条件,测定Xanthalin色谱峰的峰面积。该化合物在不同批次水防风中含量有一定差异,取其平均值。精密称取Xanthalin对照品11.21 mg,加甲醇制成每1 mL含44.84μg·mL-1的溶液,作为储备液。再将储备液逐级稀释,配制Xanthalin系列对照品溶液(浓度分别为0.22、0.36、0.45、0.89、2.23、4.45μg·mL-1),按“2.2.1”项下的色谱条件测定,以Xanthalin色谱峰的峰面积为纵坐标,浓度为横坐标,绘制标准曲线,计算得回归方程为Y=30 590+1 080.5,r=0.999 7,Xanthalin对照品在0.22~4.45μg·mL-1浓度范围内,线性关系良好。根据对照品色谱峰面积的线性关系,计算9份样品中Xanthalin的平均浓度为0.29μg·mL-1,故将龙泽熊胆胶囊中Xanthalin的检查限度拟定为0.3μg·mL-1。
2.3 超高效液相色谱-三重四极杆串联质谱法
2.3.1色谱条件 色谱柱:Aglient SB-C18(100 mm×2.1 mm,2.7μm);流动相:乙腈(A)-0.1%甲酸水溶液(B),梯度洗脱(0~10 min,5%~25%A;10~14 min,25%~62%A;14~18 min,62%~72%A;18~22min,72%~98%A;22~22.1min,98%~100%A;22.1~25 min,100%A);流速:0.25 mL·min-1;柱温:30℃;进样量:1μL。
2.3.2质谱条件 以三重四级杆质谱作为检测器,电喷雾离子源正离子模式(ESI+),进行多反应监测(MRM);利用保留时间和离子丰度判断定性结果;毛细管电压2.91 kV,干燥气温度为600℃,干燥气流速为800 L·h-1。选择m/z427.10→245.05、m/z427.10→327.05和m/z427.10→217.05为检测离子对,锥孔电压均为30 V,碰撞能量分别为25、18、25 V。
2.3.3对照品溶液的制备 精密吸取“2.2.2”项下的对照品溶液1 mL,置于50 mL量瓶中,加甲醇逐级稀释成质量浓度为6 ng·mL-1的溶液,即得。
2.3.4对照药材溶液的制备 精密吸取“2.1.3”项下的对照药材溶液1 mL,置于50 mL量瓶中,用甲醇稀释至刻度,即得。
2.3.5供试品溶液的制备 精密吸取“2.2.3”项下的供试品溶液1 mL,置于50 mL量瓶中,用甲醇稀释至刻度,即得。
2.3.6掺入10%水防风样品溶液的制备 同“2.3.5”项下。
2.3.7专属性考察 精密吸取上述溶液各1μL,注入高效液相色谱-质谱联用仪,按“2.3.1”和“2.3.2”项下的液相、质谱条件进样检测,记录色谱图。结果水防风对照药材、掺入10%水防风样品、龙泽熊胆胶囊阳性样品(G企业)m/z427.1→327.05、m/z427.1→245.05和m/z427.1→217.05的MRM图中,均检出水防风特征成分Xanthalin色谱峰(峰Ⅰ)(见图4~图7);且在一级质谱、二级质谱图中均呈现与Xanthalin对照品一致的母离子(m/z为427.10)和子离子(m/z为327.05、245.05、217.05)(见图8)。龙泽熊胆胶囊阴性样品(B企业)、防风对照药材均未检出水防风特征成分Xanthalin色谱峰(见图9~图10),在水防风特征峰Xanthalin对照处无干扰,表明方法专属性好。

图5 水防风对照药材m/z 427.1→327.05、m/z 427.1→245.05和m/z 427.1→217.05的MRM质谱图Figure 5 m/z 427.1→327.05、m/z 427.1→245.05 and m/z 427.1→217.05 MRM mass spectrums of Libanotis laticalycina reference medicinalmaterial
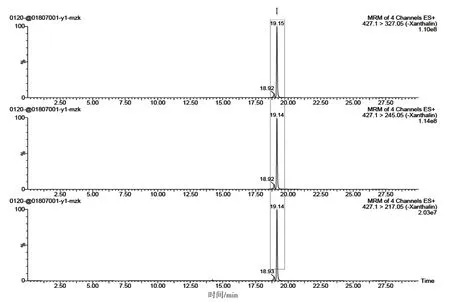
图7 龙泽熊胆胶囊阳性样品(G企业)m/z 427.1→327.05、m/z 427.1→245.05和m/z 427.1→217.05的MRM质谱图Figure 7 m/z 427.1→327.05、m/z 427.1→245.05 and m/z 427.1→217.05 MRM mass spectrums of positive sample in Longze Xiongdan Capsules(Company G)

图8 Xanthalin的一级、二级质谱图Figure 8 The primary and secondarymass spectra of Xanthalin

图9 龙泽熊胆胶囊阴性样品(B企业)m/z 427.1→327.05、m/z 427.1→245.05和m/z 427.1→217.05的MRM质谱图Figure 9 m/z 427.1→327.05、m/z 427.1→245.05 and m/z 427.1→217.05 MRM mass spectrums of negative sample in Longze Xiongdan Capsules(Company B)

图10 防风对照药材m/z 427.1→327.05、m/z 427.1→245.05和m/z 427.1→217.05的MRM质谱图Figure 10 m/z 427.1→327.05、m/z 427.1→245.05 and m/z 427.1→217.05 MRM mass spectrums of Saposhnikoviae Radix reference medicinalmaterial
2.4 样品测定按上述研究思路和方法,对市售107批次龙泽熊胆胶囊样品进行检测,发现19批次样品检出Xanthalin,说明该制剂存在水防风掺伪投料的风险,建议对该制剂投料的防风原料进行重点关注。
3 讨论
对龙泽熊胆胶囊中水防风掺伪的检测,TLC法检查应不得出现与Xanthalin对照品色谱相应的荧光斑点;若出现相应的斑点,则采用HPLC法进一步进行检测。HPLC法检查,供试品应不得出现与Xanthalin对照品保留时间相同的色谱峰;如出现保留时间相同的色谱峰,采用二极管阵列检测器检测,比较相应色谱峰在200~400 nm波长范围的紫外-可见吸收光谱;如紫外吸收光谱相同(对照品色谱峰在324 nm波长处有最大吸收),且色谱峰面积大于对照溶液的峰面积,视为阳性检出。必要时可采用超高效液相色谱-三重四极杆串联质谱法进一步确证。
3.1 薄层色谱条件的选择本研究对提取溶剂(乙醇、甲醇、乙酸乙酯)、提取时间(15、30、60 min)进行了考察。结果表明,用乙醇回流提取30 min,提取效率较高。考察了不同展开剂种类(正己烷∶乙酸乙酯、三氯甲烷∶甲醇∶水),不同展开剂配比,不同检视方法(紫外254、365 nm)对薄层色谱分析的影响,确定环己烷-乙酸乙酯(8∶3.5)为展开剂,置紫外光灯(365 nm)下检视为最佳检测条件。
3.2 液相色谱条件的选择比较了SHIMADZU InertSustain®C18(250mm×4.6mm,5μm)、SHISEIDO CAPCELL PAK C18MGⅡ(200mm×4.6mm,5μm)、Kromasil 100-5-C18(250 mm×4.6 mm,5μm)、Agilent Extent C18(250 mm×4.6 mm,5μm)等色谱柱。结果SHIMADZU InertSustain®C18(250mm×4.6mm,5μm)色谱柱对样品中Xanthalin的保留和分离效果较好,峰型尖锐,能实现水防风专属性成分的快速、有效的分离。还比较了不同流动相体系(乙腈-水、甲醇-水、乙腈-0.1%甲酸水)及不同流动相配比对色谱图峰型及待测成分分离度的影响。用乙腈-水(58∶42)作为流动相时,得到的色谱峰分离效果较好,基线较平稳。
3.3 质谱条件的优化比较了正、负离子扫描模式下,Xanthalin的响应强度。结果显示在正离子模式下该成分响应丰度高,且在MRM扫描模式下,通过改变碰撞能量,筛选出响应较高的碎片离子作为定量子离子。
3.4 限度的制订按照《中国药典》2020年版四部通则(0212)药材和饮片检定通则规定:药屑与杂质通常不得超过3%。考虑到防风药材与水防风药材性状鉴别易混淆,且存在交叉种植的可能。龙泽熊胆胶囊处方药味多,生产工艺为水煎提取,检测方法中供试品溶液的制备,可能导致Xanthalin转移率发生变化。经方法学考察,建议本品防风掺伪水防风的检查限度拟定为10%。
本研究基于TLC、HPLC、UPLC-MS/MS技术建立了龙泽熊胆胶囊中掺伪水防风的检测方法,该方法简便快速、专属性强、耐用性好。在对107批次龙泽熊胆胶囊的检验中发现,按现行《中国药典》该品种项下防风薄层色谱鉴别项检验,合格率为100%。以本研究建立的水防风成分检测方法对样品进行复检,发现19批次样品检出水防风的特征性成分Xanthalin,提示该品种存在水防风掺伪防风投料生产的情况。
中药真伪优劣鉴别是保证中药临床治疗效果、避免不良反应事件发生的关键。防风临床应用广泛,超过500种中成药含有防风,目前鉴别防风与水防风的检测方法主要针对药材和饮片[10-16],尚未见含防风制剂中水防风掺伪投料的相关研究报道。本研究建立的龙泽熊胆胶囊中水防风掺伪的TLC、HPLC、UPLC-MS/MS方法,填补了该领域研究的空白,为含防风的中成药补充检验方法提供了思路,为提升药品监管能力提供了技术支撑。

