酸藤子的化学成分研究
李婉亭,李志强,曾祥昊,余惠敏,钟国跃, 2,冯育林, 2*,何明珍, 2*
酸藤子的化学成分研究
李婉亭1,李志强1,曾祥昊1,余惠敏1,钟国跃1, 2,冯育林1, 2*,何明珍1, 2*
1. 江西中医药大学,江西 南昌 330006 2. 中药固体制剂制造技术国家工程研究中心,江西 南昌 330006
研究酸藤子的化学成分。利用硅胶、Sephadex LH-20、HP-20大孔吸附树脂、半制备高效液相等各种方法进行分离纯化,通过核磁共振波谱、质谱等对化合物的结构进行表征和解析。从酸藤子70%乙醇提取物的正丁醇萃取部位中分离得到19个化合物,分别鉴定为淫羊藿次苷D2(1)、山柰酚-3β葡萄糖-7α--鼠李糖苷(2)、反式对羟基桂皮酸(3)、咖啡酸(4)、槲皮素-3α--鼠李糖吡喃糖基-7β吡喃葡萄糖苷(5)、4-(β-吡喃葡萄糖基氧基)-苯甲醛(6)、1对羟基肉桂酰单甘油酯(7)、山柰酚-3β(2β呋喃糖基)-吡喃葡萄糖苷-7α--鼠李糖吡喃糖苷(8)、绿原酸(9)、反式咖啡酸(10)、对羟基肉桂酸甲酯(11)、反式-3香豆酰奎宁酸(12)、5-对反式香豆酰奎宁酸甲酯(13)、1-(3,4-二羟基肉桂酰基)-环戊二烯二醇(14)、槲皮素-3β呋喃芹糖-(1→2)-β吡喃葡萄糖-7α--吡喃鼠李糖苷(15)、槲皮素-3吡喃葡萄糖苷(16)、柽柳黄素3β葡萄糖苷-7α--鼠李糖苷(17)、-(3-((3,4,5-三羟基-6-(羟甲基)四氢-2-吡喃-2-基)氧基)丙基)肉桂酰胺(18)、-去氢南天竹啡碱(19)。其中化合物18为新化合物,命名为酸藤子碱苷,化合物1~3、5~8、11~15、17和19首次从酸藤子植物中分离得到。
酸藤子;淫羊藿次苷D2;反式对羟基桂皮酸;槲皮素-3α--鼠李糖吡喃糖基-7β吡喃葡萄糖苷;-去氢南天竹啡碱
酸藤子(L.) Mez为紫金牛科酸藤子属植物,是一种常用的民族药材。它广泛分布于中国、印度、越南、老挝、泰国和柬埔寨等地。酸藤子可用于治疗喉咙痛、消化不良、肠炎、月经不调、子宫出血、睾丸炎、类风湿性关节炎和外伤[1-2]。现代药理学研究表明,酸藤子具有多种生物活性,如抗肿瘤、抗氧化和抗炎活性。近年研究报道已从酸藤子中分离出多种类型的化合物,包括黄酮类、蒽醌类、木脂素、倍半萜类和酚酸类等[3]。
课题组对酸藤子70%乙醇提取物的正丁醇部位进行化学成分研究,共分离得到了19个化合物包括6个黄酮类化合物,11个苯丙素类化合物,1个苯丙醇类化合物,1个未见报道的生物碱类化合物,分别鉴定为淫羊藿次苷D2(icariside D2,1)、山柰酚-3β葡萄糖-7α--鼠李糖苷(kaempferol-3βglucose-7α--rhamnoside,2)、反式对羟基桂皮酸(-hydroxycinnamic acid,3)、咖啡酸(caffeic acid,4)、槲皮素-3α--鼠李糖吡喃糖基-7β吡喃葡萄糖苷(quercetin-3--α--rhamno- pyranosyl-7--β--glucopyranoside,5)、4-(β-吡喃葡萄糖基氧基)-苯甲醛[4-(β-glucopyranosyloxy)-benzaldehyde,6]、1对羟基肉桂酰单甘油酯(1-hydroxycinnamalyl monoglycerides,7)、山柰酚-3β(2β呋喃糖基)-吡喃葡萄糖苷-7α--鼠李糖吡喃糖苷(kaempferol-3β(2βapiofuranosyl)-glucopyranoside-7α--rhamnopyra- noside,8)、绿原酸(chlorogenic acid,9)、反式咖啡酸(-caffeic acid,10)、对羟基肉桂酸甲酯(methyl--coumarate,11)、反式-3香豆酰奎宁酸(-3coumaroylquinic acid,12)、5-对反式香豆酰奎宁酸甲酯(methyl 5--coumarylquinic acid,13)、1-(3,4-二羟基肉桂酰基)-环戊二烯二醇[1-(3,4-dihydroxycinnamoyl)-cyclopenta-2,5-diol,14]、槲皮素-3β呋喃芹糖-(1→2)-β吡喃葡萄糖-7α--吡喃鼠李糖苷(quercetin-3βfuranocelery- (1→2)-βglucopyranos-7α--rhamnopyranoside,15)、槲皮素-3吡喃葡萄糖苷(quercetin-3glucopyranoside,16)、柽柳黄素3β葡萄糖苷- 7α--鼠李糖苷(tamarixetin 3βglucoside-7α--rhamnoside,17)、-(3-((3,4,5-三羟基-6-(羟甲基)四氢-2-吡喃-2-基)氧基)丙基)肉桂酰胺[-(3-((3,4,5-trihydroxy-6-(hydroxymethyl) tetrahydro-2-pyran-2-yl)oxy)propyl)cinnamamide,18]、-去氢南天竹啡碱(-dehydronantenine,19)。其中,化合物18为新化合物,命名为酸藤子碱苷,并且化合物1~3、5~8、11~15、17和19首次从该植物中分离得到。本研究为酸藤子进一步的开发和利用提供了依据。
1 仪器与材料
Bruker avance 600型核磁共振仪(德国Bruker公司);Triple TOF 5600型高分辨质谱仪(美国AB Sciex公司);LC-XR20型高效HPLC色谱仪(日本Shimadzu公司);汉邦科技NP7005C型制备HPLC色谱仪(江苏汉邦科技有限公司);EYALA旋转蒸发仪(日本EYALA公司);MS304S分析天平 [梅特勒-托利多仪器(上海)有限公司];柱色谱硅胶(100~200、200~300、300~400目);GF254薄层色谱硅胶板(青岛海洋化工有限公司)。高效液相色谱和半制备液相色谱所使用的试剂均为色谱级,其他为分析级。
酸藤子药材于2014年9月购自安徽亳州药材市场,由江西中医药大学钟国跃教授鉴定为紫金牛科植物酸藤子(L.) Mez的干燥成熟果实。标本(20141001)保存在江西中医药大学。
2 提取与分离
酸藤子干燥果实10 kg,粉碎,用体积分数70%乙醇提取3次,每次1.5 h,合并乙醇提取液,滤过,减压浓缩溶剂至无醇味,干燥后,得粗提取物1178 g。将粗提取物加入适量水分散,依次用石油醚、二氯甲烷、醋酸乙酯、正丁醇萃取,萃取液减压浓缩、干燥得各部位提取物,其中石油醚部位112.9 g、二氯甲烷部位162.4 g、醋酸乙酯部位78.3 g、正丁醇部位180.6 g。
将正丁醇部位溶解后经HP-20大孔吸附树脂分离,依次以5倍柱体积的水、20%乙醇溶液、40%乙醇溶液、60%乙醇溶液、95%乙醇溶液梯度洗脱,得水部位35.64 g、20%乙醇部位92.51 g、40%乙醇部位79.52 g、60%乙醇部位102.80 g、95%乙醇部位30.40 g。
取20%乙醇部位(92.51 g)经MCI柱分离,依次以10%甲醇溶液、30%甲醇溶液、50%甲醇溶液、70%甲醇溶液、100%甲醇梯度洗脱,得到5个组分Fr. 1-1~1-5。组分Fr. 1-3经Sephadex LH-20凝胶柱色谱分离,甲醇-水梯度洗脱,得到5个组分Fr. 1-3-1~1-3-5,组分Fr. 1-3-3经半制备高效液相色谱分离,以甲醇-水(23∶77)为流动相,得到化合物1(7.0 mg);组分Fr. 1-3-4经半制备高效液相色谱分离,以甲醇-水(25∶75)为流动相,得到化合物3(8.6 mg)。组分Fr. 1-4经Sephadex LH-20凝胶柱色谱分离,甲醇-水梯度洗脱,得到5个组分Fr. 1-4-1~1-4-5,组分Fr. 1-4-2经半制备高效液相色谱分离,以甲醇-水(25∶75)为流动相,得到化合物2(317.3 mg);组分Fr. 1-4-4经半制备高效液相色谱分离,以甲醇-水(30∶70)为流动相,得到化合物4(15.6 mg)。组分Fr.1-5经Sephadex LH-20凝胶柱色谱分离,甲醇-水梯度洗脱,得到6个组分Fr. 1-5-1~1-5-6,组分Fr. 1-5-2经半制备高效液相色谱分离,以甲醇-水(30∶70)为流动相,得到化合物5(5.6 mg);组分Fr. 1-5-3经半制备高效液相色谱分离,以甲醇-水(31∶69)为流动相,得到化合物6(6.3 mg)。
取40%乙醇部位(79.52 g)经正向硅胶柱色谱分离,以二氯甲烷-甲醇梯度洗脱,得到9个组分Fr. 2-1~2-9。组分Fr.2-1经半制备高效液相色谱,以甲醇-水(30∶70)为流动相进行分离,得到化合物7(8.6 mg);组分Fr.2-3经Sephadex LH-20凝胶柱色谱,甲醇-水梯度洗脱,得到5个组分Fr. 2-3-1~2-3-5,组分Fr. 2-3-3经半制备高效液相色谱,以甲醇-水(33∶67)为流动相进行分离,得到化合物8(7.3 mg);组分Fr. 2-3-4经半制备高效液相色谱,以甲醇-水(36∶64)为流动相进行分离,得到化合物9(6.5 mg)。组分Fr. 2-5经Sephadex LH-20凝胶柱色谱,甲醇-水梯度洗脱,得到5个组分Fr. 2-5-1~2-5-5,组分Fr. 2-5-4经半制备高效液相色谱,以甲醇: 水(35∶65)为流动相进行分离,得到化合物10(6.4 mg)。组分Fr. 2-6经半制备高效液相色谱,以甲醇-水(34∶66)为流动相进行分离,得到化合物11(8.5 mg)。组分Fr. 2-7经Sephadex LH-20凝胶柱色谱,甲醇-水梯度洗脱,得到5个组分Fr. 2-7-1~2-7-5,组分Fr. 2-7-3经半制备高效液相色谱,以乙腈-水(15∶85)为流动相进行分离,得到化合物12(7.2 mg)。组分Fr.2-8经Sephadex LH-20凝胶柱色谱,甲醇-水梯度洗脱,得到4个组分Fr. 2-8-1~2-8-4,组分Fr. 2-8-3经半制备高效液相色谱,以乙腈-水(17∶83)为流动相进行分离,得到化合物13(11.8 mg)。组分Fr. 2-9经半制备高效液相色谱,以乙腈-水(19∶81)为流动相进行分离,得到化合物14(6.9 mg)。
取60%乙醇部位浸膏(102.80 g)经正向硅胶柱色谱分离,以二氯甲烷-甲醇梯度洗脱,得到8个组分Fr. 3-1~3-8。组分Fr. 3-3经半制备高效液相色谱乙腈-水(20∶80)分离,得到化合物15(18.6 mg);组分Fr. 3-4经半制备高效液相色谱乙腈-水(25∶75)分离,得到化合物16(15.4 mg);组分Fr. 3-6经半制备高效液相色谱乙腈-水(23∶77)分离,得到化合物17(9.5 mg);组分Fr. 3-7经半制备高效液相色谱乙腈-水(23∶77)分离,得到化合物18(8.6 mg);组分Fr. 3-8经半制备高效液相色谱乙腈-水(26∶74)分离,得到化合物19(18.5 mg)。
3 结构鉴定
化合物1:无色片晶(甲醇);HR-ESI-MS/: 299.113 6 [M-H]−(理论值299.113 1 [M-H]−),分子式为C14H20O7。1H-NMR (600MHz, DMSO-6): 7.12 (2H, d,= 8.4 Hz, H-2, 6), 6.93 (2H, d,= 8.4 Hz, H-3, 5), 4.80 (1H, d,= 7.8 Hz, H-1), 4.56 (2H, d,= 2.8 Hz, H-6), 3.56 (2H, t,= 7.2 Hz, H-α), 3.12~3.34 (4H, m, H-2~5), 2.67 (2H, t,= 7.2 Hz, H-β);13C-NMR (125 MHz, DMSO-6):156.2 (C-4), 133.2 (C-1), 130.1 (C-2, 6), 116.5 (C-3, 5), 101.1 (C-1), 77.5 (C-3), 77.1 (C-5), 73.7 (C-2), 70.2 (C-4), 62.9 (C-α), 61.2 (C-6), 38.7 (C-β)。以上波谱数据与参考文献报道基本一致[4],故鉴定化合物1为淫羊藿次苷D2。
化合物2:黄色针状晶体(甲醇);HR-ESI-MS/: 593.151 2 [M-H]−(理论值593.150 6 [M-H]−),分子式为C27H30O15。1H-NMR (600 MHz, DMSO-6): 12.61 (1H, s, 5-OH), 10.28 (1H, s, 4-OH), 8.10 (2H, d,= 8.9 Hz, H-2, 6), 6.91 (2H, d,= 8.9 Hz, H-3, 5), 6.84 (1H, d,= 2.2 Hz, H-8), 6.46 (1H, d,= 2.2 Hz, H-6), 5.56 (1H, d,= 1.8 Hz, Rha-H-1), 5.49 (1H, d,= 7.4 Hz, Glc-H-1), 1.12 (3H, d,= 6.2 Hz, Rha-H-6);13C-NMR (125 MHz, DMSO-6): 178.1 (C-4), 162.0 (C-7), 161.3 (C-5), 160.6 (C-4), 157.2 (C-2), 156.5 (C-9), 133.9 (C-3), 131.5 (C-2, 6), 121.3 (C-1), 115.6 (C-3, 5), 106.1 (C-10), 101.2 (Glc-C-1), 99.9 (C-6), 98.8 (Rha-C-1), 95.0 (C-8), 78.8 (Glc-C-5), 76.9 (Glc-C-3), 74.7 (Glc-C-2), 72.1 (Rha-C-4), 70.7 (Glc-C-4), 70.5 (Rha-C-3), 70.4 (Rha-C-2), 70.3 (Rha-C-5), 61.3 (Glc-C-6), 20.4 (Rha-C-6)。根据以上波谱数据与文献报道基本一致[5],故鉴定化合物2为山柰酚-3β葡萄糖-7α--鼠李糖苷。
化合物3:淡黄色粉末;HR-ESI-MS/: 163.040 1 [M-H]−(理论值163.039 5 [M-H]−),分子式为C9H8O3。1H-NMR (600 MHz, DMSO-6): 7.57 (1H, d,= 16.5 Hz, H-7), 7.54 (2H, d,= 8.8 Hz, H-2, 6), 6.81 (2H, d,= 8.3 Hz, H-3, 5), 6.35 (1H, d,= 16.2 Hz, H-8);13C-NMR (125 MHz, DMSO-6): 166.6 (C-9), 160.1 (C-4), 144.5 (C-7), 130.6 (C-2, 6), 125.7 (C-1), 116.3 (C-3, 5), 115.7 (C-8)。根据以上波谱数据与文献报道基本一致[6],故鉴定化合物3为反式对羟基桂皮酸。
化合物4:黄色粉末;HR-ESI-MS/: 179.035 0 [M-H]−(理论值179.034 4 [M-H]−),分子式为C9H8O4。1H-NMR (600MHz, DMSO-6): 7.48 (1H, d,= 15.6 Hz, H-7), 7.03 (1H, d,= 2.1 Hz, H-2), 6.99 (1H, dd,= 2.1, 8.2 Hz, H-6), 6.77 (1H, d,= 8.1 Hz, H-5), 6.22 (1H, d,= 15.9 Hz, H-8);13C-NMR (125 MHz, DMSO-6): 166.5 (C-9), 148.7 (C-4), 146.0 (C-7), 145.0 (C-9), 126.1 (C-1), 121.6 (C-6), 116.3 (C-8), 115.4 (C-5), 115.2 (C-2)。根据以上波谱数据与文献报道基本一致[7],故鉴定化合物4为咖啡酸。
化合物5:黄色粉末;HR-ESI-MS/: 609.145 1 [M-H]−,(理论值609.145 6 [M-H]−),分子式为C27H30O16。1H-NMR (600 MHz, DMSO-6): 7.64 (1H, d,= 2.0 Hz, H-2), 7.61 (1H, dd,= 2.0, 8.4 Hz, H-6), 6.87 (1H, d,= 8.4 Hz, H-5), 6.80 (1H, d,= 2.2 Hz, H-8), 6.44 (1H, d,= 2.2 Hz, H-6), 5.56 (1H, d,= 1.9 Hz, Rha-H-1), 5.50 (1H, d,= 7.4 Hz, Glc-H-1);13C-NMR (125 MHz, DMSO-6): 178.1 (C-4), 162.0 (C-7), 161.3 (C-5), 157.1 (C-2), 156.4 (C-9), 149.2 (C-4), 145.4 (C-3), 134.1 (C-3), 122.2 (C-6), 121.5 (C-1), 116.8 (C-2), 115.7 (C-5), 106.1 (C-10), 另外C: 101.2, 99.9, 78.1, 76.9, 74.5, 72.1, 70.7, 70.5, 70.4, 70.3, 61.4, 18.4分别为鼠李糖和葡萄糖的碳信号。根据以上波谱数据与参考文献报道基本一致[8],故鉴定化合物5为槲皮素-3α--鼠李糖吡喃糖基-7β吡喃葡萄糖苷。
化合物6:黄色粉末;HR-ESI-MS/: 283.081 9 [M-H]−(理论值283.081 8 [M-H]−),分子式为C13H16O7。1H-NMR (600 MHz, DMSO-6): 9.89 (1H, s, CHO), 7.88 (2H, d,= 8.3 Hz, H-3,H-5), 7.21 (2H, d,= 8.3 Hz, H-2, H-6), 5.05 (1H, d,= 7.2 Hz, H-1), 4.80 (2H, d,= 7.6 Hz, H-6), 3.12~3.34 (4H, m, H-2~5);13C-NMR (125 MHz, DMSO-6): 191.9 (C-7), 162.6 (C-1), 132.1 (C-5), 130.9 (C-3), 130.1 (C-4), 116.9 (C-6), 116.5 (C-2), 100.2 (C-1), 77.6 (C-3), 76.9 (C-5), 73.6 (C-2), 70.0 (C-4), 61.0 (C-6)。根据以上波谱数据与参考文献报道基本一致[9],故鉴定化合物6为4-(β-吡喃葡萄糖基氧基)-苯甲醛。
化合物7:白色无定型粉末;HR-ESI-MS/: 237.076 7 [M-H]−(理论值237.076 3 [M-H]−),分子式为C12H14O5。1H-NMR (600 MHz, DMSO-6): 10.05 (1H, s, OH), 7.56 (1H, d,= 16.6 Hz, H-α), 7.53 (2H, d,= 8.8 Hz, H-2, 6), 6.81 (2H, d,= 8.3 Hz, H-3, 5), 6.35 (1H, d,= 16.2 Hz, H-1β), 4.12 (1H, dd,= 4.7, 11.5 Hz, glycerol H-1α), 3.98 (1H, dd,= 7.7, 11.1 Hz, glycerol H-1β), 3.66 (1H, m, glycerol H-2), 3.38 (2H, m, glycerol H-3);13C-NMR (125 MHz, DMSO-6): 166.6 (C=O), 160.1 (C-4), 144.5 (C-β), 130.6 (C-2, 6), 125.7 (C-1), 116.2 (C-3, 5), 115.7 (C-α), 69.6 (C-2), 65.5 (C-1), 62.6 (C-3)。根据以上波谱数据与参考文献报道基本一致[10],故鉴定化合物7为1对羟基肉桂酰单甘油酯。
化合物8:浅黄色无定型粉末;HR-ESI-MS/: 725.193 0 [M-H]−(理论值725.192 9 [M-H]−),分子式为C32H38O19。1H-NMR (600 MHz, DMSO-6): 8.12 (2H, d,= 8.9 Hz, H-2, H-6), 6.88 (2H, d,= 8.9 Hz, H-3, 5), 6.83 (1H, d,= 2.2 Hz, H-8), 6.43 (1H, d,= 2.0 Hz, H-6), 5.63 (1H, d,= 7.6 Hz, H-1), 5.55 (1H, d,= 1.74 Hz, H-1), 5.40 (1H, d,= 1.7 Hz, H-1), 3.52~4.08 (14H, m, H-2~6, H-2, 4, 5, H-2~5), 1.28 (3H, d,= 6.0 Hz, H-6);13C-NMR (125 MHz, DMSO-6): 178.1 (C-4), 163.1 (C-7), 161.9 (C-5), 161.3 (C-2), 160.0 (C-4), 156.7 (C-9), 133.7 (C-3), 131.4 (C-2, 6), 121.2 (C-1), 115.6 (C-3, 5), 109.1 (C-1), 106.1 (C-10), 101.1 (C-1), 99.8 (C-6), 98.8 (C-1), 94.9 (C-8), 79.7 (C-3), 78.0 (C-2), 77.6 (C-3), 76.6 (C-2), 76.4 (C-5), 74.3 (C-4), 72.1 (C-4), 70.7 (C-3), 70.6 (C-2), 70.6 (C-4), 70.3 (C-5), 64.6 (C-5), 61.1 (C-6), 17.4 (C-6)。根据以上波谱数据与参考文献报道基本一致[11],故鉴定化合物8为山柰酚-3β(2β呋喃糖基)-吡喃葡萄糖苷-7α--鼠李糖吡喃糖苷。
化合物9:白色粉末;HR-ESI-MS/: 353.087 7 [M-H]−(理论值353.08 73 [M-H]−),分子式为C16H18O9。1H-NMR (600 MHz, DMSO-6): 7.48 (1H, d,= 15.8 Hz, H-7), 7.04 (1H, d,= 2.0 Hz, H-2), 6.97 (1H, dd,= 2.1, 8.2 Hz, H-6), 6.77 (1H, d,= 8.1 Hz, H-5), 6.22 (1H, d,= 15.9 Hz, H-8), 5.19 (1H, m, H-3), 3.84 (1H, m, H-5), 3.59 (1H, m, H-4), 1.82~2.07 (4H, m, H-2, 6);13C-NMR (125 MHz, DMSO-6): 177.0 (C-7), 166.6 (C-9), 148.7 (C-4), 146.0 (C-3), 144.9 (C-7), 126.2 (C-1), 121.6 (C-6), 116.3 (C-5), 115.5 (C-2), 115.1 (C-8), 73.4 (C-3), 71.6 (C-4), 71.4 (C-5), 68.0 (C-1), 36.1 (C-6), 35.8 (C-2)。根据以上波谱数据与参考文献报道基本一致[12],故鉴定化合物9为绿原酸。
化合物10:浅黄色针晶(甲醇);HR-ESI-MS/: 311.040 6 [M-H]−(理论值311.040 3 [M-H]−),分子式为C13H12O9。1H-NMR (600 MHz, DMSO-6): 7.48 (1H, d,= 15.8 Hz, H-7), 7.02 (1H, d,= 2.1 Hz, H-2), 6.98 (1H, dd,= 2.1, 8.2 Hz, H-6), 6.77 (1H, d,= 8.1 Hz, H-5), 6.22 (1H, d,= 16.0 Hz, H-8);13C-NMR (125 MHz, DMSO-6): 166.5 (C-9), 148.7 (C-4), 146.0 (C-7), 144.9 (C-3), 126.2 (C-1), 121.6 (C-6), 116.3 (C-5), 115.4 (C-2), 115.1 (C-8), 75.3 (C-10), 71.3 (C-11)。根据以上波谱数据与参考文献报道基本一致[13],故鉴定化合物10为反式咖啡酸。
化合物11:浅黄色胶状固体;HR-ESI-MS/: 177.055 3 [M-H]−(理论值177.055 2 [M-H]−),分子式为C10H10O3。1H-NMR (600 MHz, DMSO-6): 7.54 (1H, d,= 16.0 Hz, H-1), 7.49 (2H, d,= 8.2 Hz, H-2, 6), 6.82 (2H, d,= 8.5 Hz, H-3, 5), 6.31 (1H, d,= 16.0 Hz, H-2), 3.41 (3H, s, OCH3);13C-NMR (125 MHz, DMSO-6): 166.3 (C=O), 160.3 (C-4), 145.0 (C-1), 130.7 (C-2, 6), 125.6 (C-1), 115.2 (C-3, 5), 115.0 (C-2), 49.1 (-OCH3)。根据以上波谱数据与参考文献报道基本一致[14],故鉴定化合物11为对羟基肉桂酸甲酯。
化合物12:白色粉末;HR-ESI-MS/: 337.092 9 [M-H]−,(理论值337.092 3 [M-H]−),分子式为C16H18O8。1H-NMR (600 MHz, DMSO-6): 7.60 (1H, d,= 15.9 Hz, H-7), 7.56 (2H, d,= 8.7 Hz, H-2, 6), 6.81 (2H, d,= 8.5 Hz, H-3, 5), 6.43 (1H, d,= 15.9 Hz, H-8), 4.71 (1H, dd,= 2.9, 7.8 Hz, H-2), 4.11 (1H, m, H-1), 3.98 (1H, m, H-3), 1.80~2.10 (4H, m, H-4, 6);13C-NMR (125 MHz, DMSO-6): 176.0 (C-7), 166.8 (C-9), 160.2 (C-4), 144.9 (C-7), 133.1 (C-6), 130.7 (C-2), 125.6 (C-1), 116.3 (C-3), 115.2 (C-5), 115.1 (C-8), 77.4 (C-1), 74.5 (C-5), 66.8 (C-3), 64.5 (C-4), 40.5 (C-6), 38.3 (C-2)。根据以上波谱数据与参考文献报道基本一致[15],故鉴定化合物12为反式-3香豆酰奎宁酸。
化合物13:白色粉末;HR-ESI-MS/: 351.108 6 [M-H]−(理论值351.108 0 [M-H]−),分子式为C17H20O8。1H-NMR (600 MHz, DMSO-6): 7.60 (1H, d,= 15.8 Hz, H-7), 7.56 (2H, d,= 8.6 Hz, H-2, 6), 6.81 (2H, d,= 8.6 Hz, H-3, 5), 6.41 (1H, d,= 15.9 Hz, H-8), 4.71 (1H, m, H-1), 4.10 (1H, m, H-2), 3.61 (3H, s, OCH3), 3.94 (1H, m, H-3), 1.80~2.10 (4H, m, H-4, 6);13C-NMR (125 MHz, DMSO-6): 174.3 (C-7), 166.8 (C-9), 160.3 (C-4), 145.0 (C-7), 133.1 (C-2, C-6), 125.6 (C-1), 116.3 (C-3), 115.2 (C-5), 115.1 (C-8), 76.0 (C-1), 74.0 (C-5), 65.8 (C-3), 64.9 (C-4), 40.5 (C-6), 38.5 (C-2)。根据以上波谱数据与参考文献报道基本一致[16],故鉴定化合物13为5-对反式香豆酰奎宁酸甲酯。
化合物14:淡黄色固体;HR-ESI-MS/: 263.092 5 [M-H]−(理论值263.091 9 [M-H]−),分子式为C14H16O5。1H-NMR (600 MHz, DMSO-6): 7.56 (1H, d,= 16.0 Hz, H-7), 7.54 (2H, d,= 8.8 Hz, H-2, 6), 6.81 (2H, d,= 8.6 Hz, H-3, 5), 6.36 (1H, d,= 15.9 Hz, H-8), 5.23 (1H, m, H-1), 4.88 (1H, m, H-2), 3.80 (1H, m, H-5), 1.70~1.90 (4H, m, H-3, 4);13C-NMR (125 MHz, DMSO-6): 166.6 (C-9), 160.1 (C-4), 144.5 (C-7), 133.1 (C-2), 130.6 (C-6), 125.7 (C-1), 116.3 (C-3), 115.3 (C-5), 115.1 (C-8), 73.4 (C-1), 71.3 (C-2), 68.3 (C-5), 40.5 (C-3), 35.8 (C-4)。根据以上波谱数据与参考文献报道基本一致[17],故鉴定化合物14为1-(3,4-二羟基肉桂酰基)-环戊二烯二醇。
化合物15:黄色粉末;HR-ESI-MS/: 741.188 4 [M-H]−(理论值741.187 8 [M-H]−),分子式为C32H38O20。1H-NMR (700 MHz, DMSO-6): 7.72 (1H, dd,= 2.2, 8.7 Hz, H-6), 7.58 (1H, d,= 2.2 Hz, H-2), 6.84 (1H, d,= 8.5 Hz, H-5), 6.79 (1H, d,= 2.2 Hz, H-8), 6.42 (1H, d,= 2.1 Hz, H-6), 5.63 (1H, d,= 7.7 Hz, Glc-H-1), 5.56 (1H, m, Rha-H-1), 5.36 (1H, d,= 1.4 Hz, Api-H-1), 1.21 (3H, d,= 6.0 Hz, Rha-CH3);13C-NMR (125 MHz, DMSO-6): 177.9 (C-4), 161.9 (C-7), 161.3 (C-5), 156.7 (C-9), 156.3 (C-2), 149.3 (C-4), 145.5 (C-3), 133.9 (C-3), 122.6 (C-1), 121.4 (C-6), 116.4 (C-5), 115.7 (C-2), 109.1 (Api-C-1), 106.1 (C-10), 99.8 (Glc-C-1), 98.9 (C-6), 98.8 (Rha-C-1), 94.6 (C-8), 79.7 (Api-C-3), 78.0 (Glc-C-2), 77.6 (Api-C-2), 77.4 (Glc-C-5), 76.6 (Glc-C-3), 74.4 (Api-C-4), 72.0 (Rha-C-4), 70.7 (Rha-C-2), 70.6 (Rha-C-3), 70.5 (Rha-C-5), 70.3 (Glc-C-4), 64.7 (Api-C-5), 61.3 (Glc-C-6), 17.9 (Rha-C-6)。根据以上波谱数据与参考文献报道基本一致[18],故鉴定化合物15为槲皮素-3β呋喃芹糖-(1→2)-β吡喃葡萄糖-7α--吡喃鼠李糖苷。
化合物16:黄色粉末;HR-ESI-MS/: 464.088 2 [M-H]−,(理论值464.087 7 [M-H]−),分子式为C21H20O12。1H-NMR (700 MHz, DMSO-6): 12.6 (1H, s, 5-OH), 7.58 (1H, dd,= 2.0, 8.4 Hz, H-6), 7.57 (1H, d,= 2.0 Hz, H-2), 6.84 (1H, d,= 9.0 Hz, H-5), 6.41 (1H, d,= 1.9 Hz, H-8), 6.20 (1H, d,= 2.0 Hz, H-6), 5.47 (1H, d,= 7.0 Hz, Glc-H-1);13C-NMR (125 MHz, DMSO-6): 177.7 (C-4), 164.8 (C-7), 161.7 (C-5), 156.8 (C-2), 156.6 (C-9), 148.9 (C-4), 145.3 (C-3), 133.7 (C-3), 122.0 (C-6), 121.6 (C-1), 116.6 (C-5), 115.7 (C-2), 104.4 (C-10), 101.1 (C-1), 99.2 (C-6), 93.9 (C-8), 78.0 (C-5), 76.9 (C-3), 74.5 (C-2), 70.4 (C-4), 61.4 (C-6)。根据以上波谱数据与参考文献报道基本一致[19],故鉴定化合物16为槲皮素-3吡喃葡萄糖苷。
化合物17:黄色粉末;HR-ESI-MS/: 623.161 8 [M-H]−,(理论值623.161 2 [M-H]−),分子式为C28H32O16。1H-NMR (700 MHz, DMSO-6): 7.63 (1H, d,= 2.0 Hz, H-6), 7.61 (1H, dd,= 8.2, 2.2 Hz, H-2), 6.85 (1H, d,= 9.1 Hz, H-5), 6.79 (1H, d,= 2.1 Hz, H-8), 6.43 (1H, d,= 2.2 Hz, H-6), 5.55 (1H, d,= 1.8 Hz, Rha-H-1), 5.48 (1H, d,= 7.4 Hz, Glc-H-1), 3.63 (3H, s, -OCH3);13C-NMR (125 MHz, DMSO-6): 178.1 (C-4), 162.0 (C-7), 161.3 (C-5), 157.1 (C-2), 156.4 (C-9), 149.1 (C-4), 145.3 (C-3), 134.1 (C-3), 122.2 (C-6), 121.5 (C-1), 116.8 (C-2), 115.7 (C-5), 106.1 (C-10), 101.2 (Glc-C-1), 99.8 (C-6), 98.9 (Rha-C-1), 94.8 (C-8), 78.1 (Glc-C-5), 76.9 (Glc-C-3), 74.5 (Glc-C-2), 72.1 (Rha-C-4), 70.7 (Glc-C-4), 70.5 (Rha-C-3), 70.4 (Rha-C-2), 70.3 (Rha-C-5), 61.4 (Glc-C-6), 49.1 (OCH3), 20.4 (Rha-C-6)。根据以上波谱数据与参考文献报道基本一致[20],故鉴定化合物17为柽柳黄素3β葡萄糖苷-7α--鼠李糖苷。
化合物18:黄色粉末;HR-ESI-MS/: 368.170 7 [M+H]+,(理论值368.170 9 [M+H]+),结合核磁波谱数据推测分子式为C18H25NO7。1H-NMR (700 MHz, DMSO-6) 中[H7.57 (2H, d,= 7.4 Hz), 7.41 (2H, d,= 7.7 Hz), 7.37 (1H, t,= 8.0 Hz)]为1组苯环单取代信号,[H7.40 (1H, d,= 16.1 Hz), 6.65(1H, d,= 15.8 Hz)] 为反式双键信号。1H-NMR 中[H4.15 (1H, d,= 7.8 Hz)] 为糖端基质子信号,13C-NMR (125 MHz, DMSO-6) 中C103.3处的信号为糖端基碳信号,并有C73.9, 77.3, 70.5, 77.2, 61.6归属于糖基的其他碳信号,以上证明化合物18的结构中含有β葡萄糖取代基。化合物18的13C-NMR谱C165.4显示有羰基碳,1H-NMR谱中H8.12 (1H, dd,= 5.7, 11.4 Hz) 处可见活泼氢信号,推测存在酰胺基团。DEPT谱显示有3个CH2信号,分别为C36.6, 29.7, 67.1,HMBC谱(图1)中观察到3个CH2基团中氢信号与碳信号相互关联,证明了丙基的存在。且H-10 (H3.25) 与C-9 (165.4) 连。综合以上波谱数据鉴定化合物18为-(3-((3,4,5-三羟基-6-(羟甲基)四氢-2-吡喃-2-基)氧基) 丙基)肉桂酰胺,通过SciFinder检索确定为未见报道的新化合物,命名为酸藤子碱苷。其NMR数据归属见表1。
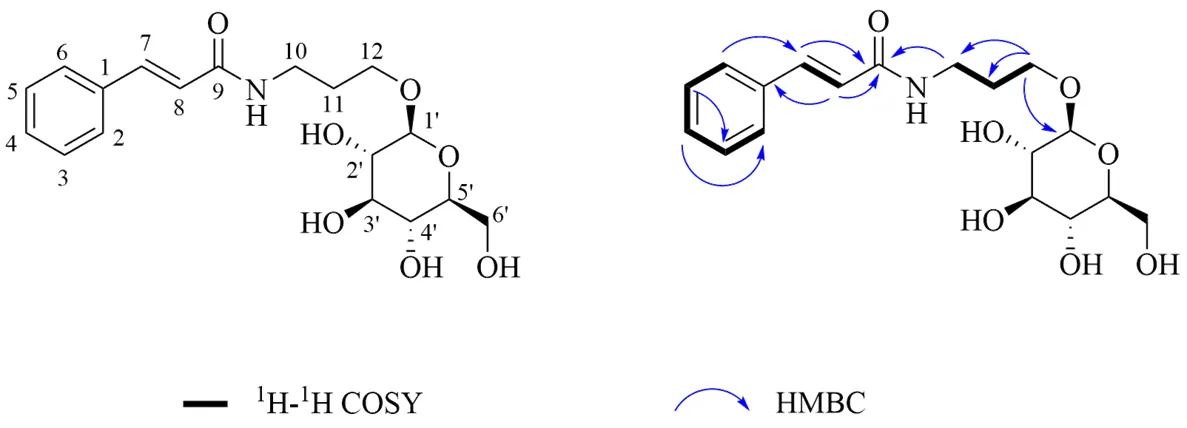
图1 化合物18的1H-1H COSY 和HMBC关键信号

表1 化合物18的NMR数据归属
化合物19:无色针状晶体(甲醇);HR-ESI-MS/: 338.139 1 [M+H]+,(理论值338.139 2 [M+H]+),分子式为C20H19NO4。1H-NMR (700 MHz, DMSO-6): 8.79 (1H, s, H-11), 7.19 (1H, s, H-8), 7.17 (1H, s, H-3), 6.60 (1H, s, H-7), 6.07 (2H, s,CH2-), 3.93 (3H, s, 1CH3), 3.76 (3H, s, 2CH3), 3.29 (4H, m, H-4, 5), 2.97 (3H, s, --CH3);13C-NMR (125 MHz, DMSO-6): 150.8 (C-2), 147.3 (C-1), 144.8 (C-9), 144.3 (C-10), 142.7 (C-6a), 131.9 (C-3a), 130.0 (C-7a), 125.1 (C-1a), 118.4 (C-3b), 118.1 (C-11a), 111.7 (C-3), 105.5 (C-11), 104.3 (C-8), 102.1 (C-7), 101.2 (-CH2-O), 59.7 (1-OCH3), 56.6 (2-OCH3), 50.1 (C-5), 31.6 (-CH3), 30.9 (C-4)。根据以上波谱数据与参考文献报道基本一致[21],故鉴定化合物19为-去氢南天竹啡碱。
利益冲突 所有作者均声明不存在利益冲突
[1] 倪绍伟, 闻程志,叶洋洋, 等. 酸藤子化学成分研究 [J]. 中药材, 2022, 45(12): 2900-2903.
[2] 张仲敏, 周凤玲, 陈振兴. 瑶药酸藤子的研究进展 [J]. 广西中医药大学学报, 2021, 24(1): 69-73.
[3] 杨林军, 黄文平, 黎田儿, 等. 酸藤子属植物的研究进展 [J]. 中药材, 2015, 38(8): 1761-1767.
[4] 邵莉, 黄卫华, 张朝凤, 等. 兜唇石斛的化学成分研究 [J]. 中国中药杂志, 2008, 33(14): 1693-1695.
[5] 昶国平, 李广雷, 刘博譞, 等. 小花棘豆的化学成分研究 [J]. 中医药学报, 2014, 42(4): 15-16.
[6] 魏健, 杨小生, 朱海燕, 等. 短尾越橘化学成分研究 [J]. 广西植物, 2008, 28(4): 558-560.
[7] 黄婉凤, 何佳, 张琛伟, 等. 救必应中2个新的咖啡酸半萜酯[J]. 中草药, 2023, 54(8): 2365-2372.
[8] 孟江, 董晓萍, 姜志宏, 等. 鲜鱼腥草的黄酮类化合物研究 [J]. 中国中药杂志, 2006, 31(16): 1335-1337.
[9] Leong G, Uzio R, Derbesy M. Synthesis, identification and determination of glucosides present in greenbeans (Andrews) [J]., 1989, 4(4): 163-167.
[10] 王伟, 丁怡, 邢东明, 等. 菠萝叶酚类成分研究 [J]. 中国中药杂志, 2006, 31(15): 1242-1244.
[11] Hisaeda A, Matsunami K, Otsuka H,. Flavonol glycosides from the leaves of[J]., 2011, 65(2): 360-363.
[12] 李菲, 赵新亚, 赵雪梅, 等. 银花青蒿栀子方抗A6型柯萨奇病毒活性成分的分离 [J]. 中草药, 2022, 53(5): 1365-1371.
[13] 粟杰, 冯艳, 林炳锋, 等. 刺五加化学成分的分离与鉴定[J]. 中草药, 2021, 52(16): 4783-4788.
[14] 曾鹏, 张勇, 潘晨, 等. 巴东过路黄酚类化学成分研究 [J]. 药学学报, 2013, 48(3): 377-382.
[15] 徐贞权, 何明珍, 姚闽, 等. 杏香兔耳风化学成分研究 [J]. 中草药, 2023, 54(6): 1728-1735.
[16] 李飞飞, 柴兴云, 徐正仁, 等. 爪哇脚骨脆的化学成分研究[J]. 中草药, 2008, 39(7): 984-986.
[17] Wang H B, Muraleedharan G. Novel antioxidant compounds from() [J]., 1999, 62: 1-3.
[18] 史小平, 苏聪, 齐博文, 等. 地桃花中黄酮苷类成分研究 [J]. 中国药学杂志, 2017, 52(19): 1670-1674.
[19] 张普照, 钟国跃, 谢文伟, 等. 熏倒牛中黄酮类成分研究 [J]. 中草药, 2016, 47(20): 3565-3568.
[20] 付文婷, 胡兰, 古丽米热·阿不都热依木, 等. 新疆中亚沙棘化学成分的分离和纯化 [J]. 新疆医科大学学报, 2009, 32(5): 570-571.
[21] Jiang H Z. Chemical composition and cytotoxic activity ofvar.[J]., 2022, 56: 101-104.
Chemical constituents of
LI Wanting1, LI Zhiqiang1, ZENG Xianghao1, YU Huimin1, ZHONG Guoyue1, 2, FENG Yulin1, 2, HE Mingzhen1, 2
1. Jiangxi University of Chinese Medicine, Nanchang 330006, China 2. National Engineering Research Center for Manufacturing Technology of Chinese Medicine Solid Preparation, Nanchang 330006, China
To study the chemical constituents fromThe compounds were separated and purified by various methods such as silica gel, Sephadex LH-20, HP-20 macroporous resin adsorption, semi-preparative high-performance liquid phase, and the structure of the compounds were identified and analyzed by nuclear magnetic resonance spectrometry and mass spectrometry.A total of nineteen compounds were isolated from the n-butanol extraction site of 70% ethanol extract ofand identified as icariside D2(1), kaempferol-3--β--glucose-7--α--rhamnoside (2),-hydroxycinnamic acid (3), caffeic acid (4), quercetin-3--α--rhamnopyranosyl-7--β--glucopyranoside (5), 4-(β-glucopyranosyloxy)-benzaldehyde (6), 1---hydroxycinnamalyl monoglycerides (7), kaempferol-3--β--(2--β--apiofuranosyl)-glucopyranoside-7--α--rhamnopyranoside (8), chlorogenic acid (9),-caffeic acid (10), methyl--coumarate (11),-3--coumaroylquinic acid (12), methyl 5--coumarylquinic acid (13), 1-(3,4-dihydroxycinnamoyl)-cyclopenta-2,5-diol (14), quercetin-3--β--furano-celery-(1→2)-β--glucopyranos-7--α--rhamnopyranoside (15), quercetin-3--glucopyranoside (16), tamarixetin 3--β--glucoside-7--α--rhamnoside (17),-(3-((3,4,5-trihydroxy-6-(hydroxymethyl)tetrahydro-2-pyran-2-yl)oxy)propyl)cinnamamide (18),-dehydronantenine (19).Among them, compound 18 is a new compound, named embelia alkali glycoside, and compounds 1—3, 5—8, 11—15, 17 and 19 were isolated fromfor the first time.
(L.) Mez; icariside D2;-hydroxycinnamic acid; quercetin-3--α--rhamnopyranosyl-7--β--glucopyranoside;-dehydronantenine
R284.1
A
0253 - 2670(2024)09 - 2868 - 07
10.7501/j.issn.0253-2670.2024.09.002
2024-03-25
国家重点研发计划课题(2019YFC1712302);国家重点研发计划课题(2019YFC1712304);中央引导地方科技发展专项项目(20221ZDD02007);江西中医药大学科技创新团队(CXTD22001)
李婉亭(1999—),女,硕士研究生,从事中药活性成分研究。E-email: 1556242497@qq.com
通信作者:冯育林,男,博士,教授,从事中药药效物质及新药研究。E-mail: fengyulin2003@126.com
何明珍,女,博士,副教授,从事中药活性成分研究工作。E-mail: hmz07@163.com
[责任编辑 王文倩]

