高频超声指导甲状腺微小乳头状癌颈部淋巴结转移识别的价值
蓝新连 华绪俊 龚旺生
福建省上杭县医院 364299
甲状腺微小乳头状癌(Papillary thyroid microcarcinoma,PTMC)是各直径均<1cm的甲状腺乳头状癌[1-2],针对其较难察觉的特点,目前临床常用超声引导下的细针穿刺细胞学检查进行确诊,细针穿刺细胞学检查虽有独特的生物学行为且预后较好[3],但仍属有创性检查。高频超声是具有可重复性且安全无创的检查方法[4],对直径2~3mm的原发结节有较高的敏感度,在诊断PTMC时常表现为结节形态欠规则,边界不清和纵横比>1,同时可清晰显示结节的部位以及与周围组织的生长关系,可为临床提供更为全面和细致的评估等辅助工作。而对PTMC颈部淋巴结转移(Lymph node metastasis,LNM)通常显示为淋巴门消失、纵横比<2、皮髓质分界不清和结节内部发生沙粒样钙化等表现。本研究旨在探讨高频超声指导PTMC患者LNM的识别价值,现报道如下。
1 资料与方法
1.1 一般资料 选取2021年1月—2023年1月在本院经病理确诊且接受手术治疗的98例PTMC患者。(1)纳入标准:①均行甲状腺(次)全切患侧/双侧淋巴结清扫术,术后经病理检查确诊为PTMC;②术前均行高频超声检查,提示结节靠近甲状腺被膜,与甲状腺被膜关系密切;③未进行药物干预或甲状腺放射性碘治疗者。(2)排除标准:①心肺功能异常,不满足手术指征;②未接受手术治疗;③结节内有粗大钙化,导致后方伴声影,影响超声图像准确分析。将所选的98例PTMC患者分组为转移组(n=34)和未转移组(n=64)。转移组男21例,女13例;年龄22~50岁,平均年龄(36.45±3.56)岁;结节部位:左侧叶18例、右侧叶10例、峡部6例;数量:单发21例、多发13例;回声:低回声22例、等(高)回声12例;边界:边界清9例、边界不清25例。非转移组男35例,女29例;年龄22~50岁,平均年龄(36.54±3.61)岁;结节部位:左侧叶28例、右侧叶26例、峡部10例;数量:单发38例、多发26例;回声:低回声39例、等(高)回声25例;边界:边界清18例、边界不清46例。两组性别、年龄以及结节部位、数量、回声、边界等指标均无显著差异(P>0.05)。
1.2 方法 采用美国GE晶准彩色多普勒超声诊断仪(型号:Logiq E9 ;探头:L6-15;频率:6~15MHz)对两组PTMC患者进行颈部扫查:(1)嘱患者取仰卧位后颈部呈过伸位,避免吞咽动作和咳嗽。(2)扫描患者双侧颈部及淋巴结区,根据结节位置调节焦点、深度,聚焦区位于甲状腺底部,采用纵、横、斜切等多平面结合方式扫描和测量结节大小、边界、数量、纵横比,观察结节位置、内部回声、结节内部钙化及周边的血流分布情况。
1.3 观察指标 比较转移组患者和未转移组结节大小、形态、内部钙化、侵及被膜和血流分布等超声特征。
1.4 统计学方法 采用SPSS22.0统计学软件进行分析整理,计数资料用率表示,采用χ2检验,采用Logistic回归分析,绘制ROC曲线评估高频超声特征对PTMC伴LNM的预测价值,P<0.05提示有统计学意义。
2 结果
2.1 两组患者超声指标特征比较 两组患者关于结节形态、内部钙化、侵及被膜和血流分布等超声特征有明显差异(P<0.05),结节大小无明显差异(P>0.05)。见表1。

表1 两组患者超声特征比较(n)
2.2 PTMC伴LNM高频超声特征Logistic分析 对PTMC伴LNM的因素进行变量赋值,大小:≥5mm=1,<5mm=0;形态:纵横比≥1=1,纵横比<1=0;内部钙化:有=1,无=0;侵及被膜:有=1,无=0;血流分布:有=1,无=0。经Logistic分析,纵横比、内部钙化、侵及被膜、血流分布对PTMC伴LNM具有正向预测价值。见表2。
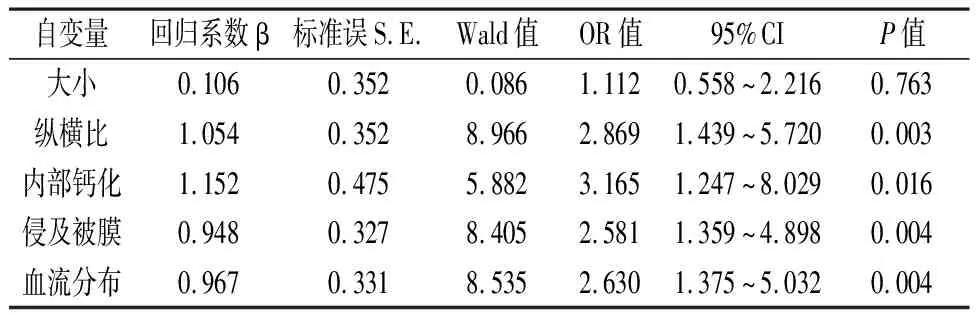
表2 PTMC伴LNM高频超声特征Logistic分析
2.3 高频超声特征对PTMC伴LNM诊断效能的ROC曲线分析 使用ROC曲线评价高频超声特征对PTMC伴LNM的预测价值,敏感度和特异度分别为88.20%、78.10%,AUC为0.832,95%CI 为0.745~0.919,见图1。
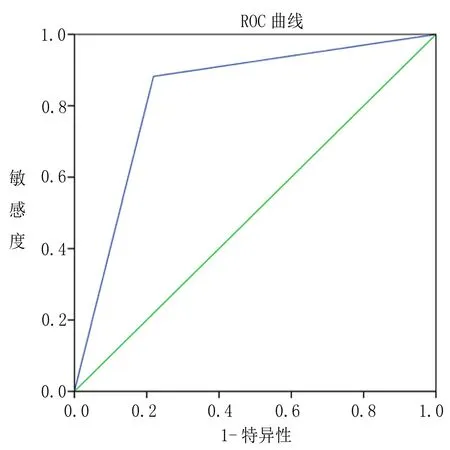
图1 高频超声特征对PTMC伴LNM诊断效能的ROC曲线分析
3 讨论
PTMC是影响患者生活质量的重要因素,其虽进展缓慢,但具有较高的侵袭性[5-7],且该区域血供丰富,生长情况较好,从而提高LNM的发生情况。常规二维超声针对颈部淋巴结形态、内部回声以及血流等特征显示欠清,且由于机体气管、锁骨和胸骨等解剖结构的干扰,对于<5mm的淋巴结敏感性较低,从而使LNM不典型图像或仅出现少数转移特征时出现漏诊情况发生。高频超声可通过对PTMC的结节特征进行扫描,并在检查过程中评估其淋巴结转移的可能性和危险性。
在本研究中,两组患者关于结节形态、内部钙化、侵及被膜和血流分布等超声特征有明显差异。因两组患者均为PTMC患者,在超声检查中结节部位、数量、回声及边界等超声指标方面均无明显差异,然而在形态、内部钙化、侵及被膜和血流分布等超声特征有明显差异。分析本研究结果,首先,高频超声是甲状腺疾病目前首选的影像学检查手段,与恶性相关的二维超声声像图表现有结节部位、数量、回声等指标,但这些指标的准确性较低,尚不能作为恶性病变和转移的诊断标准。其次,在正常甲状腺组织中,甲状腺细胞密度较低,良性病变细胞密度呈上升趋势,而PTMC患者的甲状腺细胞是由实质细胞、脂肪组织和纤维化组织所构成,病理结构较为复杂,探查PTMC的转移情况需具有高特异性指标进行诊断。最后,边界不清代表肿瘤细胞的侵袭力和增殖力较强,是LNM的常见指标[8-9],部位、数量和回声等指标也属LNM的常见指标。但内部钙化主要是因为在PTMC影响机体的前提下,部分肿瘤细胞因无法获得机体营养而发生坏死,钙盐沉积后所形成。侵及被膜是指结节达到甲状腺被膜的边界,患者发生LNM的可能性较高。血流分布是因为甲状腺内有丰富的淋巴通路,可为腺体内转移创造较好的便利条件。因转移组患者已经发生LNM,故导致上述指标发生变化。马哲强等[10]研究显示,经高频超声检测,结节内部钙化和血流分布是甲状腺癌患者合成LNM的重要指标,与本研究部分相似,说明可通过高频超声的结节形态、内部钙化、侵及被膜和血流分布等指标进行PTMC伴LNM诊断。
在本研究中,经Logistic分析,纵横比、内部钙化、侵及被膜、血流分布对PTMC伴LNM具有正向预测价值。分析本研究结果,一方面PTMC作为恶性肿瘤多呈浸润性生长,淋巴结内部结构尚不完整,而良性淋巴结分布范围较广,恶性淋巴结分布范围较为局限[11-12],恶性淋巴结通常存在纵横比>1和血流丰富的特征;结节内部钙化是因为结节坏死后液化钙盐或组织分泌的钙化物质的长期沉积所导致,在高频超声的显示下变现为多个点状强回声。另一方面,在本研究中所使用ROC曲线评价高频超声特征对PTMC伴LNM的预测价值中,敏感度和特异度分别为88.20%、78.10%,具有较高的诊断可靠性,有助于患者通过高频超声检查诊断LNM的风险,为患者的后期诊疗提供较好的选择。
综上所述,高频超声诊断PTMC伴LNM时,结节形态、内部钙化、侵及被膜和血流分布等指标具有正向预测价值。

