生酮饮食治疗CDKL5基因突变所致婴儿痉挛症1例报告并文献复习
王春雨,王琳琳,南在元,刘爽,张哲
首都医科大学附属北京儿童医院黑龙江医院(哈尔滨医科大学附属第六医院),哈尔滨 150010
CDKL5 基因全称为细胞周期依赖蛋白激酶样蛋白5(cyclin-dependent kinase-like 5,CDKL5),是X染色体连锁基因,定位于Xp22.13,编码丝氨酸-苏氨酸蛋白激酶,在大脑中广泛分布,是大脑正常发育的必需蛋白。CDKL5 蛋白在大脑中行使激酶功能,它可以通过磷酸化下游底物,从而改变其他蛋白的活性,参与神经发育及神经功能的发挥[1]。多项研究显示,CDKL5 基因突变涵盖的表型谱广泛,临床症状与婴儿痉挛症、Rett 综合征、Angelman 综合征、自闭症等存在交叉部分,多数表现为重度的发育迟缓、婴幼儿早发性难治性癫痫、重度的肌张力障碍、类Rett 综合征、类Angelman 综合征等,称为CDKL5基因相关早发性癫痫性脑病,又称CDKL5 基因相关疾病[2]。癫痫发作通常是CDKL5 基因相关疾病的核心症状,患儿通常表现出三个阶段的癫痫发作:Ⅰ期是早期癫痫,多表现为强直发作(发病1~10 周),脑电图正常。Ⅱ期是发育性癫痫,通常伴有婴儿痉挛,发作间期脑电图高度失律。Ⅲ期多表现为晚期,局灶性发作、肌阵挛发作和阵挛性发作,也可为强直发作及不典型失神发作等[3],均逐渐发展为难治性癫痫,同时可合并有严重精神运动发育迟滞,如竖头不稳、不会说话等,常有肌张力低下的表现。使用激素联合多种抗癫痫发作药物治疗欠佳的CDKL5 基因突变所致婴儿痉挛症1 例,应用生酮饮食(ketogenic diet,KD)治疗后,患儿在癫痫发作、运动及智力方面均有一定改善,特总结如下。
1 病例报告
1.1 基本情况 患儿男,2 月16 天,主因“间断抽搐20 余日”于2020 年7 月入院。患儿出生后1 月24 天起出现抽搐发作,表现为双目凝视、双拳紧握、头后仰、双侧肢体抖动,以右侧为著,每次发作持续数秒钟至1 分钟自行缓解,每日均有发作。外院给予左乙拉西坦口服无明显好转故来我院。住院后第4 天抽搐发作形式改变,表现为单下或成串的短暂点头伴四肢屈曲或伸展样强直,发作多于睡醒后短时间内出现,伴大哭,成串发作时,每串5~20 下,3~4 串/d。患儿G2P1,正常顺产,无生后窒息史,出生时无脐带绕颈,羊水及胎盘情况正常。其母孕第1 胎为死胎,母亲否认疾病史,患儿直系亲属否认癫痫病史。患儿生后混合喂养,进乳良好,体重增长良好。
1.2 体格检查 意识清楚,精神可,呼吸平稳,面色正常,头围:37 cm,体重:6.5 kg,前囟平坦,为1.0 cm×1.0 cm,周身未见皮疹及出血点,浅表淋巴结未触及肿大。咽部正常,肺部听诊未闻及干湿啰音,心脏听诊节律规整,无心律失常,心率126 次/min,未闻及收缩期和舒张期杂音。腹部平坦、柔软,肝脾肋下未触及,脊柱未见异常,四肢末梢温暖。神经系统查体:意识清楚,精神可,双球结膜无水肿,无颅神经瘫痪,四肢肌力Ⅴ级,肌张力无增高或减低,双膝腱反射、跟腱反射正常引出,浅反射正常,双巴氏征阴性,颈强阴性,克氏征、布什征阴性。
1.3 辅助检查资料 视频脑电图:高度失律,监测到痉挛发作(图1a,1b)。头磁共振+脑功能成像:双侧额颞极脑外间隙略宽;颅脑DWI 未见明显异常(图2a,2b)。血常规、血生化、血氨、血乳酸等相关代谢指标:未见明显异常。甲状腺功能、甲状旁腺素:未见异常。心脏超声、腹部超声、胸片:未见异常。血尿代谢筛查:阴性。染色体核型分析未见异常。经医院伦理委员会通过,患儿父母即监护人签署基因检测知情同意书后,同时收集患儿及父母外周血样本,委托第三方智因东方转化医学研究中心检验。患儿血液标本进行高通量测序,父母血液标本进行验证。全基因组测序结果发现:患儿CDKL5基 因chrX:18638087,c.2376+1(IVS16)G >A,(NM_001323289),嵌合新生变异,其父母无此位点的突变,为致病变异(图3a,3b,3c),为X 连锁显性遗传。
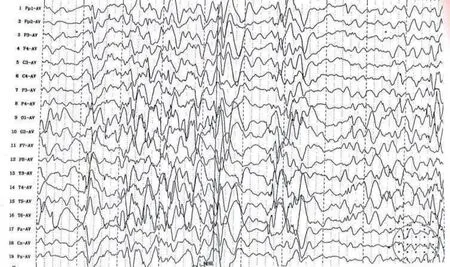
图1a 视频脑电图睡眠期高度失律

图2a 头颅磁共振水平面双侧额颞极脑外间隙略宽

图3 家系CDKL5测序峰图
1.4 诊断、治疗和随访 患者诊断:癫痫(局灶性发作、痉挛发作),婴儿痉挛症,CDKL5 相关发育性癫痫性脑病。治疗:患儿诊断为婴儿痉挛症后,给予促肾上腺皮质激素(ACTH)12.5 IU 静脉滴注2 周,减停左乙拉西坦换用托吡酯抗癫痫发作治疗,发作有减少,但仍有发作,ACTH 加量为25 IU 静脉滴注2 周,加用丙戊酸钠联合抗癫痫发作治疗,ACTH 共应用4 周发作停止,脑电图改善,序贯醋酸泼尼松口服,激素共12 周减停。1 个月后(6.5 月龄)患儿再次出现痉挛发作,5~6 串/d,5~15 下/串,且发作逐渐增多,加用氨己烯酸口服并逐渐加量,发作减少,但仍有每日3~4 串发作,并逐渐出现发育倒退。2 个月后(2021.01.05,患儿8.5 月龄)患儿仍不能独坐,出现翻身困难,四肢肌张力减低,仍有痉挛发作,每日2~3 串。患儿完善血尿代谢筛查及基因检测排除生酮饮食禁忌证后,开始给予生酮饮食治疗。生酮饮食采用生酮奶,开始时脂肪与(碳水化合物+蛋白质)的质量比为2 ∶1,根据患儿耐受情况逐渐调整至3 ∶1~4 ∶1,使血酮维持在3~5 mmol/L,血糖维持在4~5 mmol/L,口服托吡酯、丙戊酸钠、氨己烯酸抗癫痫发作。生酮饮食治疗3 个月后,癫痫发作明显减少,痉挛发作2~5 日1 次。坚持生酮饮食2 年,痉挛发作消失,运动发育进步,可翻身、独坐,脑电图改善,无高度失律(图4a,4b)。但因患儿反复患“支气管肺炎”及“重症肺炎”,进食生酮奶及生酮食品时反复呛奶及呕吐,患儿体重减轻明显,3 岁时(2023 年4 月)体重8 kg,家长难于坚持停用生酮饮食。停用生酮饮食后局灶性发作增加,每日4~5 次,每次持续数秒钟到1 分钟可自行缓解,未再有痉挛发作,目前口服丙戊酸钠、托吡酯、拉莫三嗪抗癫痫发作。
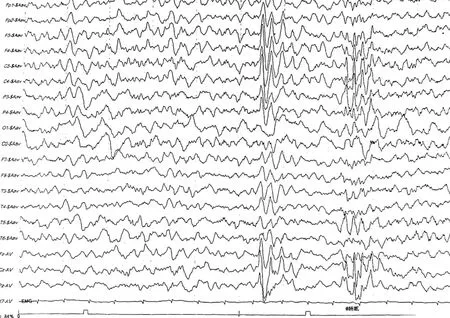
图4a 视频脑电图生酮饮食治疗后睡眠期
2 讨论
CDKL5 基因相关疾病是由于CDKL5 基因突变所引起的一种罕见的神经发育性疾病,患者的临床表现多样,主要表现为早发性难治性癫痫,以及神经系统发育迟缓导致的认知、运动、语言和视觉功能障碍[1]。CDKL5 基因相关疾病在新生儿中的发病率为1 ∶60000 至1 ∶40000,且患儿多为女性,男性患者报道较少,往往有更严重的临床表现[4]。CDKL5基因致病性变异所致癫痫主要为早发性癫痫,首发中位年龄为6 周(1 周至1.5 岁),90%的癫痫发作时间为生后3 个月内。癫痫最早被描述为三个阶段:第一阶段是早发性惊厥发作,尽管发作间期脑电图正常;第二阶段是癫痫性痉挛,高度失律;第三阶段是进行性的难治性癫痫发作;近一半的患者服用三种或三种以上抗癫痫药物,大多患者为药物难治性癫痫[5],同时可合并有严重精神运动发育迟滞,如竖头不稳、不会说话等,常有肌张力低下的表现。本例患儿癫痫发作首发年龄为1 月24 天,病初表现为局灶性发作,抗发作治疗效果不理想,继而出现痉挛发作,与国内外报道多在3 月内发病相一致。在ACTH 治疗及规律的抗癫痫发作药物治疗下,有所好转,停用激素后发作加重,多种抗癫痫发作药物联合应用难于控制,逐渐出现发育迟滞及肌张力减低。应用生酮饮食治疗后发作控制,智力、运动有所改善。停用生酮饮食后再次发作增加。
生酮饮食(ketogenic diet,KD)对难治性癫痫有较好的疗效,被越来越多地用于难治性癫痫的治疗[6-7],KD 能够减少难治性癫痫患儿的发作,改善认知、言语和行为等问题。KD 是一个脂肪高比例、碳水化合物低比例,蛋白质和其他营养素合适的配方饮食,治疗儿童难治性癫痫已有十余年的历史。可能的作用机制为:对哺乳动物雷帕霉素靶蛋白(mTOR)及免疫的调节作用,mTOR 是人类中参与调节细胞大小,生长,蛋白质合成,自噬和转录的蛋白质,KD 可通过抑制mTOR 活性来减轻免疫反应;另外糖是大脑的主要能量来源,KD 可通过减少葡萄糖对大脑的直接供应而减轻兴奋度,以此来达到抗癫痫效果[8-9]。由生酮饮食提供的多不饱和脂肪酸可能激活过氧化物酶体增殖物激活受体,该受体调节抗炎、抗氧化和线粒体基因,从而增加能量储备,稳定突触功能和限制过度兴奋。从20 世纪初生酮饮食就开始应用于药物难治性癫痫患儿。目前生酮饮食已被证实在多种癫痫综合征中疗效显著[10-12],并成为儿童难治性癫痫的重要治疗方法。近年来,生酮饮食治疗逐渐被应用到了婴儿痉挛症的治疗中。
婴儿痉挛症是一种婴儿期常见的难治性癫痫综合征,主要特点为婴儿期起病、频繁的痉挛发作、脑电图出现高度失律和智力发育障碍。3~7 个月发病者最多,发作时表现为两臂前举,头和躯干前屈,似点头拥抱状;少数患儿可呈头背后屈。患儿常成簇发作,思睡或刚醒时容易连续发生,发作时有时伴喊叫、哭吵或痛苦状,发作间期脑电图示不对称、不同步、并伴有暴发抑制交替倾向的高幅慢波,杂以多灶性尖波、棘波或多棘波,即高度失律。婴儿痉挛症病因多种多样,可分为产前因素、围生期因素及产后因素三类[13]。其中遗传因素为产前因素的一部分,此例患儿为CDKL5 基因chrX:18638087,c.2376+1(IVS16)G >A,嵌合新生变异所致的婴儿痉挛症。促肾上腺皮质激素、糖皮质激素和氨己烯酸被作为一线治疗婴儿痉挛症的短期疗法,但停用后易于复发。越来越多的研究报道生酮饮食较多的应用于婴儿痉挛症中。王竹岩[13]、胡春辉[14]等对25 例经抗癫痫治疗失败的婴儿痉挛症患儿进行生酮饮食治疗,其中7例(28%)的患者达到无临床发作,且均在治疗1 个月内显效。吴革菲等[15]通过对部分药物治疗失败的婴儿痉挛症患儿给予生酮饮食治疗达到无发作。来自国际CDKL5 基因相关疾病数据库的数据显示,生酮饮食可以降低该基因所致痉挛发作频率[16-17]。Pires等人对17 例婴儿痉挛症患儿应用生酮饮食治疗的前瞻性研究表明,开始1 个月后6 例患儿无发作(35%),13 例患儿减少>50%发作(76%)。5 例脑电图显示高度失律的患儿中,有4 例在1 个月内消失(80%)。有3 例无癫痫发作的患者有精神运动改善。在开始生酮饮食治疗3 个月后,11 例(65%)患儿无癫痫发作[18]。Kayyali 等[19]的研究表明,开始生酮饮食后3 个月,20%患儿减少>90%发作,该数据在6 个月时为22%,12 个月时为35%。研究认为尽早使用生酮饮食治疗,除可以控制癫痫发作,还可以避免大剂量应用激素带来的不良反应及降低复发风险,同时可以改善脑电图,改善患儿的认知[20]。
近年来,国内外关于生酮饮食治疗儿童难治性癫痫患儿的研究[21-23]显示,3、6、12 个月末保留率分别为62.8%~80.7%、42.0%~70.0%、24.3%~54.0%。随着生酮饮食治疗时间的延长保留率逐渐减低的原因主要为,在生酮饮食治疗实施过程中,部分患儿因生酮饮食治疗适应时间偏长或不良反应明显,不能完成营养师规定饮食,血酮在短时间内难以达到较稳定的水平,其中主要的不良反应包括初期拒食、呕吐,不能完成规定饮食,部分患儿治疗早期血酮均值<2 mmol/L。另外,生酮饮食限制严格,部分患儿及其监护人依从性差,因此提高患儿监护人对该治疗的认识,帮助其建立信心,提高患儿及其监护人在生酮饮食治疗过程中的依从性,从而提高生酮饮食治疗保留率,有助于改善生酮饮食治疗儿童难治性癫痫的疗效。本例患儿在治疗过程中先后应用左乙拉西坦、ACTH、托吡酯、丙戊酸钠、氨己烯酸、拉莫三嗪,癫痫曾一度有所控制,再次发作加重后应用生酮饮食后癫痫控制较好,且智力、运动有所改善。但由于生酮饮食患儿长期耐受欠佳,坚持2 年后停用,痉挛发作消失,局灶性发作再次出现。
综上所述,CDKL5 相关癫痫性痉挛及其相关综合征临床表现严重程度与突变位点、突变形式等密切相关,预后与临床表现严重程度密切相关,预后常不理想,在口服抗癫痫发作药物控制发作的前提下,生酮饮食治疗可减少发作、改善生活质量,癫痫症状控制后患儿智力发育可出现进步。未来还有待于更多的样本量的研究。
——生酮饮食

