基于全国抗菌药物临床应用监测网的手术组病例用药合理性分析
府裕琦 吕娟丽 陈熙 吕红梅 杨小强 赵颖波

DOI:10.13912/j.cnki.chqm.2024.31.4.01
【摘 要】 目的 分析全国抗菌药物临床应用监测网中手术组病例用药的合理性。方法 通过建立抗菌药物临床应用监测网病例评价标准,对手术组病例抗菌药物使用的合理性进行评价。结果 我国手术组病例预防用抗菌药物使用率呈下降趋势,2021年I类切口手术预防用抗菌药物的使用率为32.20%,无适应证用药的比例从2017年的11.35%下降到2021年的6.87%,抗菌药物预防使用的合理率从2017年的15.05%上升到2021年的29.73%。不合理用药情况主要表现为围手术期用药不合理,构成比5年均值为55.13%;其次为药物选择不合理,构成比5年均值为18.58%;以及每日给药次数、单次剂量不合理等。结论 需持续加强手术抗菌药物使用管理和监测力度,保障临床用药安全。
【关键词】 抗菌药物;合理用药;用药评价;围手术期;监测
中图分类号:R197 文献标识码:A
Analysis of the Rationality of Drug Use in the Surgical Group Based on the Center for Antibacterial Surveillance/FU Yuqi,LV Juanli,CHEN Xi,et al.//Chinese Health Quality Management,2024,31(4):01-06
Abstract Objective To analyze the rationality of clinical application of antibiotics in the surgical group based on the Center for Antibacterial Surveillance in China. Methods The reasonableness of the use of antibiotics in the surgical group was evaluated by establishing the case evaluation criteria of the Center for Antibacterial Surveillance. Results The use of preventive antibiotics in the surgical group showed a decreasing trend.In 2021, the use of preventive antibiotics in Class I incision surgery was 32.20%, and the rate of use without indication decreased from 11.35% in 2017 to 6.87% in 2021. The Rationalization rate of antibiotics use increased from 15.05% in 2017 to 29.73% in 2021. Irrational use of drugs was mainly due to Irrational drugs use in the perioperative period,with an average composition ratio of 55.13% in 5 years, followed by irrational medications selection,with an average composition ratio of 18.58% in 5 years, and unreasonable daily administration times and single dose. Conclusion It is necessary to strengthen the management and monitoring of antibiotics use in surgery to ensure the safety of clinical use.
Key words Antibiotics; Rational Drug-Use Evaluation; Perioperative Period; Monitoring
First-author's address National Institute of Hospital Administration,National Health Commission,Beijing,100044,China
全国抗菌药物临床应用监测网(以下简称“监测网”)创建于2004年[1],已从最初的手工上报数据发展为全信息化上报数据模式,其数据上报与统计功能不斷完善,入网医院也从最初的35家增加到7 000余家,为国家卫生健康行政部门全面掌握我国抗菌药物临床应用情况,以及制定政策法规及相应监管指标提供了数据支撑,也为各医院持续改善抗菌药物临床应用提供了可靠信息。自2016年起,国家卫生健康委依据监测网数据每年发行我国抗菌药物管理白皮书《中国抗微生物药物管理和耐药现状报告》[1]。
围手术期抗菌药物的合理应用直接关系到患者术后康复,本研究对2017年-2021年全国二级综合医院
和三级综合医院手术组病例的用药合理性进行分析,以期为围术期合理应用抗菌药物提供参考。
1 研究对象与方法
1.1 研究对象
选取2017年-2021年监测网手术组病例,采取抽查方式评价病例抗菌药物使用的合理性,先从监测网数据中选取各年度上、下半年各一个月(3月和7月)的手术病历,再从中各抽取20份作为评价病历。
1.2 评价方法与标准
建立监测网病例评价标准,其参考依据包括《抗菌药物临床应用指导原则(2015年版)》(以下简称《2015版原则》)[2]、药品说明书及相关的临床诊疗指南。评价项目主要基于有无使用抗菌药物的指征、选用的药物品种以及给药方案是否合理,具体包括适应证、药物选择、给药剂量、每日给药次数、溶媒、给药途径、联合用药、更换药品、围手术期(术前、术中、术后)等。监测网手术组病例抗菌药物使用合理性评价标准见表1。
2 评价结果
2.1 手术组病例抗菌药物使用情况
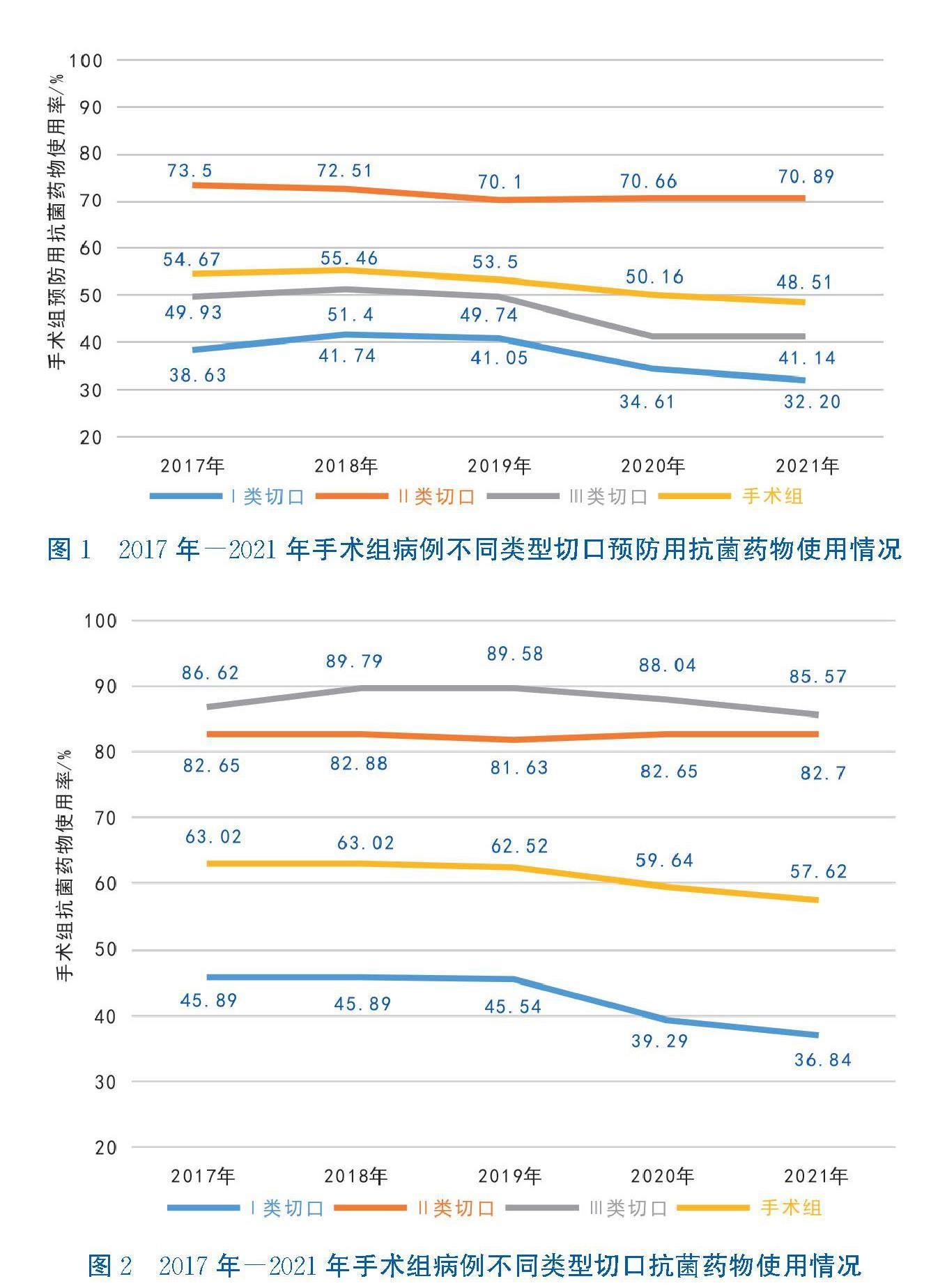
手术组病例抗菌药物使用情况包含预防用药和治疗用药。数据显示,我国手术组病例预防用抗菌药物的比例整体呈下降趋势,Ⅰ类切口手术预防用抗菌药物使用率由2017年的38.63%下降至2021年的32.20%,降幅6.43个百分点;Ⅱ类切口手术预防用药率由2017年的73.50%下降至2021年的70.89%,降幅2.61个百分点;Ⅲ类切口手术预防用药率由2017年的49.93%下降至2021年的41.14%,降幅8.79个百分点,见图1。Ⅲ类切口手术抗菌药物使用率由2017年的86.62%到2021年的85.87%,呈小幅下降趋势(见图2)。这表明Ⅲ类切口手术用药病例中近一半的用药为治疗用药。从图1和图2可知,Ⅰ类切口、Ⅱ类切口手术的抗菌药物使用率与预防用药使用率比较差别不大,说明了Ⅰ类切口、Ⅱ类切口手术中使用抗菌药物主要是预防的目的。
2.2 手术组病例合理用药评价结果
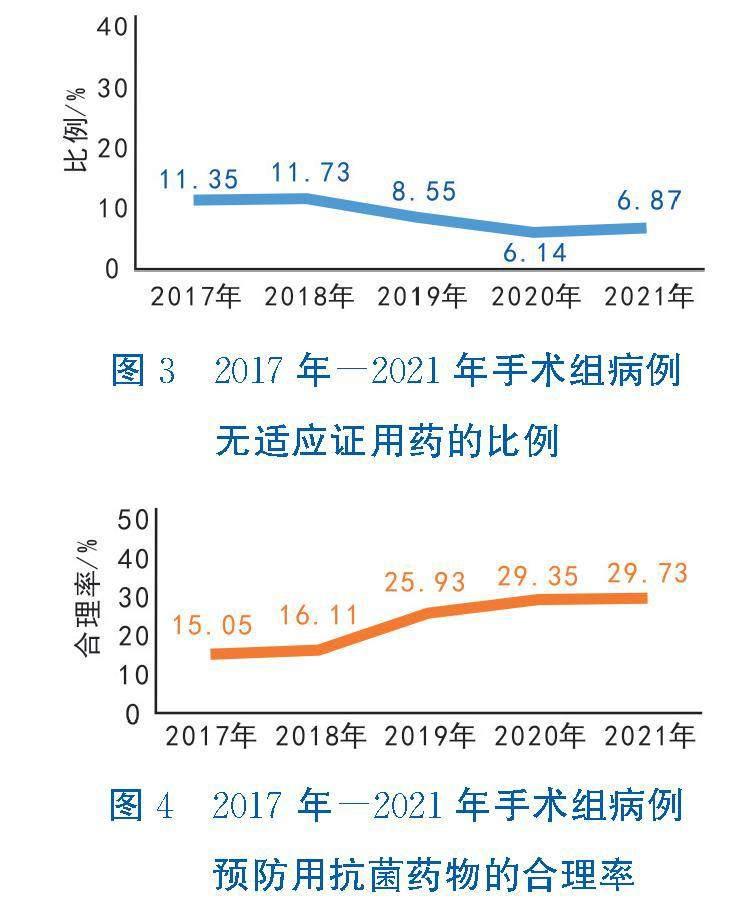
2.2.1 无适应证用药的比例 合理用药首要的评价项目是判断有无适应证,无适应证用药是抗菌药物合理用药管理的重点,也是降低Ⅰ类切口预防用药使用率的重要环节,手术组病例无适应证用药的比例从2017年的11.35%下降到2021年的6.87%,见图3。无适应证用药主要存在于Ⅰ类切口手术中,提示临床预防用抗菌药物时,需要加强适
应证的把控。
2.2.2 预防用抗菌药物的合理率 在有适应证的用药病例中,进一步评价抗菌药物使用的合理性。根据评价结果,手术组病例预防用药的合理率呈逐年小幅上升的趋势,
从2017年的15.05%上升到2021年的29.73%,平均值约为23%,见图4。整体来说,用药合理率较低,说明手术预防用药中不合理现象比较普遍。
2.2.3 手术组病例用药不合理的表现 单项用药不合理的病例构成比,从2017年的19.17%上升到2021年的25.28%,呈小幅上升,多项用药不合理的病例则从2017年的54.42%下降到2021年的38.13%,呈逐年下降趋势,见图5。
在用药不合理的病例中,围手术期不合理率占比最高,2017年-2021年5年均值为55.13%,其次为药物选择不合理,2017年-2021年5年均值为18.58%。2021年,每日给药次数不合理均值为9.86%;单次剂量不合理均值为6.86%;联合用药不合理均值为2.53%,见图6。
围手术期不合理病例中,术后用药不合理占比最高,其次为术前用药不合理,主要表现为术后用药持续时间长、无理由用药时间超过24 h等,见图7。
3 讨论与思考
3.1 适应证评价
手术预防用药的主要目的是预防手术部位感染(Suigical Site Infection, SSI),其专指围手术期发生在切口或手术深部器官或腔隙的感染,并非预防手术期间所有感染,不包括与手术无直接关系的、术后可能发生的其他部位感染。引发SSI的病
原菌主要位于患者皮肤、黏膜(胃肠道、口咽或泌尿生殖器黏膜)或空腔脏器的内源性菌丛,大多数SSI为内源性感染,仅有少部分为外源性感染。外源性感染病原体可能来源于手术小组成员、手术室环境或者手术过程中使用的医疗仪器或耗材。使用抗菌药物主要是预防内源性感染,不同类型手术SSI病原体不同。根据《2015版原则》,I类切口手术一般情况下无需预防用药,只有在手术范围大、时间长或者合并有感染的高危因素(高龄、糖尿病、免疫低下、恶性肿瘤等)时使用预防用药,II类切口手术一般有预防用药适应证,III类切口属于有污染风险的切口手术,需要使用预防用药。因此,判断有无适应证要严格根据手术的切口类型、手术部位有无污染、患者有无高危因素综合考虑。
3.2 药物选择合理性评价
手术预防用抗菌药物品种选择要综合考虑手术过程和相关危险因素的影响。它应该覆盖切口部位可能产生的微生物菌群,以及患者多种特异性危险因素影响,包括患者基础感染、近期抗菌药物的使用、在院时间、可能的定植菌、体重、基础疾病、過敏状态、肾功能、免疫状态、是否假体植入等。《2015版原则》指出,应选择针对性强、有循证医学证据的抗菌药物。例如,心血管、头颈、胸腹壁、四肢软组织、骨科等经皮肤手术,应选择头孢唑林等针对金黄色葡萄球菌的抗菌药物;结肠、直肠和盆腔等手术,应选择针对肠道阴性杆菌和脆弱拟杆菌等厌氧菌的抗菌药物。头孢类过敏者,针对革兰氏阳性菌推荐选择万古、去甲万古和克林霉素等;针对革兰氏阴性菌,推荐选择氨曲南、磷霉素或氨基甙类。《2015版原则》推荐了常见手术预防用抗菌药物的品种选择,但对于首选用药和备选用药推荐比较模糊,没有体现药物选择的优先次序,而美国医院药师学会(the American Society of Utility a-Health-System Pharmacists,ASHP)、美国感染性疾病协会(the Current Infectious Diseases Society of America,IDSA)、美国外科感染学会(the Surgical Infection Society,SIS)以及美国卫生保健流行病学协会(the Society for Health Care Epidemiology of America,SHEA)共同制定发布的《外科手术抗菌药物预防使用临床实践指南》(以下简称“ASHP/IDSA/SIS/SHEA指南”)[3],按手术部位或方式(包括介入手术)推荐首选抗菌药物及备选药物并注明推荐强度,可以借鉴。
3.3 给药方案合理性评价
3.3.1 给药剂量 监测网剂量评价标准比较笼统,剂量正确为合理,剂量过大过小均不合理,在评价过程中较难把握。《2015版原则》也未明确手术预防用抗菌药物的剂量。2009年3月,原卫生部办公厅《关于抗菌药物临床应用管理有关问题的通知》(卫办医政发〔2009〕38号)对抗菌药物常用品种做了剂量推荐,比如头孢唑啉1g~2g,头孢呋辛1.5 g等,但剂量推荐比较单一,未考虑手术部位、患者病情、生理因素对剂量的影响。如当患者肝肾功能损伤时,主要经肝、肾代谢或排泄的药物要适当减少剂量或延长给药间隔时间。同时体重也会影响药物的药代动力学参数。肥胖是手术部位感染的危险因素之一,因此ASHP/IDSA/SIS/SHEA指南推荐肥胖患者适当加大剂量。研究[4]表明,双倍剂量抗菌药物预防可降低体重在80 kg及以上患者的SSI率,而对于体重大于120 kg或体重指数≥40 kg/m2的患者有显著影响。有研究[5]结果显示,在股骨头置换手术中静脉注射2 g头孢唑林预防感染,血清和骨中药物浓度超过了甲氧西林敏感金黄色葡萄球菌的最低抑菌浓度,但未达到耐头孢唑林的凝固酶阴性葡萄球菌最低抑菌浓度,可能导致深层手术部位感染的潜在风险。可见,剂量合理性评价要综合考虑各种临床因素。
3.3.2 每日给药次数 监测网的评价标准为符合药品说明书即为合理,不符合药品说明书则为不合理,手术病例每日给药次数的评价主要考虑术后用药间隔时间。手术预防用药给药间隔时间需综合考虑药物半衰期、体内分布特点、患者生理状况等。β-内酰胺类为时间依赖性抗菌药物,药动学/药效学参数为%T>最低抑菌浓度,短半衰期的药物,应一日多次给药,如一日一次给药不能充分发挥其药效,反而会导致细菌耐药。在当前的合理用药评价工作中,给药次数不合理主要表现为术后给药次数为一日一次或一日两次。目前部分抗菌药物药品说明书中增加了关于围手术期预防用药的剂量和给药间隔时间等,但需要监管部门进一步明确,以便给予用药者足够的参考依据。ASHP/IDSA/SIS/SHEA指南中对于手术预防用药不同品种的给药间隔时间均有详细的推荐,可以参考。
3.3.3 给药途径与溶媒 围手术期预防用药的给药途径一般以静脉注射为主。特殊情况如眼科手术术前滴眼、肠道手术的肠道准备采用口服等。局部预防可能会增加抗菌药物耐药性风险,应尽量避免[6]。静脉给药的溶媒常用5%或10%的葡萄糖注射液或生理盐水,根据抗菌药物的理化性质和患者的疾病生理情况综合考虑选择。根据《2015版原则》,头孢类抗菌药物术前给药时间窗为30 min,成人的滴注速度为40滴~60滴(1 mL=15滴),30 min可滴入的液体量80 mL~120 mL。滴注速度过快容易引起不良反应,因此溶媒用量一般不超过100 mL。
3.3.4 联合用药 根据《2015版原则》,手术预防抗菌用药应尽量选择单一品种,避免不必要的联合用药。一项针对III型开放性骨折手术患者的研究中,单独使用头孢唑林或头孢唑林与氨基糖苷进行抗菌药物预防及治疗[7],结果显示,联合用药组出现感染的概率明显较高(6/15[40%]比8/53[15.1%],P=0.035);感染几率有上升趋势(优势比:2.99,95%可信区间:0.79~11.33,P=0.107);多重耐药细菌感染率更高(3/15[20%]比1/53[1.9%],P=0.046);在30天死亡率、骨折并发症导致的1年再住院率或住院时间方面没有统计学差异。结果表明,头孢唑林和氨基糖苷联合用药可能不是预防细菌感染的必要选择。《2015版原则》在涉及消化道或妇科手术时,推荐一二代头孢联合甲硝唑或头霉素类单药。在临床操作中,肝胆外科手术经常出现头霉素类联合甲硝唑,或拉氧头孢联合甲硝唑等不合理的抗菌用药现象。
3.4 围手术期评价
围手术期预防用药评价包括术前给药的时机、术中是否追加用药及术后持续时间。
3.4.1 术前首次用药的时机 《2015版原则》推荐切皮前0.5 h~1 h或麻醉开始时给药,目的是当手术切口暴露时,局部组织中已达到足以杀灭入侵(污染)切口细菌的药物浓度。万古霉素、氟喹诺酮类,在手术前1 h~2 h缓慢静脉滴注(时间不短于60 min)。眼科手术滴眼液在24 h内给药;肠道手术准备肠道术前24 h内开始给药。国外抗菌药物指南推荐在术前1 h内给药,需要 1 h 内给药的如万古霉素、氟喹诺酮类等需切皮前 2 h 内给药。研究[8]结果显示,切皮后120 min使用抗生素预防比切皮前120 min使用抗菌药物的感染风险更高。而在切皮前120 min内与切皮前60 min内实施预防用药手术部位感染率无差异。
3.4.2 术中 手术中追加抗菌药物是为了在长时间手术时确保足够的血药浓度,手术时间短于2 h,术前给药一次即可。《2015版原则》推荐“手术时间超过 3 h 或超过药物两个半衰期时或失血量>1 500 mL,术中应追加1次”,ASHP/IDSA/SIS/SHEA指南针对每种常用抗菌药物均有追加的时间推荐,更具有针对性。在肝肾功能不全等会延长抗菌药物半衰期的情况下一般不推荐追加。
3.4.3 术后 术后主要是评价手术结束后使用抗菌药物的持续时间。《2015版原则》规定,一般手术预防用药时间不超过24 h,心脏手术、污染手术必要时可延长至48 h;过度延长用药时间并不能提高预防效果,如超过48 h耐药菌感染机会增加。术后留置有引流管不是延长预防用药时间的指征。一项关于肝胆胰外科手术中抗菌药物预防作用的研究[9]表明,手术技术的改进和围手术期的管理可以产生极低的SSI,术前一次2 g头孢唑林的剂量可能足以用于手术预防。术前一次抗菌药物剂量对大多数手术来说是足够的,术后静脉注射抗生素的剂量只在特定的情况下才需要,如一些心脏和血管手术,或者下肢截肢或污染手术中。世界卫生组织[10]和美国疾病控制和预防中心[11]的指南建议,仅在手术持续期间给予抗菌药物预防,切口关闭后则不使用額外剂量。印度的一项研究[12]证明,脊柱融合术中术后72 h预防用药与24 h同样有效。ASHP/IDSA/SIS/SHEA指南[3]中表示,允许术后使用氨苄西林,但建议在24 h内停用。当前,并没有证据支持骨科手术后用药持续时间超过24 h,术后用药持续时间评价要严格遵循《2015版原则》要求。
4 小结
手术组病例预防用药的合理性是抗菌药物管理的重要内容,从适应证的把控到抗菌药物的品种选择、用法用量以及围手术期的用药时机、是否追加、术后是否需要再用等,都是用药合理性评价的重点内容。本研究不足在于合理性用药评价的样本基于小部分病例,下一步要利用信息化手段,提高病例提取数量,优化用药评价系统功能,进一步完善评价标准,确保评价的准确性和同质化,以病例合理用药评价为手段,提高临床抗菌药物使用合理性。
参考文献
[1] 卫生部办公厅,国家中医药管理局办公室,总后卫生部. 关于建立抗菌药物临床应用及细菌耐药监测网的通知:国办医发〔2005〕176号[EB/OL].(2005-11-29)[2023-04-17]. http://www.nhc.gov.cn/zwgkzt/pyzgl1/200804/18487.shtml.
[2] 国家卫生计生委办公厅,国家中医药管理局办公室,解放军总后勤部卫生部药品器材局.关于印发抗菌药物临床应用指导原则(2015年版)的通知:国卫办医发〔2015〕43号[EB/OL].(2015-07-24)[2023-04-17].http://www.nhc.gov.cn/yzygj/s3593/201508/c18e1014de6c45ed9f6f9d592b 43db42.shtml.
[3] BRATZLER DW,DELLINGER EP,OLSEN KM,et al. Clinical practice guidelines for antimicrobial prophylaxis in surgery[J].Am J Health Syst Pharm,2013,70(3):195-283.
[4] SALM L,MARTI WR,STEKHOVEN DJ,et al.Impact of bodyweight-adjusted antimicrobial prophylaxis on surgical-site infection rates[J].BJS Open, 2020, 5(1):1-6.
[5] KOJI Y,KUNIHIRO M,FUMIAKI T,et al.Are bone and serum cefazolin concentrations adequate for antimicrobial prophylaxis?[J].Clin Orthop Relat Res,2011,469(12):3486-3494.
[6] CHEN PJ, HUA YM, HAN ST,et al.Topical antibiotic prophylaxis for surgical wound infections in clean and clean-contaminated surgery: a systematic review and meta-analysis[J].BJS Open, 2021,125:1-12.
[7] DEPCINSKI SC,NGUYEN KH,ENDER PT.Cefazolin and an aminoglycoside compared with cefazolin alone for the antimicrobial prophylaxis of type III open orthopedic fractures[J].Int J Crit Illn Inj Sci,2019,9(3): 127-131.
[8] JONGE SW,GANS SL,JASPER JA,et al.Timing of preoperative antibiotic prophylaxis in 54 552 patients and the risk of surgical site infection a systematic review and meta-analysis[J].Medicine,2017,96(29):1-12.
[9] STECCANELLA F,AMORETTI P,BARBIERI MR,et al. Antibiotic prophylaxis for hepato-biliopancreatic surgery—a systematic review[J].Antibiotics,2022,11(2):194.
[10] World Health Organization. Global guidelines for the prevention of surgical site infection[Z].2016.
[11] BERRIOS TS, UMSCHEID CA, BRATZLER DW, et al. Centers for disease control and prevention guideline for the prevention of surgical site infection[J].JAMA Surg,2017,152(8):784-791.
[12] MARIMUTHU C,ABRAHAM V T,RAVICHANDRAN M,et al.Antimicrobial prophylaxis in instrumented spinal fusion surgery: a comparative analysis of 24-hour and 72-hour dosages[J].Asian Spine J,2016,10(6):1018-1022.
通信作者:
趙颖波:国家卫生健康委医院管理研究所药事管理研究部主任
E-mail:zmyzyb@163.com
收稿日期:2023-08-03
修回日期:2023-12-05
责任编辑:姚 涛

