锌有机骨架材料的合成及对水中Pb2+的萃取性能研究
高子轩,伍康宇
(烟台大学 环境与材料工程学院,山东 烟台 264005)
随着科技的发展,全球经济迅速崛起,采矿业、冶金业、化工等行业盛行,使得含有重金属离子(Pb2+,Cd2+,Hg2+,Cu2+)的行业废水被直接或者间接排放到水体中,这些重金属污染不仅对人类和其他生物物种的生命健康构成了威胁,对其生存环境更是造成了不可逆的损害[1]。铅(Pb2+)被认为是毒性最大的重金属离子之一,它广泛存在于矿石、冶金工艺、金属电镀、肥料、颜料、弹药、塑料和电池中。随着工业的发展,工业上含铅废水的排放是目前铅废水污染的重要来源之一[2]。人体吸收过量铅元素的主要途径是通过未处理干净的饮用水和被污染的可食用水生生物,由于铅在人体中不易排除,人体无法自主降解Pb2+,会严重伤害人类的身体机能,血液中Pb2+超标会严重影响新生儿的身体健康,尤其是会危害婴幼儿的智力发育[3]。因此,去除水体中的Pb2+迫在眉睫。
在过去的几十年,人们使用了许多方法从水溶液中去除Pb2+,包括蒸发法、化学沉淀法、电化学法、吸附/离子交换法、膜分离技术和萃取法[4-8]。传统的蒸发过程采用单效或多效蒸发,能耗较高、设备体积较大、依赖于外界蒸汽,且余热利用率过低,二次蒸汽无法回收。化学沉淀法需投加的化学药剂较多,导致出水的含盐量或pH值高,需要进一步处理才能达标排放。电化学技术对电力的要求很高、需要经常更换电极,这就导致成本较为高昂。吸附法存在选择性差、去除效率低且不能连续操作等问题,对于实际应用有较大的局限性。离子交换法污染较小,但是相对来说其成本较高而且总体吸附量较低。膜分离技术所用到的膜容易受到废水中的污染物污染而堵塞,投资成本较高,不利于大规模使用。萃取法因成本低、操作简单、效率高等优点,而且对复杂的现实系统的适应性和大规模操作的适用性,故具有更广阔的应用前景。
传统去除材料活性炭孔隙发达、比表面积很大,广泛应用于各个领域。但是,活性炭去除容量不大、选择性不好,因此限制了其在Pb2+去除方面的应用[9]。沸石是一种天然无机材料,价格非常低廉,易于购买,但是其去除容量并不大,因此无法在含Pb2+废水的处理中发挥出色的作用[10]。相比较其他多孔材料,例如沸石、活性炭等,金属-有机骨架(MOFs)作为一种新型的材料被广泛用于萃取水体中的重金属[11]。通常对金属-有机骨架材料的物理和化学性质可以通过对合成配体设计进行精细调整,有利于人们对其进行目的性的设计。在MOFs的合成过程当中,金属离子会和有机配体以及溶剂分子形成配位,从而满足配位数的要求。金属离子和有机配体的配位方式和配位能力存在多样性。在不同的合成方式、反应体系中,同一种配位基团可能又会有不同的配位方式,同一种配体在和性质不同的金属离子反应时又会形成不同结构的MOFs,因此在一定程度上更加丰富了MOFs结构的多样性[12],从而可以提高对重金属离子的萃取效率及萃取容量。
本文中采用溶剂热合成法设计合成了一种锌的有机骨架材料(Zn-MOF),应用于萃取水溶液中的Pb2+,通过引入具有羧基官能团,增加对水中Pb2+的萃取能力且提高了对Pb2+的萃取效率。通过萃取等温线以及萃取动力学进行模型拟合,探究了其对Pb2+的萃取性能,为金属有机骨架材料应用于污水中重金属离子的处理提供理论依据。
1 Zn-MOF的制备
称取配体5,11,17,23-四叔丁基-25,26,27,28-四羧基杯[4]芳烃(0.007 g,0.008 mmol),配体2,2′-联吡啶(0.002 5 g,0.016 mmol)和六水合硝酸锌(0.004 8 g,0.001 6 mmol)放入10 mL 的玻璃小瓶中,加入5 mLN,N-二甲基甲酰胺溶液,超声5 min后溶解。在往里加入3 mL去离子水后超声5 min使其与之前的溶液混合均匀,封闭后放入90 ℃鼓风干燥箱中反应36 h。反应结束后,放凉至室温(25 ℃)。过滤得到白色透明条状晶体即Zn-MOF。将得到的晶体放入100 ℃真空干燥箱中活化12 h,将MOF里面的溶剂分子去除。
2 铅离子的萃取实验
将7 mg的Zn-MOF置入10 mL的甲苯溶液中超声分散均匀,制备得到有机相。配制15 mL 10×10-6的Pb2+水溶液,调至pH值为3~7 (使用0.01 mol/L NaOH或0.01 mol/L HNO3溶液调整)。将制备好的有机相倒入水相中,在室温下连续搅拌。反应结束后静置,使有机相和水相分离。从图1可以看出,随着pH值增大,Zn-MOF对Pb2+的萃取效率越来越高。在pH值3时,萃取效率可达63%,随着pH值的增大在4~7时萃取效率均能达到99%。可以理解为,在酸性条件下Zn-MOF的表面官能团趋于质子化,导致Pb2+和H+在Zn-MOF的未配位的羧基竞争性相互作用。随着pH值升高,未配位的羧基与Pb2+结合位点的质子竞争力减弱,且Zn-MOF表面的活性位点大面积暴露出来,因此对Pb2+萃取效率会更高。综上选用在未调pH值6的标准Pb2+溶液中进行后续萃取实验。
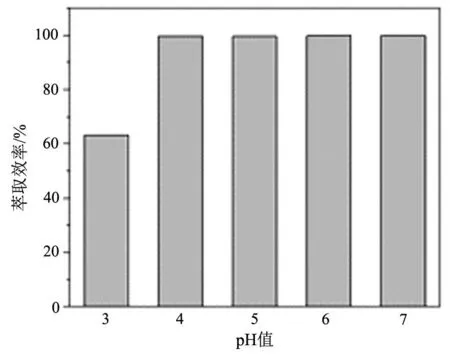
图1 溶液pH值对Pb2+萃取性能的影响
MOF材料对重金属离子的快速萃取也是十分重要的。同样地配制了15 mL 10×10-6的Pb2+水溶液,在未调pH值条件下进行了萃取动力学实验。在一定的时间间隔内取样。从图2中可看出,Zn-MOF对Pb2+在20 min内被快速萃取平衡。5 min时,萃取效率仅达53.7%;20 min时,萃取达平衡。采用了一级动力学模型和二级动力学模型对采集的数据进行拟合。拟合动力学方程如下:

图2 萃取时间对Pb2+萃取性能的影响
ln(qe-qt)=lnqe-k1t
式中:qe——平衡萃取容量,mg·g-1;
qt——某一时刻t(h)对应的吸附容量,mg·g-1;
k1——准一级动力学模型的速率常数,h-1;
k2——准二级动力学模型的速率常数,g/(mg·h)。
由图3和表1可知,二级动力学模型能较好地拟合萃取数据,线性相关系数为0.999。因此,可以用准二级动力学模型来描述Zn-MOF对Pb2+的萃取过程,说明萃取过程中化学作用占主导地位。Pb2+的快速萃取动力学实验结果表明,Zn-MOF框架中有大量未配位的羧基官能团充当与Pb2+污染物的结合位点。开始萃取时,Zn-MOF表面有大量未结合且暴露的活性位点与Pb2+结合。故开始萃取时能够达到迅速萃取。随着Pb2+与羧基官能团结合的越来越多,表面活性位点被占用,后续进入Zn-MOF框架中的Pb2+结合位点数变少,因此萃取效率降低。

表1 萃取动力学拟合数据

(a)准一级;(b)准二级。
为了研究Zn-MOF对Pb2+的最大萃取容量,将5 mg的Zn-MOF置入10 mL的甲苯溶液中超声分散均匀,制备得到有机相。萃取50 mL 5×10-6~90×10-6的系列标准Pb2+水溶液。在室温下连续搅拌,待给定时间后停止搅拌。如图4所示,随着Pb2+初始浓度的增加,Zn-MOF的萃取容量增加,最终达到最大萃取容量243.57 mg·g-1。等温线采用Langmuir模型和Freundlich模型研究如图5所示。计算方程如下:

图4 Zn-MOF对Pb2+的吸附等温线

(a)Langmuir模型;(b)Freundlich模型。
式中:qe——平衡萃取容量,mg·g-1;
qmax——最大萃取容量,mg·g-1;
Ce——反应达到平衡时,溶液中吸附质的质量浓度,mg·L-1;
KL——Langmuir常数,L·mg-1;
KF——Freundlich常数,(mg·g-1)/(mg·L-1)n;
n——无量纲常数。
从表2可以看出,Langmuir模型拟合较好,线性相关系数为0.999,说明萃取是单层均匀萃取。计算的饱和萃取容量为243.902 mg·g-1,与实验结果吻合较好,说明Zn-MOF对Pb2+的萃取符合Langmuir模型。

表2 Langmuir和Freundlich模型的拟合参数
3 结论与展望
本文采用溶剂热法合成了一种锌有机框架材料Zn-MOF,并从pH值、动力学以及萃取容量等方面探究了这种新合成的材料对水中Pb2+的萃取性能。研究结果表明,引入含有羧基官能团增加了Zn-MOF的活性位点,改善了锌有机框架材料的萃取性能,以致Zn-MOF能够在20 min内对水中的Pb2+萃取平衡。并且能在未调pH值条件下对Pb2+最大萃取容量243.57 mg·g-1。Zn-MOF对Pb2+的过程符合Langmuir方程,且满足准二级动力学方程。Zn-MOF材料有望成为一种较为理想的Pb2+的萃取材料。MOF材料比表面积比起其他材料来说更加大、性能较为优秀,但是成本太高,在水系环境中去除污染物受到多种方面的影响,包括MOF材料本身的性能、污染物的性能以及萃取时环境的影响等,在实际生活中,工业废水中的环境更加复杂,MOF材料需要克服更加复杂的环境。因此,探究在更加复杂的环境下进行萃取也是今后工作的重点。因此在实际应用方面还需要进一步研究这些影响因素和材料对污染物去除能力的关系。目前的研究已经有很多合成条件非常成熟的MOF材料,对其进行官能团的附加、修饰其表面的化学性能和调整其孔径的大小等方面的改进,也可以将MOF材料与其他材料结合形成复合材料,例如膜材料等。这样可以聚集它们的优点,改善缺点。由于大部分MOF材料的合成成本比较高、合成工艺较为复杂,商业化应用的进程仍然较为困难,时机尚未成熟,大部分MOF材料去除水中污染物的研究仍然只是停留在实验室阶段,要解决包括但不限于多次重复利用的问题、结构稳定性问题、高吸附容量的问题和寿命问题等。

