不同微创手术方式应用于累及主动脉弓部的Standford B型主动脉夹层的早期疗效
石 宇,孟金金,刁文杰,杨少峰,吴 振
(蚌埠医科大学第一附属医院心脏外科,安徽 蚌埠 233004)
主动脉夹层(aortic dissection,AD)是急性主动脉综合征的一个亚类,是常见的危及生命的主动脉病变,常合并穿透性溃疡和壁内血肿[1]。其解剖病理是异常的血流动力学导致主动脉内膜撕裂,血液从真腔通过撕裂口进入假腔,假腔随着时间的推移而扩大,病程进展可能导致压迫左室引起左室破裂[2]。国外学者首先发表并应用了Stanford分型方式,根据是否累及升主动脉将AD分为A型和B型[3]。Stanford B型AD(TBAD)常涉及左锁骨下动脉(left subclavian artery,LSA)远端的主动脉撕裂,但不累及升主动脉或LSA近端主动脉弓,然而,多达30%的此类夹层患者会出现并发症,包括持续疼痛、灌注不良、动脉瘤增大和即将破裂,胸主动脉腔内修复术(thoracic endovascular aortic repair,TEVAR)是一种可以立即重建真腔内血流、稳定病变动脉并防止破裂的手术方法,同时可以降低患者早期死亡率,并使病人长期获益[3]。长期以来,TEVAR一直被认为是TBAD的首要治疗选择,但是为了避免术后内漏,单纯TEVAR手术完成的必要前提是LSA开口距离破口处有>1.5 cm的健康主动脉组织作为锚定区域[4]。临床上部分复杂型TBAD的锚定位置距离LSA<1.5 cm,术中需要弓上分支血管重建,左颈总动脉(left carotid artery,LCA)-LSA转流术联合TEVAR(以下简称颈-锁+TEVAR)及右颈总动脉-LCA-LSA联合TEVAR(以下简称颈-颈-锁+TEVAR)的微创杂交技术和单分支覆膜支架及体外预开窗覆膜支架腔内修复等微创全腔内修复手术方式逐渐成为讨论研究的对象。本研究通过观察行不同微创手术方式的TBAD患者的围手术期相关资料及术后血管重塑情况,对不同术式的早期临床疗效进行探讨。
1 资料与方法
1.1 一般资料本文以TBAD患者的患者为研究对象,选取2020年1月至2023年2月间在蚌埠医学院第一附属医院行微创手术治疗的患者64名,男43例,女21例。其中高血压病史患者58例,合并冠状动脉粥样硬化患者22例,合并糖尿病病史患者21例,合并吸烟史患者40例。选取标准为:所有患者术前均经主动脉CT血管造影(CT angiography,CTA)检查,有明确手术指征。排除标准为:(1)严重的冠心病需手术治疗的患者;(2)对术中造影剂明确过敏的患者;(3)临床症状难以控制,行传统开放手术的TBAD患者;(4)患者家属要求行药物保守治疗;(5)严重的基础疾病无法耐受手术;(6)术后无法随访的患者等,所有患者入院后均予以心电监护床边应用,静脉联合口服降压药物控制血压,术前维持心率60~80次/min,收缩压控制低于120 mmHg,通过降糖药物应用,空腹血糖维持<10 mmol/L,根据患者临床疼痛评分,必要时给予镇痛药物应用。所有患者术前皆签署知情同意书,本研究通过蚌医一附院伦理委员会审核批准。
1.2 方法根据手术方式的不同,研究病例分为2组:A组为行微创杂交手术患者36例,男性24例,女性12例,合并高血压病患者32例,合并冠状动脉粥样硬化患者12例,糖尿病病史患者12例,吸烟史患者21例。B组为行体外预开窗/单分支覆膜支架全腔内修复术的患者28例,男性19例,女性9例,合并高血压病患者26例,合并冠状动脉粥样硬化患者10例,糖尿病病史患者9例,吸烟史患者19例。
1.3 手术方式术中所有体外预开窗覆膜支架选用先健胸主动脉支架系统,其余胸主支架均选用心脉医疗科技公司胸主动脉支架系统。所有患者手术均在杂交手术室中行全身静脉麻醉及气管插管进行。
颈-锁+TEVAR:于左锁骨上中外1/3处行6~8 cm皮肤切口,钝性游离切口周围皮下组织,于左胸锁乳头肌后方游离出左颈总动脉,于左侧前斜角肌下方游离暴露 LSA,于左颈内静脉后方建立人工血管隧道,静脉肝素化(1 mg/kg),采用Gore 6或8 mm人工血管行左侧颈锁动脉端侧吻合,动脉阻断时间均在12 min以内。常规游离右股动脉,直视下股动脉穿刺行TEVAR,通过术前CTA评估及术中造影情况,选取合适的支架血管及锚定部位,支架血管释放前予以控制性降压,支架血管释放前后常规应用标记猪尾导管置于升主动脉行主动脉造影,评估真假腔显影大小、转流血管是否通畅及释放后内漏有无,如术后造影无异常,5-0prolene线缝合股动脉,间断缝合皮下组织和皮肤。
颈-颈-锁+TEVAR:在颈-锁+TEVAR的基础上,需游离右侧颈总动脉,与人工血管吻合前,先将Gore 6~8 mm人工血管体外预缝合“Y”型,一端和右侧颈总动脉行端侧吻合,另外两端分别和LSA及LCA吻合。
体外预开窗TEVAR:常规右侧股动脉切开入路,左侧肱动脉穿刺,置入6F动脉鞘管,应用5F黄金标记导管造影,结合术前主动脉CTA及术中主动脉造影情况选择合适的先健Ankura胸主支架系统,体外释放2~3节支架血管,“8”字Mark点朝向正上方,根据术前主动脉CTA评估开窗位置,尖刀片雕刻开窗后回收支架,支架血管进入股动脉时确定开窗处位于6点方向,至主动脉弓处时确定位于12点方向,释放前控制性降压,支架血管释放前后常规主动脉造影,无异常后缝合股动脉及皮下组织和皮肤。
单分支型主动脉覆膜支架:穿刺右肱动脉,留置6 F血管鞘,置入5 F猪尾管造影;游离右股动脉,直视下留置10 F血管鞘,左肱动脉送入超滑导丝及MPA1导管至主动脉弓,右侧股动脉送入抓捕器抓捕左肱路径导丝,拉出右股动脉鞘,导管留置体内,两端固定,右侧股动脉送入猪尾导管,过程分段造影,确认全层真腔后送入加硬导丝,取出Castor支架冲洗排气准备,撤右股鞘,同时送出MPA1导管至股动脉穿刺口,撤除导丝,沿MPA1导管置入分支支架牵引导丝出左肱动脉鞘管并固定,同时送主支架经加硬导丝入右侧股动脉,肱动脉处导丝随主体支架系统的送入同步外撤,确定导丝无缠绕及主体支架血管位置无误后释放支架,释放前常规控制患者血压,支架血管释放前后常规主动脉造影,无异常后缝合股动脉及皮下组织和皮肤。
1.4 检测指标收集患者的一般临床资料,包括年龄、高血压、糖尿病、吸烟史、冠脉粥样硬化、住院费用等,所有患者术后第6个月均复查一次主动脉CTA,收集患者出院前及术后第6个月的全主动脉CTA影像学资料,通过PACS自带测量系统测量主动脉峡部及肺动脉分叉平面真假腔直径变化和胸主动脉假腔血栓化程度,用于评估主动脉重塑情况。记录术中手术时间及术后并发症(新发脑梗死、截瘫、Ⅰ型内漏、肾功能不全、肺部感染、切口感染、谵妄、弓部逆撕、死亡等)和术后住院时间。
1.5 统计学方法采用SPSS 25.0统计软件对数据进行分析,计数资料用计数资料用频数和百分比表示,组间比较采用卡方检验,计量资料用“均数±标准差”表示,组间比较采用独立样本t检验。以P<0.05表示差异有统计学意义。
2 结果
2.1 术前两组患者相关指标对比两组患者中的一般情况(年龄、吸烟史、高血压、糖尿病、冠脉粥样硬化、住院费用)比较,差异无统计学意义(P>0.05)。见表1。
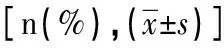
表1 两组患者一般临床资料对比
2.2 两组围手术期相关指标对比两组患者术中及术后均未出现死亡、下肢缺血、截瘫、弓部逆撕及Ⅰ型内漏,围手术期并发症(新发脑梗死、截瘫、肾功能不全、谵妄、切口感染、肺部感染等)无显著差异,B组手术时间及术后住院时间低于A组,有统计学意义(P<0.05),见表2。
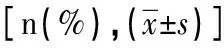
表2 两组患者术中及术后相关指标对比
2.3 术后主动脉重塑相关数据两组患者经微创手术治疗后第6个月和术前对比,主动脉峡部及肺动脉分叉平面真腔直径较术前增大,假腔直径较术前减小,差异有统计学意义(P<0.05),见表3和4,两组患者术后第6个月均可见假腔内血栓形成,A组患者术后假腔完全血栓形成31例(86.11%),B组患者术后假腔完全血栓形成23例(82.14%)。

表3 A组患者手术前后真假腔直径对比

表4 B组患者手术前后真假腔直径对比
3 讨论
国际上相关AD研究显示,急性TBAD患者发病率约为每年3~5/100 000例,该疾病如果不立即进行降压治疗或血管内介入治疗,早期死亡率>50%,单纯行药物保守治疗30 d死亡率为10%,3年后死亡率为25%[5]。TEVAR仍是目前TBAD的首选治疗方法,然而约40%的TBAD会累及主动脉弓部及弓上分支血管,由于LSA远端缺乏健康主动脉组织作为锚定区域,在许多情况下,覆膜支架血管覆盖LSA是必要的[6]。然而,单纯覆盖LSA可能会导致严重的并发症,如脊髓缺血、颅内缺血、左上肢缺血等[7]。因此,对于累及主动脉弓部的TABD,在TEVAR中是否覆盖LSA以及如何重建LSA一直是大血管腔内治疗领域存在争议和激烈争论的问题。随着腔内治疗材料和手术技术的发展,微创弓上血管转流联合TEVAR的杂交手术和应用预开窗及单分支覆膜支架血管的全腔内技术是各中心临床常用的手术方式,相比于传统的开胸大血管置换手术,新的微创手术具有创伤小、并发症少、术后恢复快等优势[8]。
主动脉重塑指主动脉夹层行腔内手术治疗后主动脉直径稳定,其真腔逐渐增大,假腔内血栓形成并完全血栓化,进一步封闭假腔异常血流,改善真腔正向血流的形态学改变[9]。腔内修复术后,人工血管支架具有自扩张特性,既封闭了腔内血管的破口,又使被压缩的真腔得到最大限度的扩张,同时挤压消除假腔,促进撕裂血管壁的重新附着,完成血管壁的重建[10]。Fanelli等[11]通过相关研究表明,良好的主动脉重塑可以有效减少TEVAR术后的主动脉相关不良事件,降低患者术后的死亡率。近年来,也有相关研究发现主动脉假腔是主动脉生长的一个预测指标,未栓塞的假腔可直接影响血流动力学的应力改变和主动脉壁的结构性削弱,这可能导致受影响的主动脉局部进行性生长,而完全血栓形成的假腔则与主动脉扩张及主动脉壁重构相关[12]。
由于患者病变存在个体差异性,累计主动脉弓部TBAD治疗尚无统一的术式。本中心微创弓上血管转流联合TEVAR适用于主动脉弓形扭曲且分支血管明显钙化的患者;破口靠近左锁骨下动脉,颈锁距离较小,且分支血管钙化不严重的患者,本中心采用Castor单分支支架血管;颈锁距离较长(至少>1.5 cm),弓部不扭曲,破口在小弯侧,首选开窗覆膜支架血管,考虑到手术安全性及术者手术经验,本中心主要采用体外开窗技术。本研究中,两组患者一般资料无明显差异,所有手术均顺利完成,术中及术后均未出现死亡,术后未出现下肢缺血、截瘫、弓部逆撕及Ⅰ型内漏,围手术期并发症(新发脑梗死、截瘫、肾功能不全、谵妄、切口感染、肺部感染等)无明显差异,说明在累及主动脉弓部及弓上分支血管的TBAD治疗中,微创杂交技术和单分支及体外开窗覆膜支架血管全腔内修复技术是安全可行且有良好的早期疗效。A组手术时间及术后住院时间高于B组,考虑可能由于微创杂交技术较全腔内手术创面较大,且术中存在阻断颈部血管影响脑部血流,说明单分支及体外开窗覆膜支架血管全腔内修复技术在不增加并发症的前提下,可以有效缩短手术时间及住院时间。
目前尚无评估主动脉形态学变化的相关参数统一指标,且不同节段术后重塑情况不同,本研究主要测量两组患者主动脉峡部及肺动脉分叉平面真假腔的直径及统计术后假腔的完全血栓化情况,用于评估术后主动脉重塑。本研究中两组患者经微创手术治疗后,所测不同平面真腔直径均较术前增大,假腔直径较术前减小,且A组患者术后假腔完全血栓形成31例(86.11%),B组患者术后假腔完全血栓形成23例(82.14%),说明微创杂交技术和单分支及体外开窗覆膜支架血管全腔内修复技术可以显著扩大TBAD真腔,缩小假腔,促进假腔的完全血栓化,有利于术后的主动脉重塑,进一步改善患者的预后。
综上所述,微创杂交手术和全腔内修复手术治疗累及主动脉弓部TBAD的早期疗效良好,且均是安全可行的。相对于微创杂交手术,全腔内修复手术可以缩短手术时间及术后住院时间,在临床治疗可优先选择。但本研究属于单中心经验总结,样本量较少、术后观察时间较短,有待扩大样本及长期疗效的研究。

