拉罗尼酶治疗黏多糖贮积症Ⅰ型药品潜在不良事件的挖掘与分析
纵尚尚,杨小娟,高茂威,陈玮
作者单位:皖北煤电集团总医院,a药学部,b药物临床试验中心,安徽 宿州234000
黏多糖贮积症Ⅰ型(mucopolysaccharidosis typeⅠ,MPS Ⅰ)是因编码a-L-艾杜糖醛酸酶的基因突变引起的一种溶酶体贮积症[1]。这种遗传性疾病导致黏多糖(GAGs)肝素和硫酸皮肤素在所有器官和组织中广泛积累,其所造成的临床症状呈多样性的特点[2]。特异性的酶替代治疗及基因治疗是该类疾病最有希望的治疗手段。其中,酶替代疗法于1991年首次用于葡糖脑苷脂病的治疗,同时也正是从2001年开始开发用于MPS Ⅰ。对a-L-艾杜糖醛酸酶缺乏的病人使用拉罗尼酶(aldurazyme)治疗一年,发现能够改善疾病的一些临床表现[3]。拉罗尼酶主要用于治疗黏多糖贮积症的非神经系统表现,研究使用过程发现该药对MPS Ⅰ病人是有效和安全的,与安慰剂组的研究结果相比,在大约26 周的治疗后,黏多糖的尿排泄量减少,肺活量也有所改善[4]。2003 年,拉罗尼酶获美国食品药品监督管理局(food and drug administration,FDA)批准用于罕见遗传性疾病黏多糖贮积症Ⅰ型的治疗药物,其他适应证还包括患有Hurler 和Hurler-Scheie 形式的黏多糖贮积症Ⅰ型的病人以及具有中度至重度症状的Scheie 形式的病人。2020 年6 月国家药品监督管理局(national medical products administration,NMPA)批准拉罗尼酶浓溶液在我国上市,其属于临床急需境外上市药品,主要用于黏多糖贮积症Ⅰ型病人的长期酶替代治疗。国内关于使用拉罗尼酶治疗MPS Ⅰ的文献报道相对较少,1 例MPS Ⅰ型病儿使用拉罗尼酶治疗,以辅助后期造血干细胞的移植,病儿使用拉罗尼酶进行两轮酶替代治疗后,临床症状有一定程度上的改善,这些和国内外使用拉罗尼酶治疗MRS Ⅰ的报道一致[5-8]。本研究旨在对FAERS 报告的不良事件(adverse event,AE)进行数据挖掘,以期为临床合理安全使用拉罗尼酶提供参考依据。
1 资料与方法
1.1 数据检索和处理本研究数据为FAERS 系统中上报的关键词为“ aldurazyme”与“ laronidase”的,截止日期为2022 年11 月10 日的所有药品不良事件,通过对比《国际医学用语词典》(medical dictionary for regulatory activities,MedDRA)(23.0 版)中系统器官分类(system organ classification,SOC)和首选术语(preferred term,PT)对挖掘出的风险信号进行描述和分类,结合EXCEL和Prism 5.0对所得数据进行整理分析以及相关图表的绘制。
1.2 数据挖掘与风险信号检测标准本研究共计检索出与拉罗尼酶相关的不良事件2 795 例,参考已有文献计算方法及风险信号检测标准[9-11],使用比例失衡法中的报告比值比法(reporting odds ratio,ROR)及综合标准法(medicines and healthcare products regulatory agency,MHRA)计算 ROR 值、ROR95%置信区间(CI)及比例报告比值(proportional reporting ratio,PRR)的值。比例失衡法四格表见表1,ROR、PRR计算公式以及检测阈值见表格2。

表1 比例失衡法四格表及相关计算公式
2 结果
2.1 筛选符合标准的拉罗尼酶相关AE事件上报情况及基本人口学资料本研究共计从FARES 数据库中筛选出AE 关键词为“ aldurazyme”与“ laronidase”的不良事件2 795例,该数据库中AE报告数据是自2003 年拉罗尼酶上市始至2022 年11 月10 日止的20 年的数据,AE 事件上报情况及基本人口学资料情况见表格3。全部筛选AE 数据中男性占1 272 例(45.5%)与女性1 242 例(44.4%),男女比例基本持平;数据上报人员类型主要是医护工作者(1 455 例,占52.1%)和消费者(1 314 例,占47.0%);AE 报告中病人年龄2 岁以下445 例(12.3%),2~17岁1 191 例(42.6%),>17~64 岁638 例(22.8%);死亡病例526 例(18.9%);AE 事件上报的数量每年虽略有起伏,但总体呈逐年递增趋势,见表3。
2.2 纳入的拉罗尼酶相关AE事件信号检测结果
2.2.1SOC 信号分析 研究中对挖掘出的AE 事件进行SOC 分类发现,上报的拉罗尼酶所有AE 事件共涉及27个SOC,排名前10的SOC信号是全身性疾病及给药部位各种反应(1 137例);感染和侵染类疾病(896 例);呼吸、胸腔和纵隔疾病(708 例);伤害、中毒和手术并发症(647 例);神经系统疾病(538例);胃肠疾病(417 例);心脏器官疾病(405 例);各类检查(388 例);各类手术及医疗操作(376 例);血管疾病(302例)。
2.2.2PT 信号分析 采用报告比值比法及比例报告比值比法对所筛选出的AE 事件进行筛选,共筛选出高度怀疑是药物不良反应(adverse drug reactions,ADR)信号共61个,主要涉及15个SOC。排名前20 位的PT 信号见表格4。由表2 可知发热(347例)、肺炎(200 例)、呕吐(153 例)、呼吸困难(142例)、咳嗽(118 例)、不适(98 例)、荨麻疹(92 例)、呼吸衰竭(76例)、癫痫(76例)与流行性感冒(71例)等是拉罗尼酶主要的不良事件。
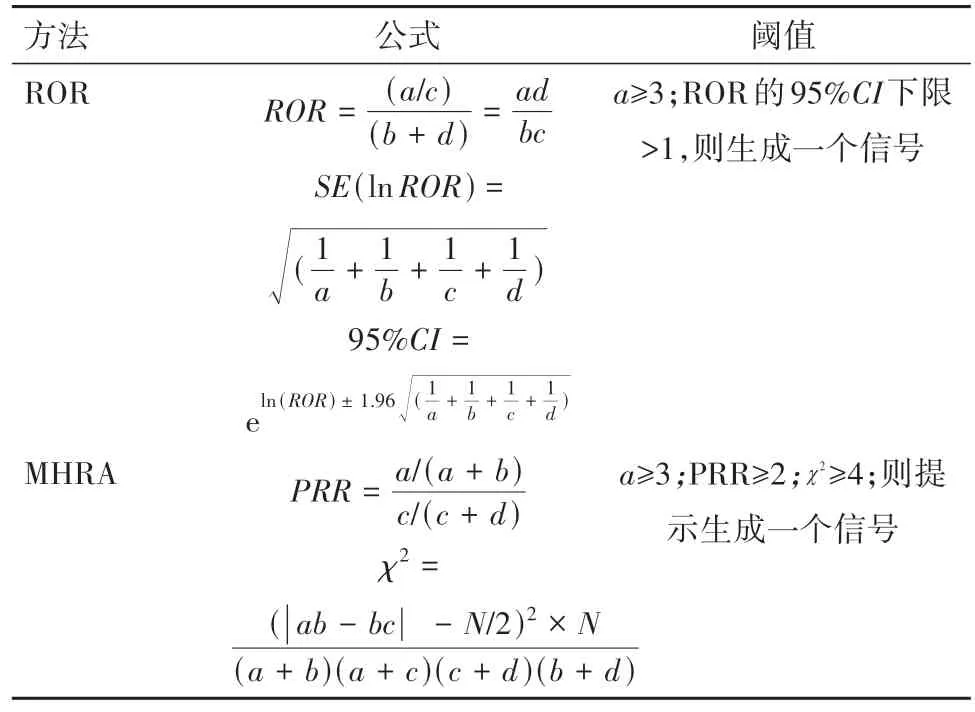
表2 ROR法及MHRA法公式及阈值
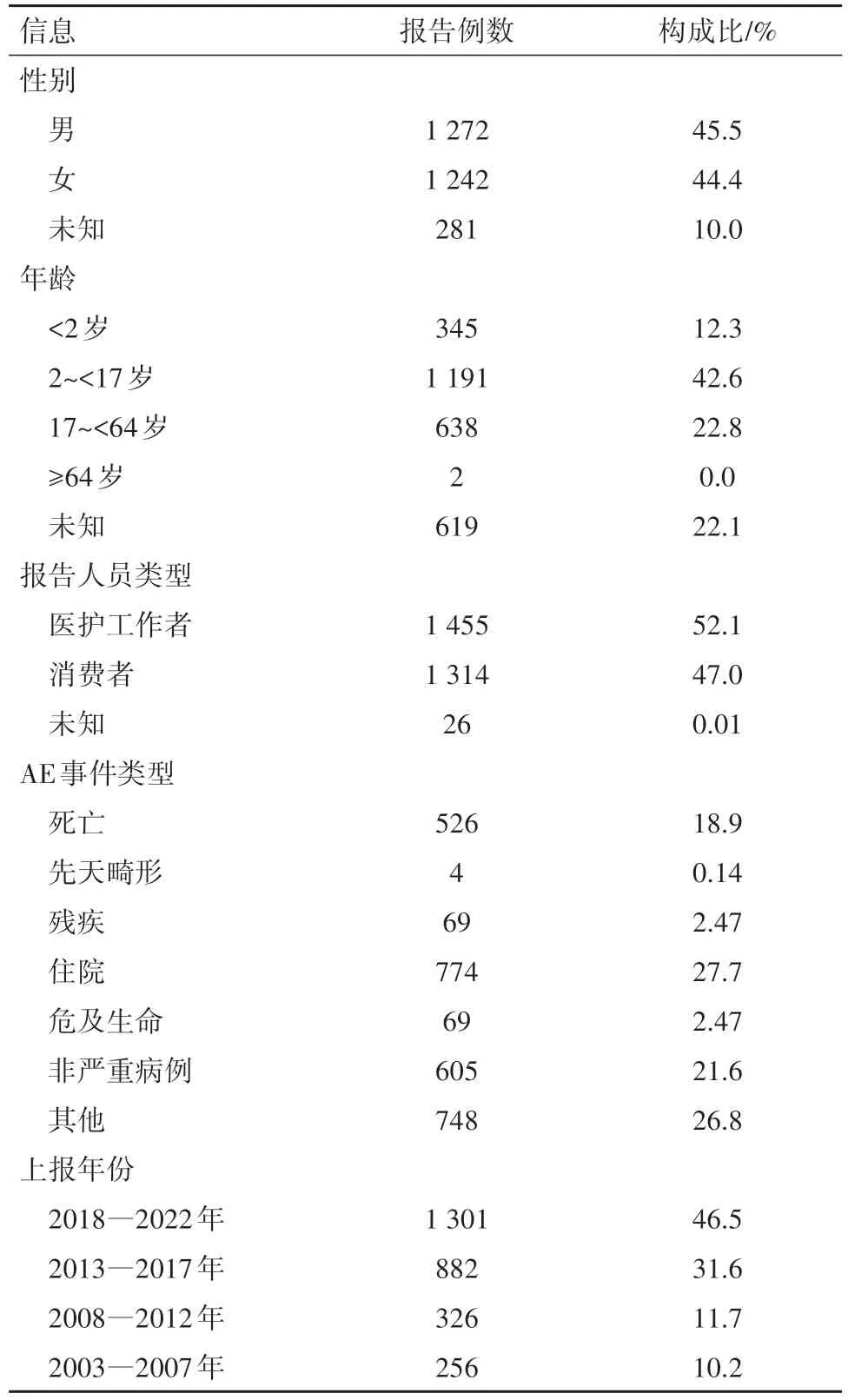
表3 符合纳入标准的AE报告上报情况及人口学资料

表4 报告数排名前20位的拉罗尼酶相关AE报告的PT信号
2.2.3各SOC 的PT 信号分布 本次研究共筛选出的61个高频信号分别映射13个SOC。见表5,6。

表5 数据库挖掘出的各SOC的PT信号分布情况

表6 数据库挖掘出的各SOC的PT信号分布情况
按照MedDRA 将61 个潜在ADR 信号对应其SOC 后,发现其主要集中于感染和侵染类疾病(10个)、全身性疾病及给药部位各种反应(9 个)、呼吸、胸腔和纵隔疾病(9个)、心脏器官疾病(8个)等。
3 讨论
拉罗尼酶是全球首个也是目前唯一批准治疗黏多糖贮积症Ⅰ型的酶替代疗法[12-14]。一项涉及10名MPS Ⅰ病人的Ⅰ/Ⅱ期临时试验数据表明,大多数研究病人临床表现有所改善,其中5 例病人在输液过程中出现短暂性荨麻疹,少数病例中还伴有血管水肿及短暂性低氧血症。尽管如此,在该项临床研究中,长达52 周的用药周期病人的耐受性良好,肝脾肿大及尿中GAG 水平明显降低,病人关节活动范围改善,心功能改善,睡眠呼吸暂停和低呼吸的发生率降低。Ⅲ期临床试验数据证明拉罗尼酶确实可改善病人的临床表现,病人在接受与Ⅱ/Ⅱ期临床试验相同的剂量和给药频次治疗26周后,部分病人出现发烧、头痛、鼻炎和皮疹等不良事件[4],出现的这些不良事件也与说明书及本研究挖掘出的不良事件信号呈现一致,这也说明通过对数据库的挖掘以发现药物潜在不良事件方法的可行性。
本次共挖掘出关于拉罗尼酶高度相关PT 信号61个,共映射15个SOC,其中发热、肺炎、呕吐、呼吸困难、咳嗽、不适、荨麻疹、呼吸衰竭、癫痫、流行性感冒为排名前10 位的不良事件,其中除癫痫外,其余不良事件在拉罗尼酶说明书中均有收录。15 个SOC 主要为全身性疾病及给药部位各种反应,感染和侵染疾病,呼吸、胸腔和纵隔疾病,神经血管疾病,血管疾病等。
通过表3 和表4 数据表明,发热是本次挖掘出的拉罗尼酶最为突出的不良反应,一项为期26周的随机、开放、多剂量优化试验中,病人接受拉罗尼酶治疗过程中出现的最为常见的药物相关不良事件是发热、呕吐、皮疹和荨麻疹等[15]。拉罗尼酶属生物酶类制剂,可产生抗药物抗体(anti-drug antibody,ADA)反应,从而降低疗效或导致过敏反应,这也正是该药物能够引起发热、皮疹及荨麻疹的原因之一[16]。药品说明书明确提出在该药输注期间,在部分病人中观察到危及生命的速发过敏反应。因此,当给予本品时,应随时提供适当的医疗支持。
在感染和侵染类疾病中,肺炎、流行性感冒、鼻咽炎、败血症、感染、尿路感染、鼻窦炎、支气管炎等为信号高频信号。有研究发现,MSP Ⅰ病人通常会发生严重的腹泻、呕吐等胃肠道疾病,但具体原因尚不清楚,研究者认为肠道微生物感染可能是MPS病人腹泻发作的重要原因。在MPS Ⅰ病人的消化道中积累的GAG 可能为微生物的生长提供了一个有利的培养基。在这种情况下,肠道菌群含量的任何变化都会使致病性菌株过度生长的可能性明显高于健康人[17]。积累的GAG也可能损害IgA的产生和/或作用,而IgA 是在肠道中占主导地位的一类抗体,这将使病人对微生物感染更加敏感[18]。其次,感染与侵染类疾病的发生通常可认为是疾病的进展或者因药物治疗无效或治疗效果不显著的信号之一,一旦发生此类疾病应当引起临床医师的高度重视,并采取相应的抗感染治疗[19]。
伴有呼吸功能受损或急性呼吸系统疾病的病人,可能因输注反应而出现呼吸系统损伤的、严重的急性加重并需要额外监测。呼吸系统上气道部分已被证明可受MPS Ⅰ的影响,阻塞性睡眠呼吸暂停的发病率最高[20]。提示我们当病人肺部存在基础疾病或疾病已进展至肺部时,应当密切关注病人的呼吸道症状,及时使用糖皮质激素进行维持治疗。神经系统疾病方面,拉罗尼酶药品说明书中并未明确标示病人可能出现癫痫、意识丧失、言语障碍、嗜睡等不良反应,但遗憾的是我们对此类疾病具体发病机制并不清楚。在对一例患有Scheie综合征的男孩进行了6.5 年的随访中,尽管进行了治疗,疾病仍显著进展,核磁共振成像结果显示颈椎管狭窄和明显的脊髓压迫症,腕管综合征的恶化也很明显。表明拉罗尼酶治疗似乎对Scheie综合征疗效并不明显[21]。此外,精神类疾病方面,本次数据挖掘发现一部分病人出现易怒的症状,这和药品说明书中标注的躁动不良反应类似,提示治疗过程中医务工作者应积极关注病人的精神状态,通过综合了解其生理、心理及社会因素,以保证病人精神状态的平稳,保障病人的用药安全。
心脏器官疾病方面高频信号事件包括心动过速、心脏疾病、心脏停搏、心力衰竭、心律不齐、肺心病、心脏瓣膜狭窄及二尖瓣增厚。根据既往研究MPS Ⅰ病人发生心脏受累较为常见,其发生率高达60%~100%,受累的表现呈多样性的特点,依据其发生率的不同依次为瓣膜结构和功能异常、心肌病、充血性心力衰竭、冠状动脉疾病和房室传导阻滞等[22-25]。心脏受累的情况随年龄的增加逐步加重,需定期监测心功能指标,定期密切随访。临床使用拉罗尼酶过程中还应注意病人随时可能发生的水肿,其主要发生于面部,导管部、肺部以及血管等部位。动态监测病人血压、心率及体温的变化。
本研究的局限性:首先是样本量的有限性,这与MPS Ⅰ较低的患病率有关,研究并不能纳入全部经拉罗尼酶治疗的MPS Ⅰ病人,因此筛选出的不良事件并不能涵盖所有服药后可能出现的不良事件;其次数据库上报人员素质参差不齐,造成数据模糊不规范,从而使结果存在偏倚;第三,本次数据分析方法为ROR法和PRR法,此类检测方法仅反映出目标药物和目标AE 之间的统计学关联,只提示ADR风险增加的潜在可能,其因果关系需要进一步的临床验证;最后,缺乏病人的临床原始病历,不能对临床用药的多样性、疗程、用药剂量以及并发症等因素进行综合考虑,因此在临床用药过程中,需要进一步关注病人服药后的症状表现,积极采取预防措施,保证病人用药安全性。
综上所述,拉罗尼酶已被证明可改变MPS Ⅰ病人的临床表现,但其在临床使用中的安全性仍需要密切关注。本研究基于FARES 数据库的挖掘分析为临床合理安全的使用拉罗尼酶提供依据。考虑本研究的局限性,拉罗尼酶应用的安全性及有效性仍需要进行长期研究,以确定其对生存和生活质量的全面影响,MPS-Ⅰ是一种多系统疾病,需要一个多学科团队的综合方法来优化病人的前景。

