SMILE和WG-FS-LASIK治疗低度无散光近视患者术后早期视觉质量比较
孔 旻, 罗武强, 李丽丽, 肖 信, 陈 琦, 林恩韦, 林 红, 甘 宇
角膜屈光手术从初代的术式经过不断的研究改进,发展为具有微创、高效、伤口恢复快、无瓣、稳定性强以及并发症少等优点的飞秒激光小切口角膜基质内透镜取出术(femtosecond laser small incision lenticule extraction,SMILE)[1],但仍然存在高度散光近视患者术后眩光、暗视力下降等视觉质量不佳情况。波前像差引导的准分子激光原位角膜磨镶术(wavefront aberration guided laser in situ keratomileusis,WG-FS-LASIK)被认为是一种有效降低中高度散光患者高阶像差的手术方式[2],患者术后视觉质量改善较好,但存在切口大、有瓣、术后可能出现瓣移位等缺点。目前,这两种术式对于低度无散光近视患者早期视觉质量恢复的研究鲜见报道。本文就此展开研究,以期为临床选择更优的术式提供参考,现报道如下。
1 对象与方法
1.1研究对象 选择2022年3月至6月在广西壮族自治区人民医院视光中心行SMILE治疗的患者15例(30眼,SMILE组),行WG-FS-LASIK治疗的患者15例(30眼,WG-FS-LASIK组)。两组年龄及视力、视觉指标比较差异无统计学意义(P>0.05),具有可比性。本研究获广西壮族自治区人民医院医学伦理委员会批准(批号:伦理-KY-SY-2022-02号),研究对象签署知情同意书。
1.2纳入与排除标准 纳入标准:(1)年龄18~38岁。(2)术前屈光度数球镜为-0.50~-3.00 D,柱镜均为0。(3)最佳矫正视力≥1.0。排除标准:(1)圆锥角膜或疑似圆锥角膜患者。(2)合并眼表疾病或影响角膜屈光手术的角膜病变患者。(3)合并自身免疫性疾病、甲亢等全身性疾病患者。(4)合并其他眼部疾病患者。
1.3手术方法 两组手术均由同一名具有丰富手术经验的高级医师进行。(1)SMILE组采用VisuMax 2.0飞秒激光手术设备(卡尔蔡司公司,德国),透镜直径6.0~6.5 mm,帽直径比透镜直径大0.8 mm,厚度110~120 mm,切口位置在12点钟方位,长度为2 mm。基质切削后通过切口钝性分离并游离透镜,将透镜取出。(2)WG-FS-LASIK组术前患者均需要暗适应20 min以上,瞳孔直径需保持4 mm及以上,由同一名熟练的技师使用iDesign波前像差仪(强生眼力健公司,美国)测量所有患者全眼波前像差数据并生成切削程序存盘。手术时先使用Intralase iFS飞秒激光器(强生眼力健公司,美国)做瓣,瓣厚95 mm,直径8.6~8.9 mm,蒂部放在12点钟方位,然后换用VISX Star S4-IR准分子激光器(威视公司,美国)在波前像差切削程序数据(于患者术前采集)的引导下进行瓣下切削,术毕用平衡液冲洗基质床碎屑,然后将瓣盖回。
1.4测量指标 于术前和术后1 d、1周、1个月测量以下指标。(1)使用我国标准对数视力表对所有患者测量术前最佳矫正视力(best corrected visual acuity,BCVA)和术后裸眼视力(uncorrected visual acuity,UCVA),将对数视力转换为LogMAR值。(2)欧卡斯测量仪双通道视觉质量分析系统(optical quality analysis system,OQAS)相关指标:应用基于双通道技术的OQAS-Ⅱ系统(西班牙Visiometrics公司),由同一名熟练的技师进行各项客观视觉质量相关指标测量,包括客观散射指数(objective scatter index,OSI)、调制传递函数截止频率(modulation transfer function cut-off frequency,MTFcut-off)、斯特列尔比(Streeler ratio,SR)和可预测对比度视力(predictable visual acuity,PVA)(包括PVA 100%、PVA 20%、PVA 9%)。测量前患者均需要暗适应20 min以上,瞳孔直径需保持4 mm及以上。(3)全眼像差:应用iDesign波前像差仪(强生眼力健公司,美国)测量所有患者全眼的慧差、三叶草像差和球差。所有检查均由同一名熟练的技师完成,检查前患者均需暗适应20 min以上,瞳孔直径需保持4 mm及以上。
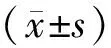
2 结果
2.1两组手术前后等效球镜及视力情况比较 两组术后等效球镜、视力情况均较术前显著改善(P<0.05),但两组各时间点比较差异无统计学意义(P>0.05),见表1。

表1 两组手术前后等效球镜、LogMAR视力比较[M(P25,P75)]
2.2两组手术前后OQAS相关指标比较 两组术后OSI、SR、PVA 9%均较术前显著改善(P<0.05)。WG-FS-LASIK组在术后1 d、1周、1个月的OSI水平均显著低于SMILE组(P<0.05)。在术后1个月,WG-FS-LASIK组PVA 9%显著高于SMILE组(P<0.05),见表2。
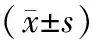
表2 两组手术前后OQAS相关指标比较
2.3两组手术前后全眼像差比较 两组术后慧差、三叶草像差、球差与术前比较差异均有统计学意义(P<0.05)。SMILE组和WG-FS-LASIK组术后慧差均呈先上升后下降的趋势,但WG-FS-LASIK组变化幅度更小,在术后1 d、1周、1个月,WG-FS-LASIK组慧差小于SMILE组,差异有统计学意义(P<0.05),见表3。
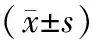
表3 两组手术前后全眼像差比较
3 讨论
3.1目前,角膜屈光手术方式多样,且手术技术发展快速,尤其是SMILE手术已具备无瓣、小切口、微创等优点,不但降低了术后角膜瓣移位的风险,而且保持了角膜前表面结构的稳定性,减少角膜上皮下神经的损伤,增加角膜生物力学的稳定性[3-4]。SMILE手术将切口缩小到2~4 mm,减少术中损伤,患者术后恢复时间更快,将角膜屈光手术带入“微创”时代[5]。但SMILE设备目前尚无法支持个性化治疗方案。
3.2本研究针对低度无散光近视矫正患者开展研究,结果显示,SMILE组术后1 d、1周和1个月的UCVA略低于WG-FS-LASIK组,但差异无统计学意义(P>0.05);在视觉质量方面,SMILE组术后1 d、1周和1个月的OSI水平均显著高于WG-FS-LASIK组(P<0.05)。OSI主要反映人眼的散射程度,值越小提示患者视觉质量越好[5]。本研究还发现SMILE组PVA 9%在术后1个月显著低于WG-FS-LASIK组(P<0.05),而两组术后各时间点SR、MTFcut-off、PVA 100%、PVA 20%比较差异均无统计学意义(P>0.05)。SR为有像差与不存在像差时光学系统成像衍射斑的中心光强度比值,值越大提示视觉质量越好。本研究中两组术后各时间点SR水平比较虽未显示出统计学意义的差异,但WG-FS-LASIK组的改善趋势较SMILE组更好。PVA仅与人眼光学系统相关,客观性更强,值越大提示视觉质量越好[6],PVA 100%、PVA 20%和PVA 9%分别对应白天、黄昏和夜间光学视力。MTFcut-off是指将0.01 MTF值对应的空间频率作为截止频率,可综合反映散射和像差对视觉成像质量的影响,值越大提示眼成像效果越好,越清晰,视觉质量更好[7]。WG-FS-LASIK组术后的UCVA较SMILE组略优。结合两组术后OSI、SR和PVA 9%的比较结果,提示SMILE组手术后1 d时患者视觉质量不及WG-FS-LASIK组。在全眼像差方面,SMILE组术后1 d、1周和1个月的慧差较WG-FS-LASIK组高(P<0.05),两组间各时间点的三叶草像差及球差比较差异均无统计学意义(P>0.05)。值得注意的是,两组术后1 d、1周和1个月的三叶草像差和球差均较术前高(P<0.05),提示无论是SMILE或WG-FS-LASIK术式,患者术后全眼像差均增加,但随后逐渐下降,相比之下WG-FS-LASIK组术后慧差变化幅度更小。
3.3SMILE利用单飞秒激光系统进行“无瓣”角膜屈光手术[8]。与传统的FS-LASIK相比,这种微创技术具有手术切口小、生物力学稳定性强、术后医源性干眼发生率低、屈光矫正所需的激光能量低等优点[9-10],得到临床医师和患者的广泛认可。SMILE在术中和术后的安全性已得到不少研究的证实,但在视觉质量方面,尤其是对于高度近视和中高度散光患者,其效果并不优于个性化的LASIK[11-12]。本研究也发现,对于早期低度无散光患者,SMILE组术后视觉质量不如WG-FS-LASIK组。彗差与屈光手术后角膜形状相关[13],三叶草像差是角膜平面的不规则性、偏中心等不对称性的表现[14]。在低度无散光患者SMILE手术中,一方面可能是角膜基质透镜取出后早期局部组织修复不均衡导致慧差增加[15];另一方面也可能是切口位于角膜上方,术后愈合早期上、下方不对称,切口造成的损伤可能向水平方向发展,从而引起三叶草像差的增加。SMILE将基质透镜分离取出,在术后早期角膜帽与基质床未完全改变时,术后伤口愈合使角膜呈现出非球面性改变,从而增加球差[16]。随着角膜逐渐愈合,角膜基质纤维会重新排列,慧差、三叶草像差和球差有所改变,呈现出逐渐下降的趋势,但仍未恢复到术前状态。
3.4临床有多种个性化手术方式,其中包含波前像差引导的个性化切削[17],WG-FS-LASIK切削是一种基于非球面设计的半飞激光切削模式,有利于降低患者(尤其是高度散光患者)的有害高阶像差,包括慧差、三叶草像差和球差等[18-19]。WG-FS-LASIK利用飞秒激光先制作呈90°切口的井盖式角膜瓣,保证了其精确性及预测性,优于机械角膜板层刀[20-21]。另外,WG-FS-LASIK的个性化切削是基于全眼的像差,针对性地消除对视觉有害的高阶像差,通过术前波前像差仪采集全眼像差,分析高阶像差所在的位置,生成个性化切削程序,在手术中引导准分子激光进行个性化切削,能有效降低已经存在的高阶像差,减少手术后引入的高阶像差[22-25],并提供功能性视觉的角膜表面区域[26-27],从而改善视觉质量。但WG-FS-LASIK属于半飞术式,且波前像差引导手术往往切削较深,因此更适用于像差较大且角膜厚度足够的患者[28],其在手术切口优势、术后角膜生物力学稳定性、降低术后干眼症发生率方面不如SMILE。
综上所述,SMILE和WG-FS-LASIK均能有效改善低度无散光近视患者的视力情况,在视觉质量方面,WG-FS-LASIK略优于SMILE。但本研究结论仍需进一步增加样本量和观察指标来进行验证,为临床医师选择合适的术式提供更好的参考证据。

