替洛利生治疗中国发作性睡病患者有效性及安全性的研究
张益萌, 程岳阳, 刘艳慧, 盛情, 符德, 黄朝阳, 李宁, 陈涛, 詹淑琴
发作性睡病(narcolepsy)作为一种罕见的慢性神经系统疾病,其特征是睡眠-觉醒维持困难。日间过度思睡(excessive daytime sleepiness,EDS)和猝倒是发作性睡病的核心症状,EDS的典型特征是反复发作无法控制的困倦感,猝倒是指突然、短暂的肌张力丧失,通常是由情绪诱发[1]。还有部分患者会出现睡眠幻觉、睡眠瘫痪等快速眼球运动睡眠期调节障碍表现。发作性睡病发病率在0.02%~0.05%[2],是国际公认的罕见病,中国也在2023年9月18日将发作性睡病纳入第二批罕见病目录中。
发作性睡病患者的药物治疗旨在减少EDS、猝倒、睡眠幻觉和睡眠瘫痪,改善夜间睡眠中断[3]。参与促进觉醒的各种神经递质(例如去甲肾上腺素、5-羟色胺、多巴胺、组胺)为药物干预提供了多个靶点。目前的治疗药物作用主要的神经递质是增加多巴和GABA的浓度,而这一类的药物都有成瘾和依赖的风险。
替洛利生(pitolisant)作为一种H3受体反向激动剂,可以干扰H3受体信号传导,阻断其抑制作用,增加脑内组胺以及5-羟色胺、去甲肾上腺素、多巴胺和其他神经递质的水平,从而促进觉醒[4]。2016年替洛利生获欧洲药品管理局(EMA)批准用于治疗伴有或不伴有猝倒的成人发作性睡病[5],2018年被美国食品和药物管理局(FDA)认定为发作性睡病的突破性治疗药物,并于2019年和2020年分别被FDA批准用于治疗成人发作性睡病患者的EDS和猝倒症状。《中国发作性睡病诊断与治疗指南(2022版)》推荐替洛利生作为治疗EDS的首选药物(Ⅰ级推荐,A级证据)和治疗猝倒的常用药物(Ⅰ级推荐,A级证据)[6]。因此,本研究通过在中国大陆纳入1型或2型发作性睡病患者,评估替洛利生治疗中国成人发作性睡病患者的安全性和耐受性,并评估替洛利生在治疗发作性睡病EDS和猝倒等症状的有效性。
1 资料与方法
1.1 实验方案
本研究采用开放、单臂的观察性研究方法,项目于2021年8月获得了海南省人民医院伦理委员会的批准。所有受试者被告知项目的真实目的,可自主选择是否同意参加本项目,在入组之前需签署项目告知书及保险授权书。
1.2 研究人群
2021年5月1日—2022年8月30日共有146例患者参与了本项目筛选。对登记的受试者进行入选和排除标准的筛查。所有纳入研究的受试者必须满足ICSD-3中发作性睡病1型和2型的诊断标准,并且入组时Epworth嗜睡量表(ESS)评分应≥14分。在基线访视前至少14 d内受试者应停止接受精神兴奋剂和镇静药物,或三环类抗抑郁药治疗。有重度猝倒的受试者可使用除三环类抗抑郁药以外的抗猝倒治疗,但需要在入组前该治疗已稳定剂量使用至少1个月,且在整个研究期间保持该剂量不变。146例患者中有13例由于年龄<18岁,7例不符合诊断标准,11例存在辅助检查异常,14例无法停用合并药物,67例由于个人意愿退出研究,最后共有34例受试者通过筛选。最初4例患者在筛选时尚未获得本项目伦理委员会批准,且缺乏基线ESS评分等基线数据而未纳入分析。最终纳入分析的受试者共30名(见图1)。

图1 入排流程图
1.3 给药方法
对30名受试者进行基线数据采集后开始接受替洛利生治疗,前3周为灵活剂量滴定到最佳剂量后,稳定剂量持续给药5周,共治疗8周。替洛利生在早晨随早餐单次服用,1次/d,服用剂量采用向上滴定,根据个体的反应和耐受性使用最低有效剂量,最大有效剂量不得超过36 mg/d(见图2)。

图2 受试者用药流程示意图
在试验过程中,临床医生根据受试者对药物的反应调整了用药剂量。其中11例受试者在(D15~D16)采用27 mg/d作为18 mg/d~36 mg/d剂量之间的过渡,1例受试者2次服用22.5 mg/d(D8及D9),1例受试者4次服用13.5 mg/d(D13~D16),1例受试者以27 mg/d完成最后3周治疗(W1066、D36~D56),其他日期均按照以上方案执行。
从剂量递增访视到末次访视期间(D15~D56)接受相同药物剂量的受试者定义为接受稳定剂量替洛利生的受试者,30例受试者中,最后6周内20例受试者以40 mg的稳定剂量治疗,其中10例受试者在D15及D16遵医嘱服用27 mg/d,1例受试者因COVID-19管控断药1 d(D32),1例受试者因感冒自行停药1 d(D51)。1例受试者以18 mg的稳定剂量治疗。
1.4 疗效性及安全性评估
主要疗效指标为使用ESS问卷评估受试者的嗜睡情况。计算关于ESS的应答率,当ESS末次评分不超过10或较基线改变≥3时,认为受试者对治疗有应答。受试者的猝倒次数通过睡眠日记以电子问卷的形式收集。要求受试者每天早晨起床后记录前1晚的睡眠日记,每次评估涵盖的时间段为24 h。在计划访视的前7 d记录猝倒发作的次数以确定猝倒发作频率。次要疗效分析指标使用研究者评估的临床总体印象严重程度量表(Clinical Global Impression of Severity,CGI-S)和临床总体印象病情变化量表(Clinical Global Impression of Change,CGI-C)来测定EDS和猝倒的严重程度。安全性指标评估是通过记录不良事件,比较治疗结束期和基线的实验室检查参数。在本试验中,于筛选时和D56访视中对受试者进行了实验室评估,包括血常规、血生化等。因为受到COVID-19疫情的影响,仅有部分受试者完成了D56的实验室评估。另外,由于各医院的实验室检测差异,个别指标数值可能存在缺失。
1.5 统计学分析
采用SPSS 23.0软件进行统计学分析,符合正态分布的计量资料采用(±s)表示,不符合正态分布的计量资料采用中位数(四分位数)[M(P25,P75)]表示。计量资料采用例数和百分比表示。使用t检验进行符合正态分布的组间比较,使用Wilcoxon检验进行不符合正态分布的组间比较,取P<0.05时有统计学意义。对于在D56时没有ESS评分的受试者,ESSF为末次观察值结转值。对于次要终点的缺失数据不予填补。若发作性睡病确诊日期有缺失,如果年份和月份已知,则使用已知月份的第1天(-01)进行填补。如果只有年份已知,则使用已知年份的1月份第1天(01-01)进行填补。
2 结果
2.1 人口学特征
本研究共纳入分析30例发作性睡病受试者,其中男性23例(76.67%),女性7例(23.33%)。30例受试者的年龄最小20岁,最大54岁,中位年龄为27岁,平均身高为172.53 cm,平均体重为82.43 kg,平均BMI为27.62 kg/m2。
按照中国肥胖工作组和中国糖尿病学会的定义,体质指数(body mass index,BMI)<18.5 kg/m2定义为体质量过低,18.5 kg/m2≤BMI<23.9 kg/m2定义为正常体质量,24.0 kg/m2<BMI<27.9 kg/m2定义为超重,BMI>28.0 kg/m2定义为肥胖。按照此标准,本项目中有50%的受试者超重(15/30),40%的受试者为肥胖(12/30)(见表1)。
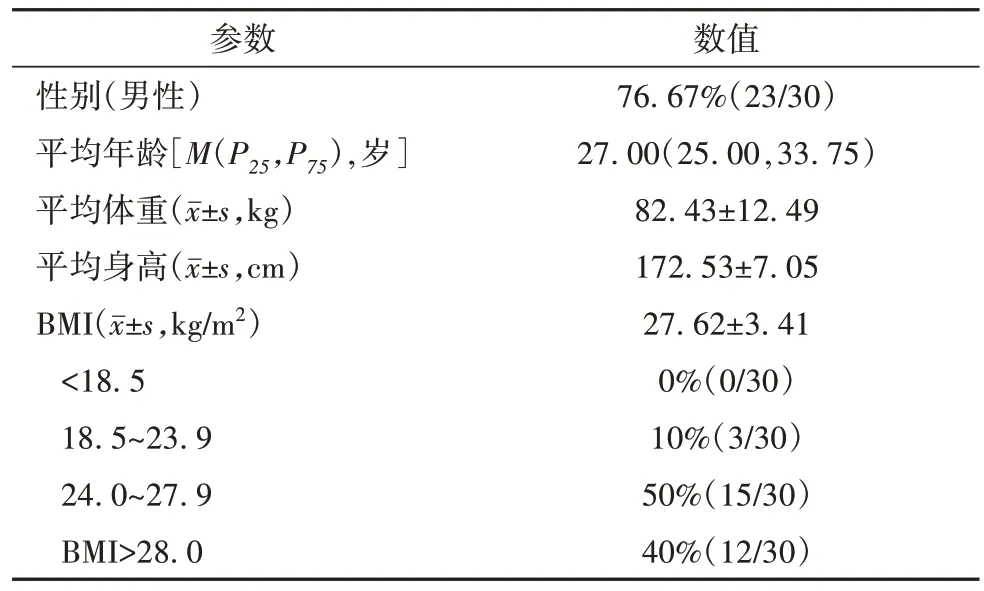
表1 人口学特征总结
2.2 基线临床特征分析
30例受试者中有28例诊断为1型发作性睡病(93.33%)。受试者从确诊发作性睡病到使用替洛利生的中位病程为32.68月(6.91~81.32),最短0.57月,最长244.43月。基线ESS、CGI-S(EDS)、CGI-S(猝倒)评分定义为填写入组申请表时的评分,其中,76.67%(23/30)受试者ESS评分达到重度日间过度思睡(ESS评分≥16分)。受试者出现典型发作性睡病临床症状及量表评分的具体数据见表2。

表2 受试者基线临床特征总结
2.3 替洛利生治疗发作性睡病的疗效评估
2.3.1 替洛利生治疗日间思睡的疗效
2.3.1.1 ESS评分及应答率 受试者接受替洛利生治疗后,2周内ESS评分显著降低,此后持续稳定,与基线相比,各访视点ESS评分相较于基线的差异均有显著变化(P<0.001),至治疗结束时(D56),ESS评分相较基线下降了(-7.63±4.79)分,具体数值和变化趋势(见表3、图3)。
表3 各访视点ESS评分及相对基线评分变化(±s)
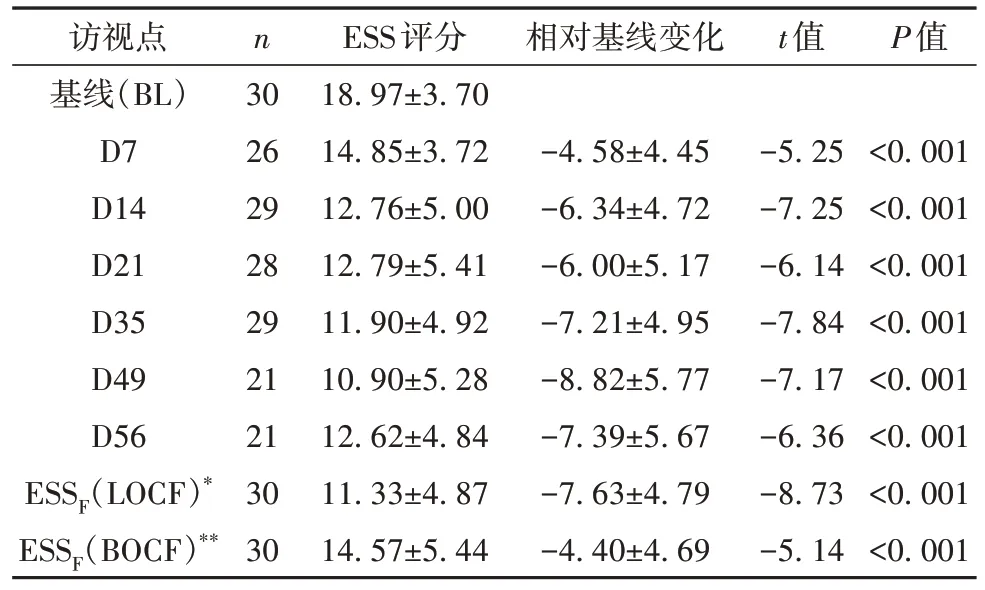
表3 各访视点ESS评分及相对基线评分变化(±s)
*LOCF:如果末次ESS评分[ESSF]缺失,则采用末次观察值结转法替换ESSF。**BOCF:如果ESSF缺失,则采用基线观察值(ESSBL)替换ESSF。
访视点基线(BL)D7 D14 D21 D35 D49 D56 ESSF(LOCF)*ESSF(BOCF)**n 30 26 29 28 29 21 21 30 30 ESS评分18.97±3.70 14.85±3.72 12.76±5.00 12.79±5.41 11.90±4.92 10.90±5.28 12.62±4.84 11.33±4.87 14.57±5.44相对基线变化-4.58±4.45-6.34±4.72-6.00±5.17-7.21±4.95-8.82±5.77-7.39±5.67-7.63±4.79-4.40±4.69 t值-5.25-7.25-6.14-7.84-7.17-6.36-8.73-5.14 P值<0.001<0.001<0.001<0.001<0.001<0.001<0.001<0.001
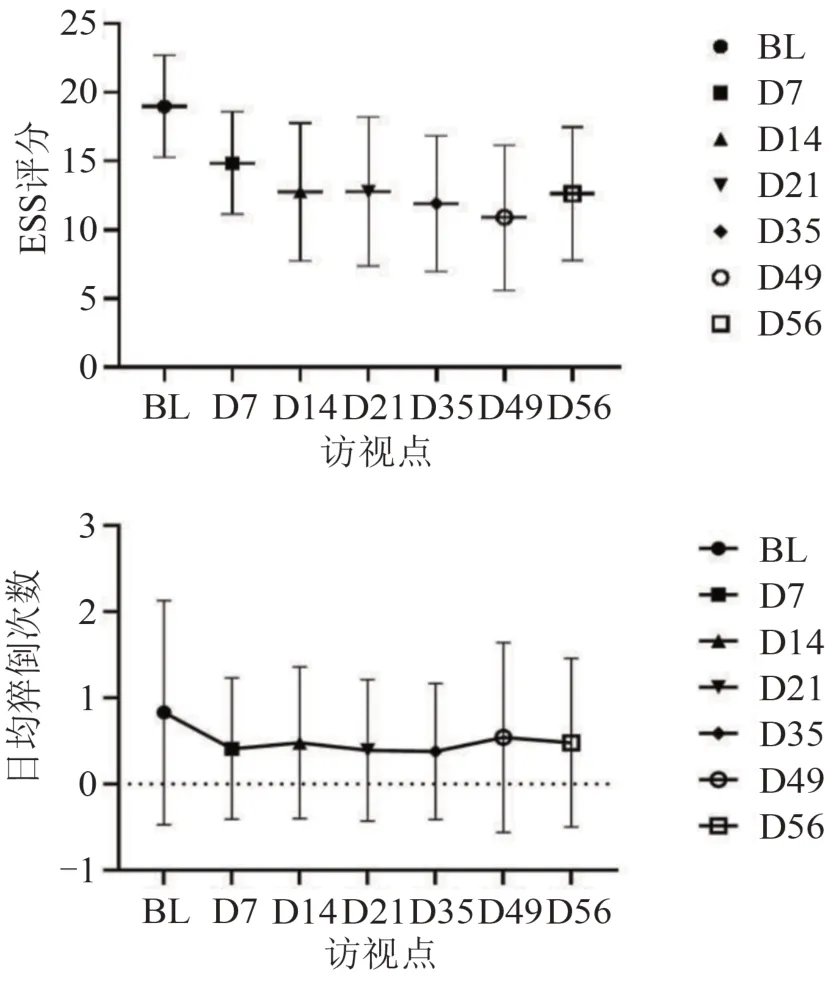
图3 ESS评分及日均猝倒次数的变化趋势
分别采用两种标准计算ESS应答率,若①ESSF(末次ESS评分)≤10或②ΔESS≥3或ESSF≤10,将受试者视为应答者,ESS应答率(见表4)。
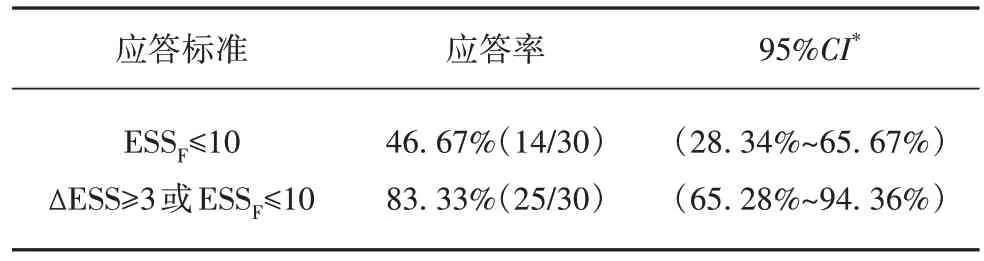
表4 ESS评分应答率
2.3.1.2 CGI-S和CGI-C评估EDS 在基线时,使用 CGI-S 问卷评估 EDS 的严重程度。不同严重程度对应的评分如下:0=未评估;1=正常,没有生病的迹象;2=非常轻微;3=轻微;4=中度;5=重度;6=严重;7=极其严重。基线CGI-S 评分为6.00(4.75,7.00),D56 时CGI-S评分为3.00(2.00,4.00)。经过8周替洛利生治疗后,EDS严重程度中位数由基线时 “严重”改善为“轻微”。治疗前后CGI-S评分具有统计学差异(P<0.001)(见图4)。

图4 治疗前后EDS症状与CGI-S评分比较
通过CGI-C分析EDS的变化,结果显示替洛利生治疗7 d时,受试者获得改善(即,报告的EDS为“显著改善”“改善”或“稍改善”)的受试者比例为76.92%(20/26),治疗56 d时,获得改善的受试者比例为85.71%(18/21)。以上结果与在主要终点观察到的结果一致,即在日常生活的常见情况下,使用替洛利生治疗可改善日间思睡。
2.3.2 替洛利生治疗猝倒的疗效
2.3.2.1 日均猝倒次数 通过睡眠日记得到的受试者基线日均猝倒次数为0.83次,经过替洛利生治疗1周后下降至0.41次,降幅达到50.60%。22例受试者在筛选期及接受8周替洛利生治疗过程中至少有1次猝倒发作。对这些受试者基线及治疗过程中的猝倒发作次数计算几何平均值。对发作次数为0时按0.5/d数进行填补。日均猝倒率几何平均值相较基线均有下降,其中接受替洛利生治疗3周和5周(D21、D35)的日均猝倒率相较于基线的下降是显著的(P<0.05)。其他各访视日均猝倒次数、日均猝倒次数几何平均值和趋势(见表5、图3)。

表5 日均猝倒次数及几何平均值
2.3.2.2 CGI-S和CGI-C评估猝倒 对入组时报告有猝倒发作的28例受试者进行CGI-S和CGIC评估猝倒症状的改善程度。在基线时,使用 CGI-S量表评估的猝倒严重程度。基线CGI-S评分为3.00(2.00,4.00)。D56时CGI-S评分为1.00(1.00,2.00)。经过8周替洛利生治疗,猝倒严重程度由基线时“轻微”改善为基本“正常”。治疗前后CGI-S评分具有统计学差异(P<0.001)(见图4)。
CGI-C评分结果显示替洛利生治疗7 d时,受试者获得改善(即,报告的猝倒为“显著改善”“改善”或“稍改善”)的比例为67.86%(19/28),治疗56 d时,获得改善的受试者比例为69.23%(18/26)。以上结果与在主要终点观察到的结果一致,使用替洛利生治疗可改善猝倒发作。
2.3.3 不良事件(AE)及实验室检查指标
2.3.3.1 不良事件记录 在接受替洛利生用药的所有30例受试者中,共有8例(26.7%)受试者报告了18例次AE。在本项目中报告的所有AE均被评价为与替洛利生可能有关或很可能有关。所有受试者均未报告严重不良事件(SAE)。按照系统器官分类(SOC)和首选术语(PT)显示。
按照SOC分类,最常见(≥2例受试者报告)的SOC为“精神病类”,共有6例(20.0%)受试者报告6例次AE,包括中间易醒型失眠和失眠;其次为SOC“各类神经系统疾病”,共有3例(10.0%)受试者报告5例次AE,包括头痛、头晕和感觉减退;其余SOC均仅有1例(3.3%)受试者报告。
按照PT分类,最常见的PT为“中间易醒型失眠”,共有5例(16.7%)受试者报告5例次;其次为“头痛”和“头晕”,分别各有2例受试者(6.7%)报告2例次;其余PT均仅有1例(3.3%)受试者报告1例次。
最终经评估,所有AE中,除1例(3.3%)受试者的肝酶升高,AE为中度并停药接受了药物治疗外,其余AE均为轻度,未采取任何药物治疗。
2.3.3.2 治疗前后实验室检查指标评估 各个实验室参数正常(在正常值范围内)和异常(超出正常值范围)的受试者比例分析。大多数受试者在研究期间的实验室检查值都在正常范围内,且异常值都与基线病史、合并疾病等有关。治疗前后指标的改变没有统计学意义。
3 讨论
发作性睡病(narcolepsy)作为一种罕见的慢性神经系统疾病,好发于儿童青少年,高峰发病年龄在10~15岁,呈双高峰现象,男女发病比例相当。典型的症状包括EDS、猝倒、睡眠幻觉、睡眠瘫痪和夜间睡眠紊乱[7]。发作性睡病有两种类型:1型发作性睡病(narcolepsy type 1,NT1) (伴有猝倒发作和/或脑脊液食欲素水平低)和2型发作性睡病(narcolepsy type 2,NT2)[不伴有猝倒和(或)脑脊液食欲素水平无减低][8]。目前认为NT1的发病机制可能是由激活免疫通路的遗传因素(如HLA-DQB1*06:02)和环境因素(如感染)导致的下丘脑外侧分泌食欲素的神经元选择性丧失引起,而NT2的病理生理学尚不太清楚[9]。
美国食品和药物管理局(FDA)批准用于治疗成人发作性睡病EDS的药物包括传统兴奋剂(如安非他明、哌甲酯)、促醒药(如莫达非尼、阿莫达非尼)、多巴胺和去甲肾上腺素再摄取抑制剂(索安非托)等[10]。此外,选择性5-羟色胺再摄取抑制剂(SSRIs)、5-羟色胺和去甲肾上腺素再摄取抑制剂(SNRIs)等抗抑郁药也被超说明书范围使用。由于猝倒、睡眠瘫痪和睡眠幻觉都是REM睡眠调节障碍的表现[11],所以对猝倒有效的药物也有望减轻其他REM睡眠相关症状。然而,迄今来自对照临床试验的确证性数据有限。多巴胺是一种促觉醒的神经递质,传统兴奋剂和促醒药,例如安非他明和莫达非尼,是通过增加多巴胺的突触浓度来促进觉醒的。索安非托是一种多巴胺和去甲肾上腺素再摄取抑制剂,其治疗发作性睡病患者的EDS的疗效已经得到证实,然而其对猝倒似乎没有明显的改善[12]。由于多巴胺也参与其他的行为和心理过程,例如动机和奖励,可能会导致促醒之外的辅助作用:药物滥用和成瘾。去甲肾上腺素和5-羟色胺参与猝倒的发生机制,因此抗抑郁药如TCAs、SSRIs和SNRIs常被超说明书范围使用,但这一治疗方案缺乏大型临床试验证实[13],且停药可能会导致反跳性的猝倒。综上所述,一方面,目前缺乏同时对EDS和猝倒均有显著改善的药物;另一方面,传统的发作性睡病治疗药物均存在自己的短板。因此,发作性睡病的药物治疗亟待探索。
组胺是一种单胺类信号分子。在大脑中,组胺主要是作为促进觉醒以及抑制快眼动睡眠的神经递质发挥功能。在大脑中,结节乳头体核(TMN)是脑组织中组胺的唯一神经源性的来源。组胺可以通过四种不同的G蛋白耦联受体(H1-H4)发挥作用,其中H1、H2以及H3受体都在脑组织中表达[14]。H3受体是一种一致性的自身受体。当组胺水平增高时,组胺可以与结节乳头体核神经元的H3受体相结合,使这些细胞超极化并降低这些细胞的活性[15]。H3受体也在多种神经元上表达异种受体,包括制造多巴胺、5-羟色胺、去甲肾上腺素、乙酰胆碱、GABA以及谷氨酸能神经元。H3受体目前已经成为治疗发作性睡病的新的药物靶点。
替洛利生(pitolisant)作为一种H3受体反向激动剂,可以干扰H3受体信号传导,阻断其抑制作用,增加脑内组胺以及5-羟色胺、去甲肾上腺素、多巴胺和其他神经递质的水平,从而促进觉醒[16]。在缺乏食欲素的小鼠中,替洛利生增加了觉醒,减少了NREM睡眠,并且减少了猝倒[17]。在随机安慰剂对照试验(RCT)中,替洛利生对减少成人发作性睡病患者EDS和猝倒的疗效也得到了证实[18]。
在本试验中,ESS评作为主要观察的疗效指标,受试者在接受替洛利生治疗后ESS评分较基线评分有了明显改善(P<0.001),同样的结果也出现在睡眠日记记录的猝倒发生频率中。次要疗效观察指标CGI-S和CGI-C评分呈现出同样的趋势。全球关键研究HARMONY Ⅰ期中也将ESS评分作为主要观察指标[19]。与HARMONY Ⅰ期相比,本试验在基线、治疗结束(F)和△ESS(FLOCF-BL)方面均无显著区别。HARMONY Ⅰ期研究中采用ESSF≤10计算患者应答率,替洛利生治疗组中有45.2%患者为应答者。使用相同标准时,本项目患者应答率为46.67%。采用Fisher精确检验验证本研究与HARMONY Ⅰ期在应答率(ESSF≤10)方面的差异时,没有显著区别,表明替洛利生在中国发作性睡病患者中降低发作性睡病EDS方面的疗效与全球关键临床研究趋势一致,具体比较见表6。

表6 本研究和HARMONY I研究 ESS评分和应答率比较(ESSF≤10)
通过对睡眠日记记录的受试者发生猝倒的频率进行评估,本试验和HARMONY Ⅰ期研究中分别有22例和20例患者在筛选期及接受8周替洛利生治疗过程中至少有1次猝倒发作,针对这些患者睡眠日记中记录的猝倒频率进行评估,根据患者猝倒次数的终末/基线的比值(rate ratio,RR)的几何均值和CV,经Log转换后采用t检验计算,本试验得到的比值比与HARMONY Ⅰ期研究相比未见显著区别(P=0.53),说明替洛利生在控制患者猝倒方面与全球关键研究未见显著差异(见表7)。

表7 本研究与HARMONY I 研究猝倒每日发生率(DCR)比较
从安全性角度来看,所有30例患者中有8例(26.7%)患者报告了18例次AE。最常见(≥2例患者报告)的AE为失眠、头痛和头晕,未发生严重不良事件或死亡。仅1例(3.3%)患者因AE而导致停用药物。基线和D56访视的临床实验室数据结果未见重要的安全性发现。总体来看,替洛利生的耐受性良好,观察到的安全性结果与替洛利生已知的安全性特征象一致。HARMONY Ⅰ期研究中与替洛利生相关的不良反应发生率在治疗的前几周最高,并随着时间的推移而下降。值得注意的是,HARMONY Ⅰ期研究中只有1例接受替洛利生治疗的患者因AE退出研究[19]。这一发现表明,停药并不能解释AE频率随时间推移的减少,提示副作用可能通过继续治疗而缓解[20]。
由于本试验与HARMONY Ⅰ期研究的持续时间相对较短(即3个月),不能排除继续用药后可能出现耐受性和新的治疗紧急不良事件。但是HARMONY Ⅲ期临床研究在真实世界环境和自然条件下进行了为期12个月的前瞻性纵向随访,以评估使用替洛利生的长期安全性和有效性。HARMONY Ⅲ期研究的主要目的是确认在真实生活条件下,在有或无猝倒的成人发作性睡病患者中使用替洛利生的长期安全性,结果显示,替洛利生长期疗效稳定,具有良好的耐受性和安全性,在这项现实的研究中,替洛利生单药治疗或联合治疗患者的不良事件发生率在前3个月内最高,这表明医生和患者在前3个月内应更加关注不良事件的发生。同时,长期使用替洛利生能显著降低Epworth嗜睡量表(ESS)评分和显著改善猝倒发作。日间思睡的最大改善在第6个月时出现,有1/3的受试者在使用替洛利生后日间思睡恢复到正常(ESS<10分)。猝倒的改善也十分显著,在治疗12个月后,每日发生部分性和全身性猝倒的频率都下降了65%和76%。同样的改善也发生在睡眠幻觉和睡眠瘫痪症状中[21]。同时,替洛利生不会刺激与药物滥用有关的伏隔核多巴胺的释放,因此不会出现药物滥用及戒断症[22]。因此,替洛利生已经成为发作性睡病患者安全、有效的治疗新选择。
本研究证实了替洛利生对中国发作性睡病患者的两大症状:日间过度思睡和猝倒发作均有明显改善作用,耐受性总体良好,并且观察到研究结果与全球关键临床研究HARMONY Ⅰ期治疗趋势一致的有效性和安全性,进一步证实了替洛利生在治疗发作性睡病患者的强大能力。
伦理学声明:本研究方案经由海南省人民医院医学伦理委员会审批,批号:医伦乐[2021]第22号,患者均签署知情同意书。
利益冲突声明:所有作者均声明不存在利益冲突。
作者贡献声明:张益萌、陈涛负责设计实验、文章撰写、数据分析、论文审阅;程岳阳负责实施研究、采集受试者数据;刘艳慧负责实施研究、采集受试者数据;盛情负责实施研究、采集受试者数据;符德、黄朝阳、李宁负责统计分析、资料整理;詹淑琴负责研究指导、论文审阅并最后定稿。

