成人慢性活动性EB病毒感染1例*
李 阔 廖大忠 李 艳 西南医科大学附属中医医院 肿瘤血液病科 皮肤科,四川省泸州市 646000
慢性活动性EBV感染(CAEBV)是一种与EBV相关的进行性淋巴增生性疾病,临床少见,预后差。该病皮肤表现独特,系统症状明显,临床预后差,发病机制尚不明确。CAEBV儿童的发生率相对较高,与EB病毒感染有着极为密切的联系,故国内儿童报道较多,成人发病的报道较少。现报道1例以全身皮损、发热、淋巴结肿大、肝脾大为主要表现的成人CAEBV患者,以提高对本病的认识。
1 病例资料
患者男,29岁,已婚,苗族,装修工人。因双上肢红斑、丘疹、水疱、结节伴疼痛、发热2+年,泛发全身1+年,于2020年6月来我院就诊。2+年前无明显诱因双上肢出现散在黄豆大小类圆形红斑、丘疹、水疱、结节,自觉皮损微痛,触及明显,无瘙痒感,自行于当地诊所用药后症状缓解。后患者皮损反复发作,伴体温升高,最高体温达42℃,于当地医院就诊后有所缓解。1+年前皮损加重泛发至全身,四肢为甚,可见大量黄豆大小类圆形红斑、丘疹、水疱、结节,部分呈血疱改变,自诉水疱干涸后形成浅表溃疡,其上可见暗褐色痂壳,皮损遇热及日晒后无改变,初期结节处有轻微触痛,伴有反复体温升高,最高达42℃。1周前,患者上述皮疹再次复发加重,伴发热、四肢乏力、双下肢水肿来我院就诊。个人史:吸烟9年,20支/d,饮酒5年,量少,已戒酒2年。既往史无特殊。家庭成员无类似病史。
全身查体:T 37.3℃,P 101次/min,R 20次/min,BP 103/60mmHg(1mmHg=0.133kPa),全身散在黄豆大小类圆形水肿型红斑、丘疹、水疱、结节,颜色呈淡黄色至暗褐色,部分皮损形成浅表溃疡及坏死,其上覆暗褐色痂壳,四肢可见少许黄豆大小血疱及水疱,皮损以四肢为甚,面部可见不均匀色素脱失斑(见图1)。右侧颈部、双侧腋窝扪及淋巴结,大者约0.8cm,质中,无压痛,活动度尚可,心肺查体无明显阳性体征。腹部膨隆,腹部触诊稍硬,触及肝脏长大,右侧锁骨中线肋缘下约5cm,剑突下约5cm,质中,无压痛,脾脏长大,第1线约5cm,第2线约6cm,第3线约-3cm,移动性浊音阳性。

图1 皮肤表现
实验室检查:血常规:白细胞18.11×109/L,异型淋巴细胞 35.0%,血红蛋白94g/L,淋巴细胞比率74.5%,淋巴细胞绝对值13.49×109/L,血小板计数82×109g/L,超敏C-反应蛋白6.91mg/L。肝肾功能:白蛋白27.3g/L,球蛋白37.1g/L,天门冬氨酸氨基转移酶 117U/L,丙氨酸氨基转移酶 72U/L,γ-谷氨酰基转移酶184U/L。免疫球蛋白:免疫球蛋白G22.70g/L,免疫球蛋白A 3.51g/L,补体C4 0.41g/L。凝血功能:凝血酶原时间16.9sec,部分凝血酶原时间 60.6sec,凝血酶时间测定22.0sec,D-二聚体 0.91mg/L。优生十项:HSV-Ⅰ型抗体-IgM 8.75 AU/mL、HSV-Ⅰ型抗体-IgG 185.67 AU/mL、巨细胞病毒抗体-IgG >1 000.00AU/mL、风疹病毒抗体-IgG 128.75AU/mL、弓形虫抗体-IgG 21.95AU/mL。肿瘤标记物:糖链抗原CA-125 46.18U/mL。EB病毒DNA 1.95×106IU/mL。自身抗体谱:PM-Scl抗体 阳性,ANA滴度1∶100;ANCA 阴性。血清蛋白电泳:血白蛋白 39.53,血α1-球蛋白5.04,血γ-球蛋白38.25,血清蛋白电泳图谱中未发现M蛋白。感染性标志物、BNP、心肌三项、心电图未见异常。
骨髓涂片:目前骨髓增生活跃,异型淋巴细胞占4.5%;骨髓流氏细胞学结果:骨髓中可见约34.33%异常淋巴细胞,怀疑T淋巴细胞或NK细胞淋巴瘤;TCR重排检测:检测到TCRγ基因发生重排:TCRG B(+);IGH重排检测(-)。
影像学检查:胸腹部CT:双肺散在炎症;双侧胸膜增厚,双侧胸腔少量积液;双侧腋窝淋巴结增大;肝脏增大,脾脏增大。腹部彩超:肝大伴实质回声改变,脾大,腹腔积液,胆壁增厚,双肾结石。
病理检查:皮肤组织病理示:“左上肢、右下肢”皮肤组织2块,见皮肤角化过度,皮下血管周及汗腺周多灶性淋巴细胞浸润,玻变胶原纤维内多灶性坏死。免疫组化:CD(-)、CD79a(-)、CD3(少+)、CD5(-)、Ki-67(+20%)、CD21(-)、Vimentin(+)、CD138(-)、CD1a(-)、CD4(少+)、CD8(-),见图2。骨髓活检病理及免疫组化:结合HE及免疫组化结果:骨髓增生活跃,以粒细胞系统为主,未见淋巴细胞增多。免疫组化:CD(+)、CD79a(+)、CD5(+)、CD20(+)、CD34小血管(+)、圆核细胞(-)、CD56(-)、GrB(-)、MPO粒细胞系统(+),见图3。
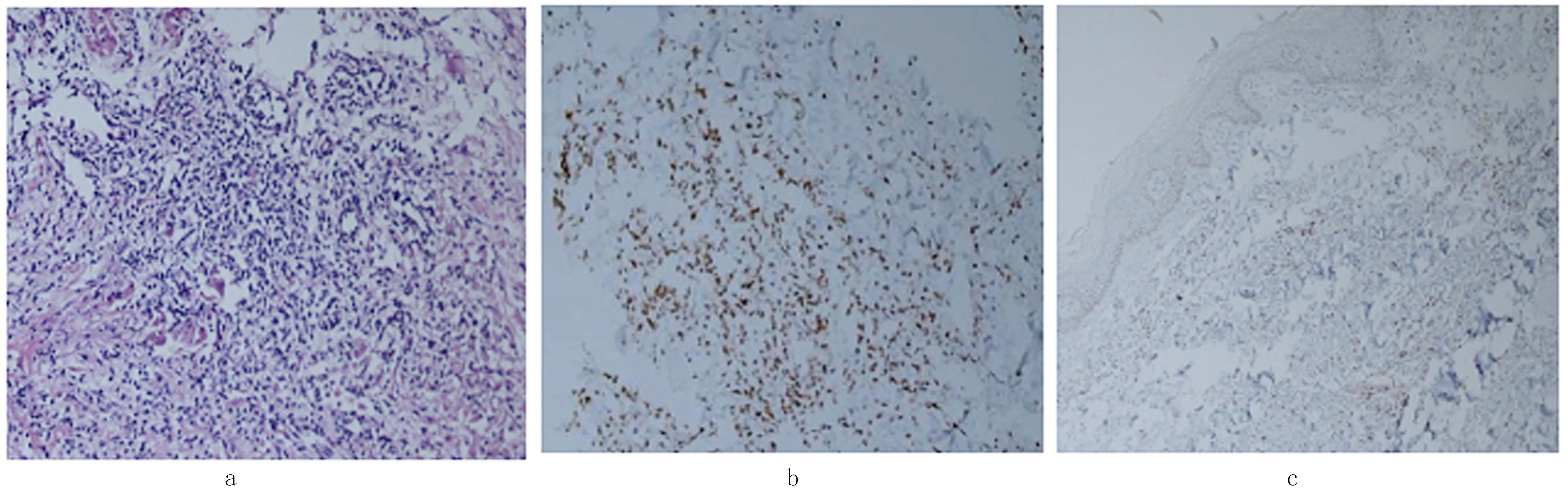
图2 皮肤组织病理及免疫组化

图3 骨髓活检病理及免疫组化
治疗及随访:治疗方案:依托泊苷1.5mg/m2biw w1~2,qw w3~8+地塞米松10mg/m2w1~2,5mg/m2w3~4,2.5mg/m2w5~6 1.25mg/m2w7。化疗第3周时患者肝功能、凝血功能好转,无发热、新发皮疹,肝脾较前缩小。于化疗第4周,患者再次高热、肝脾较前肿大,加用吉西他滨1.4g qw w5~6。其间予以头孢唑肟、更昔洛韦及止呕、抑酸护胃等对症处理。完成化疗7周因经济原因自动出院,第8周化疗未使用。出院时患者仍间断发热(36.5~39.2℃),体重较入院前下降5kg。全身查体:皮肤表现同前,无新发皮疹,颈部、腋窝、腹股沟扪及淋巴结,约0.8cm,质中,无压痛,活动度可,腹部膨隆,肝脾仍肿大同前,移动性浊音阴性。随访:2020年11月20日死亡。
2 讨论
CAEBV是一种以克隆性增殖和活化的EBV感染的T或NK细胞为特征的疾病,伴有慢性炎症和T或NK细胞肿瘤。好发于东亚。CAEBV是由EBV感染所致,发病机制仍不明确,临床表现主要为长期反复发热、肝脾肿大、淋巴结肿大、乏力、贫血等,部分可出现危及生命的并发症,如噬血细胞综合征、间质性肺炎、恶性淋巴瘤等[1]。2016年WHO诊断标准,同时满足:(1)持续或反复发作3个月以上的传染性单核细胞增多症的样症状;(2)EBV感染及引起组织病理损害的证据[2]。治疗CAEBV的目的是控制疾病的两方面:肿瘤和炎症疾病,可抗病毒治疗、免疫调节治疗、联合化疗,但作用有限,目前治疗方法中allo-HSCT是唯一得到肯定的能够治愈CAEBV的方法[3]。多种针对程序性死亡受体1等免疫检查点的单克隆抗体对CAEBV的疗效处于临床试验阶段。
CAEBV多见于儿童和青年人,也可在成人中发现,发生率低,死亡率高,而成年人患者往往进展迅速,预后更差[4]。 国内关于CAEBV的研究相对来说数目过少,主要为儿童病例报道。在28例成年人的研究提示成人CAEBV发病年龄中位数为45岁[5]。本例患者29岁成年发病,有其独特的皮肤表现,皮损呈多样性,包括类圆形水肿型红斑、丘疹、水疱、溃疡、坏死及结痂,愈合后可见瘢痕,主要累及四肢暴露部位,同时该例患者每次发病均伴有反复高热、逐渐出现肝脾大、胸腹腔积液、凝血功能异常、肝功能不全、低蛋白血症等多器官损害。同时实验室检查外周血EBV的DNA载量增高,组织病理提示淋巴细胞浸润真皮全层血管周围,但无明显细胞异形性,且表达多种T淋巴细胞标志物,故CAEBV诊断明确,为其中一种独特皮肤性CAEBV,即种痘样水疱样淋巴细胞增生性疾病。该患者因经济原因拒绝allo-HSCT,予抗病毒治疗、免疫调节治疗及化疗,疗效差,最终死亡。
目前成人CAEBV报道较少,因其发病率低,临床表现重,抗病毒治疗及免疫调节治疗效果仍不明确,目前仍是治疗难点。

