鹅骨鲜味肽的发酵工艺优化及多肽组学分析
冯芯蕊,王冉,章宝,张云凯,2,蔡克周*
(1.合肥工业大学 食品与生物工程学院,安徽 合肥 230031;2.安徽鹅门在鲜食品科技有限公司,安徽 合肥 231131)
中国是世界上较大的鹅养殖生产国之一,年产量达数百万吨。同时,也会产生数量庞大的副产物如鹅骨、鹅血等。鹅骨,作为主要副产物含有肽、氨基酸和钙、磷、铁等丰富的矿物质,以及具有特殊风味的脂肪酸、人类所必需的维生素等其他营养物质[1]。然而,中国对骨资源的综合利用起步较晚,多数还停留在传统加工方式上,比如将鲜骨粉碎成骨粉当作饲料或肥料,甚至直接丢弃。这不仅造成了优质骨资源的浪费,还会造成一定程度的环境污染。因此,提取这些营养物质并充分利用是鹅骨高值化利用的重要途径。
研究表明,鹅骨中富含多种可溶性蛋白质,具有提取生物活性肽的潜力。例如,Zhang 等[2]利用牛骨制备出的胶原蛋白肽-钙螯合物(collagen peptide-calcium chelate,CPs-Ca)具有良好的热加工稳定性,且在胃肠道中可以稳定消化,该研究为制备新型钙补充剂提供了科学依据,提高了牛骨的高值化利用率;Ding 等[3]从鲣鱼(Katsuwonuspelamis)骨中获得了抗氧化胶原蛋白肽,其可有效清除DPPH 自由基、超氧阴离子自由基和ABTS+自由基,能够广泛应用于食品、化妆品和制药等行业;Luo 等[4]从大西洋鲑鱼骨中提取出了胶原蛋白肽(CPs),其具有抗炎作用,可以有效阻止骨关节炎的进一步发展。然而,目前利用鹅骨加工鲜味肽的研究鲜见报道。
鲜味肽是近年来提出的一种新型鲜味物质,不仅呈鲜味,而且可以与NaCl、味精(monosodium glutamate,MSG)协同增鲜[5-6],还可以通过美拉德反应增强食品原有风味[7]。由于鲜味肽具有诱人的口感、良好的加工属性和营养价值,人们从豆类、菇类、发酵产品等不同食物来源中发现了大量鲜味肽。例如,Zhao等[8]通过乙醇沉淀和大孔树脂法,结合感官评价,首次从腌制蚕豆中发现了7 种新型鲜味肽,增强了鲜味和咸味;Kong 等[9]从香菇水解液中分离、鉴定出2 个三肽和3 个二肽,并通过感官评价结合电子舌分析确定了肽的鲜味强度;Wang 等[10]从干腌西班牙鲭鱼中分离出4 条有增鲜作用的鲜味肽。此外,鉴于摄入过量味精在一定程度上会对人体健康产生潜在的不利影响[11],人们越来越意识到鲜味肽作为天然风味来源的重要性。因此,从不同食物中获取有价值的鲜味肽成为研究的重点。
鲜味肽的常见制备方法有酶解法、化学合成法、基因工程法、微生物发酵法等。例如,Shen 等[12]利用风味蛋白酶和木瓜蛋白酶从猪骨中分离并鉴定出了5 种鲜味肽。酶解法在工业上应用广泛,但产品会存在不良风味[13];化学合成法不易控制,产品得率低,实际生产受限;基因工程法表达目标肽的技术尚未成熟,有待进一步研究。利用微生物发酵可以提供多种多样的蛋白酶,而不仅仅是某个单一的酶发挥作用,且蛋白酶活性高,从而可以使前体蛋白分解成不同序列和大小的肽[14],生产成本低、产量高、便于工业化生产和大规模推广[15],是制备鲜味物质的一种经济有效且安全的方法[16]。乳酸菌属和葡萄球菌属都是蛋白酶分泌能力较强的菌种[17-18],理论上会有较高的多肽得率,是理想的发酵菌种。发酵过程中还存在很多其他因素的影响,要得到更多鲜味肽就必须控制发酵条件。
基于质谱的代谢组学、蛋白组学、多肽组学等分析研究在食品、生物、医药等各个领域发挥重要作用。基于多肽组学制备食源性鲜味肽成为食品科学领域的热点研究内容[19]。本研究以鹅骨为原料,利用乳酸菌属和葡萄球菌属进行液态发酵以制备鲜味肽,通过单因素试验和响应面分析,探究底物添加量、菌株接种量、发酵温度、发酵时间对可溶性肽含量和鲜味强度的影响,优化其发酵条件,并在最优工艺条件下对多肽进行鉴定及多肽组学分析,以期为鹅骨的精深加工与高值化应用、研发新型食品鲜味添加剂、畜禽副产物的综合利用提供新思路,为多肽组学在食品研究中的应用提供方向。
1 材料与方法
1.1 材料与试剂
植物乳杆菌[(Lactobacillusplantarum,LP)LP-7、LP-9、LP-12]、木糖葡萄球菌(Staphylococcusxylosus,SX)SX-14、戊糖片球菌(Pediococcuspentosaceus,PP):合肥工业大学食品与生物工程学院肉品加工与健康创新团队微生物实验室保藏;白鹅:安徽鹅门在鲜食品科技有限公司。
MRS 培养基、MRS 肉汤培养基、营养琼脂(nutrient agar,NA)培养基、营养肉汤(nutrient broth,NB)培养基:广东环凯微生物科技有限公司;三氯乙酸(trichloroacetic acid,TCA)、邻苯二甲醛(o-phthalaldehyde,OPA)、甲醇、十二烷基硫酸钠(sodium dodecyl sulfate,SDS)、四硼酸钠、β-巯基乙醇(均为分析纯)、乙腈(acetonitrile,ACN)、甲酸(formic acid,FA)(均为色谱级):国药集团化学试剂有限公司;丝氨酸(分析纯):北京索莱宝试剂有限公司。
1.2 仪器与设备
电子天平(AL204 型)、精确天平(GB/T 23111):梅特勒托利多科技有限公司;华布斯药材粉碎机(800C型):东莞市华太电器有限公司;叠加式振荡培养箱(单层Esci-2010 型):安徽尚科质仪器有限公司;高速冷冻离心机(Sigma3-30N 型):德国Christ 公司;酶标仪(H1型):美国佛蒙特州维诺斯基博腾仪器公司;味觉传感系统电子舌(SA402B 型):日本智能传感器技术有限公司;高效液相色谱仪(EASYnLC1200 型)、质谱仪(QExactive HFX):美国Thermo 科技公司;超净工作台(KLCZ-880A 型):北京亚泰科隆仪器有限公司。
1.3 方法
1.3.1 鹅骨预处理
将鹅骨洗净后剁成小块,去除肌肉、筋腱和软骨等非骨成分。通过反复蒸煮去除上层油脂,然后在80 ℃条件下烘干至完全干燥。最后,使用高速粉碎机将骨头粉碎,得到骨粉(发酵底物),并储存在4 ℃冰箱中待用。
1.3.2 发酵菌株种子液的制备
在无菌超净台中将保存于甘油保藏管中的LP-7、LP-9、LP-12、SX-14 和PP 用无菌接种环取出,分别接种于对应的肉汤培养基(LP-MRS、SX-NB、PP-MRS)中,在35 ℃、130 r/min 条件下活化24 h,然后分别取出于相同条件下二次活化12 h,使培养基中的菌体浓度都达到109CFU/mL,得到各菌株的种子液。
1.3.3 鹅骨发酵液和粗肽的制备以及发酵菌株的选择
将活化后的种子液在8 500 r/min,4 ℃条件下离心15 min,收集沉淀并用无菌生理盐水洗涤2 次,然后将各菌株洗涤后的菌液依次接入发酵培养基,在35 ℃、150 r/min 条件下发酵24 h。发酵培养基配方:以100 mL 发酵液为基准,骨粉4%(4 g),蔗糖2%(2 g),种子液3%(3 mL)。发酵24 h 后取出发酵液,在85 ℃条件下水浴加热15 min 以灭酶,然后在12 000×g、4 ℃条件下离心10 min,取上清液于-20 ℃条件下保存待用。
将各菌株的发酵液按上述方法处理后,分别测定其发酵液中的多肽浓度,选择多肽浓度最高的菌株确定为发酵菌株。采用发酵菌株在上述条件下对鹅骨进行发酵并对发酵液进行灭酶、离心10 min(12 000×g,4 ℃)处理,取出上清液用0.45µm 微孔滤膜过滤,得到滤液即为鹅骨鲜味肽粗肽溶液,冻干后于-80 ℃储存。
1.3.4 指标测定
1.3.4.1 多肽浓度
参考鲁伟等[20]和Yu 等[21]的方法并略作修改,采用OPA 法测定多肽浓度。
溶液的配制:0.6 mol/L TCA 溶液:准确称取9.8 g TCA 固体溶于100 mL 蒸馏水;OPA 试剂:A 液(40 mg OPA 溶于1 mL 甲醇)与B 液(100µL β-巯基乙醇、0.5 g SDS、0.95 g 四硼酸钠溶于50 mL 蒸馏水)混合。
标准曲线的制作:依次配制浓度为0、0.5、1.0、1.5、2.0、2.5、3.0 mg/mL 的丝氨酸(Ser)标准溶液,分别按Ser∶OPA 为1∶20(体积比)混合,避光反应2 min 后于340 nm 下测定OD 值,以第一组(0 mg/mL Ser)为空白对照,Ser 浓度为横坐标x(mg/mL),OD 值为纵坐标y,制作标准曲线。
多肽浓度的测定:取处理后的发酵上清液1 mL,加入2.2 mL 0.6 mol/L TCA 溶液,静置10 min 后于16 200×g、4 ℃条件下离心10 min,取上清液与OPA 试剂按1∶20(体积比)(上清液∶OPA,1∶20)分别取出10µL、200µL 混合,并避光反应2 min,随后于340 nm条件下测定OD 值,代入标准曲线即可求得样品溶液中的多肽浓度。
1.3.4.2 鲜味强度
采用电子舌进行检测分析,参考Zhang 等[22]的方法并稍作调整,测试前将鲜味(AAE)、涩味(AE1)、苦味(C00)、酸味(CA0)、咸味(CT0)和甜味(GL1)传感器在参比溶液(含0.3 mmol/L 酒石酸的30 mmol/L KCl 溶液)中活化24 h。通过监测参比电极的相移来检测味觉传感器薄膜的电位,模拟电子传感器信号被转换成数字信号进行数据处理。每个样品在25 ℃条件下分析5 次,记录每种味道最后3 个数据点的平均值作为最终响应值。
1.3.5 单因素试验
1.3.5.1 菌株接种量的选择
固定2% 蔗糖,4% 底物添加量,设置接种量分别为1%、3%、5%、7%、9%,在35 ℃发酵24 h,测定各组的可溶性肽含量及其鲜味强度。
1.3.5.2 底物添加量的选择
固定2% 蔗糖,3% 接种量,设置底物添加量分别为2%、4%、6%、8%、10%,在35 ℃发酵24 h,测定各组的可溶性肽含量及其鲜味强度。
1.3.5.3 发酵时间的选择
固定2% 蔗糖,3% 接种量,4% 底物添加量,在35 ℃分别发酵12、24、36、48、60 h,测定各组的可溶性肽含量及其鲜味强度。
1.3.5.4 发酵温度的选择
固定2% 蔗糖,3% 接种量,4% 底物添加量,分别在20、25、30、35、40 ℃发酵24 h,测定各组的可溶性肽含量及其鲜味强度。
1.3.6 响应面优化试验
分析单因素试验结果,在此基础上,采用响应面设计的Box-Behnken 设计方法,运用Design-Expert 8.0.6软件进行响应面优化试验。选择对多肽浓度和鲜味强度影响显著的3 个影响因子(接种量、底物添加量、发酵温度),以的可溶性肽含量和鲜味强度为响应值,设计三因素三水平的Box-Behnken 响应面试验,对发酵条件进行优化设计,各因素及水平见表1。
1.3.7 可溶性肽含量计算
可溶性肽含量按下列公式计算。
式中:M为可溶性肽含量,mg/g;c为依据标准曲线得到的多肽浓度,mg/mL;v为发酵液体积,mL;m为发酵液中底物的质量,g。
1.3.8 纳米液相色谱-串联质谱分析法(nano-liquid chromatography-mass spectrometry,nanoLC-MS/MS)鉴定发酵液中的多肽
在最优工艺条件下对鹅骨进行发酵,并将发酵液通过高效液相色谱仪进行鉴定和多肽组学分析。取4µL 样品经高效液相系统进行分离后联用配备纳升离子源的质谱仪进行数据采集。流动相采用乙腈-水-甲酸体系,以0.1%甲酸-98%水溶液(乙腈为2%)为流动相A,以0.1% 甲酸-80% 乙腈溶液(水为20%)为流动相B。色谱柱以100% 的A 相平衡后,样品由自动进样器直接上样到色谱柱,再经色谱柱梯度分离,流速300 nL/min,梯度时长60 min。洗脱程序见表2。
1.4 数据分析
数据结果采用平均值±标准差形式表示。试验数据采用SPSS 19.0 软件进行处理和单因素方差分析,P<0.05 为差异显著。响应面优化试验设计及分析使用Design-Expert8.0.6。采用GraphPad Prism 8 和Origin 2018 软件进行作图。
2 结果与分析
2.1 多肽浓度的标准曲线
以Ser 标准溶液浓度为横坐标,OD340值为纵坐标的标准曲线如图1 所示,其回归方程为y=1.043 9x+0.104,R2=0.994 7。
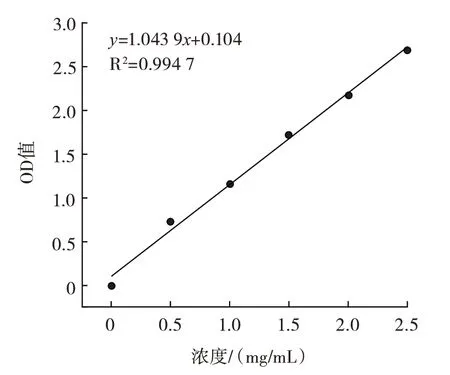
图1 丝氨酸标准曲线Fig.1 The standard curve of serine
2.2 发酵菌株的确定
各菌株发酵液的可溶性肽含量如图2 所示。

图2 接种菌株对发酵液可溶性肽含量的影响Fig.2 Effect of inoculated strains on the soluble peptide content of fermentation broths
由图2 可知,用LP-12 发酵鹅骨所得可溶性肽含量最高,达到41.75 mg/g(P<0.05)。
2.3 鹅骨发酵条件的单因素试验结果
2.3.1 接种量对发酵液中可溶性肽含量及鲜味强度的影响
接种量对发酵液中可溶性肽含量及鲜味强度的影响如图3 所示。

图3 接种量对发酵液中可溶性肽含量及鲜味强度的影响Fig.3 Effects of the inoculation amount on the soluble peptide content and the umami intensity in fermentation broths
由图3 可知,接种量的增加导致发酵液的鲜味强度显著降低(P<0.05),这是由于植物乳杆菌在发酵过程中会产酸,酸味积累会直接影响鲜味强度,接种过多则使鲜味强度降低。可溶性肽含量随着接种量的增加先上升后下降,这是因为在底物浓度一定时,接种量较低使微生物分泌的蛋白酶较少,导致蛋白分解速率慢,从而使得可溶性肽含量较低[23];而随着接种量的继续增加,底物不足以提供微生物生长的营养条件,同时,之前生成的多肽被继续水解成氨基酸,都会导致可溶性肽含量的降低。当接种量大于7% 时,可溶性肽含量没有显著变化(P>0.05),这一趋势与盖梦[24]的研究结果一致。在接种量为5% 时,可溶性肽含量达到了最大值39.84 mg/g,但此时的鲜味强度值较低。综合考虑,选择接种量3%为最佳水平。
2.3.2 底物添加量对发酵液中可溶性肽含量及鲜味强度的影响
底物添加量对发酵液中可溶性肽含量及鲜味强度的影响如图4 所示。
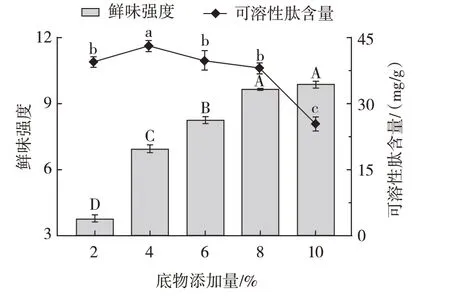
图4 底物添加量对发酵液中可溶性肽含量及鲜味强度的影响Fig.4 Effects of the substrate addition amount on the soluble peptide content and the umami intensity in fermentation broths
由图4 可知,当底物添加量为4%时,可溶性肽含量达到了最大值43.19 mg/g,但此时的鲜味强度较低。随着底物添加量的增加,发酵液的鲜味强度显著增大(P<0.05),当底物添加量高于8%时,鲜味强度无显著变化(P>0.05),而此时的可溶性肽含量迅速下降且降低幅度大,这是由于接种量一定时,在适宜底物浓度范围内,微生物生长条件适宜,可以产生较多的肽,而在高底物浓度下,酶已经达到饱和,菌体代谢速率降低,且前期生成的多肽水解为氨基酸,从而导致可溶性肽含量下降。综合考虑,选择底物添加量8%为最佳水平。
2.3.3 发酵时间对发酵液中多肽浓度及鲜味强度的影响
发酵时间对发酵液中可溶性肽含量及鲜味强度的影响如图5 所示。
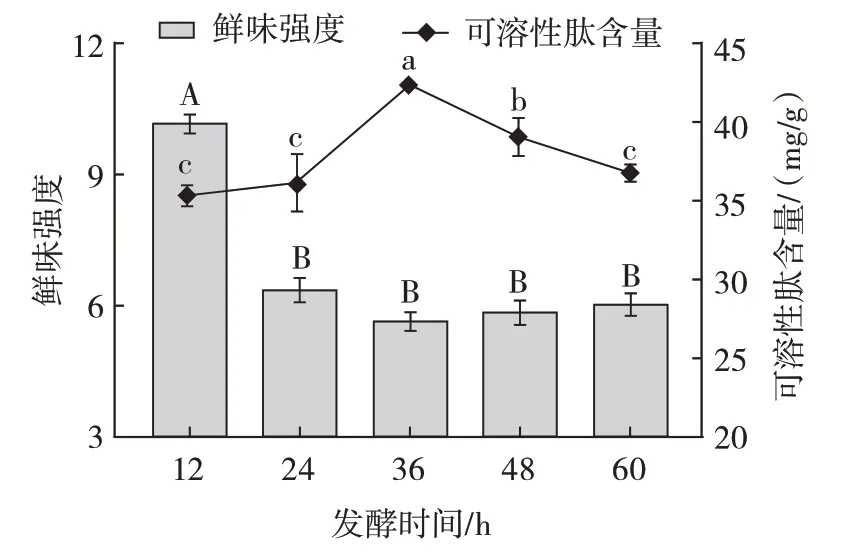
图5 发酵时间对发酵液中可溶性肽含量及鲜味强度的影响Fig.5 Effects of the fermentation time on the soluble peptide content and the umami intensity in fermentation broths
由图5 可知,发酵12 h 时鲜味强度最高(P<0.05),在24~60 h 时,发酵液的鲜味强度均低于12 h且无显著差异(P>0.05),这是由于随着发酵时间延长,乳酸积累导致鲜味强度降低。而多肽浓度随发酵时间的延长先上升后下降,这是由于在发酵初期,发酵产物少,蛋白分解慢,可溶性肽含量低[25],随着发酵时间的延长,微生物大量增殖,产生了更多的可溶性肽。在发酵36 h 达到最大值42.43 mg/g。综合以上分析并考虑时间成本,将发酵时间定为24 h,不列入响应面试验中的因素。
2.3.4 发酵温度对发酵液中可溶性肽含量及鲜味强度的影响
发酵温度对发酵液中可溶性肽含量及鲜味强度的影响如图6 所示。
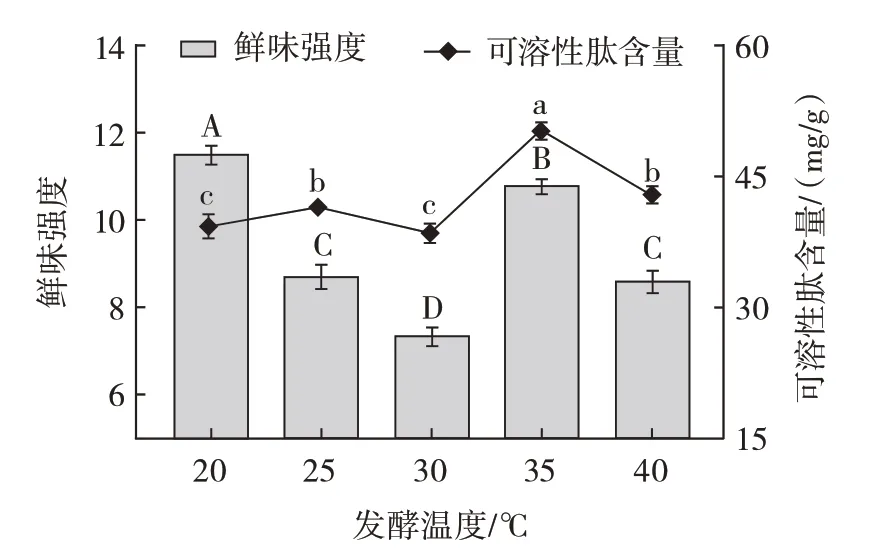
图6 发酵温度对发酵液中可溶性肽含量及鲜味强度的影响Fig.6 Effects of the fermentation temperature on the soluble peptide content and the umami intensity in fermentation broths
由图6 可知,在20 ℃下发酵,鲜味强度达到最高值11.48,而此时可溶性肽含量也较少;其次是35 ℃,鲜味强度为10.72,此时可溶性肽含量最多,达到50.05 mg/g。由于发酵温度过低会导致微生物生长缓慢,而温度过高会使菌体死亡[26],均不利于微生物的生长[27],所以综合考虑,选择发酵温度35 ℃为最佳水平。
2.4 响应面Box-Behnken 试验设计优化
2.4.1 响应面优化结果和方差分析
根据单因素试验结果,三因素三水平Box-Behnken响应面试验的设计方案及结果如表3 所示。
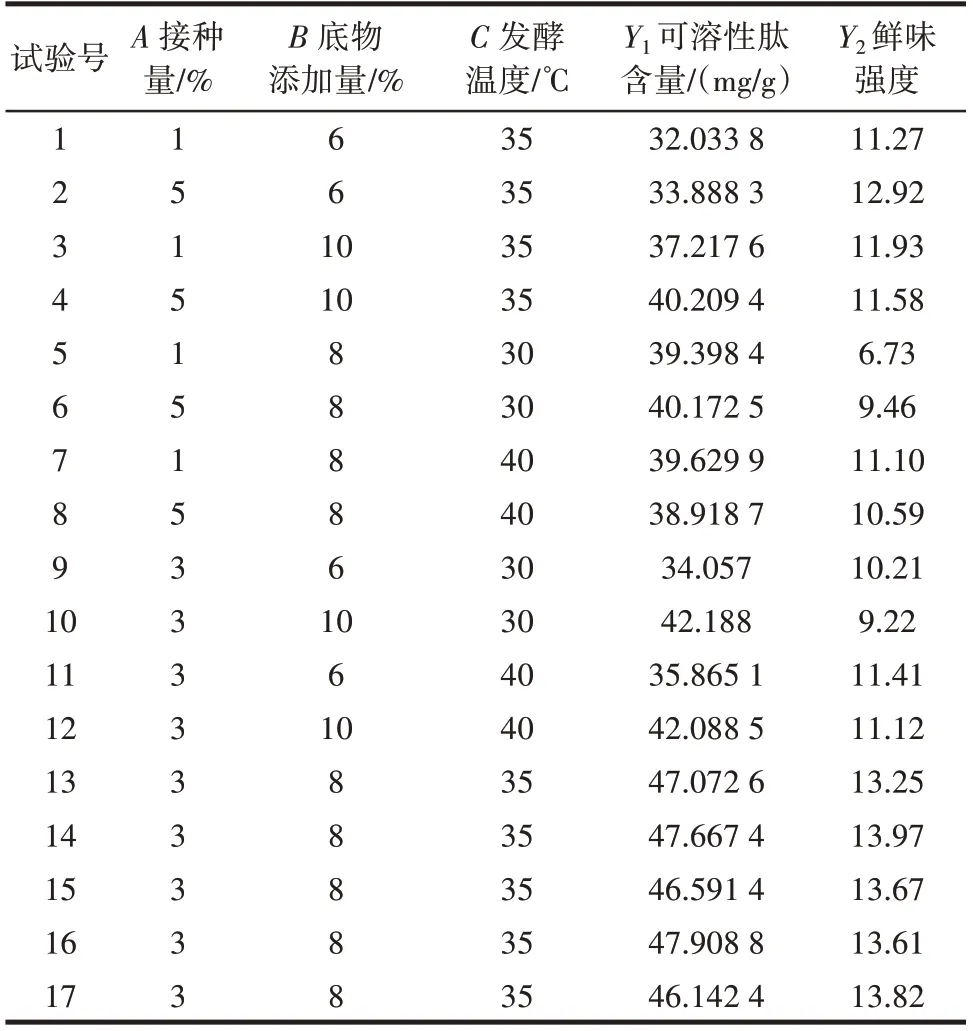
表3 响应面设计方案及结果Table 3 Design scheme and the results of Box-Behnken response surface experimental
利用Design-Expert 8.0.6 软件对试验数据进行二次多元回归拟合,得到发酵液的可溶性肽含量(Y1)与鲜味强度(Y2)对编码自变量A(接种量)、B(底物添加量)、C(发酵温度)的回归方程为Y1=47.08+0.61A+3.23B+0.068C+0.28AB-0.37AC-0.48BC-5.13A2-6.11B2-2.42C2;Y2=13.66+0.44A-0.25B+1.07C-0.5AB-0.81AC+0.17BC-1.38A2-0.36B2-2.82C2。对上述回归模型进行方差分析,结果见表4 和表5。
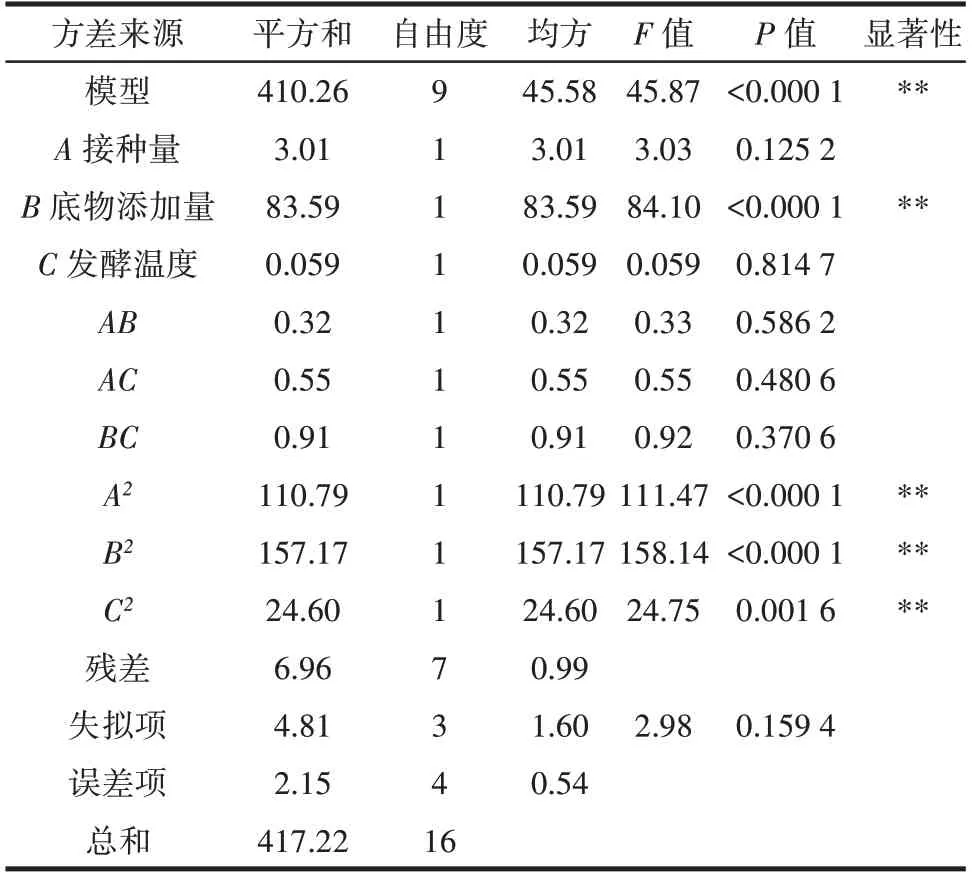
表4 可溶性肽含量方差分析Table 4 Analysis of variance(ANOVA)for the soluble peptide content
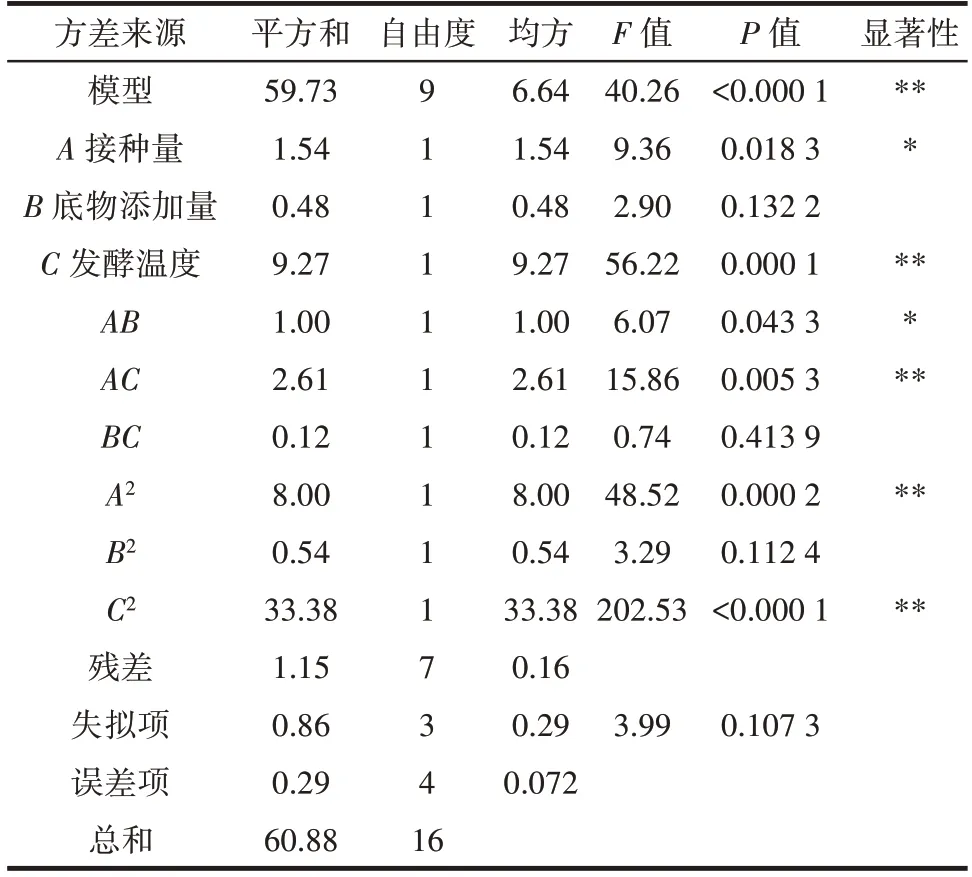
表5 鲜味强度方差分析Table 5 Analysis of variance(ANOVA)for the umami intensity
由表4 可知,可溶性肽含量的回归模型达到极显著水平(P<0.000 1),方程的失拟项不显著(P=0.159 4>0.05),说明该模型拟合度良好,回归方程的可信度高,适用于发酵工艺的优化。信噪比为19.357(>4),R2=0.983 3,说明多肽浓度的预测值与实际值直接有很好的拟合度;由表5 可知,鲜味强度的回归模型达到极显著水平(P<0.000 1),方程的失拟项不显著(P=0.107 3>0.05),信噪比为20.932(>4),R2=0.981 0,说明鲜味强度的预测值与实际值直接有很好的拟合度。综上,可以用此模型预测和分析微生物发酵鹅骨制备鲜味肽的发酵工艺。各因素交互作用对可溶性肽含量及鲜味强度的影响见图7。

图7 各因素交互作用对可溶性肽含量和鲜味强度影响的等高线图和响应曲面图Fig.7 Contour maps and response surface plots of the effects of factor interactions on the soluble peptide content and the umami intensity
2.4.2 模型验证
利用Design-Expert 8.0.6 软件预测出鹅骨鲜味肽的最佳发酵工艺条件为菌株接种量3.14%、底物添加量8.38%、发酵温度35.67 ℃,预测可溶性肽含量为47.444 1 mg/g,鲜味强度为13.712 5。根据试验的实际操作条件,对发酵的工艺参数调整为接种量3%、底物添加量8.5%、发酵温度36 ℃,在此条件下对模型进行验证,得到实际的可溶性肽含量为45.86 mg/g(误差3.34%);鲜味强度为14.03(误差2.32%)。因此,基于响应面法得到的优化工艺参数准确、可靠,可用于实际运用。
2.5 多肽鉴定及组学分析
根据文献报道,大多数鲜味肽所含的氨基酸数量通常在10 个以内,如Gao 等[28]从蛋黄中分离出的六肽APYSGY、七肽AGFMPLP 和十肽VAMNPVDHPH;Li等[29]从蛤蜊水提物中分离出的八肽RPNPFENR;Xie等[30]从火腿中分离出的九肽GPAGPAGPR 等。利用这一特点,对质谱鉴定出的肽进行了初步简单的筛选,共筛选出147 条氨基酸数量在10 个及10 个以下的肽,如图8 所示。

图8 初筛后所得潜在鲜味肽的长度分布Fig.8 The kength distribution of potential umami peptides obtained after primary screening
由图8 可知,本研究得到的发酵液中潜在的鲜味肽集中在六到十肽,其中六肽最多,达到67 条,占比45.58%,其次是七肽(34 条,占比23.13%),这可能是由于分子量较小的肽具有更强的鲜味强度[31]。
对初筛得到的肽的来源蛋白进行分析,结果如图9 所示。

图9 初筛后所得潜在鲜味肽的来源蛋白统计Fig.9 Source protein statistics of potential umami peptides obtained after primary screening
由图9 可知,鹅骨发酵所得的潜在鲜味肽来自胶原蛋白(31.97%)、锌指蛋白(3.4%)及其他杂蛋白,其中主要来源是胶原蛋白。
3 结论
本研究以可溶性肽含量为指标,筛选出植物乳杆菌LP-12 用来发酵鹅骨,制备了鲜味肽粗提物。对影响发酵的接种量、底物添加量、发酵时间、发酵温度进行了单因素试验,并在此基础上设计了Box-Behnken试验进行响应面优化,以可溶性肽含量和鲜味强度为响应值,优化出最佳发酵工艺条件:LP-12 接种量3%、底物添加量8.5%、发酵温度36 ℃、发酵时间24 h,此时,可溶性肽含量为45.86 mg/g,鲜味强度为14.03。对鲜味粗肽鉴定及筛选后得到147 条氨基酸数量在10 以下的潜在鲜味肽,通过多肽组学分析得知,其中大多数肽来源于胶原蛋白。本研究为鹅骨的高值化应用及鲜味肽的开发利用提供了理论支撑与试验依据,并为胶原蛋白的应用开辟了新的研究方向。
综上所述,通过微生物发酵鹅骨可以有效获得潜在的鲜味肽,但是成分依然繁杂不纯,且鲜味特征和呈鲜机制并不明晰。后续的研究应致力于建立一条快速的鲜味肽纯化及筛选路线,尽可能得到较纯的鲜味肽,并探明其具体的味觉特征,阐明其鲜味作用机制。

