助剂对ZnO/ZrO2物化性质及催化性能的影响
任启霞,杨 坤,刘 飞,姚梦琴,曹建新
(1.贵州大学化学与化工学院,贵州贵阳 550025;2.贵州省绿色化工与清洁能源技术重点实验室,贵州贵阳 550025;3.贵州省工业废弃物高效利用工程研究中心,贵州贵阳 550025)
随着化石燃料的过度利用,大量CO2气体排放造成的生态环境问题越发严峻,解决CO2排放问题迫在眉睫[1]。利用可再生能源H2将CO2转化成甲醇不仅可以解决CO2排放问题,还可以有效缓解人类对不可再生能源的依赖[2-3],是实现碳中和目标的有效途径。
目前,CO2加氢制甲醇催化剂主要分为金属基(Cu 基[4-5]、Pd 基[6]、Pt 基[7]、Au 基[8]等)、硫化物基(MoS2[9-10]、MoS2@C[11])和金属氧化物基催化剂。金属基催化剂和硫化物基催化剂在180~250 ℃附近具有良好的甲醇选择性,但往往受限于CO2转化率低。由于CO2本身非常的稳定,较高的温度更有利于CO2的活化转化。然而随着反应温度的升高,金属基催化剂面临着非常严重的逆水煤气反应,极易烧结失活[12]。硫化物基催化剂在高温下则会过度氢化生成甲烷,甲醇选择性大幅降低[10]。为了获得高CO2转化率,在高温下具有优异性能的金属氧化物基催化剂近年来备受关注。已报道的ZrO2基(ZnO/ZrO2、In2O3/ZrO2等)双金属氧化物催化剂对催化CO2加氢制甲醇均表现出较高的CO2转化率和甲醇选择性[13-15]。研究结果表明,良好的催化性能是由双金属氧化物协同作用带来的。在CO2加氢制低碳烯烃中,ZrO2基双金属氧化物催化剂也被广泛应用[16-19]。虽然基于ZrO2基双金属氧化物体系的开发已经取得了较多进展,但受限于有限的双金属氧化物协同效应,在催化活性和甲醇选择性上还需取得进一步突破。
为了提高催化活性,添加助剂来调控催化剂的表面结构和物化性质被视为一种有效的策略。通常来说,增强催化剂表面氧空位含量和H2吸附活化能力有利于催化性能的提升。金属元素(Ga、In、Al、Ce、La、Cr)的相关金属氧化物在CO2加氢制甲醇领域中均有较为突出的表现,并且这些金属元素也作为助剂被广泛地应用于催化剂的优化改性,进一步促进催化剂上氧空位的形成或提升H2吸附活化能力。WANG 等[20]在In2O3催化剂中引入Cr 发现,Cr的引入不仅产生了更多氧空位,还可以增强HCOO*物种与催化剂间的相互作用,降低CH3OH的生成能垒。对于Cu/ZnO负载型催化剂而言,已有相关报道In2O3、Al2O3、CeO2均可以作为助剂[21-23],促进催化剂对CO2和H2的吸附活化能力,产生更多的氧缺陷位点。对于Zr基固溶体催化剂而言,研究发现适量La和Ga 的掺入可以诱导ZnZrOx表面形成更多的氧空位[24-25],从而促进CO2的吸附活化,生成更多的HCOO*和CH3O*中间体。在CeZrOx催化剂中掺入适量的In,也会使其产生更多的氧空位用于吸附活化CO2[26]。此外,XU等[27]在ZnZrOx固溶体催化剂上引入少量的Cu,发现Cu 的掺杂提高了催化剂的加氢能力,增强的H2吸附活化能力加速了HCOO*向CH3O*的转变,促进了甲醇的形成。PdZnZrOx和PtZnZrOx催化性能的提高也表现出H2吸附活化能力对催化性能提高的直接作用[28-29]。然而CuZnZrOx催化剂在提高CO2转化率时,甲醇选择性有所下降。这也表明,同时获得高CO2转化率和甲醇选择性仍具有一定挑战。
本文采用浸渍法在ZnO/ZrO2催化剂的研究基础上制备得到三元复合金属氧化物催化剂。通过元素筛选(金属元素Ma=Ga、In、Al、Ce、La、Cr)和助剂掺杂比例的优化,以期在提高ZnO/ZrO2催化CO2转化率的同时,也保持较高甲醇选择性。通过X 射线衍射(XRD)、N2吸脱附、高分辨率透射电子显微镜(HRTEM)、XPS、电子顺磁共振(EPR)、H2-TPR、CO2-TPD、H2-TPD 等多种表征手段,进一步地研究掺杂助剂对ZnO/ZrO2催化剂物化性质的影响,建立其与催化性能的构效关系,并通过原位漫反射傅里叶变换红外光谱明确掺杂助剂对催化反应的促进作用。这项研究将有助于设计具有多种活性组分的高性能ZrO2负载型催化剂。
1 实验部分
1.1 原料
二氯二茂锆(Cp2ZrCl2)、硝酸锌[Zn(NO3)2·6H2O]、硝酸镓[Ga(NO3)3·xH2O]、硝酸铟[In(NO3)3·xH2O]、硝酸铈[Ce(NO3)2·6H2O]、硝酸镧[La(NO3)3·6H2O]、硝酸铬[Cr(NO3)3·9H2O]、硝酸铝[Al(NO3)3·9H2O]、丙酮、氨水,均为分析纯。
1.2 催化剂制备
采用溶剂热法制备ZrO2载体。将0.2 g 二氯二茂锆溶解在60 mL丙酮中,磁力搅拌5 min直到二氯二茂锆完全溶解。随后,将2 mL的氨水慢慢滴加到之前的溶液中,得到的溶液转移到100 mL 不锈钢水热反应釜中,将其密封并放入200 ℃的烘箱中反应12 h。所得沉淀用丙酮、乙醇和去离子水分别离心3次,并在80 ℃下干燥过夜。最后,样品在500 ℃下煅烧2 h。
采用浸渍法制备ZnO/ZrO2和Ma-ZnOx/ZrO2(Ma=Ga、In、Ce、La、Cr、Al)催化剂。据相关研究报道发现,金属元素的掺杂需要适量,掺入过多并不会促进产物的生成,5%(质量分数)的金属元素掺杂量往往表现出更好的催化性能[30-32]。因此,结合前期研究工作,本研究中所有催化剂均固定n(Ma)∶n(Zn)∶n(Zr)=5∶20∶75不变。以5%Ga-ZnOx/ZrO2为例,按照比例称取Ga(NO3)3·xH2O和Zn(NO3)2·6H2O,溶于适量蒸馏水中。将该溶液浸入1 g 200 目ZrO2载体,随后混合物在室温下放置24 h,并在80 ℃下干燥过夜。最后,样品在500 ℃下煅烧2 h。
1.3 催化剂表征
采用D8 ADVANCE 型X 射线衍射仪(XRD)对制备得到的催化剂进行物相、结晶度分析;采用ASAP 2460型N2等温吸脱附分析仪对催化剂的比表面积和孔隙结构进行评估;采用JEM200 型高倍透射电子显微镜(HRTEM)对催化剂微观形貌结构进行分析和能量色散X 射线分析(EDX);采用KAlpha Plus 型X 射线光电子能谱(XPS)对催化剂的表面物种元素价态和氧空位进行分析;在EMX PLUS 上对各催化剂氧空位进行EPR 表征;采用Auto Chem Ⅱ 2920 型程序化升温脱附分析仪进行H2(H2-TPD)和CO2(CO2-TPD)的程序化升温脱附,研究催化剂对H2和CO2的吸附能力;采用Auto Chem Ⅱ 2920 型H2程序升温还原分析仪(H2-TPR)测试分析催化剂的还原行为;采用Thermo Fisher IS50 型原位漫反射傅里叶变换红外光谱仪(in situDRIFTS)对催化剂结构进行分析。
1.4 催化性能评价
通过高压固定床反应装置对制得的催化剂进行CO2加氢制甲醇性能评价。将0.1 g 催化剂(40~80 目)与0.4 g 石英砂(40~80 目)均匀混合并装入反应管,催化剂在反应温度下用10%H2/N2(0.1 MPa 和20 mL/min)进行预处理。相关研究报道,催化剂的催化性能会随着温度、空速、压力及V(H2)/V(CO2)比的增大而增大[25,33]。为了在更大程度发挥催化剂作用的同时节省能耗,催化反应的条件:P=3 MPa、T=320 ℃、V(H2)∶V(CO2)=4∶1、WHSV(质量空速)=24 000 mL/(g·h),出口气体温度保持在200 ℃,并立即送入配备火焰电离检测器(FID)和热导检测器(TCD)的GC2014C型气相色谱仪进行在线测试。
CO2转化率、CH3OH 选择性、CO 选择性和CH3OH时空产率通过以下公式计算:
式中:X(CO2)为CO2转化率,%;S(CH3OH)为甲醇的选择性,%;S(CO)为CO选择性,%;STY(CH3OH)为甲醇的时空产率,mg/(g·h);φ(CO2)为原料气中CO2的体积分数,%;M(CH3OH)为甲醇相对分子质量;WHSV 为质量空速,mL/(g·h);n是每种物质的浓度乘以其含碳数量。
2 结果与讨论
2.1 催化剂性能评价
2.1.1 不同金属元素掺杂的5%Ma-ZnOx/ZrO2催化剂性能评价
图1 为不同元素掺杂的5%Ma-ZnOx/ZrO2催化剂的催化性能。由图1 可知,未掺杂的ZnO/ZrO2催化剂CO2转化率为6.2%,甲醇选择性为74.8%,甲醇时空产率为324 mg/(g·h)。随着第三元金属元素的掺入,5%Ma-ZnOx/ZrO2催化剂的催化性能差异较大。掺入5%Cr时该催化剂的评价性能最差,CO2转化率急剧下降仅为1.7%,甲醇时空产率为71 mg/(g·h)。事实上,已有相关研究发现第三元金属元素的引入会使催化剂的物化性质发生改变,从而影响催化剂的催化性能。WANG 等[34]发现在CuO-ZnO-ZrO2(CZZ)中引入Cr、Mo、W时,CZZCr的比表面积及CO2吸附活化能力均较CZZ 有所下降,其催化性能表现出相似规律。GAO等[35]在探究不同金属元素对Cu/Zn/Al催化剂性能的影响时,发现掺杂元素对催化剂的比表面积及H2、CO2吸附活化能力的影响与其对催化性能的影响规律一致。当Ma=In、Al、Ce、La、Cr时,5%Ma-ZnOx/ZrO2催化剂的CO2转化率和甲醇产率较ZnO/ZrO2而言均有不同程度的下降。结合上述研究,这一现象可能是由于第三元金属元素的掺杂,减小了催化剂的比表面积或降低了其对H2、CO2的吸附活化能力。值得注意的是,只有Ga的掺入使催化剂的CO2转化率、甲醇选择性有所提升,这可能是由于Ga 掺入提高了催化剂的比表面积或H2、CO2吸附活化能力。

图1 不同元素掺杂的5%Ma-ZnOx/ZrO2催化剂的催化性能Fig.1 Catalytic performance of 5%Ma-ZnOx/ZrO2 catalysts doped with different elements
2.1.2 不同Ga 掺量的x%Ga-ZnOx/ZrO2催化剂性能评价
图2a为不同Ga掺量的x%Ga-ZnOx/ZrO2催化剂的催化性能。由图2a可知,各催化剂的甲醇选择性较ZnO/ZrO2而言均有所提高,这是因为Ga物种的掺入增强了催化剂的H2吸附活化能力,可以促进反应中间体加氢形成甲醇[36]。当Ga 掺量为5%时,催化剂的性能提升最为显著,5%Ga-ZnOx/ZrO2催化剂在上述反应条件下,CO2的转化率为7.2%,甲醇选择性为81.0%,甲醇时空产率可达410 mg/(g·h),是ZnO/ZrO2催化剂的1.26倍。对于锆基金属氧化物催化剂而言,氧空位是CO2吸附活化的主要催化位点[37]。ZHANG 等[24]和SHA 等[25]指出,掺入适量第三元金属元素可以在催化剂上构建更多的氧缺陷,掺量过多反而不利于产物的生成。当Ga掺量从5%开始增加时,Ga-ZnOx/ZrO2催化剂的CO2转化率及甲醇时空产率都存在一定程度的下降,10%Ga-ZnOx/ZrO2催化剂的甲醇时空产率低于ZnO/ZrO2。这一现象表明Ga的掺入可能改变了各催化剂的氧空位含量,从而显著影响催化剂吸附活化CO2的能力。在催化剂应用中,除了关注催化剂的催化性能外,催化剂的稳定性也是实际应用中的一项重要指标。图2b、c 为5%Ga-ZnOx/ZrO2催化剂催化CO2加氢制甲醇连续反应100 h 的催化性能。由图2b、c 可知,在连续反应时间长达100 h时,5%Ga-ZnOx/ZrO2催化剂的CO2转化率、甲醇选择性及甲醇时空产率均无明显下降趋势,说明该催化剂具有优异的稳定性,有较好的工业应用前景。
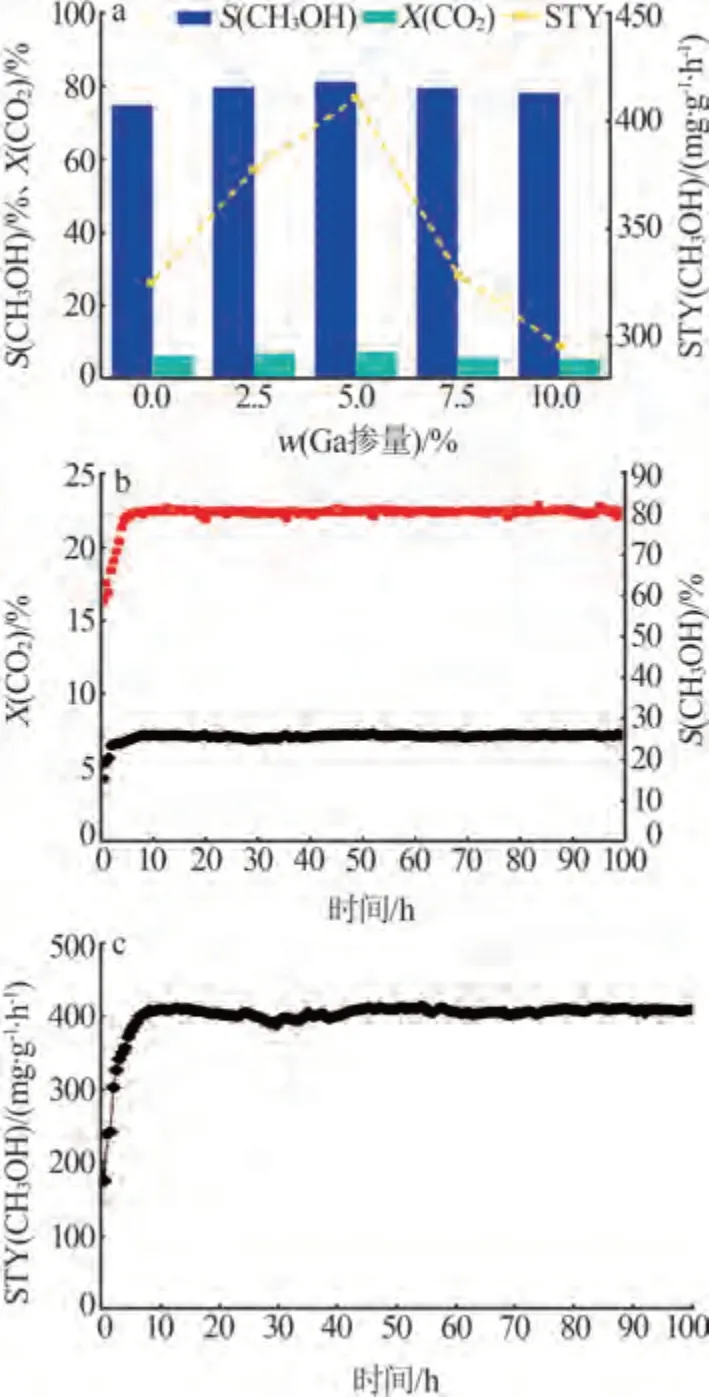
图2 不同Ga掺量的x%Ga-ZnOx/ZrO2催化剂的催化性能(a)和5%Ga-ZnOx/ZrO2催化剂的稳定性测试(b、c)Fig.2 Catalytic performance of x%Ga-ZnOx/ZrO2 catalysts with different Ga additions(a) and stability test of 5%Ga-ZnOx/ZrO2 catalyst(b,c)
2.2 催化剂物化性质分析
图3 为不同Ga 掺量下x%Ga-ZnOx/ZrO2催化剂的结构表征。由图3a可知,所有催化剂均具有t-ZrO2、m-ZrO2和ZnO 的特征衍射峰并表现出良好的结晶度。其中,2θ为17.4°、24.0°、28.2°、31.5°、34.2°和50.1°处的特征峰对应m-ZrO2(PDF 37-1484)的(011)(110)(-111)(111)(200)和(022)晶面;2θ为30.3°、35.3°、50.4°和60.2°处的特征峰对应t-ZrO2(PDF 50-1089)的(011)(110)(112)和(121)晶面;2θ为31.7°、34.4°和36.2°处的特征峰对应典型的六方ZnO(PDF 36-1451)的(100)(002)和(101)晶面。Ga助剂的掺入和增加并不会改变催化剂的晶体结构,各催化剂中t-ZrO2仍是主晶相。随着Ga掺入量的提高,各催化剂均未出现明显的Ga2O3特征峰,表明掺入的Ga助剂可能在催化剂上呈高度分散或非晶态状态。所有催化剂均表现出良好的结晶度。

a—XRD谱图;b—N2-吸脱附曲线图;c—孔径分布图。图3 不同Ga掺量下x%Ga-ZnOx/ZrO2催化剂的结构表征Fig.3 Structural characterization of x%Ga-ZnOx/ZrO2 catalyst under different Ga additions
由图3b可知,各催化剂的吸附等温线皆在较高的相对压力范围内出现了H3型滞后环,属于Ⅳ型等温线,均表现出介孔性质。从图3c 可以看出,不同Ga 掺量对催化剂的吸脱附曲线和孔径分布影响较小,各催化剂均呈现出多级孔分布。通过BET 计算方法和BJH理论得出催化剂比表面积和孔结构参数如表1所示。由表1可以看出,随着Ga掺量的增加,各催化剂的比表面积和孔容都呈火山型曲线趋势。这表明掺入适量的Ga,可以增大催化剂的比表面积和孔容。对于负载型催化剂而言,反应通常发生在表面活性位点上,比表面积越大意味着活性位点越多,整体催化活性增强,并且良好的孔容和多级孔分布也更有利于传质[38-39]。

表1 不同Ga掺量下x%Ga-ZnOx/ZrO2催化剂的物理特性Table 1 Physical properties of x%Ga-ZnOx/ZrO2 catalysts with different Ga additions
图4a、b 为负载前后催化剂的TEM 照片。由图4a、b可知,在ZrO2载体上负载ZnO和Ga助剂并不会破坏催化剂的结构形态,ZrO2载体和5%Ga-ZnOx/ZrO2催化剂均为立方框架形态。图4c 为5%Ga-ZnOx/ZrO2催化剂的HRTEM 照片。由图4c 可知,该催化剂上出现了ZnO(100)、m-ZrO2(-111)和t-ZrO2(011)晶面,未出现Ga2O3的相关晶面,说明样品具有良好的结晶度与XRD 结果相符。图4d 为5%Ga-ZnOx/ZrO2的EDX-mapping 图。由图4d 可以看出,5%Ga-ZnOx/ZrO2催化剂的Ga和Zn元素高度均匀分散在ZrO2载体上。结合图3a可知Ga物种在催化剂上呈高度分散的非晶态形式存在。

a—ZrO2载体的TEM;b—5%Ga-ZnOx/ZrO2的TEM;c—5%Ga-ZnOx/ZrO2的HRTEM;d—5%Ga-ZnOx/ZrO2的EDX-mapping。图4 ZrO2载体和5%Ga-ZnOx/ZrO2催化剂的形貌表征Fig.4 Morphological characterization of ZrO2 carrier and 5%Ga-ZnOx/ZrO2 catalyst
通过XPS 分析进一步研究Ga、Zn 和Zr 物种的表面化学环境,图5 为不同催化剂的XPS 谱图。从图5a 可以看出,纯Ga2O3在1 117.7、1 144.5 eV 处出现了两个特征峰,分别属于Ga3+组分的Ga 2p3/2和Ga 2p1/2。随着Ga掺入到ZnO/ZrO2催化剂上,各催化剂Ga 物种的结合能发生了偏移。类似的情况同样可以从图5b 和5c 看出,Zn 和Zr 物种的轨道结合能随着Ga 的掺入也发生了偏移,并且随着Ga 掺入量的增加偏移的更大,这一结果表明三组分之间存在一定的相互作用。利用O 1s 谱进一步研究x%Ga-ZnOx/ZrO2催化剂表面氧空位浓度。通常情况下,峰值在529.5~530.5 eV 处属于晶格氧(OL),在530.5~531.5 eV 处属于表面氧空位(OV)附近的氧原子,在531.5~532.5 eV 处对应羟基氧(OOH)[40-43]。氧空位(OV)的相对浓度可由3 种不同氧物种的峰面积计算,计算方法为OV/(OL+OV+OOH)。从图5d 可以看出,Ga助剂的掺量不同会显著影响各催化剂的相对氧空位含量。随着Ga掺量的增加,各催化剂的相对氧空位含量呈先增大后减小的火山型曲线趋势。已有相关文献报道,在催化剂的掺杂改性中,适量助剂的掺入可以诱导催化剂产生更多的氧空位,从而促进CO2的吸附活化,并且研究发现随着助剂掺量的增加,相对氧空位含量均呈现火山型曲线趋势[24,26]。对于ZnO/ZrO2负载型催化剂而言,氧空位主要是在ZrO2载体及ZnO与ZrO2相互作用的界面上产生。当掺杂助剂含量过高时,催化剂中ZrO2的相对含量必然降低,反而不利于氧空位的形成,5%Ga-ZnOx/ZrO2催化剂具有最高相对氧空位含量(39.53%)。

a—Ga 2p;b—Zn 2p;c—Zr 3d;d—O 1s。图5 不同催化剂的XPS谱图Fig.5 XPS patterns of different catalysts
EPR 对氧空位捕获的未配对电子很敏感,信号强度与未配对电子数量成正比,因此采用EPR 对ZnO/ZrO2和不同Ga 掺量的x%Ga-ZnOx/ZrO2催化剂氧空位相对密度进一步表征[25]。图6a为不同Ga掺量的x%Ga-ZnOx/ZrO2催化剂氧空位相对密度的EPR。由图6a可知,各催化剂的EPR信号有明显差异,5%Ga-ZnOx/ZrO2表现出最强的氧空位信号,在g=2.002~2.004 处的信号一般对应于氧空位上捕获的电子[25,36,44],这与催化剂的XPS 表征结果一致。图6b为不同Ga掺量的x%Ga-ZnOx/ZrO2催化剂氧空位浓度与甲醇时空产率关系。由图6b可知,适量Ga助剂的掺入可以促使催化剂产生更多的氧缺陷,提高吸附活化CO2的能力从而提高催化活性。

图6 不同Ga掺量的x%Ga-ZnOx/ZrO2催化剂的EPR(a)和氧空位浓度与甲醇时空产率关系(b)Fig.6 EPR(a) and oxygen vacancy concentration versus methanol space-time yield(b) of x%Ga-ZnOx/ZrO2 catalysts with different Ga additions
图7 为不同Ga 掺量的x%Ga-ZnOx/ZrO2的催化性能分析。采用H2-TPR 实验研究ZnO/ZrO2和不同Ga 掺量的x%Ga-ZnOx/ZrO2催化剂的还原行为。据文献报道,Ga2O3、ZnO、ZrO2在低温范围内几乎没有明显的H2消耗,说明单一氧化物很难被还原[14,25]。由图7a可知,各催化剂主要出现两个明显的还原峰(<400 ℃和>400 ℃),高温处(>400 ℃)的还原峰可归因于ZrO2的体相还原,低温处(<400 ℃)的还原峰可以归因于催化剂界面上Ga物种和Zn物种的还原[25,45]。引入Ga 后x%Ga-ZnOx/ZrO2的还原行为与ZnO/ZrO2相比发生了显著的变化,表明三组分之间存在相互作用。随着Ga 助剂掺量的增加,各Ga-ZnOx/ZrO2催化剂的低温还原峰强度呈先增加后下降的趋势,在250 ℃和550 ℃处的还原峰较ZnO/ZrO2催化剂而言提前发生。5%Ga-ZnOx/ZrO2催化剂在低温范围内表现出最大的还原性。这表明适量Ga助剂的掺入可以加强金属氧化物间的相互作用,提高催化剂上活性位点的活性,促进了催化剂表面氧空位的形成[46-47]。
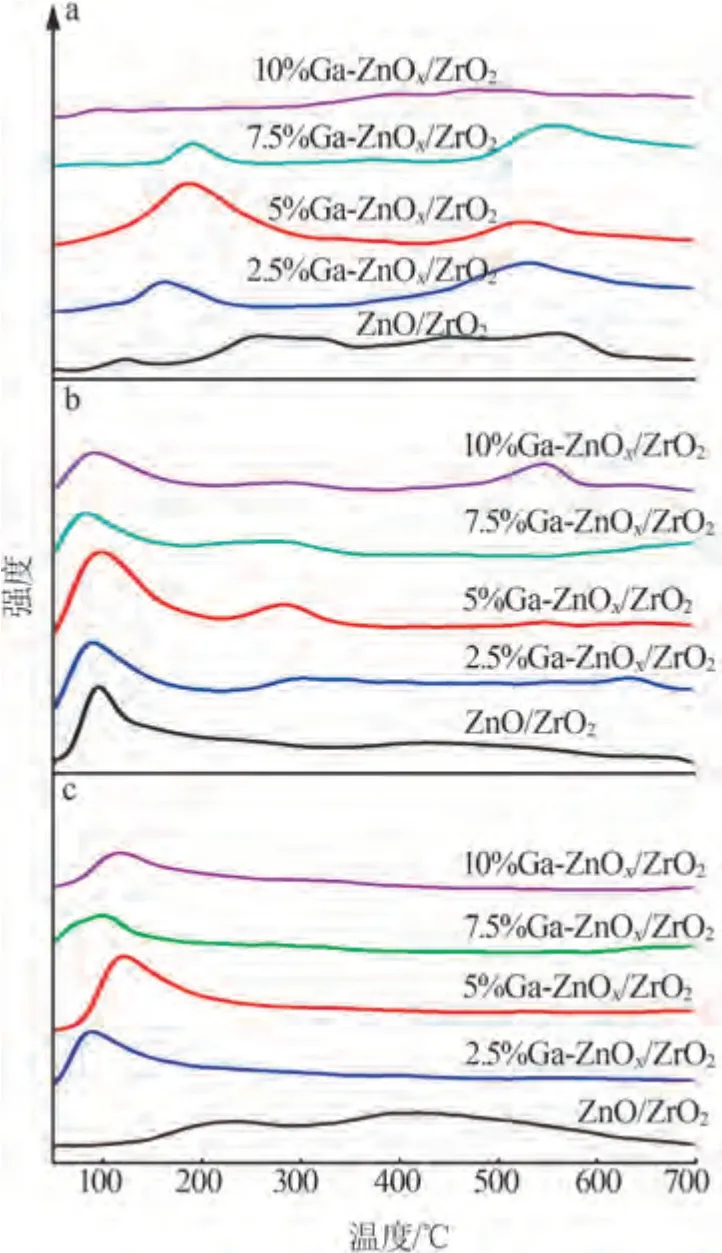
a—H2-TPR;b—CO2-TPD;c—H2-TPD。图7 不同Ga掺量的x%Ga-ZnOx/ZrO2的催化性能分析Fig.7 Analysis of catalytic performance of x%Ga-ZnOx/ZrO2 with different Ga additions
为了探究Ga 助剂的掺量对催化剂催化性能的影响,分别研究了ZnO/ZrO2和不同Ga掺量的x%Ga-ZnOx/ZrO2催化剂对CO2和H2的吸附活化能力。催化剂对CO2的有效吸附活化是将CO2转化为甲醇的必要前提。图7b 为各催化剂的CO2-TPD 曲线图。由图7b可知,ZnO/ZrO2主要出现了两个CO2吸附峰,随着Ga的掺入x%Ga-ZnOx/ZrO2的CO2吸附峰增多,表明Ga的掺入增加了催化剂上吸附CO2的位点[38]。x%Ga-ZnOx/ZrO2催化剂上出现了3 个CO2吸附峰:弱碱性位点(<200 ℃)、中等碱性位点(200~350 ℃)和强碱性位点(>350 ℃)。ZHANG等[24]和KATTEL等[48]报道,样品表面对CO2的吸附过强反而不利于甲醇的形成,因此弱碱性中碱性位点的增强更有利于催化活性的提升。与ZnO/ZrO2相比,5%Ga-ZnOx/ZrO2中等碱性位点的峰明显增强,这可能是由于Ga的掺入促进催化剂表面氧空位的形成,加强了其对CO2的吸附活化能力。通过H2-TPD 实验可以获得催化剂表面氢物种相对浓度[25]。对于ZnO/ZrO2而言,出现了两个H2解吸峰,低温解吸峰和高温解吸峰。由图7c 可知,Ga 助剂的掺入对催化剂H2活化能力影响显著,各Ga-ZnOx/ZrO2催化剂在低温处的解吸峰位置均有提前。由于催化反应是在350 ℃以内进行的,因此H2低温解吸峰的出现与催化活性密切相关[46,49]。5%Ga-ZnOx/ZrO2在低温处具有最大的H2解吸强度,表明适量Ga的掺入可以增强催化剂的H2吸附活化能力。
结合多种表征结果发现,在ZnO/ZrO2催化剂上引入适量的Ga可以增大催化剂的比表面积,促进氧空位的形成,有效增强催化剂对CO2和H2的吸附活化能力,进而提高催化活性。
2.3 反应机理分析
在280 ℃、V(CO2)∶V(H2)=3∶1、P=0.5 MPa 反应条件下,采用原位红外研究x%Ga-ZnOx/ZrO2催化剂表面的反应中间体,探究Ga助剂的掺入对ZnO/ZrO2催化剂的影响,并揭示Ga-ZnOx/ZrO2催化剂的反应机理,如图8 所示。1 300~1 400 cm-1、1 582、2 879、2 973 cm-1处的特征峰可归属于甲酸盐物种(HCOO*)[24,26,50];1 051、2 827、2 937 cm-1处的特征峰为甲氧基物种(CH3O*)[25,27,51]。由图8可知,反应刚开始x%Ga-ZnOx/ZrO2催化剂均出现了明显的HCOO*物种特征峰,这是碳物种加氢的结果。CH3O*物种可由HCOO*物种逐级加氢形成。HCOO*从催化剂吸附的CO2转变而来是一个动力学快速反应,而HCOO*转化为CH3O*存在更高的能垒,因此HCOO*氢化为CH3O*反应的发生较为困难。随着反应时间增加,各催化剂位于2 827cm-1和2 937cm-1处的CH3O*物种特征峰开始增强。从图8也可以明显看出,各催化剂中HCOO*物种的特征峰强度始终高于CH3O*物种,这也进一步地表明了CH3O*物种是由HCOO*物种逐级加氢形成的[25]。随着Ga掺量的增加,x%Ga-ZnOx/ZrO2催化剂上甲醇中间体特征峰强度有着明显的变化。各催化剂表面HCOO*物种和CH3O*物种的浓度呈火山型曲线趋势,5%Ga-ZnOx/ZrO2催化剂上甲醇中间体浓度更高。
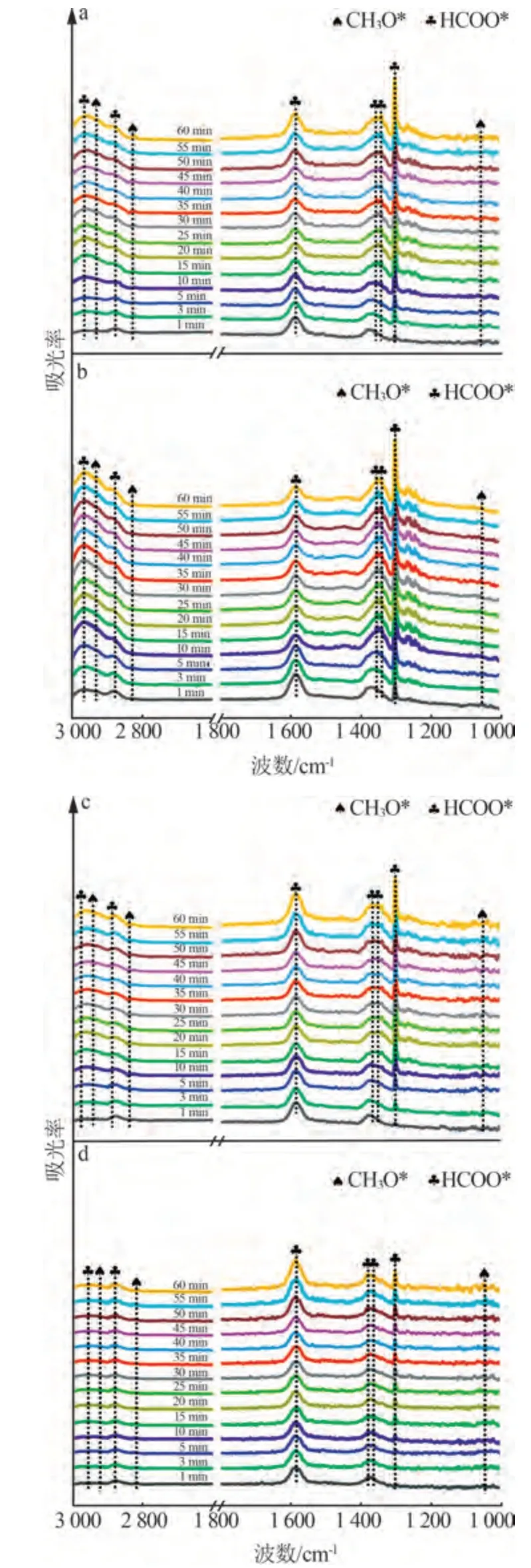
a—2.5%Ga-ZnOx/ZrO2;b—5%Ga-ZnOx/ZrO2;c—7.5%Ga-ZnOx/ZrO2;d—10%Ga-ZnOx/ZrO2。图8 不同催化剂的CO2加氢原位漫反射傅里叶变换红外光谱图Fig.8 In situ DRIFTS spectra of CO2 hydrogenation with different catalysts
图9为不同催化剂在反应时间为60 min时的原位漫反射傅里叶变换红外光谱图。由图9a可知,与ZnO/ZrO2相比,x%Ga-ZnOx/ZrO2催化剂均在1 307cm-1处出现了一个HCOO*物种的特征峰,这可能与Ga掺入形成的新活性位点有关。在5%Ga-ZnOx/ZrO2催化剂上,位于1 300~1 400 cm-1、2 879、2 973 cm-1处的HCOO*物种及2 937 cm-1处的CH3O*物种的浓度明显高于其他催化剂。并且随着Ga 助剂掺量的增加,x%Ga-ZnOx/ZrO2催化剂的CH3O*物种特征峰强度先增大后减小,但始终强于ZnO/ZrO2催化剂(图9b)。这表明Ga 的掺入增强了催化剂对CO2和H2的吸附活化能力,可以加快HCOO*物种向CH3O*物种的转变,这也与各催化剂的催化性能相符。

a—1 000~3 000 cm-1;b—2 800~3 050 cm-1。图9 不同催化剂在反应时间为60 min时CO2加氢原位漫反射傅里叶变换红外光谱图Fig.9 In situ DRIFTS spectra of CO2 hydrogenation on various catalysts at 60 min
3 结论
为了获得高活性、高选择性催化剂,本文在ZnO/ZrO2催化剂上掺入第三元金属元素,明确掺杂助剂对金属氧化物催化剂的物化性质及催化CO2加氢制甲醇性能的影响。通过金属元素筛选和掺入比例的优化,采用多种表征手段探究助剂对金属氧化物氧空位浓度及CO2、H2吸附活化能力的影响,进一步建立三元金属氧化物物化性质与催化性能的构效关系。采用原位漫反射傅里叶变换红外光谱明确反应机理得到以下结论。
1)通过掺杂金属元素(Ma=Ga、In、Al、Ce、La、Cr)的筛选发现,掺入Ga 助剂显著提升ZnO/ZrO2的催化性能。5%Ga-ZnOx/ZrO2具有最大的比表面积和孔容量。在ZnO/ZrO2催化剂中加入适量的Ga 可以形成更多吸附活化CO2的氧空位,并提高对H2的吸附活化能力。
2)5%Ga-ZnOx/ZrO2三元金属氧化物催化剂表现出优异的催化剂性能,在反应条件为P=3 MPa、T=320 ℃、V(H2)∶V(CO2)=4∶1、WHSV=24 000 mL/(g·h)时,CO2转化率为7.2%,甲醇选择性为81.0%,甲醇STY 可达410 mg/(g·h),是ZnO/ZrO2的1.26 倍,且在反应100 h内催化性能无明显衰减。
3)原位漫反射傅里叶变化红外结果表明,x%Ga-ZnOx/ZrO2催化剂合成甲醇均遵循甲酸盐-甲氧基路径,且甲氧基是由甲酸盐逐级加氢形成的,随着Ga助剂掺量的增加,各催化剂的CH3O*特征峰强度先增大后减小,但始终强于ZnO/ZrO2催化剂。这表明Ga 的掺入增强了催化剂对CO2和H2的吸附活化能力,可以促进HCOO*物种向CH3O*物种的转变。具有最优催化性能的5%Ga-ZnOx/ZrO2催化剂的甲醇中间体浓度明显高于其他催化剂。

