月季花标准汤剂UPLC指纹图谱及多指标成分定量研究
何民友,王利伟,周湘媛,刘晓霞,李振雨,陈向东,孙冬梅
广东一方制药有限公司 广东省中药配方颗粒企业重点实验室,佛山 528244
月季花又名月月红、长春红等,为蔷薇科植物月季RosachinensisJacq.的干燥花,在我国各个地区均有种植,全年可采收,花微开时采摘,阴干或低温干燥。月季花药用价值最早记载于李时珍的《本草纲目》,其味甘,性温,归肝经;具有活血调经和疏肝解郁的功效,主要用于气滞血瘀、月经不调、胸胁胀痛等症候诸疾的治疗[1-3]。月季花含有多种化学成分,包括黄酮类、酚酸类、芳香油、鞣质和色素等,其中黄酮类和酚酸类被认为是月季花的主要药效成分[4,5]。黄酮类成分占主要成分,包括槲皮苷、槲皮素、山柰素-3-O-鼠李糖苷、山柰黄素、琥珀酸、没食子酸、没食子酸乙酯、金丝桃苷、胡桃苷、异槲皮苷等[6,7],具有抗病毒、抗氧化、增强机体免疫及抗癌等生物活性[8-10]。
中药成分复杂,其发挥药效作用的基础是多种有效成分之间多靶点、多途径及整体性的相互协同作用,发挥对机体的调节作用[11]。中药指纹图谱建立在中药化学成分系统研究的基础上,从物质群出发将中药成分信息全面展现,以反映中药化学成分的整体情况,一种综合的,可量化的有效技术手段[12]。本研究通过UPLC法建立20批月季花标准汤剂的指纹图谱结合化学模式识别技术,分析探讨影响月季花标准汤剂的主要特征成分,并进行多指标成分定量分析,以期为月季花标准汤相关制剂开发、质量标准研究提供参考。
1 仪器、试剂与试药
1.1 仪器
Waters H-Class型超高效液相色谱仪(美国Waters公司);Thermo Vanquish Flex超高效液相-Thermo Fisher QE高分辨质谱联用仪、Compound Discoverer 2.1质谱分析软件(美国Thermo Fisher Scientific公司);Agilent ZORBAX SB C18(2.1 mm×150 mm,1.8 μm)色谱柱;XP 26型百万分之一分析天平(瑞士梅特勒-托利多公司)。
1.2 试剂
甲醇、乙醇(西陇科学股份有限公司)为分析纯;色谱磷酸(天津市科密欧化学试剂有限公司)、色谱乙腈(德国默克公司)。
1.3 试药
没食子酸(批号:110831-201906,含量:91.5%)、鞣花酸(批号:111959-201903,含量:88.8%)、金丝桃苷(批号:111521-201809,含量:94.9%)、异槲皮苷(批号:111809-201804;含量:97.2%)、槲皮苷(批号:111538-202007;含量:93.5%)和槲皮素(批号:100081-201610;含量:99.1%)对照品(中国食品药品检定研究院);紫云英苷(批号:DSRDZ 000101,含量:99.19%)、阿福豆苷对照品(批号:DSTDA 002901,含量:99.85%)(上海诗丹德标准技术服务有限公司)。
本实验通过实地采集20批月季花药材,经广东一方制药有限公司孙冬梅教授鉴定为蔷薇科植物月季RosachinensisJacq.的干燥花,经质量中心按《中华人民共和国药典》(2020年版)月季花项下性状、鉴别、检查、含量测定进行检验,所采集样品均符合性状、显微、薄层、水分、灰分、重金属、农药残留、含量测定等相关规定,样品信息见表1。

表1 样品信息表
2 方法与结果
2.1 月季花饮片标准汤剂制备
依据《中药配方颗粒质量控制与标准制定技术要求》和《医疗机构中药煎药室管理规范》中相关规定,通过考察后确定月季花标准汤剂的制备工艺为:取月季花饮片100 g,加水煎煮两次,一煎加12倍量水,浸泡30 min,煎煮30 min,二煎加10倍量水,煎煮25 min,趁热过滤,滤液迅速用冷水冷却,合并两次滤液。减压浓缩至约150 mL,冷冻干燥,制得月季花标准汤剂冻干粉。
2.2 供试品溶液的制备
取月季花标准汤剂冻干粉适量,研细,取约0.2 g,精密称定,置具塞锥形瓶中,精密加入50%甲醇50 mL,称定重量,超声处理(功率250 W,频率50 kHz)30 min,放冷,再称定重量,用50%甲醇补足减失的重量,摇匀,滤过,取续滤液,即得。
2.3 对照品溶液的制备
取没食子酸对照品、鞣花酸对照品、金丝桃苷对照品、异槲皮苷对照品、紫云英苷对照品、槲皮苷对照品、阿福豆苷对照品和槲皮素对照品适量,精密称定,加50%甲醇制成每1 mL含没食子酸、鞣花酸各50 μg,金丝桃苷、异槲皮苷、紫云英苷、槲皮苷各20 μg,阿福豆苷、槲皮素各10 μg的混合对照品溶液,即得。
2.4 指纹图谱的建立及分析
2.4.1 色谱条件
采用Agilent SB C18(2.1 mm×150 mm,1.8 μm)色谱柱;流动相为乙腈(A)-0.2%磷酸水溶液(B),梯度洗脱:0~1 min,3%A;1~2 min,3%→10%A;2~8 min,10%→11%A;8~11 min,11%→15%A;11~14 min,15%A;14~16 min,15%→19%A;16~19 min,19%A;19~25 min,19%→40%A;体积流量为0.40 mL/min;柱温35 ℃;检测波长254 nm;进样量2 μL;按鞣花酸峰计算理论塔板数不低于5 000。
2.4.2 质谱条件
流动相为乙腈-0.1%甲酸水溶液,梯度洗脱条件同“2.4.1”项。采用电喷雾离子源(ESI),喷雾电压为3.20 kV,正、负离子模式扫描。离子源主要参数:离子源温度为300 ℃,脱溶剂温度为250 ℃,脱溶剂气流为5 L/min,毛细管电压为3.5 kV,锥孔电压为80 V,碰撞能量为40 eV;正、负离子的采集范围为m/z120~1 000。
2.4.3 精密度试验
取月季花标准汤剂冻干粉(编号:S8)适量,研细,取约0.2 g,精密称定,按“2.2”项下方法制备供试品溶液,按“2.4.1”项下色谱条件连续进样6次,以鞣花酸对照品相对应的色谱峰为参照峰S,计算得到各共有峰的相对保留时间和相对峰面积的RSD分别为0.070%~0.24%和0.16%~0.61%,均小于3.0%,表明仪器精密度良好。
2.4.4 稳定性试验
取月季花标准汤剂冻干粉(编号:S8)适量,研细,取约0.2 g,精密称定,按“2.2”项下方法制备供试品溶液,按“2.4.1”项下色谱条件,分别在0、2、4、8、12、18、24 h进样测定,以鞣花酸对照品相对应的色谱峰为参照峰S,计算得到各共有峰相对保留时间和相对峰面积的RSD分别为0.13%~0.83%和0.31%~1.1%,均小于3.0%,表明供试品溶液在24 h内稳定性较好。
2.4.5 重复性试验
取月季花标准汤剂冻干粉(编号:S8)适量,研细,取约0.2 g,精密称定,平行6份,按“2.2”项下方法制备供试品溶液,按“2.4.1”项下色谱条件进样分析,以鞣花酸对照品相对应的色谱峰为参照峰S,计算得到各共有峰相对保留时间和相对峰面积的RSD分别为0.12%~0.86%和0.27%~1.8%,均小于3.0%,表明该方法重复性良好。
2.5 指纹图谱建立和化学计量学分析
2.5.1 指纹图谱的建立及共有峰标定
分别取20批月季花标准汤剂冻干粉适量,研细,取约0.2 g,精密称定,按“2.2”项下方法制备20份供试品溶液,分别按“2.4.1”项下色谱条件进样测定,记录各批次月季花标准汤剂样品的指纹图谱,采用《中药色谱指纹图谱相似度评价系统(2012版)》进行数据处理。设定S1为参照图谱,采用平均数法,进行多点校正和全谱峰匹配,20批月季花标准汤剂指纹图谱确立了15个共有峰,以中位数法生成月季花标准汤剂对照指纹图谱(见图1)。

图1 20批月季花标准汤剂UPLC指纹图谱及对照指纹图谱Fig.1 UPLC fingerprint of 20 batches of standard decoction of RCF and reference fingerprint
2.5.2 主要化合物的确证
取月季花标准汤剂冻干粉(编号:S8)适量,研细,取约0.2 g,精密称定,按“2.2”项下方法制备供试品溶液,按“2.4.2”项下色谱条件用UPLC-Q-Exactive Orbitrap-HRMS系统测定,分别采集供试品溶液在正、负离子模式下总离子流图(TIC)及紫外吸收色谱图(见图2)。采用Compound Discoverer 2.1分析软件对采集的质谱图进行分析,通过确定目标化合物的精确分子量和碎片离子信息对比,结合mzCloud标准数据库和自建数据库进行对比,指认出1号峰为没食子酸,6号峰为鞣花酸,7号峰为金丝桃苷,8号峰为异槲皮苷,10号峰为紫云英苷,11号峰为槲皮苷,13号峰为阿福豆苷,15号峰为槲皮素。化合物信息见表2。对质谱指认的化合物通过对照品保留时间及吸收光谱进一步确证,结果与指认一致(见图3)。
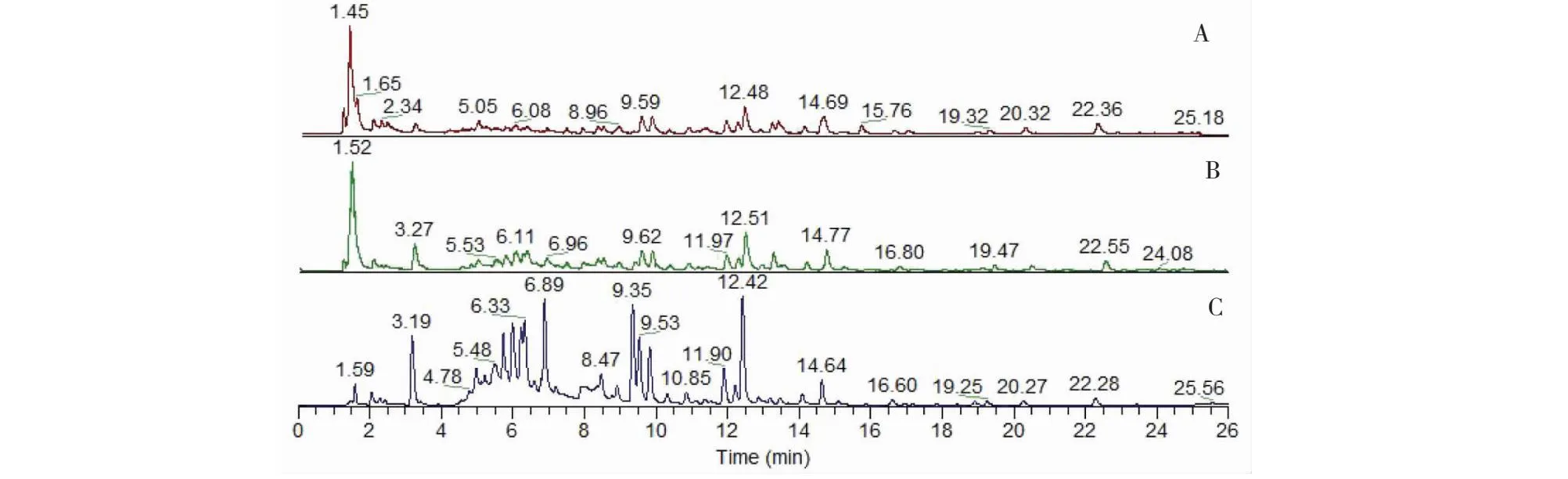
图2 月季花标准汤剂正(A)、负(B)离子模式TIC和紫外色谱图(C)Fig.2 TIC in positive (A) and negative (B) ion mode and UV chromatogram (C) of standard decoction of RCF
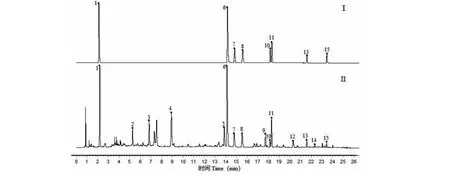
图3 混合对照品(Ⅰ)和月季花标准汤剂(Ⅱ)色谱图Fig.3 Chromatograms of mixed reference (Ⅰ) and standard decoction of RCF (Ⅱ)

表2 月季花标准汤剂指纹图谱共有峰的质谱指认结果
2.5.3 指纹图谱的相似度评价
将“2.5.1”项下采集的20批月季花标准汤剂指纹图谱导入《中药色谱指纹图谱相似度评价系统》(2012版)进行全谱峰匹配,生成相对应的对照图谱,计算月季花标准汤剂指纹图谱与对照指纹图谱的相似度,结果见表3。结果显示,20批样品的相似度在0.983~0.999,说明月季花标准汤剂在制备过程中各工艺稳定可靠,可用于月季花标准汤剂的质量评价。

表3 相似度评价结果
2.5.4 聚类分析
以共有峰的相对峰面积为变量,采用SPSS 25.0软件,以组间链接结合平方欧式距离(d)为样本测度的系统聚类法进行分析,建立月季花标准汤剂的聚类分析谱系图(见图4)[13]。HCA结果表明,当组间距离为15时,20批月季花标准汤剂聚为四类,S1~S6为第一类,S7~S10为第二类,S11~S13为第三类,S14~S20为第四类。聚类分析(hierarchical cluster analysis,HCA)结果显示,云南、河北、河南、山东4个产地样品各自归为一类,说明各批次月季花标准汤剂与产地存在一定的关联,同一产地样品差异不明显,不同产地样品存在一定差异。
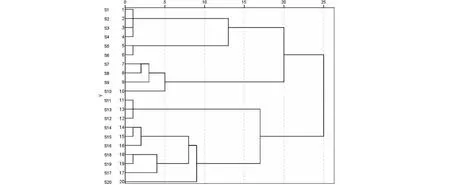
图4 20批月季花标准汤剂聚类树状图Fig.4 Dendrogram of 20 batches of standard decoction of RCF
2.5.5 主成分分析
为进一步探究月季花标准汤剂质量稳定性差异的原因,以20批标准汤剂共有峰的相对峰面积为变量,使用SIMCA 14.1软件进行无监督模式识别方法主成分分析观察样品的自然聚集(见图5)[14],生成4个主成分,累计贡献率为96.1%,Q2为0.832(>0.5),将样品分为3类,S1~S6为第一类,S7~S10为第二类,S11~S13为第三类,S14~S20为第四类,主成分分析(principal component analysis,PCA)结果与聚类分析结果一致,进一步证明前4个主成分可代表样品的整体质量情况,通过指纹图谱各色谱峰相对峰面积可以将不同产地样品进行分类。
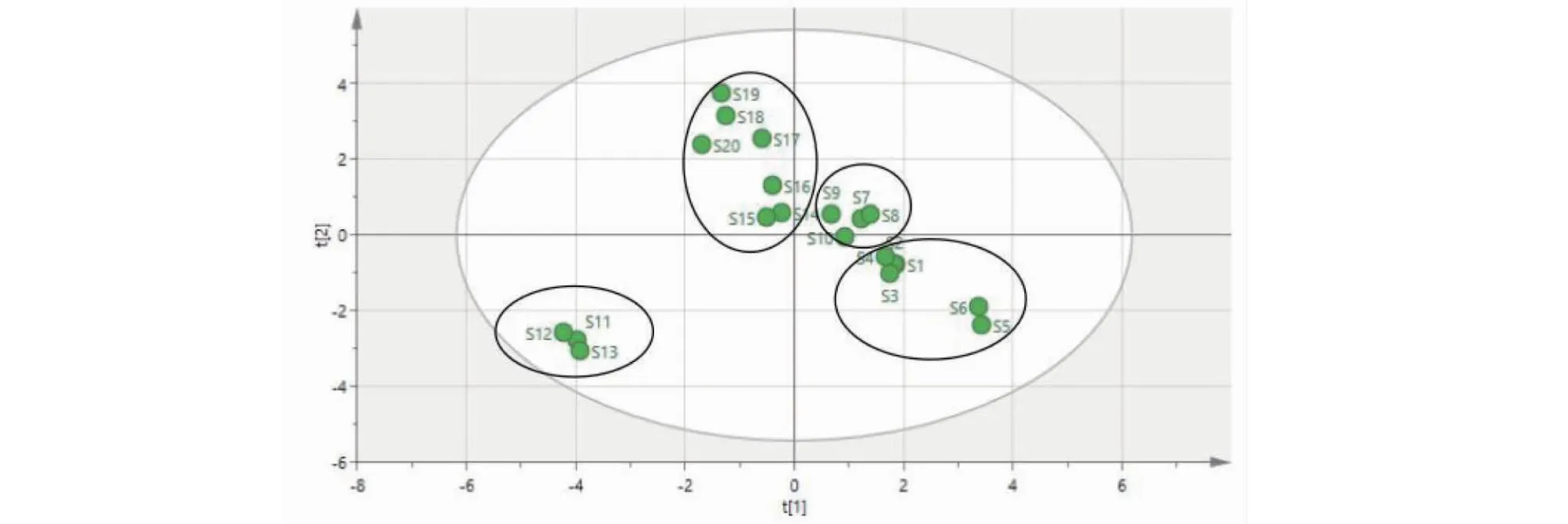
图5 20批月季花标准汤剂主成分分析Fig.5 PCA of 20 batches of standard decoction of RCF
2.5.6 正交偏最小二乘法-判别分析
基于HCA和PCA分析表明,不同产地的月季花标准汤剂存在质量稳定性差异。采用可消除无关噪音的正交偏最小二乘法-判别分析(orthogonal partial least squares discriminant analysis,OPLS-DA)对HCA和PCA的分析结果做进一步分析,以确定导致月季花标准汤剂质量差异的主要标志物并进行控制[15]。
建立的OPLS-DA模型共筛选4个主成分,其R2Y为0.883和Q2为0.800,均大于0.5且接近1,表明该模型稳定性和预测能力均较好。200次置换检验结果表明,R2与Y轴正半轴的截距为0.032 5(<0.4)和Q2与Y轴负半轴的截距为-0.692(<-0.05),证明建立的模型稳定有效,不存在过拟合情况,可进一步应用于月季花标准汤剂质量稳定性差异标志物的筛选(见图6)[16]。进一步进行OPLS-DA,结果表明OPLS-DA得分模型中(见图7),4组样品聚类良好,分离更加显著,与HCA、PCA结果一致,从而进一步验证了分析的合理性。变量重要性投影值(variable importance in projection,VIP)是OPLS-DA模型筛选潜在差异标志物最重要的分析,成分指标VIP值越大,表示其对于解释变量的贡献越大和差异相关性越高[17]。以VIP值>1和P<0.05为标准,共筛选得到11个质量差异标志物的共有峰(见图8),按VIP大小顺序依次为4号峰>14号峰>1号峰(没食子酸)>9号峰(异槲皮苷)>11号峰(槲皮苷)>13号峰(阿福豆苷)>7号峰(鞣花酸)>8号峰(异槲皮苷)>15号峰(槲皮素)>10号峰(紫云英苷)>5号峰,这些成分可能是导致不同产区月季花标准汤剂质量稳定性差异的主要原因。为确保月季花标准汤剂的药效成分质量稳定性,在建立质量标准时可选取以上差异标志性成分作为定量控制指标进行控制,为月季花标准汤剂的质量控制提供一定依据。

图6 OPLS-DA模型置换检验图Fig.6 OPLS-DA model permutation test diagram

图7 OPLS-DA得分图Fig.7 OPLS-DA scores diagram

图8 OPLS-DA模型VIP图Fig.8 VIP diagram of OPLS-DA model
2.6 多成分含量测定
2.6.1 精密度试验
取月季花标准汤剂冻干粉(编号:S8)适量,研细,取约0.2 g,精密称定,按“2.2”项下方法制备供试品溶液,按“2.4.1”项下色谱条件连续进样6次,记录没食子酸、鞣花酸、金丝桃苷、异槲皮苷、紫云英苷、槲皮苷、阿福豆苷和槲皮素所对应的色谱峰的峰面积,并计算峰面积RSD依次为0.11%、0.82%、0.34%、0.61%、0.57%、0.05%、0.58%、0.36%,均小于3.0%,表明仪器精密度良好。
2.6.2 线性关系考察
取没食子酸对照品、鞣花酸对照品、金丝桃苷对照品、异槲皮苷对照品、紫云英苷对照品、槲皮苷对照品、阿福豆苷对照品和槲皮素对照品适量,精密称定,加50%甲醇制成浓度分别为96.350、91.597、98.222、101.477、99.388、98.222、103.694、99.546 μg/mL的混合对照品储备液。精密吸取上述对照品0.2、0.5、1.0、2.0和5.0 mL分别置10 mL量瓶中,加入50%甲醇定容至刻度,即得线性各浓度点。按“2.4.1”项下色谱条件连同储备液依次进样2 μL,记录色谱峰面积。以峰面积为纵坐标(Y),对照品浓度为横坐标(X),绘制标准曲线(见表4)。结果表明,8种成分在各自浓度范围内线性关系良好(r>0.999),可准确定量待测成分。

表4 8种成分的回归方程、相关系数和线性范围
2.6.3 稳定性试验
取月季花标准汤剂冻干粉(编号:S8)适量,研细,取约0.2 g,精密称定,按“2.2”项下方法制备供试品溶液,按“2.4.1”项下色谱条件,分别在0、2、4、8、12、18、24 h进样测定,记录没食子酸、鞣花酸、金丝桃苷、异槲皮苷、紫云英苷、槲皮苷、阿福豆苷和槲皮素所对应的色谱峰的峰面积,并计算峰面积RSD依次为0.86%、1.0%、1.3%、0.47%、1.4%、1.9%、0.44%、2.2%,均小于3.0%,表明供试品溶液在24 h内稳定性良好。
2.6.4 重复性试验
取月季花标准汤剂冻干粉(编号:S8)适量,研细,取约0.2 g,精密称定,平行6份,按“2.2”项下方法制备供试品溶液,按“2.4.1”项下色谱条件进样分析,计算得到没食子酸、鞣花酸、金丝桃苷、异槲皮苷、紫云英苷、槲皮苷、阿福豆苷和槲皮素的含量依次为25.68、5.75、7.19、5.70、2.00、8.05、3.46、0.18、0.11 mg/g,RSD均小于3.0%,表明该方法重复性较好。
2.6.5 加样回收率试验
取同一批月季花标准汤剂冻干粉(编号:S8)6份,每份约0.1 g,精密称定,加入浓度分别为51.360、11.502、14.381、11.413、4.018、16.109、6.924、0.362、0.223 μg/mL的没食子酸、鞣花酸、金丝桃苷、异槲皮苷、紫云英苷、槲皮苷、阿福豆苷和槲皮素的混合对照品溶液50 mL,按“2.2”项下方法制备供试品溶液,按“2.4.1”项下色谱条件进样分析,计算得到没食子酸、鞣花酸、金丝桃苷、异槲皮苷、紫云英苷、槲皮苷、阿福豆苷和槲皮素的平均加样回收率依次为98.24%、97.89%、101.05%、103.40%、98.47%、98.05%、99.06%、100.18%、99.13%,RSD依次为0.89%、0.75%、1.1%、2.0%、1.5%、0.57%、1.4%、1.6%,均小于3.0%,加样回收率符合《中国药典》的9101回收限度标准,表明建立的含测方法回收率良好和准确度高。
2.6.6 样品含量测定
取20批月季花标准汤剂冻干粉,按“2.2”项下方法制备供试品溶液,按“2.4.1”项下色谱条件进样分析,计算没食子酸、鞣花酸、金丝桃苷、异槲皮苷、紫云英苷、槲皮苷、阿福豆苷和槲皮素的含量,结果见表5。结果显示,河南省周口市的月季花原料制备的标准汤剂金丝桃苷、槲皮素和阿福豆苷含量与其他产地差异不显著,但没食子酸、鞣花酸、异槲皮苷、紫云英苷和槲皮素含量均显著高于其他产地的样品。

表5 20批月季花标准汤剂中各化合物含量测定结果(n = 3)
3 讨论与结论
为保证标准汤剂的代表性,本研究对月季花原料药材主产地信息进行了调研,共收集20批样品,实地取样包括河北省保定市、河南省周口市、山东省菏泽市、山东省临沂市、云南省大理州等主产地和道地产地。根据《中药配方颗粒质量控制与标准制定技术要求》的指导原则,并参照《医疗机构中药煎药室管理规范》对标准汤剂的前处理方法(煎煮次数、加水量、煎煮时间等指标和参数)进行工艺考察,确定最佳的制备工艺;采用低温浓缩和冷冻干燥,制成月季花标准汤剂冻干粉。
在指纹图谱方法建立的过程中,考察了供试品的提取溶剂(甲醇、70%甲醇、50%甲醇、乙醇、70%乙醇、稀乙醇)、提取方式(超声、回流)和提取时间(10、30、45、60 min)对指纹图谱的影响。从提取充分性、稳定性及操作简便性等考虑,最终选择50%甲醇超声处理30 min。采用二极管阵列检测器对月季花标准汤剂样品进行全波长扫描(200~400 nm),比较不同波长下色谱图的峰数、响应值及分离度。结果发现采用254 nm作为检测波长的色谱峰数较多且响应值较大,基线平稳,干扰较小。同时对色谱条件的流动相水相、柱温及流速等进行了考察,最终确定以0.2%磷酸溶液为流动相的水相,流速为0.4 mL/min,柱温为35 ℃。
采用指纹图谱结合化学模式识别技术对不同产地月季花标准汤剂进行分析比较,结果表明,无监督的HCA和PCA分析发现不同产地的样品可聚4类。OPLS-DA分析共筛选得到11个差异标志物,其主要为黄酮类和酚酸类成分,对于区分不同产地的月季花标准汤剂起到了重要作用,可作为月季花标准汤剂的质量控制指标,为月季花配方颗粒的原料来源提供更为全面地参考。
本研究采用指纹图谱结合聚类、主成分分析、正交偏最小二乘法-判别分析并结合多指标成分含量测定,对20批月季花标准汤剂质量进行了初步研究,该方法可以较快地筛选出影响不同批次药材质量的关键色谱峰,其中通过高分辨及对照品光谱比对指认出没食子酸、鞣花酸、金丝桃苷、异槲皮苷、紫云英苷、槲皮苷、阿福豆苷和槲皮素。结果表明,酚酸类及黄酮类成分含量较高的均为河南省采集样品,归属HCA和PCA分析中的S11~S13,含量最低的均为云南省采集样品,归属第一类S1~S6。可为后续月季花标准汤剂的原料药采集产地的选择提供依据。目前研究显示,月季花主要含有黄酮类、黄酮苷类和酚酸类化合物,有抗氧化、抗病毒、抗真菌、抗癌、抗肿瘤和抗衰老等生物活性[10,18],后期将结合药效进行深入研究,为月季花标准汤剂及其相关制剂的质量控制提供参考依据。