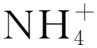不同酸碱体系中Pt/SiO2催化肼分解产生自由基
李 斌,郝 帅,张秋月,夏良树,何 辉
1.中国原子能科学研究院 放射化学研究所,北京 102413;2.南华大学 核科学技术学院,湖南 衡阳 421001
四价铀(U(Ⅳ))作为一种无盐还原剂,广泛应用于乏燃料后处理厂中,其作用是将1AP(有机相)中的Pu(Ⅳ)还原为不易被萃取的Pu(Ⅲ)进入水相,而U(Ⅵ)仍保留在有机相中,从而实现U与Pu的分离[1]。U(Ⅳ)溶液由于易被氧化而不够稳定,需要在后处理厂专门制备以满足需求。传统采用的工业规模制备U(Ⅳ)的工艺主要有电解还原工艺以及催化加氢工艺[2]。近些年,以贵金属Pt作为催化剂、硝酸肼为还原剂制备U(Ⅳ)的工艺,由于其具备U(Ⅳ)的转化率高、反应条件温和、易于规模化生产等优点成为了研究热点[3-6]。
目前Pt催化肼还原U(Ⅵ)生成U(Ⅳ)的研究主要集中在催化剂筛选、反应条件、反应动力学以及反应产物等方面,对反应机理的研究还不是很深入,有限的关于反应历程以及反应机理方面的研究报道,都是根据实验数据进行的推测,并没有对反应的化学本质研究的报道,且不同学者的推测结果不尽一致[7-10]。
本课题组[15]以5,5-二甲基-1-吡咯啉-N-氧化物(2,2-dimethyl-1-oxido-3,4-dihydropyrrol-1-ium, DMPO)作为自由基捕捉剂,采用电子自旋共振(ESR)分析Pt催化分解肼反应过程中产生的自由基,研究酸性溶液中Pt催化肼的分解机理,发现酸性体系中肼只会分解产生游离的氨基自由基而没有发现游离的氢基自由基,并且溶液中只获得DMPO-OH ESR信号。这与Ananiev等[16-18]的推断催化肼断键会产生氢基自由基存在一定差异。另外,Ananiev等[16-17]的研究表明,在酸性溶液中Pt催化肼分解断键产生了大量的氨基自由基并被还原成NH3,但氨基自由基如何被还原成NH3仍不清楚。为了弄清楚这个问题,进一步研究了碱性体系下Pt催化肼分解的过程,发现在碱性体系中获得了DMPO-H和DMPO-NH2ESR信号,这与酸性体系中的发现不相同[18]。那么酸性溶液中氨基自由基如何被还原成NH3,本工作通过ESR法研究比较Pt催化肼在酸、碱不同介质中分解产生的自由基及产物存在的差异,明确Pt催化肼分解产生还原性物质的机理,揭示Pt催化肼断键的本质,从而直观地认识Pt催化肼还原U(Ⅵ)制备U(Ⅳ)的具体反应过程,最终确定Pt催化肼还原U(Ⅵ)制备U(Ⅳ)的反应机理。
1 实验部分
1.1 仪器与试剂
A300型电子顺磁共振测量仪(ESR),德国Bruker有限公司;pH滴定仪,赛多利科学仪器有限公司;数显加热磁力搅拌机,力辰科技有限公司;玻璃毛细管(50 μL),德国布兰德有限公司。
自由基捕捉剂,5,5-二甲基-1-吡咯啉-N-氧化物(DMPO),北京酷尔化学有限公司,其用于捕获溶液中寿命极短、氧化还原活性强的自由基,并转化生成寿命较长的有机自由基。盐酸肼、高氯酸,国药化学试剂有限公司;Pt/SiO2,自制。
1.2 ESR分析
利用DMPO捕获溶液反应产生的自由基。实验将试剂按所需比例混合并按照以下顺序进行:将氮气(纯度99.999%)通入反应溶液5 min除去溶液中可能存在的氧气,加入DMPO(一般5 μL)进行捕获反应,实验过程中,将捕获反应的样品置于室温下搅拌;捕获反应90 s后,立即将样品转移到玻璃毛细管(50 μL)中,并用橡皮泥封住底部,插入ESR光谱仪的特殊石英管中。一般情况下,ESR设置微波功率为4.4 mW,频率为9.84 GHz,中心磁场为3 505 G,调制宽度为0.5 G。ESR信号的峰高用Bruker A300电子顺磁共振测量仪的相对强度表示。所有超精细分裂常数均以毫特斯拉(mT)为单位。
2 结果与讨论
Ananiev等[16-17]通过对不同酸度条件下肼分解产物的分析得出了反应体系中H+浓度会影响肼分解的方式、速率,但肼分解过程中的中间态过程仍不明确。首先,明确了DMPO-OH ESR信号是由[NH3·H2O]·+引起的[15,19],即说明了酸性溶液中Pt催化肼存在着N-N断键,并且说明了肼断键生成的氨基自由基由附着态游离到溶液中随即生成了[NH3·H2O]·+,但是在碱性和酸性溶液中N-N断键和N-H断键在催化剂表面吸附、解离的差异及变化仍是不明确的。本工作将对Pt催化肼分解断键从pH=12.8到 pH=0.0进行详细的探讨。
2.1 碱性溶液中pH变化对肼分解的影响
由于碱性体系中pH>13后碱性环境过强,加入的DMPO会被OH-破坏,不会有ESR信号产生。所以,配制0.125 mol/L高氯酸肼溶液,加入NaOH分别调节pH为12.8、11.9、11.2、9.8、8.9、7.8,来探究碱性溶液中pH变化对N-N断键和N-H断键的影响,使用ESR侦测了Pt催化肼断键产生的自由基信号,结果示于图1。

图1 碱性溶液中Pt催化N2H4分解的ESR图谱(pH=7.8~12.8)Fig.1 ESR spectrogram of Pt catalyzed decomposition of N2H4 in alkaline solution(pH=7.8-12.8)
由图1可知:从图1(a)→(c),DMPO-NH2ESR信号缓慢减小, DMPO-OH ESR信号已明显消失,图1(c) DMPO-H信号出现。这说明在pH=7.8~9.8范围内,随着OH-浓度升高,pH>9.8之后[NH3·H2O]·+全部消失,游离态的氨基自由基也逐步减少,而pH=9.8时溶液中出现了游离态的氢基自由基。从图1(c)→(e) DMPO-H ESR信号迅速增强,而DMPO-NH2ESR信号迅速减小至消失。这说明了在pH=11.2~12.8范围内,随着OH-浓度升高,附着态的氢基自由基变成了游离态,且迅速增多,而溶液中游离态氨基自由基迅速减少至消失。图1(f)(pH=12.8)由于碱性条件太强,DMPO被破坏严重,所以自由基信号微弱。
在pH=7.8~12.8范围内OH-浓度升高的过程中,游离态的氨基自由基开始缓慢减少至消失,游离态的氢基自由基出现之后迅速增强。这说明,在Pt金属表面N-N断键产生的氨基自由基减少到不足量,在金属表面就全部转化成了NH3分子,所以无法解脱到溶液中,即N-N断键速率是不断减小甚至可能消失的;而大量附着态氢基自由基增加到过量,以至于在Pt金属表面无法全部转化成H2或NH3分子,从而大量地从Pt金属表面脱落下来,即N-H断键速率是迅速增大的。
2.2 酸性溶液中pH变化对肼分解的影响
DMPO及自由基加合物在酸性溶液中较为稳定,所以,配制0.125 mol/L高氯酸肼溶液,加入高氯酸分别调制出pH为6.9、5.8、5.1、3.9、2.8、1.1、0.0的反应溶液,来探究酸性溶液中pH变化对N-N断键和N-H断键的影响。使用ESR侦测了Pt催化肼断键产生的自由基信号,结果示于图2。
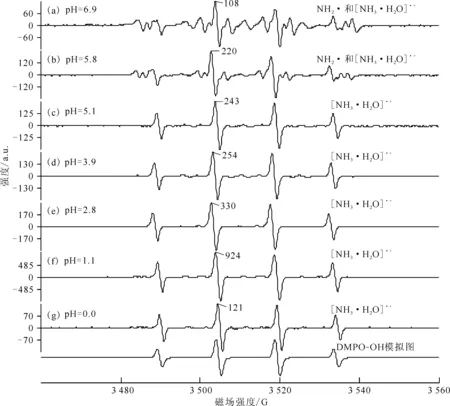
图2 酸性溶液中Pt催化N2H4分解的ESR图谱(pH=0.0~6.9)Fig.2 ESR spectrogram of Pt catalyzed decomposition of N2H4 in acidic solution(pH=0.0-6.9)
由图2可知:图2(a)→(c) DMPO-NH2ESR信号迅速减小至消失。这说明了在pH=5.1~6.9范围内,随着H+浓度升高,附着态的氨基自由基变成了游离态[NH3·H2O]·+,并迅速增多,而溶液中游离态的·NH2迅速减少至消失。图2(a)→(f)DMPO-OH ESR信号强度随着H+浓度升高而迅速增强,并在图2(f)达到最强,随后图2(f)→(g) DMPO-OH ESR信号强度迅速减弱。这说明了在pH=1.1~6.9范围内,随着H+浓度升高,附着态的氨基自由基大量增加,并且迅速以[NH3·H2O]·+形式从催化剂表面解脱成游离态,pH<1.1后[NH3·H2O]·+数量迅速减少。
在pH=1.1~6.9范围内H+浓度升高的过程中,pH<5.1之后附着态的氨基自由基便不再以·NH2形式游离到溶液中,而随着H+浓度上升,氨基自由基数量急剧增长并有大量附着态氨基自由基从Pt金属表面解脱到溶液中并转化成[NH3·H2O]·+,表明游离态的[NH3·H2O]·+与H+浓度成正强相关性。这说明H+促进了氨基自由基从Pt金属表面脱落下来生成[NH3·H2O]·+,大量[NH3·H2O]·+需要由N-N断键产生,那么随着H+浓度升高,也在一定程度上促进了N-N断键,在此H+浓度范围内,随着H+浓度升高,N-N断键速率随着H+浓度升高而迅速上升,并在pH=1.1时N-N断键速率达到最大,pH<1.1之后DMPO-OH ESR信号迅速下降,N-N断键随H+浓度升高开始受到了抑制。而在酸性条件下,未发现DMPO-H ESR信号,说明酸性条件下的肼会被催化产生N-H断键,生成的氢基自由基少,附着态的氢基自由基不会解脱到溶液中变成游离态。
2.3 N-N和N-H断键在酸碱性条件下的差异
碱性条件下pH=8.9~9.8附近,峰值最弱,能捕捉到的游离自由基最少,并随着氢基自由基出现,氨基自由基消失,这是由于OH-易与N2H4上的H形成氢键, 会降低N2H4上N-H断键的反应能垒,N-H断键被催化活性位点催化断键的可能性大大提高,N-H断键数量也就升高,所以在碱性体系中易发生N-H断键,反应溶液中存在大量的OH-呈强负电性,OH-易与氢基自由基形成氢键从而促进了N-H断键产生大量附着态的氢基自由基从催化剂表面扩散到溶液中。催化剂活性位点数量不变,随着溶液酸性增强,N-N断键数量增多,所以N-H断键相对减少,附着在催化剂表面的N-H断键生成氢基自由基较少,附着态的氨基自由基易于被周围大量的氢基自由基还原,从而仅有极少量的附着态氨基自由基游离到溶液中,随着溶液碱性增强进一步游离到溶液中。从而在侦测反应中间态的ESR图谱中,DMPO-NH2ESR信号微弱及消失而DMPO-H ESR信号逐步增强,在产物中更是氢气占比高[18]。

上述讨论结果表明,Pt催化N2H4反应中N-N断键与N-H断键共存,在酸性条件下体系中的氢基自由基总是不足量的,而N-N断键产生氨基自由基需要氢基自由基还原才能完成转化,否则两个氨基自由基又会结合转化成肼分子,所以在酸性体系中N-H断键决定着肼分解速率,而碱性条件下氢基自由基两两结合就可以转化为H2,肼发生脱氢反应可以迅速转化为H2和N2,并不依赖于N-N断键产生的氨基自由基,所以在整个酸碱性条件下N-H断键都起着主导作用。
3 反应机理探讨
从催化肼断键的Pt催化剂的催化原理来看,f层的空轨道能提供孤电子对的容纳从而吸引分子过来配合,而Pt的价电子层轨道是5d96s1,5d9和6s1要完整排满均缺失一个电子,其产生的势阱即为活性位点,其它分子的成键电子云靠近活性位点时,被吸引落入势阱中难以逃脱,从而成键电子对被破坏引起断键,所以就催化剂本身而言,它是没有选择性的,只是破坏落入势阱中的成键电子对。从化学结构的角度去分析,酸碱性条件下溶液环境影响了肼分子N-H键与N-N键的成键电子对运动范围,从而改变N-H键与N-N键的反应能垒,进一步影响肼分解的断键。
4 结 论
(1) pH>9.8时,溶液中肼分子主要以N2H4形式存在,并且随着OH-浓度升高,N-H断键被促进,肼分解速率提高。1.1 宏观整体来看,在酸碱变化过程中,N-H断键作为整个反应的控速步骤起着主导作用,决定了肼分解速率,随着酸度升高,肼分解速率下降。