脂质体的制备方法及应用的研究进展
王兴芝,代英辉*,王东凯
(1. 沈阳药科大学 中药学院,辽宁 沈阳 110016;2. 沈阳药科大学 药学院,辽宁 沈阳 110016)
1 脂质体概述
1.1 脂质体的概念
1965 年,英国的 Bangham 等[1]发现脂质体(liposomes, LPs)后,人们开始了对脂质体的研究。脂质体是指将药物包封于类脂质双分子层薄膜中间所制成的超微球形载体制剂。当两性分子(如磷脂)在水相中分散时,疏水尾部为避开水相倾向于聚集在一起,形成尾对尾的结构;而亲水头部暴露在水相中,形成头对头的结构,这样的聚集方式就形成了具有双分子层结构的中空囊泡[2],就可以利用中空囊泡的结构进行装载药物。
1.2 脂质体的分类
1.2.1 普通脂质体
普通脂质体是由一般脂质组成的脂质体,包括单层脂质体和多层脂质体。单层脂质体是由单层双分子脂质膜形成的封闭囊泡。在单层脂质体中,根据其大小又可分为小单层脂质体和大单层脂质体。多层脂质体是由多层双分子脂质膜与水交替形成的封闭囊泡[3]。
1.2.2 长循环脂质体
长循环脂质体又称为隐形脂质体和空间稳定脂质体,由神经节苷脂、唾液酸衍生物等在其表面进行修饰后所形成的脂质体。普通脂质体在人体内大部分经过网状内皮系统吸收,将脂质体被动靶向运送到肝脏和脾脏处,长循环脂质体经聚乙二醇修饰后可以在脂质体表面形成“构象云”和水化膜,延长出的亲水性长链与普通脂质体相比,增加了亲水性和空间位阻,使脂质体的稳定性增加,降低了网状内皮系统的识别和摄取。延长了脂质体制剂在体内的循环时间[4],可在除肝脏和脾脏处以外的地方,发挥诊断或治疗作用。目前,长循环脂质体常应用于抗肿瘤、抗高血压、抗病毒、抗糖尿病等[5]疾病的治疗。
1.2.3 热敏脂质体
热敏脂质体是由相变温度(Tc)稍高于体温的脂质组成的脂质体,其药物的释放对温度具有温度敏感性,局部加热可促使药物在肿瘤部位快速释放,可减少用药剂量[6]。
1.2.4 pH 敏感脂质体
pH 敏感脂质体是使用对 pH 值(特别是低 pH 值)敏感的脂质作为膜材组成的脂质体。当 pH值 < 6.0 时,脂质体释放内容物。POPE、CHOH、PE、DOPE 等可作为 pH 敏感脂质体的膜材[7]。
1.2.5 配体修饰脂质体
配体修饰脂质体是指加入具有靶向功能的配体或将该配体通过化学连接到脂质体表面,形成的脂质体,其核心机制就是通过配体与受体之间的特异性结合来改变药物的体内分布,因此,要正确选择配体和受体,让其大部分只在病灶处表达[8]。
1.2.6 免疫脂质体
免疫脂质体是指掺入抗体或将抗体通过共价结合的方式连接到脂质体表面,修饰形成的具有免疫活性的脂质体。其通过抗原与抗体之间的特异性结合来消灭肿瘤细胞,达到靶向治疗的目的[9]。
1.3 脂质体的理化性质
1.3.1 相变温度
当升高温度时,脂质双分子层中的酰基侧链从有序状态变为无序状态,这种变化引起脂膜的物理性质发生一系列变化,可由“胶晶”态转为“液晶”态,会导致膜的横切面增加,双分子层厚度减小,膜的流动性增加,这种转变时的温度称为相变温度[10]。因此,在脂质体制备时,应选择具有适宜链长和饱和度的磷脂。一般磷脂脂肪酸链越长,相变温度越高;链越短,则相变温度越低,所以,选择短链脂肪酸的磷脂更有利于形成体积小的脂质体,并能够增强双分子层的流动性[11]。Nagase 等[12]通过研究发现,调控磷脂的相变温度,可以制备 pH 敏感脂质体作为有效的siRNA 载体,其转染特性可以通过温度进行调节。
1.3.2 膜的通透性
脂质体的通透性是指给定物质在一定条件下通过脂质体膜的速率,直接影响了药物的包埋和释放[13]。对于不同物质,其通透性也有很大不同。尹长城等[14]研究发现,pH 和 温度均会引起脂质体膜的通透性的变化。当脂质体的磷脂发生相变时,脂质体膜的通透性增加。
1.3.3 膜的流动性
脂质体的流动性是脂质体的一个重要物理性质,膜的流动性大,脂质体的稳定性就小、药物释放快[15]。尉青[16]研究了胆固醇在细胞膜中的作用时发现,胆固醇对膜的流动性起着重要的调节作用。在温度较高、磷脂分子运动较强时,胆固醇可以降低膜的流动性;反之,胆固醇又可提高膜的流动性,使其保持在相对稳定的状态。
1.3.4 脂质体的荷电性
含酸性脂质的脂质体呈荷负电,含碱基脂质的脂质体呈荷正电,不含离子的脂质体显电中性。脂质体的荷电性也会影响脂质体的稳定性。而我们皮肤角质层在生理条件下带有负电荷性,可能会对载体中正电荷的成分产生吸引作用。林宏伟[17]研究发现,携带正电荷的脂质体比携带负电荷的脂质体的药物经皮渗透效率更高,可能是因为电荷间静电吸引作用促进了药物的吸收渗透。相反,如果脂质体呈荷负电,也可能会因为静电排斥作用,减少药物的渗出,提高了脂质体的稳定性。
1.4 脂质体的质量评价
1.4.1 包封率与载药量
包封率是评价脂质体的重要指标,它指的是包封在脂质双分子层中的药物含量占总投药量的百分比,能反映出脂质体中药物包封程度的高低[18],通常要求脂质体的药物包封率达80%以上。常用的包封率测定方法有:离心法、超滤离心法、葡聚糖凝胶柱法、微柱离心法、透析与反透析法、鱼精蛋白凝聚法等。张鑫等[19]研究波棱素脂质体包封率测定的方法及其在体外释药特性。方法采用薄膜分散法制备脂质体,分别采用超滤法、高速离心法、透析法分离脂质体和游离药物,计算脂质体包封率。结果三种方法中,超滤法最适合用于测定包封率,脂质体包封率为(98.9 ± 0.13)%;脂质体 24 h 内累计释放量为 88.31%,72 h 基本上完全释放,药物释放符合 Higuchi 方程。证明超滤法为波棱素脂质体最佳包封率测定方法,波棱素脂质体体外释放具有缓释特点。载药量指脂质体中所包封药物重量的百分率。载药量的大小影响药物的临床应用剂量,载药量越大,越容易满足临床需要。
1.4.2 形态与粒径
脂质体的微观形态一般为球状,可通过透射电镜观察脂悬液或扫描电镜观察冻干粉,合格的脂质体需形态规整、分散均匀。脂质体的粒径大小及分布决定了其与体内细胞作用的部分以及吸收和分布[20]。脂质体的形态与粒径均可影响包封率及稳定性。储晓婷等[21]制备了 3 种 VK1 脂质体(Lip-180、Lip-120、Lip-60),通过对其进行体内外评价,得出结论:聚乙二醇化 VK1 脂质体分布均匀,稳定性高,释放缓慢,口服生物利用度高,体内促凝效果较好,优选粒径最小的Lip-60,小粒径脂质体更具有优势。
1.4.3 泄漏率
脂质体中药物的泄漏率表示脂质体在贮存期间包封率的变化情况,是评价脂质体稳定性的重要指标。若因脂质体不稳定造成包载药物的泄漏,不仅会使药物代谢动力学过程和药效发生改变,还可能增大药物的毒性[22]。
1.4.4 磷脂的氧化程度
磷脂在分子结构上多数都含有不饱和的脂肪酰链,容易出现氧化降解反应,称为磷脂的过氧化。脂肪酸链不饱和度越高,越容易氧化。当过氧化反应发生时,会影响脂质体膜结构的改变,造成脂质体功能的改变,渗透性升高[23]。能引起磷脂氧化的因素有很多,如温度、辐射、氧气、金属离子、光源、包装材料等[24]。耿亚男[25]经过添加多种抗氧化剂发现,二丁基羟基甲苯(BHT)的抗氧化效果最为显著。
2 脂质体的制备方法
2.1 被动载药法
2.1.1 薄膜分散法
薄膜分散法是最早发现并且直到现在仍常用的一种脂质体制备方法,是将磷脂等膜材料和脂溶性物质溶解到一定量的有机溶剂(如氯仿)中,进行旋转减压蒸发,以除去有机溶剂,在瓶壁内侧形成一层薄膜,最后加入水相介质(如 PBS)充分振摇,进行洗膜操作,经水化后脱落,所得到的即是脂质体[26]。但形成的脂质体粒径大且不均匀,需要将得到的脂质体通过如超声、过膜挤压等方法使其粒径减小。Zhang 等[27]按照薄膜分散法设计了用 Gal-PEG-DSPE 修饰的羽扇豆醇脂质体,并对其进行了体内外抗肿瘤作用的考察。孙庆雪等[28]通过薄膜分散法制备了褪黑素脂质体,得到的褪黑素脂质体,包封率较高,体外释药有明显的缓释效果。但由薄膜分散法制备的脂质体载药量少,包封率低。
2.1.2 逆向蒸发法
逆向蒸发法最早由 Szoka[29]发现,是脂质体装载亲水性药物的最佳方式。对于亲水性药物,囊泡内水相是唯一可以装载药物的区域。因此,在该方法中,可以在脂质体形成过程中包裹大量亲水性药物,从而达到高载药量的效果。逆向蒸发法的制法是通过将亲水性药物溶解在水中并将磷脂溶解在与水不混溶的溶剂(如氯仿)中来制备的 W/O 乳剂,然后在减压蒸发下缓慢除去有机溶剂,形成凝胶。随着有机溶剂的进一步蒸发,产生脂质体分散体,药物就可大量保留在囊泡内的水相中[30]。通过此方法制得的脂质体与薄膜分散法相比,载药量和包封率均有提升,但所需有机溶剂多,易造成有机溶剂的残留[31]。
2.1.3 溶剂注入法
溶剂注入法多采用乙醇注入法和乙醚注入法,此类方法是将类脂等脂质溶于有机溶剂中(油相),然后将油相匀速注入水相中(含水溶性药物),搅拌挥尽有机溶剂,再超声得到脂质体。乙醇注入法简便易操作,且包封率高,但制备速度缓慢,粒径大小不均一,不适合大量制备[32]。刘金丽等[33]应用溶剂注入法制备的利奈唑胺脂质体包封率为 82.36%,RSD = 1.32%,在显微镜下观察,利奈唑胺脂质体粒径较均一、形态圆整。
2.2 主动载药法
2.2.1 pH 梯度法
pH 梯度法通过控制脂质体膜内外的 pH 浓度,形成一定的 pH 梯度差,弱酸或弱碱药物则顺着 pH 梯度,以分子形式跨越磷脂膜而使以离子形式被包封在内水相中[34]。因此,通常 pH 梯度越大,载入脂质体内的药物越多,包封率也越高。周艳艳等[35]通过被动载药法和 pH 梯度法成功制备了两种 Len 脂质体,主动载药法制备的 Len 脂质体具有更高的包封率和更显著的缓释效果,具有较好的临床应用潜力和产品开发价值。
2.2.2 硫酸铵梯度法
硫酸铵梯度法设计原理是化学平衡移动,其通过游离氨扩散到脂质体外,间接形成 pH 梯度,使药物积聚到脂质体内。尹飞等[36]应用硫酸铵梯度法制备盐酸表阿霉素长循环脂质体,对处方优化后制备的盐酸表阿霉素长循环脂质体包封率高、粒度分布范围较窄、平均粒径较小。姜爱玲等[37]通过实验认为硫酸铵梯度法可有效提高小檗碱的载药量和包封率。
2.2.3 醋酸钙梯度法
醋酸钙梯度法通过醋酸钙的跨膜运动产生的醋酸钙浓度梯度(内部的浓度高于外部),使得大量质子从脂质体内部转运到外部产生的 pH 梯度。胡艳秋等[38]通过醋酸钙梯度法制备盐酸法舒地尔脂质体方法可行,所制得载药脂质体包封率为 80.94% 达到制剂学要求,且重现性好。蔡丽杰[39]应用醋酸钙梯度法成功制备了三氧化二砷脂质体,方法简单可行;纳米粒粒径小而均匀,形态较好,包封率较高;三氧化二砷脂质体释药缓慢,无突释效应;三氧化二砷脂质体可明显增长大鼠的消除半衰期。
2.3 主动载药法与被动载药法的区别
被动载药法与主动载药法各有优势,对于脂溶性且与磷脂膜亲和力高的药物,被动载药法较为适用。而对于两亲性药物,其油水分配系数受介质的 pH 和离子强度的影响较大,包封条件的较小变化就有可能使包封率有较大的变化。此时,可采用主动载药法,且主动载药法包封率高,稳定性高,但需要透析除盐等步骤,且操作时间长[40]。
3 脂质体的应用
3.1 脂质体在食品领域中的应用
3.1.1 包埋脂类
许多食物中脂类含有许多不饱和键,容易发生氧化、结构改变等问题,还容易发生降解。随着对脂质体的深入研究,发现可以将其用于包埋某些特殊性脂质,对其进行保护。何娜[41]就采用了脂质体包埋脂类的技术,具有保护有效成分活性、提高有效成分的生物利用率、掩盖不愉悦气味、延长有效成分保质期、定向靶向释放等优点。
3.1.2 包埋抗氧化剂
脂质体也被应用于包埋抗氧化剂,可有效隔离光、热、氧气等因素,保证了抗氧化剂的效用,在不同抗氧化剂中脂质体也相应的会发生变化。应用脂质体可提高抗氧化剂的稳定性。梁提松[42]研究了脂质体包埋杨梅花色苷的方法,实验结果表明,纳米脂质体作为一种载体系统,对花色苷的抗氧化活性有一定的保护作用,可减少外界环境因素对其生理活性的影响。
3.1.3 包埋蛋白质和酶
蛋白质的稳定性差,在过酸、过碱或温度过高时,都容易发生分解,结构发生改变。对其进行包埋,利用脂质体特殊的靶向性,可让蛋白质和酶在特定部位或时机进行释放[43],可保护蛋白质的完整性,发挥更大的效应。
3.1.4 包埋维生素
维生素的稳定性差,在光、氧气等条件下易发生氧化变质等现象,失去其活性。对其进行包埋,可有效降低光和氧气等的影响,减少加工过程中的损失。周瑶等[44]用脂质体包埋维生素 C,并对其稳定性进行检查,得出结论:维生素 C 脂质体具有分散度好、形态稳定等特性,并能增加维生素 C 的脂溶性,提高其吸收、避免氧化、发挥缓释作用,增加其保质时间等。
3.1.5 应用实例
脂质体包埋脂肪酶和蛋白酶,可有效防止酪蛋白在奶酪制作过程中过早的水解[45];包埋维生素 D,可增加奶酪中维生素 D 的回收率[46];包埋茶多酚,可提高其生物利用度[47]。脂质体还可在许多食品基质(如牛奶、奶酪、酸奶、果汁、糖果)中应用,还可应用于封装调味剂和营养剂[48]。
3.2 脂质体在医药领域中的应用
脂质体充当抗肿瘤药物、抗癌药物、抗细菌药物、抗寄生虫药物、基因等的载体发挥着极其重要的作用,能够提高治疗效果,还可以降低药物的毒副作用。表 1 列举了部分脂质体药物的应用与研发实例。
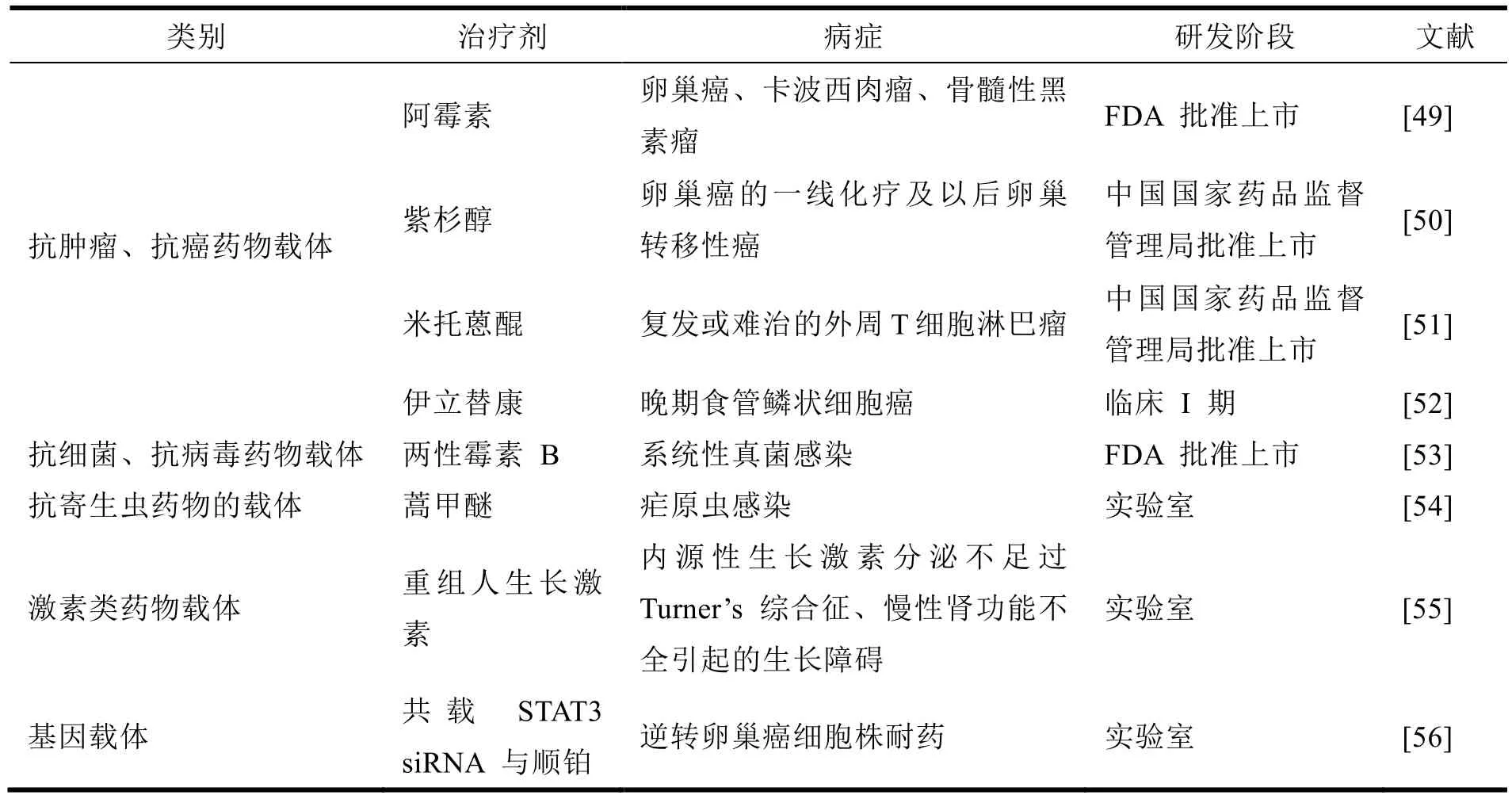
Table 1 Examples of liposomal drug application development表 1 脂质体药物应用研发实例
3.2.1 抗肿瘤、抗癌药物载体
脂质体可作为抗肿瘤药物载体,其特殊的靶向性可增加与肿瘤细胞的亲和力,有降低药物剂量、降低毒副作用等特点。Doxil 是一种脂质体形式的化疗药物——阿霉素,已被 FDA 批准上市,其可以将更高浓度的药物输送到病变处,可用于治疗卵巢癌、卡波西肉瘤、骨髓性黑素瘤[49]。紫杉醇脂质体是于 2004 年被我国药监局批准上市的第一个脂质体药物,也是国际首次上市的注射用紫杉醇脂质体药物,可用于卵巢癌的一线化疗及以后卵巢转移性癌的治疗[50]。可采用薄膜分散法或喷雾干燥法来制备紫杉醇长循环脂质体,该方法制得的紫杉醇脂质体制剂具有毒性小、稳定性高的优点[57]。2023 年 1 月,盐酸米托蒽醌脂质体注射液被中国国家药监局获批用于治疗复发或难治的外周 T 细胞淋巴瘤(PTCL),也是全球首个米托蒽醌脂质体药物获批上市[51]。食管鳞状细胞癌在所有食管癌患者中占比 90%,成为欧洲和亚洲最常见的病理类型。晚期食管鳞状细胞癌可选择的治疗方法有限,顺铂联合 5-氟尿嘧啶是一线治疗常选择的化疗方案,但经一线治疗后仍有失败情况。柳韵[52]应用伊立替康脂质体治疗一线化疗失败的晩期食管鳞癌,对其疗效、安全性、药代动力学等进行评价与分析,正处于 Ⅰ 期临床研究中。
3.2.2 抗细菌抗病毒药物载体
脂质体可将抗生素等药物包裹起来,利用其两亲性,可穿过细胞膜,即能将药物带入细胞内,杀死细菌,达到治疗效果。AmBisome 是一种两性霉素 B 的单层脂质体制剂,已被 FDA 批准可用作对系统性真菌感染的治疗[53]。由于细菌生物膜对抗生素具有高度耐药性,随着药物使用时间的延长,缺乏新的抗生素替代,就只能通过加大剂量来确保疗效,但抗生素的毒副作用也会增加。孙月林[58]进行了溶菌酶修饰的庆大霉素脂质体对抗细菌生物膜的研究,得出结论:溶菌酶修饰的庆大霉素脂质体能够在一定程度上降低抗生素的使用剂量,减缓耐药菌株的形成,同时,也有助于减小抗生素的毒副作用。该项研究为使用抗生素治疗细菌生物膜相关的顽固性感染提供了一种新的方案。
3.2.3 抗寄生虫药物的载体
脂质体可作为抗寄生虫药物的载体,由于脂质体的天然靶向性,经静脉注射脂质体后,大部分可迅速被网状内皮系统快速吞噬或摄取。利用这一特点可以用含药脂质体治疗网状内皮系统疾病,如利什曼病和疟疾就是某种寄生虫侵入网状内皮细胞引起病变。而用于治疗利什曼病需使用含锑和砷的药物杀死寄生虫,但此类药物毒性很大,随着对脂质体研究的迅速发展,人们发现当用脂质体进行包埋后,就可以大大降低药物的毒性,避免了心肌炎和肾炎的发生[59]。卢栩[54]通过其研究所制备的修饰靶头 CSA 的蒿甲醚脂质体,能够靶向感染红细胞中的恶性疟原虫蛋白VAR2CSA,通过其靶向作用可提高蒿甲醚抗疟作用,有效抑制疟原虫感染,生物安全性较好,具有良好的治疗效果。
3.2.4 激素类药物的载体
脂质体进入人体后,大部分被网状内皮系统吞噬,从而激活免疫功能,改变被包封药物的体内分布,提高药物的生物利用度,减少药物的治疗剂量和降低药物的毒性。重组人生长激素主要用于内源性生长激素分泌不足的 Turner’s 综合征、慢性肾功能不全引起的生长障碍的治疗。但其作为一种蛋白质激素给药具有半衰期短、稳定性差的缺点,临床用药需频繁注射给药,且某些患者体内会出现抗生长激素抗体或出现超敏反应。而使用脂质体对其进行包埋,充当载体,则能提高药物的稳定性和生物利用度,延长药物半衰期,从而提高疗效[55]。
3.2.5 基因的载体
基因工程在中国医学领域应用十分广泛,胰岛素就是通过基因工程来实现大批生产的。随着对脂质体的研究,发现脂质体可应用于基因工程中,应用脂质体可保护基因不被 DNA 酶降解。脂质体作为目的基因的载体具有很大优势,安全、易于合成、可大规模生产;还可以通过结构修饰改变载体性质,提高载体转染效率和细胞靶向性等。有学者[60]研究脂质体在心血管疾病基因治疗中的应用中,发现阳离子脂质体与核酸带阴离子的磷酸集团通过静电相互作用紧密结合,可形成脂质体—核酸复合物,能防止核酸被血液中的核酸酶降解。钱艺美等[56]通过实验室研究发现,共载信号转导和转录激活子 3(STAT 3)si RNA 与顺铂(DDP)纳米脂质体(STAT3/DDP-Lip)可以在体内外抑制 DDP 耐药性卵巢癌 SKOV3 细胞株的生长。汪琼卉等[61]总结阳离子脂质体在基因治疗中的研究进展时发现,在基因治疗中包括 pDNA、mRNA、siRNA、microRNA 和其他类型的反义寡核苷酸可通过阳离子脂质体进入细胞达到治疗目的。
3.3 脂质体在化妆品领域中的应用
化妆品中如含有脂质体可比传统化妆品更具有穿透性,能使功能性成分有效透过皮肤,到达更深处,可起到对其进行修护或治疗等作用。且其具有多重功效,因脂质体具有双亲性,当用它作为载体时,亲脂性和亲水性物质均可结合,如可结合 Vc 和 Ve 等营养成分,扩大了化妆品中含有的有效成分。同时添加了脂质体的化妆品会使营养更长效,具有超强吸收、护肤的作用[62]。
最早加入脂质体的化妆品是迪奥于 1986 年推出 Capture,在大豆卵磷脂脂质体中含有胸腺提取物、胶原蛋白、弹性蛋白肽和透明质酸,公司申请了脂质体化妆品专利 SG55887。目前,日本 Nikko Chemicals Co.Ltd 根据专利技术(JP 21242088A)生产的 Nikko Aquasorae 系列脂质体化妆品,是用氢化卵磷脂制成包埋 VA、VE 醋酸盐和脾脏提取物等的脂质体作为化妆品的组分。欧莱雅也推出了一种含有前视黄醇 A 的抗皱脂质体产品 Revitalift Double Lifting[63]。隆力奇的蛇油 SOD 蜜蕴含高纯度精制蛇油和脂质体 SOD,能迅速被肌肤吸收,并在皮肤表面形成一层养护膜,可深层滋养,有效对抗皮肤衰老。美加净的保湿润肤露,采用特有的脂质体技术,深入肌肤持续释出易于吸收的养分[64]。
4 总结与展望
脂质体作为近几十年来发现的新型制剂,已经得到了广泛的发展,且其发展十分迅速,在食品、医药、化妆品等领域都发挥了极大的作用。近些年,通过研究发现,脂质体在传染病、寄生虫病、抗真菌、免疫佐剂、抗心脑血管疾病和抗精神疾病等方面的应用也取得了极大的进展,还能作为解毒剂载体使用。但脂质体药物的研究中仍存在一些问题,对脂质体进行功能性修饰后,功能性材料的安全性和有效性仍需进一步考察。对脂质体进行质量评价时,通常采用体外实验,但是对于体内外存在很大差异,而在体内不能实时监测。同时,对脂质体的体内分布的机制了解还不够完善,且其对生物膜的亲和力高,易被其他组织识别、吸收,导致到达作用部位时,药物浓度较低,也存在生产成本贵、不能大批量生产等问题。
将“liposomes”设置为关键词,在 PubMed 上搜索 2017~2021 年近五年来与脂质体相关的文献。根据搜索结果进行统计可知:随着时间的推移,脂质体的研究文献数量呈现递增趋势,与 2017年相比,2018 年文献数量增长 4.6%,2019 年增长 7.1%,2020 年增长 11.8%,2021 年增长 21.8%。这说明脂质体的研究仍在继续,还有待去发掘出更多的优势,完善现有脂质体的不足。
在未来的研究中,我们需要寻找更加经济实惠的原材料,寻找可批量生产的方法,设计新的技术提高包封率,研究好其体内分布、清除机制,发现更加适合于在体内进行脂质体追踪实验的技术,确保功能性材料的安全性和有效性。随着对脂质体更加的深入了解,可能会对癌症等现有不能治愈的疾病,在这些疾病治疗中取得突破性的进展,让脂质体在医学领域中发挥更大的价值。
- 中国药剂学杂志(网络版)的其它文章
- 抗肿瘤刺激响应型凝胶的制剂新进展
- 2D-LC 与质谱联用技术及其在药物质量研究中的应用
- 杠柳毒苷理化性质研究

