芽孢表面展示系统及其在水产疫苗研发中的应用
昝子叶 柯 飞 赵威山 邹 红 王桂堂 吴山功
(1. 中国科学院水生生物研究所, 农业农村部淡水养殖病害防控重点实验室, 水产品种创制与高效养殖重点实验室(中国科学院), 武汉 430072; 2. 中国科学院大学, 北京 100049)
近年来, 随着养殖密度不断提高, 加之种质退化、水环境污染加剧、病原微生物大量滋生, 养殖水产动物疾病频繁发生, 给水产养殖业造成了巨大的经济损失, 因此疾病防治受到越来越多的重视[1]。抗生素等化学药物是疾病防治的常用药物, 然而这些化学药物的使用会产生耐药性及药物残留问题[2]。疫苗可以预防传染病暴发, 又不会导致细菌的耐药性及药物残留, 因而成了未来鱼病防治的重要发展方向[3]。但传统注射和浸泡疫苗有诸多不便, 口服的方式更加方便快捷。不过, 动物的胃肠道环境制约了口服疫苗的研发及使用, 因此亟须寻找高效的抗原呈递平台。
芽孢杆菌(Bacillusspp.)是水产养殖中常用的益生菌, 不仅能改善养殖环境、减少疾病发生, 还能促进水产动物的生长发育[4,5]。芽孢杆菌也是异源蛋白表达的安全宿主(Generally Recognized As Safe), 已被开发为成熟的蛋白表达系统[6]。芽孢杆菌的芽孢对高温、酸碱环境、裂解酶和多种化学物质等具有很强的抗逆性, 因此可利用芽孢的衣壳蛋白(如CotC、CotB和CotG等), 在芽孢的内生过程中, 将异源抗原稳定地展示在芽孢表面, 构建芽孢表面展示系统, 使其成为口服疫苗抗原递送的理想平台[7]。枯草芽孢杆菌(Bacillus subtilis)是迄今为止研究最为清楚的芽孢杆菌, 目前枯草芽孢杆菌芽孢表面展示(Bacillus subtilisSpore Surface Display)已成功地用于药物或抗原的呈递[8]、工业酶类的展示[9]、环境污染物的监测与降解[10]、化学物质和重金属物质的生物吸附[11,12]及生物传感器的构建[13]等多个领域。
芽孢表面展示基因工程口服疫苗能够克服传统疫苗在胃肠道中易受到胃酸和消化酶作用而降解的弊端, 将抗原稳定呈递到肠道, 发挥更加高效的免疫性能[14]。因而, 芽孢杆菌芽孢表面展示系统引起了科研人员的广泛兴趣。目前芽孢杆菌芽孢表面展示系统已被用于畜禽[15—17]及水产动物[18—20]疫苗开发, 本文介绍了水产动物疫苗研发中芽孢杆菌芽孢和感受态, 以及芽孢表面展示系统, 并特别介绍了芽孢作为口服疫苗载体在预防水产动物细菌病、病毒病和寄生虫病方面的研究与应用现状,以期为水产动物高效稳定口服疫苗的开发提供参考。
1 芽孢杆菌特殊形态结构
芽孢杆菌是一类好氧或兼性厌氧、能产生抗逆性内生芽孢的革兰氏阳性菌, 菌体呈杆状, 有鞭毛。芽孢杆菌的形态结构对其生长繁殖以及适应特殊环境具有非常重要的作用。芽孢和感受态这两种特殊形态结构是芽孢杆菌在长期的自然进化过程中形成的生存适应能力, 也是细胞高度有序的遗传调控的结果[21]。在枯草芽孢杆菌生长发育后期, 当环境中出现密度增加、营养物质匮乏等生存压力时, 芽孢杆菌会通过激活鞭毛运动、分泌抗生素和大量水解酶等方式减轻环境压力, 但若未产生太大效果, 其中50%—70%的细胞将进入芽孢形成途径, 而进入芽孢形成途径中的少数细胞(≤20%)会进入感受态形成途径[22—24]。
芽孢对极端温度、压力、酸碱环境、紫外线、辐射和多种化学物质等有很强的抗逆性[25—27],强抗逆性主要基于成熟芽孢的“新结构”, 这些结构被两层膜分隔为3个同心小室, 呈现出同心壳层形式的多层结构; 由外向内包括芽孢外壁(Exosporium)、芽 孢 衣 壳(Spore coat)、外 膜(Outer membrane)、皮层(Cortex)、生殖细胞壁(Germ cell wall)、内膜(Inner membrane)及芽孢核心(Spore core), 其中核心中贮存遗传物质DNA, 芽孢衣壳作为芽孢杆菌芽孢表面展示的重要结构, 主要由内层衣壳(Inner spore coat)和外层衣壳(Outer spore coat)构成[28—31](图1)。
感受态是细胞的一种瞬时生理状态, 此时, 细胞能从环境中摄取外源DNA分子[32]。通常在对数生长期后期, 枯草芽孢杆菌能形成自然感受态细胞[33],但群体中仅有10%的细胞可以分化形成感受态, 因此转化效率一般比较低。芽孢杆菌感受态的形成首先受到群感效应(Quorum sensing)和情景选择(Episodic Selection)的限制, 然后受到一种二元信号转导系统的精密调控, 复杂的信号转导系统保证了机体特异感受态信息素(ComX和CSF)被适当激活,进而刺激感受态形成[34—36]。
2 芽孢表面展示系统
首个芽孢表面展示系统由Isticato等[37]于2001年构建, 通过将破伤风毒素C片段(Tetanus Toxin Fragment C, TTFC)中459个氨基酸片段与枯草芽孢杆菌芽孢衣壳蛋白CotB融合, 转化后在淀粉酶基因amyE处发生同源重组, 最终将TTFC抗原展示在芽孢表面, 开发了一种新型高效的抗原呈递模式。芽孢表面展示系统具有很多独特的优势: (1)可展示分子量较大外源蛋白和多聚体外源蛋白[38]; (2)外源蛋白随芽孢的内生而展示, 不需要跨越细胞膜[39,40];(3)有一套完整消耗ATP的分子伴侣体系, 帮助外源蛋白快速正确折叠, 使其保持原有空间构象和生物活性[28,41]; (4)芽孢抗逆性扩大了外源蛋白的应用范围, 可抵抗高温、强酸碱和辐射等不良环境长时间存活[42,43]。因此基因工程技术与芽孢表面展示系统相结合, 构建重组型芽孢表面展示系统的研究受到了科研人员越来越多的关注。
一个完整的芽孢表面展示系统主要由宿主菌、锚定蛋白和表达载体三个部分组成。此外, 连接肽能够提高表面展示效率, 也常常被用于芽孢表面展示系统中。
2.1 宿主菌
目前芽孢表面展示常用宿主菌有苏云金芽孢杆菌(Bacillus thuringiensis)[44]、炭疽芽孢杆菌(Bacillus anthracis)[45]和枯草芽孢杆菌[37]三种。枯草芽孢杆菌是目前研究最多的代表菌种, 已在农业、工业等领域被广泛使用[46—49]。苏云金芽孢杆菌是农业上重要的生物防治菌株[50]。与另外两种宿主菌相比, 枯草芽孢杆菌具有很多优势: (1)研究最早且最深入, 基因组注释信息清楚, 已建立完善遗传操作体系; (2)芽孢结构研究较深入, 解析最全面[51,52];(3)不含毒素, 是公认安全且可直接食用的微生物,目前已作为益生菌在人类和其他动物中广泛使用[53]。
枯草芽孢杆菌168菌株是最早被发现可在自然状态下形成感受态, 并实现外源DNA转化的芽孢杆菌菌株[54]。基于这一发现, Anagnostopoulos与Spizizen[55]于1960年建立了168菌株感受态细胞的化学制备体系, 为枯草芽孢杆菌的分子遗传操作奠定了基础。1997年日本和欧洲的几个实验室联合完成了Bacillus subtilis168菌株基因组的全基因组测序[56]。近年来, 研究人员对枯草芽孢杆菌遗传转化和表达系统进行了更加深入的研究, 越来越多枯草芽孢杆菌工程菌株, 如WB600、WB700和WB800等的出现, 为芽孢表面展示系统的研究与应用提供了更多的可能性。但目前芽孢表面展示系统宿主菌的选择还是比较有限, 还应该挖掘更多适应不同环境的菌种(株), 如地衣芽孢杆菌(Bacillus licheniformis)是水产养殖中常用的益生菌, 以地衣芽孢杆菌作为宿主菌, 可能实现在展示特定外源蛋白的同时, 还能够作为益生菌发挥益生功能。
2.2 锚定蛋白
芽孢表面展示所使用的锚定蛋白一般是芽孢衣壳蛋白, 在选择衣壳蛋白时需要考虑其位置和丰度, 以实现较好的表面展示效率。已报道的可用作锚定蛋白的芽孢衣壳蛋白包括CotB、CotC、CotG、CotX、CotY、CotZ和OxdD等, 其中CotB、CotC和CotG三种衣壳蛋白是目前研究最多且深入的, 它们位于芽孢外衣壳层, 其位置和丰度都保证了展示的外源蛋白与外界环境有高水平的接触[57]。
CotB是首个应用于芽孢表面展示系统以展示外源蛋白的衣壳蛋白, 其与外源蛋白通过C端、N端和中间融合三种方式融合, 以不同的长度(包括全部氨基酸序列或N端部分氨基酸序列), 均可将有活性的外源蛋白成功展示在芽孢表面[37,58]。目前CotB已成功用于多种抗原和酶类的表面展示, 如炭疽芽孢杆菌的保护性抗原PA[59]、艰难梭菌(Clostridium difficile)的鞭毛帽蛋白FliD[60]和酯酶[61]等。基于CotC的芽孢表面展示均使用其全长氨基酸序列,C端和N端融合方式均可实现表面展示[62—64]。目前CotC已成功用于多种酶类的表面展示, 如尿素酶A亚基UreA[65]、乙醇脱氢酶[42]和β-半乳糖苷酶[66]等, 可显著提升酶对恶劣环境的耐受能力。基于CotG的表面展示均以CotG的完整氨基酸序列作为锚定蛋白, 大部分以C端融合的方式进行。Kim等[38]通过CotG将四聚体外源蛋白链霉亲和素成功展示到芽孢表面。目前CotG已涉及单体、二聚体和四聚体等外源蛋白表面展示, 如N-乙基神经氨酸醛缩酶[67]、ω-转氨酶[68]、腈水解酶[69]等。
此外, 其他锚定蛋白如CotX、CotY、CotZ和OxdD, 已成为后起之秀。以绿色荧光蛋白(Green Fluorescent Protein, GFP)作为报告基因, CotX作为锚定蛋白, 李倩等[70]观察到重组芽孢表面发出绿色荧光,证明CotX可作为锚定蛋白进行表面展示。类似地,将增强型绿色荧光蛋白(Enhanced Green fluorescent protein, EGFP)与锚定蛋白CotY通过C端融合的方式, 可以成功将其展示在芽孢表面[71]。而CotZ是位于更接近芽孢表面的外衣壳蛋白, 利于外源蛋白充分展示在芽孢表面, Negri等[61]以CotZ为锚定蛋白, 成功在芽孢表面展示鞭毛蛋白FliD。值得关注的是, OxdD是目前报道的唯一可作为锚定蛋白的芽孢内衣壳蛋白, 植酸酶与OxdD通过C端融合的方式, 成功地将植酸酶展示在芽孢表面并具有相应的酶活性[72]。
越来越多的可用于芽孢表面展示的衣壳蛋白的发现, 为提高表面展示效率提供了新的思路, 利用多种衣壳蛋白同时展示同一种外源蛋白或不同种外源蛋白, 增加表面展示的外源蛋白数量和种类,是值得进一步探索的方向, 将为芽孢表面展示系统研究与应用提供更多的可能性。
2.3 表达载体
芽孢表面展示系统的构建可以通过基因重组(图2)和非基因重组两种方法进行[73]。
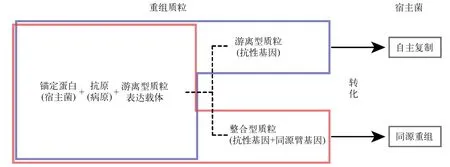
图2 基因重组法构建芽孢表面展示系统示意图Fig. 2 Schematic representation of spore surface display system constructed by genetic recombination strategy
通过基因重组方法构建时使用的质粒有两种,整合型和游离型[74]。整合型质粒转化进入感受态细胞后, 与枯草芽孢杆菌基因组发生重组, 目的基因整合到基因组中, 后在特定启动子作用下开始表达[75]。整合策略有单交换和双交换两种, 其中双交换是目前研究中使用最多的。构建双交换整合型载体时, 选择的同源臂多为破坏后不影响芽孢杆菌正常生长的基因, 如lacA、scaA、gltA、trpC、amyE和pyrD等[8,76,77,78]; 同源臂的长度至少为400—500 bp,才能发生有效重组[79]。淀粉酶基因amyE是使用最多的同源臂基因, 整合后因外源基因的插入使amyE被破坏, 宿主菌失去分解淀粉的能力。游离型质粒携带目的基因转化进入枯草芽孢杆菌感受态细胞后可进行独立复制与表达[74]。使用游离型载体构建表面展示系统操作简单, 转化率相对较高, 但质粒遗传不稳定, 容易随着宿主菌的分裂增殖而丢失,给后续实验带来一定的风险[80]。因此, 寻找遗传稳定不易丢失的穿梭型质粒是未来探究的方向。非基因重组方法是将纯化的外源蛋白与芽孢共同培养, 由于两者之间存在静电和疏水作用可相互结合,最后吸附于芽孢表面, 或使用交联剂将它们固定在孢子表面, 最终发挥作用[81,82]。
总之, 无论是基因重组方法, 还是非基因重组的方法, 都可以将外源目的蛋白展示在芽孢表面, 进而发挥作用。表面展示效率是系统构建的关键, 容易在体外得到大量纯化的外源蛋白, 可先通过基因重组方法将其展示到芽孢表面, 再利用非基因重组方法, 将外源蛋白吸附于芽孢表面, 两种方法结合将更多的外源蛋白展示于芽孢表面, 提高表面展示效率。
2.4 连接肽
在锚定蛋白和外源蛋白之间插入合适的连接肽, 可使锚定蛋白和外源蛋白之间形成空间位阻,利于两者正确进行空间折叠, 保证表面展示外源蛋白的活性[83]。GGGGS和EAAAK是目前常用的两种连接肽[84,85]。连接肽(GGGGS)n(n≤6), 由于甘氨酸含量高, 使其柔软易弯曲, 因此也被称为柔性连接肽[84]。但柔性连接肽存在一些弊端, 过于柔软导致融合蛋白整体易对折靠拢形成二聚体, 导致外源蛋白活性下降。随后研究人员在两种绿色荧光蛋白之间引入了能形成α-螺旋结构的(EAAAK)n(n=2—5)序列, 该序列可有效控制两种蛋白间的距离, 减少功能域之间的干扰, 也被称为刚性连接肽[85]。其后, Huang等[86]将柔性连接肽GGGGS (F)和刚性连接肽EAAAK (R)结合形成RRRRR、FFFFF及FFFRR三种连接肽, 进一步构建酸性磷酸酶-绿色荧光蛋白融合蛋白PhoC-GFP, 比较分析发现连接肽的灵活性可以有效调节PhoC-GFP的活性, 在使用FFFRR连接肽时, PhoC-GFP的酶活性最高。综上所述, 适当地利用连接肽可一定程度上提升外源蛋白展示的稳定性和高效性, 在构建芽孢表面展示系统时加入连接肽是非常有必要的。
3 芽孢表面展示系统在水产养殖中的应用
从动物福利、经济成本和方便程度等角度考虑, 口服接种是水产动物较理想的免疫接种方式[87]。口服免疫主要是通过刺激鱼体肠道黏膜系统来产生免疫应答反应, 但口服后抗原会受到高浓度胃酸和肠道蛋白酶的作用而被破坏, 免疫原性降低, 保护效果不佳, 这是阻碍水产动物口服疫苗发展的主要原因[88,89]。研究表明, 芽孢杆菌芽孢可以作为免疫佐剂, 还可作为疫苗的呈递载体[90]。在具有适应性免疫系统的脊椎动物中, 芽孢能被肠道中特异性上皮细胞微褶细胞摄取, 与Peyer氏斑中的淋巴细胞和抗原提呈细胞发生相互作用, 刺激机体产生免疫应答; 在不具有适应性免疫系统的无脊椎动物中, 芽孢能够刺激细胞吞噬作用和非特异性免疫保护[91—93]。芽孢具有强抗逆性, 因此芽孢表面展示系统可作为口服疫苗抗原递送的理想平台, 目前芽孢表面展示系统已经在预防水产动物细菌性疾病、病毒性疾病和寄生虫病方面有相关报道(表1)。

表1 芽孢表面展示系统在水产疫苗研发中的研究进展Tab. 1 Research progress of spore surface display systems in aquatic vaccine development
3.1 细菌病疫苗
罗非鱼链球菌病是严重威胁罗非鱼(Oreochromis mossambicus)养殖产业健康发展的一类疾病, 发病率和死亡率高, 造成严重的经济损失[94]。致病的病原菌有无乳链球菌(Streptococcus agalactiae)和海豚链球菌(Streptococcus iniae), 其中无乳链球菌是主要病原, 属于链球菌科(Streptococcace),链球菌属(Streptococcus), 而Sip蛋白是位于大部分无乳链球菌表面的一种蛋白, 具有高度保守性[95]。Yao等[96]利用衣壳蛋白CotC在芽孢表面展示Sip蛋白, 用重组芽孢GC5-Sip口服灌胃免疫罗非鱼, 发现GC5-Sip组血清中存在Sip特异性抗体, 脾脏和肠道中免疫相关基因TNF-α、TGF-β、MHC-I和T-bet的表达水平显著提高。攻毒试验后GC5-Sip对无乳链球菌感染的相对保护率(Relative Percentage Survival,RPS)达到41.7%, 表明重组芽孢GC5-Sip可诱导鱼体的细胞免疫和体液免疫反应, 在一定程度上保护罗非鱼免受无乳链球菌感染。
弧菌病是水产养殖中最严重的细菌性疾病之一, 能感染各种淡水和海水鱼类、虾类和双壳类动物, 引起出血性败血症, 死亡率高, 制约水产养殖业可持续发展[97]。弧菌属(Vibriospp.)细菌, 如副溶血弧菌(Vibrio parahaemolyticus)、鳗弧菌(Vibrio anguillarum)和哈维氏弧菌(Vibrio harveyi)等均可引起弧菌病[98]。外膜蛋白OmpK是致病性弧菌的共同抗原, Gonçalves等[19]利用衣壳蛋白CotY在芽孢表面成功展示OmpK蛋白, 以重组芽孢CotY-OmpK浸泡免疫斑马鱼(Danio rerio)幼鱼,V.parahaemolyticus或V.anguillarum感染斑马鱼后, 幼鱼存活率分别提高了40%和85%; 继而口服免疫欧洲齿舌鲈(Dicentrarchus labrax)幼鱼,V.anguillarum感染鲈后, 结果CotY-OmpK组幼鱼存活率从60%提高至87%, 表明芽孢可以作为弧菌病口服疫苗载体, 提高鱼类感染致病弧菌后的存活率。
目前虽然可以使用灭活疫苗或者减毒活疫苗预防细菌性疾病, 但这些疫苗主要通过注射方式来进行接种, 使用极不方便。如果利用非基因重组的方式, 将灭活疫苗吸附于芽孢表面, 芽孢作为免疫佐剂, 将灭活疫苗呈递到水生动物肠道, 进而发挥更加高效、安全、快捷的免疫保护效果, 将能够大大降低水生动物细菌性疾病的发病率。
3.2 病毒病疫苗
草鱼出血病 草鱼出血病是危害我国草鱼(Ctenopharyngodon idella)养殖行业最严重的一种病毒性疾病, 患病草鱼死亡率高达70%—80%, 几乎每年都会造成巨大的经济损失[99]。该病病原是草鱼呼肠孤病毒(Grass Carp Reovirus, GCRV), 隶属呼肠孤病毒科(Reoviridae), 水生呼肠孤病毒属(Aquareovirus), 不仅能感染草鱼, 而且还能感染其他经济鱼类; 病毒的11个基因片段共编码13个蛋白, 包括7个结构蛋白(VP4、VP7和VP56等)和6个非结构蛋白(NS31、NS38和NS80等)[100]。
任鹏丽[101]构建重组芽孢CotC-VP4并口服免疫草鱼, 以注射珠江水产研究所商品化减毒活疫苗为阳性对照组, 基础饲料为阴性对照组。研究发现,与阴性对照相比, CotC-VP4组血清中特异性IgM抗体水平和肾脏中免疫相关细胞因子IgM和TLR22表达水平显著升高, 表明CotC-VP4可使鱼体产生一定的抗病毒免疫效应, 在病毒入侵时提供保护作用,但免疫保护效果不及阳性对照组显著。Jiang等[102]也构建了重组芽孢CotC-VP4口服疫苗并免疫草鱼,以注射商品GCRV减毒疫苗为阳性对照, 基础饲料为阴性对照。结果发现与阴性对照相比, CotC-VP4可诱导肠黏液中特异性IgZ抗体水平升高, 多个免疫相关基因的表达水平显著上调; 在GCRV攻毒后,CotC-VP4组草鱼存活率为57%, RPS 47%, 表明该重组芽孢可触发鱼体免疫反应, 提高草鱼抗GCRV感染的能力, 但整体保护效果低于阳性对照组(存活率达89%)。
Chen等[103]利用鱼源枯草芽孢杆菌GC5菌株,构建重组芽孢CotC-VP4和CotC-NS38, 经口灌服免疫草鱼后, 发现均提高了草鱼抗GCRV感染的能力。进一步研究发现, CotC-VP4主要通过诱导IgT转录水平上调, 引发鱼体特异性抗体反应; 而CotCNS38通过诱导炎症反应和主要组织相容性复合物(MHC)的表达, 最终保护草鱼免受GCRV感染。Sun等[104]分别以淀粉酶基因amyE和芽孢萌发必需基因cwlJ为整合位点, 构建重组芽孢ΔamyECotB-VP7和ΔcwlJCotB-VP7。在口服免疫草鱼后, 各实验组均可诱导血清中特异性IgM抗体水平、肾脏中免疫相关基因IL-1β、TNF-α、MHCII和CD4L的表达水平上调, 在感染GCRV后, ΔamyECotB-VP7和ΔcwlJCotB-VP7的RPS分别达到28.09%和50.66%。但ΔcwlJCotB-VP7可引发草鱼更高的免疫反应水平,可能是因为其一直处于芽孢状态, 可持续呈递抗原[104]。而Gao等[105]将编码VP56蛋白的基因分成4个片段,筛选得到最佳抗原VP56-2, 继而构建重组芽孢CotC-VP56-2并口服免疫草鱼。结果显示, CotCVP56-2诱导了脾脏和头肾中更高的特异性IgM抗体水平, 以及免疫相关细胞因子IL-1β、TNF-α、IFN1和MHC-Ⅱ的转录表达, 在感染GCRV后, 肾脏和脾脏组织中病变范围明显缩小, 病毒载量降低, 有效保护草鱼抗GCRV感染。
大口黑鲈蛙虹彩病毒病大口黑鲈蛙虹彩病毒病会在短时间内造成大口黑鲈(Micropterus salmoides)暴发疾病并大规模死亡, 导致大口黑鲈养殖产业遭受重大经济损失[106]。该病由大口黑鲈蛙虹彩病毒(Largemouth bass virus, LMBV)引起, LMBV属于虹彩病毒科(Iridoviridae), 蛙病毒属(Ranavirus),其MCP蛋白对于病毒颗粒的组装和诱导免疫反应至关重要[107]。Wang等[20]利用衣壳蛋白CotC表面展示MCP, 构建重组芽孢CotC-LMBV, 口服免疫大口黑鲈后发现, CotC-LMBV组鲈血清中特异性IgM抗体水平显著升高, 脾脏中免疫相关基因CD4-1、IgM、IL-6和IFN-γ表达水平显著上调; 攻毒试验表明, CotC-LMBV组鲈的存活率提高, RPS达45.0%,表明鲈的先天性和适应性免疫被激活, 以提供免疫保护作用。
鱼类病毒性神经坏死症鱼类病毒性神经坏死症, 作为世界动物卫生组织(Office International Des épizooties)必报的传染病之一, 危害多种海水和淡水鱼类, 感染后幼鱼的死亡率高达80%—100%[108]。该病的病原为神经坏死病毒(Nervous Necrosis Virus, NNV)[109], 其主要衣壳蛋白MCP是保守的, 在病毒侵袭和复制中发挥重要作用[110]。Mai等[111]构建重组芽孢CotC-MCP, 口服免疫石斑鱼(Epinephelusssp.)幼鱼, 发现CotC-MCP组肾脏中免疫相关基因TNF-α、IL-1β、MHCI、IgD和IgM的转录水平均显著提高, 在感染试验后, CotC-MCP组幼鱼相对存活率达88.89%, 对照组成活率为0, 说明展示的MCP发挥了很好的免疫保护效果。
对虾白斑综合征对虾白斑综合征是严重危害对虾(Penaeus)养殖业健康发展的病毒性疾病之一, 会引起对虾暴发性死亡, 该病病原为白斑综合征病毒(White Spot Syndrome Virus, WSSV), 属线头病毒科(Nimaviridae), 白斑病毒属(Whispovirus)[112]。VP26和VP28蛋白是WSSV两种最主要的囊膜蛋白,约占囊膜蛋白的60%[113]。
Ning等[114]构建重组芽孢CotB-VP28和CotCVP28, 口服免疫克氏原螯虾(Procambarus clarkii)后, 进行感染试验, 发现重组芽孢组克氏原螯虾的存活率均提高, RPS分别为37.9%和44.8%。这是首次在水生无脊椎动物中使用芽孢表面展示系统, 所展示的抗原都有免疫保护效果, 但免疫保护效果的高低与锚定蛋白的选择相关。而后Nguyen等[115]构建重组芽孢CotB-VP28, 口服免疫南美白对虾(Litopenaeus vannamei)后, 发现CotB-VP28组超氧化物歧化酶和酚氧化酶活性均有增加的趋势, 表明对虾的先天免疫反应在一定程度上被激发。Pham等[116]也构建重组芽孢CotB-VP28, 口服免疫斑节对虾(Penaeus monodon), 发现CotB-VP28诱导血液中产生更多的总血细胞、透明细胞和颗粒细胞, 以及血清中更高的酚氧化酶活性(1.26倍); 在病毒感染后,CotB-VP28组对虾存活率达75%, 表现出更强的免疫保护效果。此外, Valdez等[93]构建了重组芽孢CotC-VP26和CotC-VP28, 口服免疫南美白对虾, 感染试验发现CotC-VP26和CotC-VP28芽孢可保护100%和90%的幼虾免受WSSV感染, 显示VP26具有更强的免疫保护效果。
以上研究表明, 利用芽孢表面展示系统展示病毒抗原片段, 对于病毒的感染具有一定的保护效果,但保护效果低于直接注射减毒疫苗, 可能是由于目前的研究展示的病毒抗原较单一。此外, 胃肠道环境对疫苗的破坏、接种的疫苗难以突破黏膜屏障、抗原呈递细胞对芽孢表面展示抗原的识别效率低, 这些因素都会影响到疫苗的免疫保护效果。每一个病毒颗粒都有很多的不同抗原片段, 若将多个抗原蛋白通过多个锚定蛋白同时进行表面展示,并使用连接肽以减少不同抗原蛋白相互之间的干扰, 将可能提高表面展示效率, 刺激机体产生更强的免疫反应。
3.3 寄生虫病疫苗
华支睾吸虫(Clonorchis sinensis)是重要的鱼源性人畜共染寄生虫, 能够引起华支睾吸虫病, 严重危害人类和动物的健康[117,118]。华支睾吸虫的生活史包括成虫、虫卵、毛蚴、胞蚴、雷蚴、尾蚴、囊蚴及后尾蚴等阶段, 其中当尾蚴遇到合适的第二中间宿主(一些淡水鱼或虾)时, 可寄生其体内并形成囊蚴[119]。
华支睾吸虫的半胱氨酸蛋白酶(CsCP)与其孵化、营养获取、免疫逃避等密切相关[120], Tang等[121]构建重组芽孢CotC-CP, 口服免疫草鱼, 发现CotCCP组血清、胆汁、肠黏液和体表黏液中特异性IgM抗体水平显著提高, 低密度尾蚴(50尾/每尾鱼)感染试验发现CotC-CP芽孢可提供100%的保护率, 表明重组CotC-CP芽孢可预防囊蚴的形成和感染。烯醇化酶(CsENO)是华支睾吸虫行寄生生活时, 宿主与病原体相互作用的表面受体[122]。Jiang等[123]构建重组芽孢CotC-CsENO, 口服免疫草鱼, 发现CotCCsENO诱导血清、肠黏液和体表黏液中特异性IgM抗体水平提高, 脾脏、头肾和后肠中多个免疫相关基因转录水平显著上调, 表明CotC-CsENO芽孢可诱导体液免疫、细胞免疫及全身和局部的黏膜免疫, 为草鱼提供免疫保护。华支睾吸虫副肌球蛋白(CsPmy)是蠕虫类寄生虫的一种参与肌肉生理收缩和免疫调节的多功能分子[124], 也是囊蚴阶段囊壁的重要组成部分[125], Sun等[18]构建重组芽孢CotC-CsPmy, 在口服免疫草鱼后, 发现CotC-CsPmy可诱导血清、胆汁、肠黏液和体表黏液中特异性IgM抗体水平显著上调, 以及脾脏和头肾中IgM、IgZ、IL-8和TNF-α的mRNA水平显著提高, 感染试验发现, 每克鱼肉中囊蚴数量明显减少, 表明CotC-CsPmy重组芽孢可预防尾蚴粘附或入侵草鱼, 进而影响囊蚴的形成。
目前芽孢表面展示系统在寄生虫病方面的研究还局限在华支睾吸虫一种寄生虫上, 对水产养殖动物危害严重的寄生虫如小瓜虫、三代虫等, 尚未涉及。将重要寄生虫病原的抗原蛋白展示到芽孢表面, 用于预防鱼类寄生虫的感染, 将能够降低寄生虫病的发病率。
4 展望
尽管芽孢表面展示系统在水产养殖方面的应用还不是很多, 但目前在重要的细菌[96]、病毒[104]和寄生虫[18]病原中的研究已表明其作为口服疫苗抗原递送平台的优势及可行性。我国水产养殖动物品种众多, 重要病原也很多, 如嗜水气单胞菌(Aeromonas hydrophila)、鳜传染性脾肾坏死病毒(Infectious spleen and kidney necrosis virus)、桃拉综合征病毒(Taura syndrome virus)、小瓜虫(Ichthyophthirius)和三代虫(Gyrodactylus)等[126—128]。未来可针对重要病原, 利用芽孢表面展示系统开发更多的水产动物口服疫苗, 提供一种新型高效的病害防控手段。另外, 提高抗原呈递效率和免疫保护效果也是未来的研究方向之一。影响抗原的呈递效率的因素很多, 包括锚定蛋白的定位和特性、展示的抗原蛋白的性质、连接方式、表达载体的类型及连接肽的种类等[129], 都可以进行优化以提高抗原呈递效率。也可以利用多个不同的锚定蛋白, 在芽孢衣壳表面展示多种不同的抗原, 制备多价重组抗原疫苗。可以通过优化免疫时间、免疫次数和免疫接种量[130], 以及优化抗原片段(寻找高特异性和高敏感性的抗原)等方法提高免疫保护。目前所使用的宿主菌多数为工程菌株, 虽然遗传操作容易,但水生动物消化道环境未必适合其定植, 会影响免疫保护效果, 因此发掘更多水产动物来源的益生芽孢杆菌[87], 构建重组芽孢, 表面展示重要病原的抗原片段, 不但能提供免疫保护, 还可以发挥益生菌的作用。有效的口服疫苗除了在递送部位提供黏膜局部免疫, 还应该诱导全身系统免疫。深入研究表面展示口服疫苗进入水产养殖动物消化道后发挥作用的机制, 开发高效安全的口服疫苗对预防鱼病的发生, 减少化学药物的使用, 促进我国水产养殖行业的绿色健康发展非常必要。

