术中静脉注射不同剂量的艾司氯胺酮对乳腺癌患者术后焦虑、抑郁的影响
季 涛 刘 苏 苏高伟 吴南玲 王瑶琳 陈秀侠
乳腺癌已成为位居全球发生率第1位的癌症[1]。研究表明,大约40%的乳腺癌患者围术期存在焦虑或抑郁,处理不当会增加患者术后不良反应的发生率,降低患者免疫功能,延长住院时间[2~5]。早期干预,减轻患者的焦虑抑郁情绪,有利于减少患者术后并发症的发生。艾司氯胺酮作为氯胺酮的右旋异构体,因其较氯胺酮效价更高,不良反应更少而越来越多的用于抗抑郁治疗[6, 7]。迄今为止,尚鲜有研究报道艾司氯胺酮在乳腺癌患者术后焦虑治疗中的应用。本研究通过在乳腺改良根治术中应用不同剂量艾司氯胺酮,观察其改善患者术后焦虑抑郁的效果,探索最佳治疗剂量。
资料与方法
1.一般资料:本研究经徐州医科大学附属医院医学伦理学委员会批准(伦理学审批号:XYFY2022-KL066-01),在中国临床试验中心注册(ChiCTR2100051169)。所有患者或家属均于术前签署知情同意书。选择徐州医科大学附属医院2022年2~11月择期全身麻醉下行乳腺癌改良根治术患者96例,患者年龄18~60岁,ASA分级Ⅰ~Ⅱ级,术前无睡眠障碍且签署知情同意书并愿意接受随访者。排除标准:①术前存在明显的心脏、肺、肝脏、肾脏功能异常者及凝血功能异常者;②既往青光眼病史患者;③存在语言理解障碍、精神疾病等不能配合的患者;④既往长时间服用抗抑郁药亦或者是镇静药者;⑤未经治疗或治疗不足的甲状腺功能亢进患者;⑥艾司氯胺酮禁忌证患者(动脉硬化、冠心病、心功能不全、肺心病、肺动脉高压);⑦既往乳腺手术史。剔除标准:①患者术中出现严重不良反应如术中大出血等;②手术时长≥3h;③在随访过程中接受其他临床试验。
2.麻醉方法:按随机原则将患者分为艾司氯胺酮L组(0.15mg/kg)、M组(0.30mg/kg)、H组(0.50mg/kg)和C组(生理盐水组),每组各24例,根据患者体重抽取药物稀释成10ml,对照组给予等量的0.9%氯化钠溶液。所有患者术前禁水、禁食,入室后监测生命体征、开放静脉通路。预充氧后静脉依次注射咪达唑仑0.05mg/kg、依托咪酯0.3mg/kg、舒芬太尼0.5μg/kg、罗库溴铵0.6~1.0mg/kg,L组静脉注射0.15mg/kg艾司氯胺酮;M组静脉注射0.30mg/kg艾司氯胺酮;H组静脉注射0.50mg/kg艾司氯胺酮;C组静脉注射等量0.9%氯化钠溶液。2~3min后喉罩置入行机械通气。静脉泵注丙泊酚2~5mg/(kg·h)、瑞芬太尼0.1~0.3μg/(kg·min)、吸入七氟烷浓度1%~2%使BIS维持在40~60之间。术中维持血压和心率为在基础值±20%,依据需要使用血管活性药物。术毕前30min停七氟烷吸入,手术结束时停用其他维持药。术毕转入麻醉后监测治疗室(postanesthesia care unit,PACU),待患者完全苏醒达到拔管指征后拔除喉罩,达到出PACU标准时送回病房。
3.观察指标:术前记录患者一般资料(性别、年龄、BMI、ASA分级、病史等),记录患者术前1天(D1)、术后1天(D2)、术后3天(D3)、术后5天(D4)、术后7天(D5)的状态焦虑量表(state anxiety scale,SAI)评分、蒙哥马利抑郁量表(montgomery depression scale,MADRS)评分;记录术中患者瑞芬太尼使用量、去氧肾上腺素使用量、手术时长、手术结束至拔管时间;记录PACU停留时间、术后谵妄、恶心、呕吐、头晕、嗜睡以及病房镇痛补救情况。
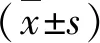
结 果
1.4组患者一般资料比较:4组患者年龄、体重指数(body mass index,BMI)、ASA分级、高血压、糖尿病比较,差异无统计学意义(P>0.05, 表1)。
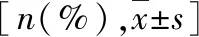
表1 4组患者一般资料比较
2.4组患者临床特征资料的比较: 4组患者手术时间、拔管时间、去氧肾上腺素用量及在PACU的停留时间比较,差异无统计学意义(P>0.05)。H组瑞芬太尼用量较其他3组减少(P<0.05,表2)。

表2 4组患者临床特征资料比较
3.4组患者不同时间点各项指标的比较:D1、D2、D4、D5时各组SAI评分差异无统计学意义;D3时,H组较其他3组有更低的SAI评分(P<0.05);与D1时比较,C组、L组、M组的D4、D5时SAI评分明显下降(P<0.05);H组D3、D4、D5时SAI评分下降(P<0.05);D3、D4时H组MADRS评分较另外3组降低(P<0.05);与D1时比较各组的MADRS评分随着时间的延长逐渐下降(P<0.05),差异有统计学意义(表3)。

表3 4组患者不同时间点各指标评分比较分)
4.4组患者术后不良反应发生率比较:4组患者术后谵妄、恶心、呕吐、补救镇痛、头晕嗜睡、发热等不良反应发生率比较,差异无统计学意义(P>0.05,表4)。
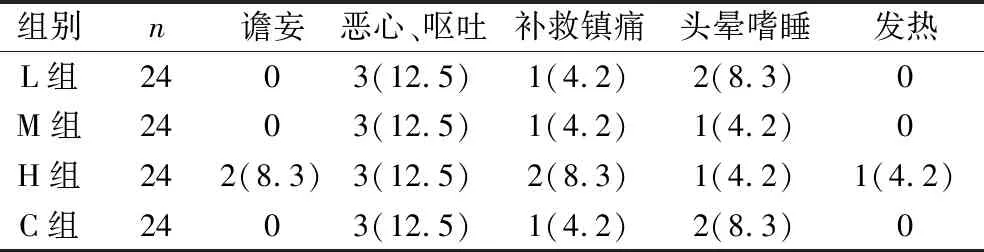
表4 4组患者术后不良反应发生率[n(%)]
讨 论
目前关于术后焦虑、抑郁的治疗主要包括药物治疗及行为认知疗法。药物疗法往往具有恶心、呕吐、食欲改变等不良反应,有时甚至造成呼吸、循环抑制以及耐药性的增加[8]。行为认知疗法具体疗效不够确切,只能作为乳腺癌患者术后焦虑的辅助治疗。研究发现艾司氯胺酮主要通过阻断NMDA受体通道,参与突触传递及可塑性信号的调控,补充因焦虑、抑郁消耗的突触数量从而达到快速的抗焦虑、抑郁作用[9,10]。
Falk等[11]回顾性研究发现晚期癌症患者的姑息治疗中单次静脉注射艾司氯胺酮可有效改善患者的焦虑抑郁,且以缓解焦虑为主。本研究发现,H组患者在术后第3天时较其他各组有更低的SAI评分(P<0.05),此外与D1时比较,C组、L组、M组在D4、D5时SAI评分明显下降(P<0.05),而H组在D3、D4、D5时SAI评分下降(P<0.05),表明H组在术后第3天时SAI评分就较术前开始下降,而C组、L组以及M组在术后第5天才开始下降。
Franz 等[12]给予难治性抑郁症患者0.2~0.4mg/kg艾司氯胺酮静滴后2h,患者抑郁症状缓解,并持续到术后3天。另有研究显示艾司氯胺酮的抗抑郁作用可持续1周甚至1个月[13,14]。随访了术后患者第1天、第3天、第5天以及第7天的抑郁评分,发现H组的患者,术后第3天和第5天时较其他3组具有更低的抑郁评分,说明0.5mg/kg艾司氯胺酮可以改善患者术后早期的抑郁症状。但在本研究中,术后1周时各组的抑郁评分比较,差异无统计学意义(P>0.05),这与既往研究结果相似[15]。但这并不能排除围术期使用艾司氯胺酮治疗术后抑郁的可能性。随着时间的推移,即使不加干预,患者的抑郁心理也会逐渐减轻,其次乳腺癌患者随着术后放化疗的进行,也有可能导致后期观察到的艾司氯胺酮的抗抑郁作用减弱。
本研究发现,4组患者手术时长、拔管时长、PACU滞留时间以及术中血管活性药物的使用情况无差异,这与王雪力等[16]研究结果不同,可能与乳腺改良根治术相较于其他手术较为简短,麻醉药物很少有蓄积有关。此外本研究发现,0.5mg/kg艾司氯胺酮有助于减少术中阿片类药物的使用,更有助于患者术后苏醒。近年来研究表明,疼痛和抑郁密切相关[17]。疼痛会改变海马体和前额叶皮质的突触连接,以及改变来自腹侧被盖区域的多巴胺信号,从而引起抑郁。本研究发现H组的艾司氯胺酮虽然能改善患者术后抑郁,但相较于其他组并未较少术后的镇痛补救的次数,这有可能与本研究的样本量较小以及乳腺改良根治术手术创伤较小有关。
既往研究显示,术中静注一定剂量的艾司氯胺酮可能会增加术后恶心、呕吐的发生率,但临床作用值得商榷,因为不同类型的手术由于刺激的不同,以及需要维持的腹内压不同,术后恶心、呕吐的发生率也不同。本研究发现,术中静注艾司氯胺酮与对照组比较并不能增加术后恶心、呕吐、谵妄、头晕、发热等不良反应的发生率,这可能与术中较少的阿片药物使用有关。
艾司氯胺酮静脉注射的生物利用度为100%,临床上常用的艾司氯胺酮静脉注射方案是在麻醉诱导前或切皮前静脉注射艾斯氯胺酮0.5~1.0mg/kg,麻醉维持0.5~3.0mg/(kg·h)[18]。既往多项研究证实该方案可以安全地应用于临床,未出现严重的中枢神经系统和心血管损害事件,因此本研究中的艾司氯胺酮使用剂量被认为是安全的。本研究存在一定的局限性:①只评估了术后1周焦虑、抑郁情况,未能随访更长时间;②未对患者的术前焦虑、抑郁严重程度进行分层分析;③本研究作为一个单中心的试验,临床证据可能较弱,因此本研究所得到的结论还需要开展更大样本量、多中心、前瞻性的研究予以进一步证实。
综上所述,术中静脉注射0.5mg/kg艾司氯胺酮可以更加安全、有效地应用于乳腺改良根治术的患者,减轻患者术后早期的焦虑、抑郁,减少围术期阿片类药物使用,且不增加术后不良反应的发生率。

