依赖于端粒延长替代机制的胶质瘤临床前模型及应用现状*
仝津恺 闫思翔 张艳多 侯凯龙 张科 张昊楠 常顺 贾舒婷**
(1)昆明理工大学医学院衰老与肿瘤分子遗传学实验室,昆明 650500;2)云南省第一人民医院神经外科,昆明 650032)
胶质瘤主要起源于神经胶质细胞,有部分来源于神经干细胞,是中枢神经系统最常见的恶性肿瘤,发病率约占中枢神经系统恶性肿瘤的80%,恶性胶质瘤5年死亡率仅次于肺癌和胰腺癌[1]。2021年WHO中枢神经系统肿瘤分类中根据不同组织的表型及基因型将中枢神经系统分为1、2、3、4级,其中1、2级属于低级别胶质瘤,3、4级属于高级别胶质瘤,不同胶质瘤的正确分级和分类不仅取决于他们的组织学特征,还取决于分子特征,如一些基因(IDH1、ATRX、TP53、CDK2A、BRAF、FGFR1和PDGFRA)的改变和甲基化特征[2]。高级别胶质瘤生长较快、浸润性强且预后较差,3级胶质瘤的中位总生存期(overall survival,OS)约为3年,而4级胶质瘤,尤其是胶质母细胞瘤(glioblastoma,GBM),仅为15个月,且只有0.05%~4.7%的患者在诊断后存活5年[3]。目前胶质瘤的治疗手段还比较单一,仍然是手术切除后辅以放化疗的综合治疗,尽管这些治疗手段可以一定程度上改善胶质瘤患者的生存时间和生存质量,但其OS时间仍然很短。事实上,胶质瘤患者的低生存率部分归咎于胶质瘤细胞侵袭性生长以及与周围正常脑组织交错,因而手术难以完全切除,同时由于其异常的生物学特性,对放疗和化疗的耐受,导致术后放化疗失败,而且经常以同级别或高级别复发。因此,新的治疗方法和新的治疗药物的开发对于胶质瘤的治疗十分必要。
端粒长度的维持对于肿瘤细胞的生存起着至关重要的作用,大多数肿瘤细胞会通过激活端粒酶活性延长端粒长度[4-5]。端粒酶是一种逆转录酶,以其自身RNA作为模板在DNA前导链的3'端添加端粒序列使端粒延长[6-8]。然而,大约10%~15%的人类肿瘤并不是通过激活端粒酶去维持或延长端粒长度,而是通过端粒延长替代机制(alternative lengthening of telomeres,ALT)去延长端粒[9-10]。目前对ALT机制的了解仍不明确,人们普遍认为ALT是依赖于端粒序列特异性的同源重组(homologous recombination,HR)机制延长端粒[11]。已有研究表明,ALT途径的激活通常与几种典型的表型有关,包括高度异质性的端粒长度,端粒姐妹染色单体交换(telomere sister chromatid exchange,T-SCE),丰富的染色体外端粒重复序列(extrachromosomal telomeric repeats,ECTRs)以及出现ALT途径相关的早幼粒细胞白血病小体(ALT-associated PML bodies,APBs)[10]。在很多类型的肿瘤中,都可以观察到ALT的存在,其中骨肉瘤和胶质瘤中ALT的发生率相比于其他癌症类型更高。尤其在胶质瘤中,ALT的发生率约占30%,其中弥漫型星形胶质瘤ALT发生率为55%,少突星形细胞瘤ALT发生率为60%,间变性星形细胞瘤ALT的发生率更是高达65%[12]。越来越多的研究发现,ALT胶质瘤的发生和维持与某些基因的功能异常有关,如:IDH1突变、ATRX缺失、p53突变等,提示这些基因可以成为ALT胶质瘤治疗的靶点[13-14](图1)。而最近的一些关于ALT胶质瘤靶向治疗的研究通过体内或体外的实验证明了这些靶点的有效性。因此本文通过综述ALT胶质瘤的细胞及动物模型的研究进展,为靶向ALT胶质瘤的研究提供可以参考的资料。
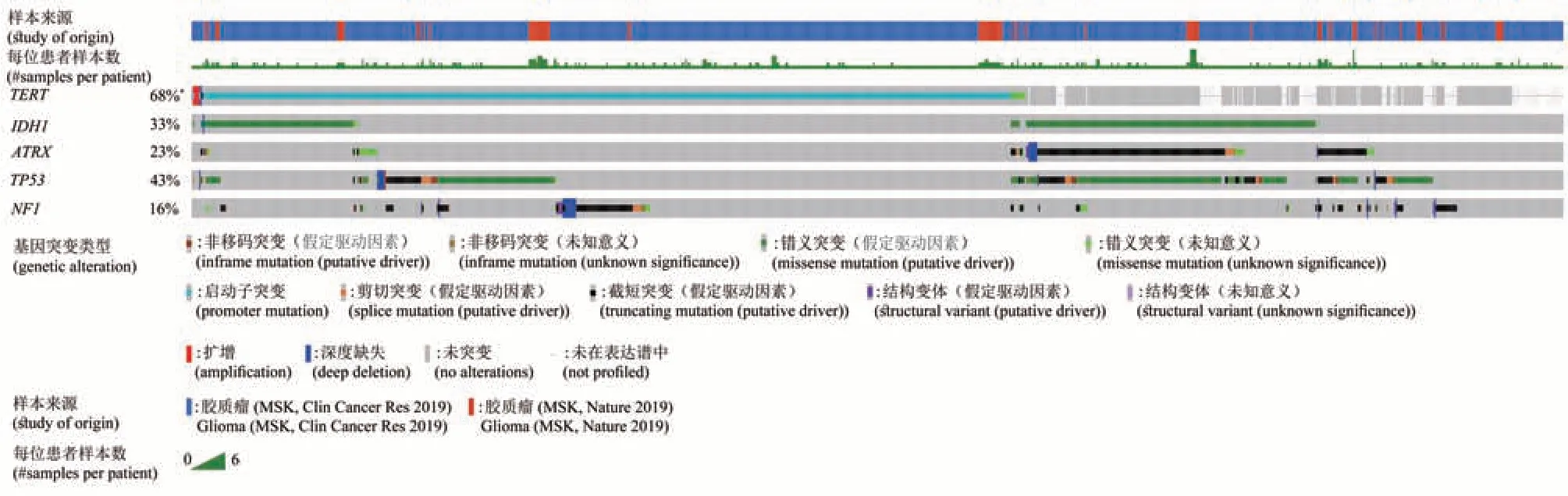
Fig.1 ATRX mutation was highly correlated with IDH1 mutation and was more common in gliomas without telomerase reverse transcriptase(TERT) activation图1 对不同胶质瘤患者的基因分析,ATRX突变和IDH1突变高度相关且常见于端粒酶逆转录酶没有激活的胶质瘤患者
1 ALT胶质瘤细胞系模型研究进展
ALT胶质瘤的细胞系模型的建立对于移植瘤模型或者胶质瘤靶点以及药物筛选都有着十分重要的作用。目前已经有多篇报道描述了ALT胶质瘤细胞系的建立过程以及通过这些细胞系模型进行后续的药物筛选或者做一些移植瘤模型(表1)。

Table 1 ALT glioma cell line表1 ALT胶质瘤细胞系
由于ALT胶质瘤的发生率较低且体外培养较困难,直到2015年,Jeitany等[15]首次从ALT胶质瘤中分离出TG20细胞。他们证明了TG20具有胶质瘤干细胞的所有特征,包括神经干细胞标志物的表达,在NOD-SCID-IL2Rc(NSG)小鼠和裸鼠模型体内均可以产生脑内肿瘤,且ALT表型稳定。TG20细胞以及用其构建的小鼠模型是一种有效的ALT胶质母细胞瘤的临床前模型,对开发针对ALT机制的抗癌策略起着十分积极的作用。作者进一步通过该模型证明了G4体稳定剂360B是治疗ALT肿瘤的潜在药物。此外Jeitany等[16]以TG20为模型开展了ALT相关机制的研究,发现P300/CBP相关因子(PCAF)的下调使ALT细胞的T-SCE的频率降低,而与PCAF同源的赖氨酸乙酰转移酶GCN5(general control non-derepressible 5)的下调则会使ALT细胞的T-SCE频率升高,提示GCN5和PCAF在调控ALT细胞端粒重组中相反的作用。他们还进一步证明了组蛋白乙酰转移酶抑制剂漆树酸(anacardic acid,AA)会抑制ALT细胞中APBs和T-SCE的水平,促进ALT细胞死亡。而且与端粒酶阳性肿瘤细胞相比,AA特异性地使人ALT肿瘤细胞对辐射敏感,这可能是由于AA降低了ALT细胞的活性导致的,提示赖氨酸乙酰转移酶可能是ALT胶质瘤治疗的新靶点[17]。
随着对ALT机制研究的不断深入,目前已有研究揭示了ALT胶质瘤的产生与一些基因的突变有关,如:ATRX缺失、IDH1突变、p53突变等[14]。因此,许多实验室通过在胶质瘤细胞系中敲除这些基因得到了具有ALT表型的胶质瘤细胞系,并通过这些细胞系进行了一些靶向药物筛选的工作。
Brosnan-Cashman团队[13]和Li团队[18]分别于2018年和2019年通过在胶质瘤细胞系中对ATRX基因进行基因敲除,成功在胶质瘤细胞系中诱导出ALT表型。其中,Brosnan-Cashman等[13]分别在4个端粒酶阳性人胶质瘤细胞系Mogg-UVW、SF188、U-251和UW479中进行了ATRX基因敲除。其中U-251和UW479显示出ALT阳性细胞的多种特征,包括超亮的端粒DNA信号、ALT相关的PML小体和C环。然而,Mogg-UVW和SF188细胞系在对ATRX基因进行基因敲除后没有出现ALT表型,提示除了ATRX缺失外,其他基因组或表观遗传学事件对于肿瘤细胞中ALT机制的诱导也是必要的。同样,Li等[18]通过CRISPR/Cas9在端粒酶阳性的人脑星形胶质母细胞瘤细胞U87中对ATRX基因进行基因敲除后也诱导出了ALT的表型。进一步的机制研究表明,ATRX和DAXX的基因敲除造成了端粒处的损伤及复制压力,进一步促进了ALT表型的出现,表现为APBs和C环的水平上升,激活了ALT相关的DNA修复。但是,这种ATRX和DAXX的缺失引起的ALT相关的DNA修复并不会迅速出现,在作者的研究中提示,ATRX的缺失导致H3.3组蛋白无法正常沉积于端粒上,造成了端粒处的复制压力,而U87细胞本身的端粒酶活性并不足以克服ATRX缺失相关的端粒功能障碍,表现出了生长活性降低的现象,迫使ATRX缺陷细胞在生长过程中不得不采用基于同源重组的ALT途径作为替代的端粒维持机制。对这些新的ALT胶质瘤细胞系进行研究和实验,将进一步加深对ALT分子机制的理解,有助于为ALT阳性肿瘤的治疗开拓新的抗癌疗法。
之后,有研究人员在ATRX基因敲除或突变的基础上进一步将其他与ALT胶质瘤高度相关的基因,如IDH1和p53同时突变,成功在胶质瘤细胞系中诱导出ALT的表型,进一步锁定了诱导ALT胶质瘤发生的必需基因。Mukherjee等[14]为了证明IDH1突变和ATRX丢失可能以某种方式协同作用,有效地解决端粒酶逆转录酶(telomerase reverse transcriptase,TERT)缺陷细胞的端粒功能障碍,并促进胶质瘤的形成。他们通过在TERT阴性的人星形胶质细胞中引入病毒蛋白E6和E7,使其p53和pRB功能丧失,然后通过CRISPR系统对ATRX进行基因敲除后过表达IDH1突变体,以此成功的诱导出了ALT表型。利用这个系统,作者发现IDH1突变会介导RAP1下调,RAP1作为端粒保护蛋白之一,已经被证明会抑制HR的发生[19],其下调促进了功能失调的端粒处启动DNA损伤反应。同时IDH1突变也下调了XRCC1的表达,XRCC1是aNHEJ途径的关键组成部分[20]。因此,突变的IDH1介导的RAP1和XRCC1的下调会导致细胞不通过aNHEJ途径修复功能失调的端粒,而是更依赖于HR等途径,从而促进ALT的发生[14]。这些发现有利于对ALT胶质瘤的发生有进一步的认识,同时对ALT胶质瘤的治疗也有很重要的指导意义。
综上所述,以上实验室通过肿瘤原代细胞培养或基因编辑的方法,成功建立了一些ALT胶质瘤细胞系临床前模型,一定程度上反应了ALT胶质瘤的生理和病理情况。ALT胶质瘤细胞系临床前模型的建立为临床前针对ALT胶质瘤的药物和新疗法的开发具有十分重要的作用。
2 ALT胶质瘤小鼠临床前模型研究进展
尽管体外的细胞模型研究提供了许多显著的益处,但它们具有一个主要的缺点,即无法模拟药物如何与复杂器官中存在的所有分子相互作用。而体内研究能够解决体外研究的局限性,它能够证明药物对个体的影响,可以更好地体现出药物在机体中和器官或者其他体内途径的相互作用,从而改善药物在临床使用前安全性、毒性和功效的测试。这有助于研究者对于人类疾病靶向药物的研发。在胶质瘤的临床前抗肿瘤治疗效果的研究中,使用的主要是动物异种移植瘤模型。
然而在近十年的研究过程中,才逐渐出现了ALT相关的胶质瘤小鼠模型,目前主要的方法是将临床上获得的病人来源的ALT胶质瘤细胞系或者将现有的胶质瘤细胞系诱导为ALT细胞后,通过原位或异位的方法注射到SCID小鼠或裸鼠体内,从而建立异种移植模型用于临床前靶向药物作用研究。Jeitany等[15]为了证明TG20细胞具有胶质瘤干细胞的所有特征,在NOD-SCID-IL2Rc(NSG)小鼠和裸鼠模型中用TG20细胞在脑内进行了原位移植,成功在动物模型中形成了可以连续移植的脑肿瘤。并且进一步在动物模型水平上验证G4体稳定剂360B对ALT胶质瘤的抑制作用。2014年Wakimoto等[24]将20例来自临床的IDH1突变的胶质瘤切除的肿瘤标本植入免疫力低下的小鼠脑内,成瘤后进行体外培养,获得了一些细胞系,这些细胞系在组织学上都与亲本肿瘤表型十分相似。其中MGG119在体外培养后成为了可以稳定传代的细胞系。虽然Wakimoto等当时并没有讨论关于MGG119是否是ALT胶质瘤,但在后续其他研究中,对MGG119进行了关于ALT表型的检测,确定了这株细胞具有ALT细胞系的特征[14]。除了ATRX、IDH1等基因和ALT的发生高度相关,其他一些基因,比如NF1和ALT的发生同样关系密切。最近发现,在NF1相关肿瘤尤其是星形细胞肿瘤,ALT发生的机率比较大,且常常伴随着ATRX突变和NF1突变[25-26]。Yuan等[22]在2022年,利用患者来源的NF1缺陷和ATRX突变的ALT神经胶质母细胞瘤细胞在裸鼠上的异种移植模型,证明了ATRi(ATR inhibitor)具有特异性抑制NF1缺陷细胞的能力ALT细胞系的能力。
虽然异种移植为颅内肿瘤的研究提供了许多优点:重复性好,生长速度标准化,死亡时间和肿瘤定位方便。然而,由于用于植入的人工、侵入性手术方法以及准确复制人类胶质瘤的组织学特征的能力有限,这些模型具有花费的时间较长,成本较高,移植成功率不确定,很难完整的复制患者数据等局限性[27]。而转基因自发脑胶质瘤动物模型的出现在一定程度上解决了上述的问题。近几年来,虽然还没有成功构建自发ALT胶质瘤动物模型的报道,然而通过在动物水平上进行与ALT相关的基因的编辑,一些动物模型表现出较高水平的胶质瘤形成几率,提示该模型具有自发形成ALT胶质瘤的潜能。
在2016年,Koschmann等[28]通过睡美人转座酶系统(Sleeping Beauty(SB)Transposase System)建立了ATRX基因缺陷小鼠,这种小鼠会在出生一定时间后出现自发的胶质瘤,揭示了ATRX缺失对胶质瘤肿瘤增殖的影响。这种小鼠模型可以很大程度地模拟人体自发形成肿瘤的过程,这一成果也为深入了解ATRX突变在人脑胶质瘤中的作用提供了依据。有研究已经提示了NF1与ALT星形细胞肿瘤发生高度相关,而2021年,Pan等[29]使用的由神经纤维瘤病1肿瘤抑制基因(NF1)5突变驱动的视神经胶质瘤(optic pathway gliomas,OPG)的小鼠模型,证明了刺激视神经活动会促进视神经胶质瘤的生长,以及通过光剥夺减少视觉体验可以防止肿瘤的形成和维持。这种NF1基因敲除的小鼠模型表现出胶质瘤高发的特性,虽然还没有NF1小鼠确实是自发ALT肿瘤模型的报道,但他有望成为一种新型的自发ALT肿瘤小鼠模型。
3 总结与展望
由于ALT的发生机制目前还不明确,因此靶向ALT肿瘤药物的研究较少。而在这些研究中,有相当一部分研究都是通过上述的ALT胶质瘤细胞模型或动物移植瘤模型完成的。如前文中提到的G4体稳定剂360B以及组蛋白乙酰转移酶抑制剂AA都是基于TG20细胞模型发现的具有靶向ALT活性的药物。而ATR抑制剂VE-822、AZD6738和VE-821以及PARP抑制剂Olaparib、Talazoparib、Niraparib等都被证明在ALT胶质瘤或者ALT胶质瘤小鼠模型体内具有较好的杀伤作用[22,30-31]。虽然目前ALT胶质瘤的临床前模型较少,但是已经建立的这些ALT细胞模型和小鼠模型已经在药物筛选等方面发挥了重要作用,尤其是原代培养的胶质瘤细胞系,能很好地反映胶质瘤在体内的生长状态,获得的数据也更加准确真实。ALT胶质瘤动物模型能更好地反映人类肿瘤的遗传、形态和免疫学特征。本实验室近几年通过ALT相关机制的研究,也有望在自发ALT胶质瘤小鼠模型的建立上取得突破。这些胶质瘤小鼠模型的建立将为更详细的研究胶质瘤的发生过程和更准确地评估治疗的安全性及有效性提供了有利的条件。

