光催化材料石墨相氮化碳的合成、改性及应用
杨文科, 卢连雪, 李 鹏, 张 健, 胡绍争
(1. 辽宁石油化工大学 石油化工学院,辽宁 抚顺 113001; 2. 辽阳石化公司研究院,辽宁 辽阳 111003)
当今社会在快速发展的同时伴随着能源短缺、环境污染等危机,这些危机对人类社会构成了严重威胁[1]。因此,开发低成本、无污染、可再生的新能源对经济的长远发展与可持续发展具有重要意义。
太阳能是随处可取、方便转化的清洁能源,运用半导体催化技术可以吸收太阳光并将其转化为其他能量加以利用或存储,转化效率的高低与所采用的光催化剂有关[2-3]。石墨相氮化碳(g-C3N4)是一种有机非金属半导体光催化剂,因成本低、物化性质稳定、可见光响应能力强等优势在光催化领域颇受欢迎。2009 年,王心晨课题组报道了g-C3N4半导体材料,该材料表现出优越的可见光催化析氢性能[4],这一重大成果的发现使有机半导体光催化研究开始蓬勃发展。
本文对近年来g-C3N4基光催化材料的合成方法、改性策略及应用进行了综述,着重总结了光催化材料g-C3N4在废水处理降解污染物、产H2与产H2O2等领域的优异成果,最后对g-C3N4的发展趋势进行了展望。
1 g-C3N4的制备方法
g-C3N4的制备方法主要有物理法和化学法两大类。物理法一般用于制取g-C3N4薄膜或大量粉末,有离子注入、机械球磨等方法。目前,绝大多数g-C3N4的制备主要是通过化学法来获取,包括溶剂热法、电化学沉积法、固相反应法、热缩聚合成法等[5]。g-C3N4合成方法的优缺点如表1 所示。g-C3N4的结构示意图如图1 所示。

图1 g-C3N4的结构示意图Fig.1 Structure diagram of g-C3N4

表1 g-C3N4合成方法的优缺点Table 1 The advantages and disadvantages of g-C3N4 synthesis methods
1.1 溶剂热法
溶剂热法是将碳氮化物作为前驱体,同时在反应容器内加入一定量的溶剂,在特定条件下反应制备g-C3N4的方法。L.JIA 等[6]以水杨酸为溶剂,使其与三聚氰胺在高温下反应后继续煅烧,制得了纳米管状g-C3N4。结果表明,水杨酸及其分解产物抑制了g-C3N4晶体的生长。Y.J.CUI 等[7]以三聚氯胺和三聚氰酰氯为前驱体、乙腈为溶剂,成功制备了一种对氯苯酚有降解能力的棒状纳米g-C3N4。
1.2 电化学沉积法
电化学沉积法是制备g-C3N4薄膜的常用方法。C.LI 等[8]在室温条件下,将氰尿酰氯和六羟甲基三聚氰胺混合制成饱和乙腈溶液,在电流作用下,使饱和乙腈溶液在底部慢慢沉积形成一层g-C3N4薄膜。结果表明,氰尿酰氯和六羟甲基三聚氰胺的物质的量比影响所制备催化剂的组成、C 和N 的化学键态及晶体结构的形成。
1.3 固相反应法
固相反应法通常是在高温高压条件下进行,通过含有三嗪结构单元的化合物与含氮化合物的化学反应合成g-C3N4。Z.ZHANG 等[10]以三聚氰胺和三聚氰氯为前驱体,在1.0~1.5 GPa、500~550 ℃的条件下进行固相反应,最终得到了具有二维C6N9H3结构及C3N3空隙的有序排列的催化剂。其结构中有许多较大的空隙被氯离子占据,在框架上氯离子的数量与氮原子的数量相等,为了实现电荷平衡氮原子被质子化。
1.4 热缩聚合成法
热缩聚合成法是近年来制备g-C3N4的最常用方法。该方法所使用的原料大多为三聚氰胺、尿素。姜鹏程等[12]以三聚氰胺为原料,分别在空气与氩气两种不同气氛下制备了薄片状g-C3N4。图2 为氩气气氛下三聚氰胺经不同温度热处理后产物的SEM 图。

图2 氩气气氛下三聚氰胺经不同温度热处理后产物的SEM 图Fig.2 SEM images of pyrolysis products of melamine as-calcined at different temperatures in an argon atmosphere
由图2 可以看出,经500 ℃热处理后片层状产物最有序,热处理温度升高后堆积厚度降低;经700 ℃热处理后产物结构单元已有所断裂。综上可知,与氧气气氛下相比,氩气气氛下制得的g-C3N4表面较光滑,堆积程度与稳定性更好。
1.5 微波辅助加热法
微波辅助加热法合成g-C3N4的基本原理和热缩聚合成法类似,都是通过加热升温促使有机物的分解与聚合。在微波辐射下,前驱体内部的偶极子在电磁场中被打散形成新的排列顺序,并通过内摩擦作用以相同的交替往复移动速度随电场的变化而快速变化[14]。
2 g-C3N4的改性方法
g-C3N4虽然在光催化转化利用太阳能领域有广泛的应用价值,但受比表面积小、光生载流子分离能力弱等因素的限制而不能最大限度地发挥光催化性能。针对这些不足,研究者们提出通过元素掺杂、贵金属沉积、形貌调控、半导体复合[15]等多种改性策略来提高其光催化能力,以便发挥更大的应用价值。
2.1 元素掺杂
利用元素掺杂对g-C3N4改性的方法最常见,其原理是将某种有独特性能的元素掺入g-C3N4晶格中并取代部分C 或N 元素,从而改变g-C3N4本身的能带结构[16]。该方法可掺入非金属元素或金属元素,也可将两种或两种以上的不同元素同时引入催化剂中。
2.1.1 非金属元素掺杂
常用于对g-C3N4进行掺杂修饰的非金属元素包括I、S、O 和卤化物等。图3 为B 掺杂g-C3N4载流子转移机理示意图。

图3 B 掺杂g-C3N4载流子转移机理示意图Fig.3 Carrier transfer mechanism of B-doped g-C3N4
非金属掺杂可使g-C3N4共轭体系内电子运动范围变化更灵活,从而光生电子能够更快、更高效地分离、迁移;与此同时,g-C3N4的带隙宽度也会随之减小,可见光吸收范围增大,从而提升g-C3N4的光催化性能[17]。
G.LIU 等[18]首次在H2S 气氛下处理纯g-C3N4粉末,制备了S 掺杂的g-C3N4。结果表明,S 原子均匀分散并取代部分晶格氮,形成了新的电子结构,同时禁带宽度变窄;掺杂S 的g-C3N4在波长为300、420 nm 下的析氢活性均提高了8.0 倍左右。S.C.YAN 等[19]以三聚氰胺和氧化硼为前驱体,将其在高温高压下混合加热,制备了掺杂B 的g-C3N4。结果表明,掺杂B 后,催化剂对罗丹明B(RhB)的光催化降解性能提高了3.6 倍。
2.1.2 金属元素掺杂
K+、Fe2+、Co2+、Cu+、Zn2+和Ag+等金属离子是有效的电子受体,将其掺入g-C3N4晶体结构中时,因金属离子本身的特性会形成独特的电子结构,原有的能带结构发生改变,电子-空穴对的分离效率得到提升[20]。
张仰全等[21]以盐酸胍和Zr(NO3)4·5H2O 为前驱体,制备了引入Zr 元素的Zr/g-C3N4复合光催化剂。结果表明,引入Zr 元素后,因Zr 本身良好的能带结构和导电能力,复合催化剂的可见光吸收范围增大,电子迁移速率加快,光生电子空穴对快速分离。图4 为g-C3N4和Zr/g-C3N4的质量对光催化降解RhB 的影响。由图4 可知,当降解时间为60 min 时,3 种不同质量的Zr/g-C3N4均表现出超过99%的降解率。X.Y.CHANG 等[22]以三聚氰胺和硫代乙酸钾为前驱体,通过一步热缩聚法合成了K+和氰基修饰的g-C3N4。结果表明,引入K+后增加了g-C3N4原本结构中七嗪环的离域π 键的电子云密度,使更多的电子能够被激发并快速转移。同时,对该复合催化剂进行了双酚A 的降解实验。通过密度泛函理论计算并分析得出,该复合催化剂对双酚A 的降解包括去甲基化和羟基化两种途径,大大提高了降解率。
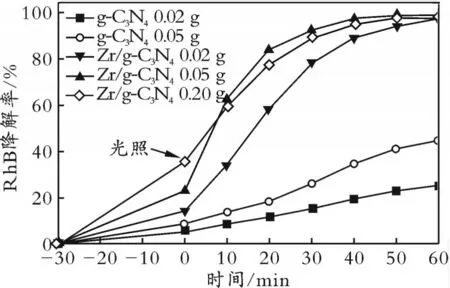
图4 g-C3N4和Zr/g-C3N4的质量对光催化降解RhB 的影响Fig.4 Effects of the mass of g-C3N4 and Zr/g-C3N4 on the photocatalytic degradation of RhB
2.1.3 共掺杂
为了克服g-C3N4的不足而掺入一种元素,很难全面提升其光催化活性,故可采用共掺杂的方式,即利用具有各种优点的多种元素合成复合催化剂,从而全面提升光催化反应活性。
马琳等[23]以双氰胺、硝酸铁和磷酸氢二铵为前驱体,成功制备了Fe-P 共掺杂的g-C3N4。结果表明,Fe 以Fe-N 的形式存在于不同结构间隙内,同时引入掺杂剂阻碍了g-C3N4的晶粒生长。彭小明等[24]制备了一种N 掺杂的原子级分散的催化剂Fe-g-C3N4。结果表明,该催化剂在活化过硫酸盐亚甲基蓝的降解实验中催化效率较高。其中,g-C3N4基体中N 与孤立Fe 原子形成的配位点Fe-Nx是降解亚甲基蓝的关键,该配位点是通过激活过一硫酸盐(PMS)产生的高价铁氧化物来实现上述降解的。Fe-g-C3N4在提升光催化活性的同时还具有优异的稳定性。
2.2 贵金属沉积
贵金属沉积修饰的基本原理有两种:一种是由于费米能级的差异,在g-C3N4和贵金属之间出现特殊的肖特基结,这种电子捕获结对光生电子空穴对的分离具有促进作用[25];另一种是利用金属的等离子共振与良好的导电性能,使贵金属与光催化剂结合,加快电子的迁移速率[26-27]。
肖开棒等[28]采用热缩聚合成法,分别以钼酸钠(MA)和四乙酰丙酮合钼(MC)为原料合成了含Mo的光催化g-C3N4复合材料。结果表明,Mo 改性后制得的催化剂具有不规则的凹凸状结构,孔隙结构更加发达,比表面积增大;以MC 为原料合成的复合光催化剂的性能提升最为显著,同时该催化剂吸收边发生红移,可为反应的进行提供更多的活性位点。
2.3 形貌调控
在一般情况下制备的g-C3N4结构常为堆积的片层块状,比表面积较小。在制备催化剂的过程中,可通过控制反应条件调控催化剂的结构。将g-C3N4结构调控为纳米结构,使其本身的物化及光学性质产生差异,也可通过调控g-C3N4氧化还原反应位点的数量、活性物种到达活性位点的运动距离来提高g-C3N4的性能[29]。将g-C3N4形状调控为纳米棒状、纳米球状,以及塔状、多孔微球状、树状等多种特殊形貌[30]。图5 为树状g-C3N4的SEM 图像、TEM图像、元素映射图像和EDS 谱图。

图5 树状g-C3N4的SEM 图像、TEM 图像、元素映射图像和EDS 谱图Fig.5 SEM images,TEM images,element mapping patterns,and EDS spectra of dendritic g-C3N4
X.H.WU 等[31]对g-C3N4进行简单的水热处理后经冷冻干燥合成了可溶性g-C3N4纳米片,该催化剂能够很好地溶于水且均匀分散在溶液中。Y.CHEN 等[32]采用热缩聚合成法,以超分子组装的方式制备了一种孔状结构多的g-C3N4复合光催化剂,其比表面积较改性前提升了8.0 倍。W.B.WANG等[33]采用气相合成法,以管状埃洛石为模板,制备了g-C3N4纳米管。结果表明,形貌调控后的纳米管孔径变大,在光催化析氢实验中表现出比纯g-C3N4高14.3 倍的析氢效率,其原因除了与增大的比表面积有关外,还与电子空穴对的低复合率有关,说明通过形貌调控不仅能调节催化剂的结构,还可以提升催化剂的电子转移能力,降低电子空穴对的复合率等性能。
2.4 半导体复合
半导体复合是指使g-C3N4与其他半导体材料结合,在不同界面构建形成异质结的方法。因异质结本身的特性,其内部的电子迁移加快,同时异质结的形成过程会增大催化剂的比表面积。常见的半导体复合材料有TiO2、SnO2、石墨烯等[34]。
J.H.GE 等[35]在高温下,以Ni3N 纳米颗粒为活性助催化剂,通过对半导体表面的改性合成了一种光催化剂。结果表明,Ni3N 纳米颗粒负载在氮化碳的表面,作为金属化合物,Ni3N 纳米颗粒与g-C3N4形成金属-半导体界面,光生电子能够从g-C3N4转移到Ni3N 纳米颗粒上。因此,将适量的Ni3N 纳米颗粒负载到g-C3N4上有利于g-C3N4光生电子-空穴对的分离,从而提高光催化活性。
3 g-C3N4的应用
3.1 在废水处理中的应用
g-C3N4优异的光催化性能使其在水污染的处理方面有很大的应用价值。在可见光照射下,g-C3N4的价带电子被激发进入导带,价带上留下带正电的空穴。光生电子可以直接消耗污染物,也可以与O2反应生成超氧化物自由基降解污染物。空穴可以直接与污染物发生氧化还原反应,也可以通过与H2O 进行反应产生·OH,通过·OH 将污染物矿化为CO2和H2O[36-37]。
废水中含有的许多重金属离子对周围环境造成影响,如果处理不当会污染水源与土壤,威胁生态安全[38]。研究表明,g-C3N4对光催化降解水中污染物具有显著影响,对灭活水体中的细菌及有害微生物有良好的处理效果[38]。王文耀等[39]以盐酸胍为前驱体,制备介孔结构的g-C3N4,并进行了亚甲基蓝的降解实验。结果表明,制备的催化剂比表面积大、表面碱性位丰富、化学稳定性良好,并且能够多次重复利用。
四环素也是废水中常见的污染物之一。殷超等[40]通过简单的热缩聚合成法和原位沉积法,在g-C3N4表面构建了BiOI 与g-C3N4质量比不同的含BiOI/g-C3N4异质结的复合催化剂。结果表明,该复合催化剂界面耦合强度高,光生电子迁移速率和光生载流子分离速度加快;当灯光照射60 min 时,在复合催化剂与过硫酸盐(PS)形成的催化体系中,质量浓度为10 mg/L 的四环素降解率接近90%。
此外,g-C3N4在降解废水中的各种色素时也能发挥很好的效果。苏荣军等[41]提出了通过g-C3N4光催化废水中常见色素的处理方案。例如,饮料、糖果中的酒石黄,以及在造纸、纺织等领域广泛应用的靛蓝胭脂红等。各种g-C3N4复合催化剂对不同色素均有非常高的降解率,甚至能够100%降解。
3.2 光催化产H2O2
H2O2被列为最重要的100 种化学品之一[42],在各行各业被广泛应用。工业上H2O2的合成主要采用蒽醌法,该方法比较简便,但能耗大,且产生有害物质。也有直接混合H2与O2制备H2O2的报道,但该方法操作难度大,且需大量的H2,这与当代绿色、节能的可持续发展理念相悖[43]。研究发现,在可见光照射下,H2O 与O2进行简单反应可生成H2O2,此方法符合安全、绿色和可持续性合成H2O2的要求[44]。文献[45]表明,改性后的g-C3N4能级发生适当变化,形成氧化还原双通道,因此可通过双通道路径生产H2O2,为H2O2光催化剂的高效制备提供了另一种理论基础。
研究者们对g-C3N4复合光催化剂产H2O2的研究已有了良好的进展,表2 归纳了多种g-C3N4复合光催化剂产H2O2的性能评价。

表2 多种g-C3N4复合光催化剂产H2O2性能评价Table 2 Performance evaluation of various composite photocatalysts g-C3N4 for H2O2 production
3.3 光催化产氢
利用光催化产H2,是解决目前能源危机问题的一种可取的办法,其面临的最主要问题是研制性能更优更高效的光催化剂。g-C3N4作为一种特别适用于光催化的非金属半导体材料,在光催化制氢领域受到诸多研究者的关注[54]。为了克服g-C3N4光催化剂的不足,可以考虑从增大比表面积、减小带隙、改善电子结构等方面提高g-C3N4复合光催化剂的析氢性能[55]。
Q.S.YANG 等[56]在微波辅助加热下,通过三聚氰胺与NH4Cl 共聚一步合成了g-C3N4纳米片。在催化剂的制备过程中,随着NH4Cl 的分解产生大量气体,从而导致g-C3N4的堆积块状之间因气体的膨胀而分离形成纳米片层状结构。与堆积块状g-C3N4相比,片层状g-C3N4有更强的光吸收能力。这种因前驱体在制备过程中发生分解而使催化剂结构发生变化的方法,为催化剂的改性提供了另一种思路。
解众舒等[57]通过BTD 共轭交联对g-C3N4进行了改性,提高了g-C3N4的光催化产氢性能。结果表明,共轭交联修饰后,催化剂能保持连续还原水且生成氢气的状态;氢速率随着修饰量的增大而提高;g-C3N4-BTD160的光催化效率优异,光学性能稳定,并且能够多次重复利用,为其大规模应用提供了可能。
T.HUANG 等[58]通过前驱体修饰策略成功合成了一种自修饰的薄多孔富氨基g-C3N4,其结构特征为薄且孔洞多,比表面积明显增大,可使光生电子空穴快速分离并转移。平面内3s-三嗪环上丰富的末端氨基使其CB 位更负,光生电子的还原性更强。
X.H.YU 等[59]通过聚合方法将过渡金属Fe、Co 和Ni 掺杂到g-C3N4的框架中,实现了g-C3N4的原子级结构工程。金属原子掺杂后与g-C3N4形成金属-N,光生电子随着金属-N 的转移加速电荷分离。金属元素的存在降低了H+的吸收,同时减小了带隙,使改性后的催化剂还原能力更强,使析氢更容易。这种原子级结构工程可有效提高催化剂活性,为设计更高效的光催化剂提供了启发。
4 结 论
g-C3N4具有来源广泛、制备过程简单、性质稳定等优势,是一种应用前景良好的非金属半导体催化剂。本文对g-C3N4的制备与改性方法进行了阐述,并对诸多研究者在g-C3N4光催化处理废水中的污染物、产H2与产H2O2三大应用方面的研究成果进行了对比及简要评价。虽然各种复合g-C3N4光催化剂的催化性能较改性前有了很大提升,但仍无法实现将其大规模应用到实际中,故还需继续借鉴前人的设计思路与实验结果,研发出性能更优异的光催化剂。
未来可以从以下几方面进行研究:①复合催化剂制备要始终遵循节能、环保、高效、低消耗的宗旨;②在已有N 缺陷、共轭交联等修饰的基础上,继续设计制造各种缺陷,研究其他高质量的异质结构及协同效应对电荷分离、光生载流子移速等方面的影响;③在催化剂微观结构方面,继续采用先进的表征测试,研究催化剂制备过程中内在因素的影响,为性能更优异的复合催化剂的设计提供理论基础。
——潘桂棠光生的地质情怀

