两种桑黄多糖的结构分析及其抗炎活性研究
刘利娜,王仁中,吴丝雨,金传山,2
(1.安徽中医药大学,安徽 合肥 230012;2.中药饮片制造新技术安徽省重点实验室,安徽 合肥 230012)
桑黄始载于《神农本草经》,名曰“桑耳”,为桑黄孔菌属真菌桑黄Sanghuangporussanghuang的子实体,分布于中国暖温带和温带多个省份以及韩国、日本和缅甸[1]。桑黄具有活血止血、化饮、止泻之功效[2]。现代药理研究[3-5]表明,其具有抗肿瘤、抗炎、抗氧化、降糖等多种生物活性。由于生境和生长年限的制约,野生桑黄难以满足市场的需求,人工培植的瓦尼桑黄S.vaninii和鲍姆桑黄S.baumii等已成为市场主要产品[6-7]。多糖是桑黄的主要活性物质,存在于子实体、菌丝体及发酵液中,在抗肿瘤、免疫调节、抗炎和抗氧化等方面表现出的生物活性使其成为研究和开发应用的热点[8-10]。本实验观察了人工培育的瓦尼桑黄子实体中两种酸性多糖分离纯化过程,分析其结构特征,以及对以脂多糖(lipopolysaccharide, LPS)诱导的小鼠RAW264.7巨噬细胞中一氧化氮(nitric oxide,NO)及炎症因子的影响,为桑黄资源的高效利用及桑黄多糖产品的开发提供理论依据。
1 材料
1.1 仪器 F50型全波长酶标仪:美国Tecan公司;傅里叶变换红外光谱(Fourier transform infrared spectroscopy,FT-IR)仪:美国赛默飞世尔科技有限公司;SIGMA HD扫描电子显微镜(scanning electron microscope, SEM):德国蔡司公司;CO2培养箱:美国Thermo公司;ICS5000离子色谱仪:美国Thermo公司;U3000高效液相色谱仪:美国Thermo公司;Optilab T-rEX示差检测器和DAWN HELEOS Ⅱ激光散射检测器:美国Wyatt 科技;凝胶排阻色谱柱Ohpak SB-805 HQ(8 mm×300 mm)、Ohpak SB-804 HQ(8 mm×300 mm)和Ohpak SB-803 HQ(8 mm×300 mm):日本昭和电工株式会社。
1.2 药材与试剂 桑黄采自安徽省森湶谷药业股份有限公司种植基地,经安徽中医药大学杨青山副教授鉴定为瓦尼桑黄Sanghuangporousvaninii(Pilát) L.W. Zhou &Y.C. Dai的子实体,标本保存于安徽中医药大学药学院标本中心,标本号为AHTCM20220520。岩藻糖、鼠李糖、阿拉伯糖、半乳糖、葡萄糖、木糖、甘露糖、果糖、核糖、半乳糖醛酸、葡萄糖醛酸、甘露糖醛酸和古罗糖醛酸标准品:美国Sigma-Aldrich化学有限公司;二乙氨基纤维素-52(diehlaminowthy, DEAE-52)(批号120D014)和Sephadex G-100(批号1018B021):北京索莱宝科技有限公司;RAW264.7细胞:中国科学院上海生科院细胞资源中心;胎牛血清(批号11011-8611):浙江天杭生物科技股份有限公司;DMEM高糖培养基(批号C11885500):上海玉博生物科技有限公司;LPS(批号S11060):上海源叶生物科技有限公司;NO试剂盒(批号S3090):上海碧云天生物技术有限公司;白细胞介素-6 (interleukin-6, IL-6)ELISA试剂盒(批号110712001202681104)、肿瘤坏死因子-α (tumor necrosis factor-α, TNF-α)ELISA试剂盒(批号110712001104841104)和白细胞介素-1β(interleukin-1β, IL-1β)ELISA试剂盒(批号110712001184421104):上海将来实业股份有限公司。
2 方法
2.1 桑黄多糖的制备 取瓦尼桑黄子实体1.0 kg,粉碎,加10倍量水,煎煮3次,每次2 h。合并提取液,减压浓缩,加4倍量乙醇沉淀,放置过夜,抽滤。沉淀用蒸馏水溶解,醇沉,反复3次,干燥,获得桑黄粗多糖(Sanghuang Polysaccharide, SHP)提取物。粗多糖提取物用Sevage法(氯仿—正丁醇4∶1)脱除蛋白,经3 500 Da截留量的透析袋透析48 h处理,袋内溶液浓缩,冷冻干燥得到SHP[11]。将SHP溶解于蒸馏水中,流经DEAE-52纤维素柱(1.6 cm×35 cm),分别用蒸馏水和不同浓度(0.1~0.5 mol/L)的NaCl溶液以1 mL/min流速洗脱,硫酸—苯酚法检测,收集各高峰部分洗脱液,合并,浓缩,透析,冷冻干燥,得到0.1 mol/L和0.2 mol/L NaCl中获得的两个组分,分别命名为SHP-1和SHP-2。二者经Sephadex G-100 进一步纯化,得到SHP-1-1和SHP-2-1。
2.2 桑黄多糖结构特征分析
2.2.1 化学组成分析 总多糖含量以葡萄糖对照品为对照,苯酚—硫酸法测定[12]。蛋白质含量以牛血清白蛋白为对照,考马斯亮蓝染色法测定[13]。糖醛酸含量测定时,以半乳糖醛酸对照品为对照,采用间羟基联苯法测定[14]。
2.2.2 分子量的测定 取SHP-1-1和SHP-2-1样品适量,精密称定。置于2 mL容量瓶中,加0.1 mol/mL NaNO3水溶液(含0.02% NaN3,w/w)中,配制成终浓度为1 mg/mL的样品溶液,经0.45 μm微孔滤膜滤过,备用。100 μL样品溶液经凝胶排阻色谱[Ohpak SB-805 HQ(8 mm×300 mm)、Ohpak SB-804 HQ(8 mm×300 mm)和Ohpak SB-803 HQ(8 mm× 300 mm)串联],以0.1 mol/mL NaNO3(含0.02% NaN3)水溶液为流动相,柱温45 ℃,流速0.5 mL/min,等度洗脱,测定分子量。
2.2.3 单糖组成检测 取适量SHP-1-1和SHP-2-1粉末,于5.0 mL三氟乙酸溶液(2 mol/L)溶解,120 ℃水解2 h。取出,氮气吹干。加入甲醇溶解,氮气吹干,重复3次,除去多余的酸。残渣加入1 mL超纯水溶解,经0.45 μm微孔滤膜过滤,备用。取单糖标准品适量,加去离子水配制成10 mg/mL单糖标准溶液贮备液,临用时配制成不同浓度的混合标准品溶液,备用。经Thermo ICS5000离子色谱系统,电化学检测器对单糖进行检测。采用DionexTMCarboPacTMPA20色谱柱(150 mm×3.0 mm,10 μm),柱温30 ℃;以流动相A(H2O)、流动相B(0.1 mol/L NaOH)、流动相C[0.1 mol/L NaOH)水溶液(含0.2 mol/L NaAc)]组成流动相进行梯度洗脱。洗脱条件:0~26 min,95%~85% A,5%~5% B;26~42 min,85%~85% A,5%~5% B;42~52 min,85%~60% A,5%~0% B;52~60 min,60%~95% A,0%~5% B,流速0.5 mL/min;进样量为5 μL。
2.2.4 FT-IR分析 称取4.0 mg的SHP-1-1和SHP-2-1干燥粉末,置于石英研钵,加入200 mg KBr,研匀,压片。于FT-IR上,采集400~4 000 cm-1范围内吸收数据。
2.2.5 SEM分析 将适量的SHP-1-1和SHP-2-1干燥粉末均匀平铺在导电胶上,真空喷镀仪在其表面喷一层导电膜,SEM观察两种多糖的表面微观结构(加速电压3.0 kV)。
2.3 抗炎活性研究
2.3.1 RAW264.7细胞活力测定 取对数生长期的RAW264.7细胞,以1×105/mL密度铺于96孔板中培养24 h,弃去培养液,正常组加入100 μL DMEM培养基,给药组加入100 μL DMEM溶解的多糖样品溶液(浓度为10、15、50、100、200、400 μg/mL),每孔各加100 μL,重复6次。培养24 h后,每孔加10 μL CCK8,继续培养2 h,取出,避光,于酶标仪450 nm波长处测定吸收度(A),计算细胞活力。细胞活力=[A(给药组)-A(空白组)]/[A(正常组)-A(空白组)]×100%。
2.3.2 RAW264.7细胞中NO含量及炎症细胞因子水平测定 取对数生长期的细胞,以1×105/mL铺于96孔板中培养24 h,弃去培养液,正常组(高糖培养基)、模型组(培养基+0.5 μg/mL LPS溶液)和药物组(培养基+0.5 μg/mL LPS溶液+培养基溶解的不同浓度多糖),每孔各加100 μL,设置6个复孔,培养24 h。将细胞培养液1 000 r/min离心5 min后收集上清。采用NO检测试剂盒检测NO含量。采用ELISA试剂盒检测细胞中IL-6、IL-1β和TNF-α水平。
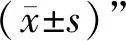
3 结果与分析
3.1 分子量的测定 经凝胶渗透色谱—示差—多角度激光散器 (gelpermeation chromatography-refractive index-multi angle laser scattering, GPC-RI-MALS) 分析后,运用马克·霍温克方程计算每个组分对应的分子量。SHP-1-1的重均分子量(weight-average molecular weight,Mw)、数均分子量(number-average molecular weight, Mn)和均分子量(average molecular weight, Mz)分别为333.599、43.427、3 516.544 kDa,多分散系数(polydispersity, Mw/Mn)为7.682。SHP-1-1的Mw、Mn和Mz分别为563.032、59.641和4 205.062 kDa,Mw/Mn为9.44。二者的Mw/Mn表明桑黄酸性多糖是具有较宽分子量分布的高度异质多糖。SHP-1-1和SHP-2-1的分子构型图均产生一条斜率小于1/3的线,表明SHP-1-1和SHP-2-1均是一种球形分子。见图1、图2。
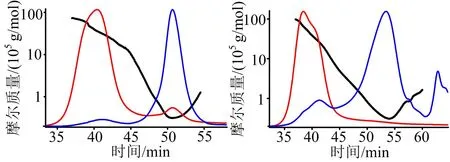
注:绝对分子量分析图中红线表示多角度激光光散射信号;蓝线表示差信号;黑线表示两种信号拟合出的分子量
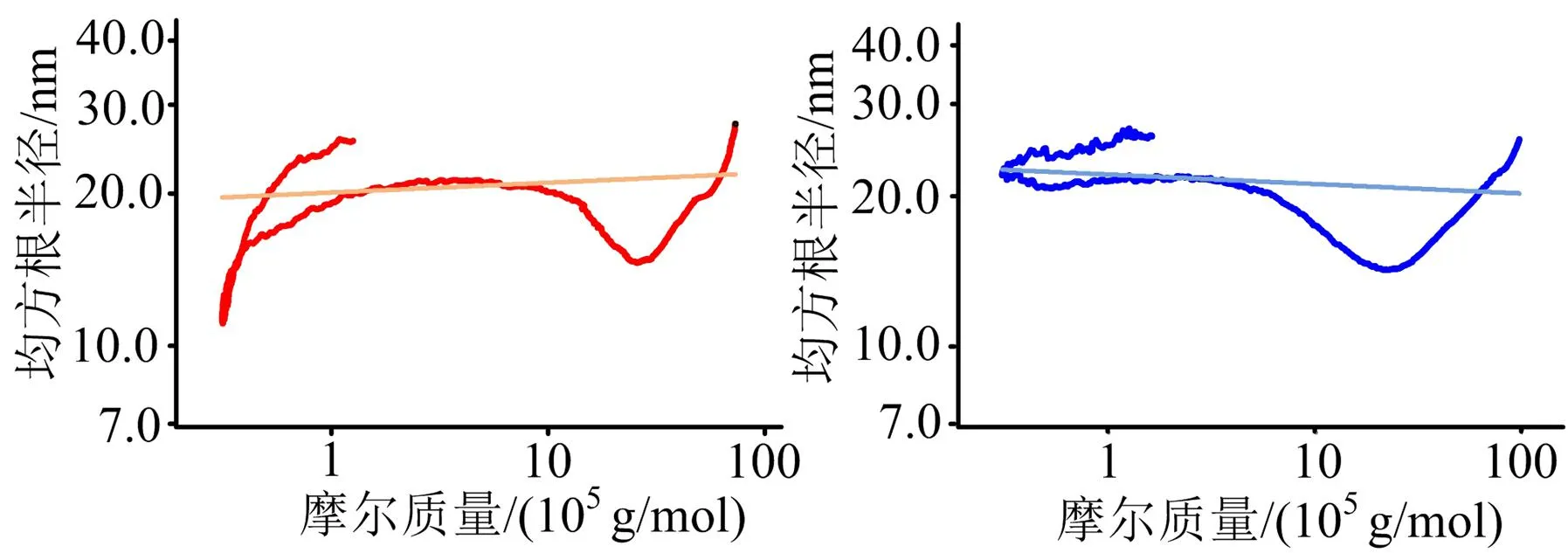
图2 SHP-1-1(左)和SHP-2-1(右)的分子构型图
3.2 单糖组成测定 将SHP-1-1和SHP-2-1用三氟乙酸水解,离子色谱法测定单糖组成。SHP-1-1由岩藻糖、阿拉伯糖、鼠李糖、半乳糖、葡萄糖、木糖、甘露糖、葡萄糖醛酸组成,其摩尔比为11.48∶0.18∶0.28∶17.86∶27.71∶0.64∶11.75∶0.94;SHP-2-1由岩藻糖、阿拉伯糖、鼠李糖、半乳糖、葡萄糖、木糖、甘露糖、葡萄糖醛酸组成,其摩尔比为0.73∶0.14∶0.32∶1.13∶14.96∶1.04∶3.79∶1.50。SHP-1-1主要由葡萄糖、甘露糖、半乳糖以及岩藻糖4种单糖组成,SHP-2-1主要由葡萄糖、甘露糖和甘露糖醛酸3种单糖组成。见表1。

表1 SHP-1-1和SHP-2-1单糖组成分析
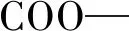
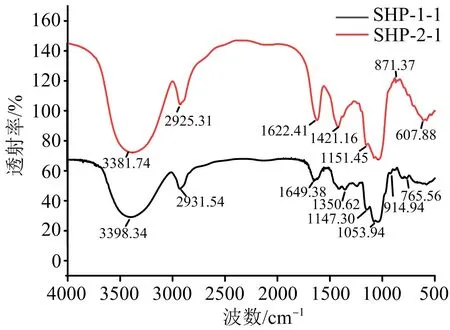
图3 SHP-1-1和SHP-2-1 的FT-IR光谱图
3.4 SEM分析 SEM图中可以观察到,SHP-1-1呈不规则片状,较为完整,表面相对光滑,部分凹凸不平,有孔洞,部分区域有不规则碎屑出现;SHP-2-1呈不规则碎片状,相互堆积结果表面粗糙无孔洞。从放大5 000倍的SEM图中可以观察到,SHP-1-1表面形态为多孔网状结构,且相互连接,可能与多糖分子间受力作用不同有关。SHP-2-1表面粗糙,有不规则结晶状凸起,可能是多糖晶体结构。见图4。

图4 SHP-1-1和SHP-2-1 SEM图
3.5 SHP-1-1和SHP-2-1抗炎活性研究
3.5.1 SHP-1-1和SHP-2-1对RAW264.7细胞活力的影响 SHP-1-1和SHP-2-1在10~400 μg/mL浓度范围内未呈现明显细胞毒活性;与对照组比较,SHP-1-1组和SHP-2-1组RAW264.7细胞活力显著升高,且在10~100 μg/mL范围内呈剂量依赖性。见图5。
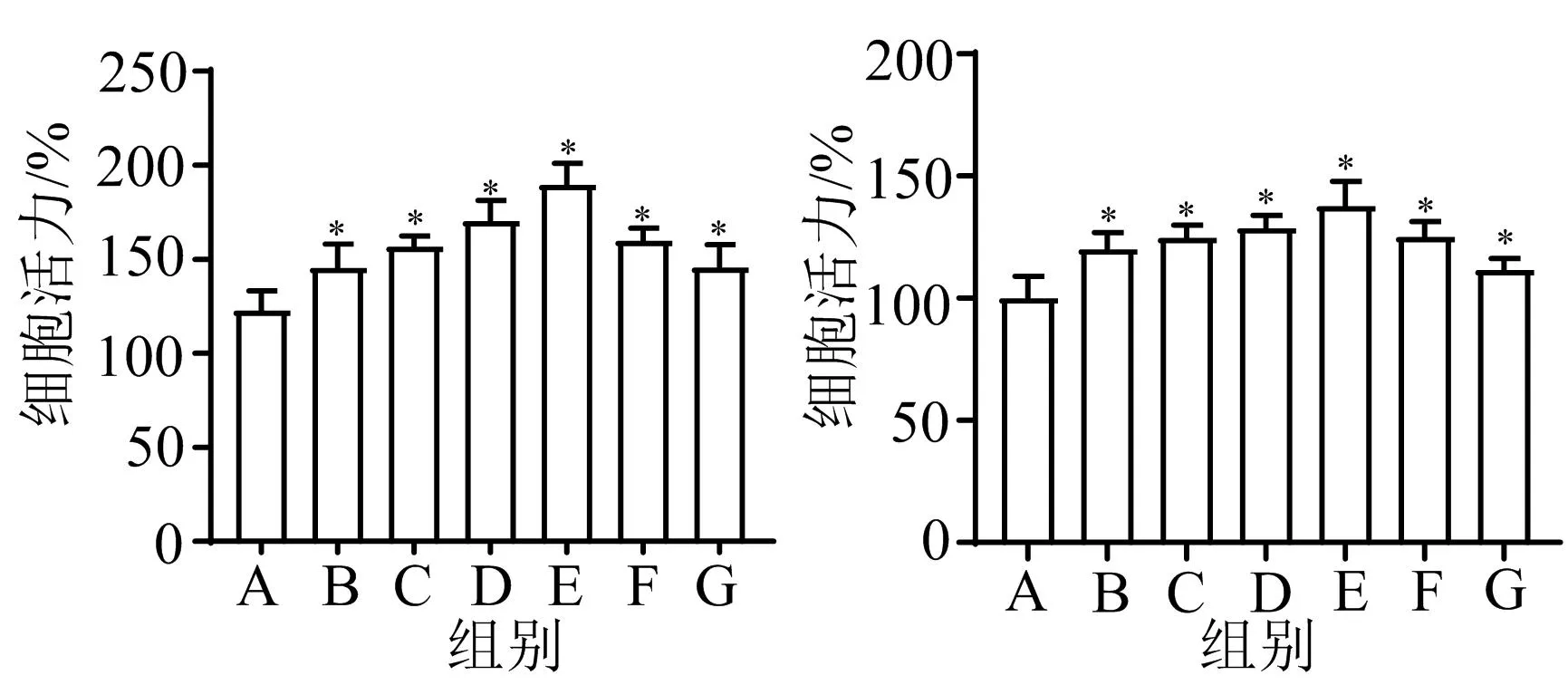
注:A.正常组;B.10 μg/mL组;C.25 μg/mL组;D.50 μg/mL组;E.100 μg/mL组;F.200 μg/mL组;G.400 μg/mL组;与正常组比较,*P<0.05
3.5.2 SHP-1-1和SHP-2-1对LPS诱导的RAW264.7细胞释放NO含量及炎症细胞因子分泌的影响 SHP-2-1对LPS诱导的RAW264.7细胞释放的NO及分泌的炎症细胞因子的半抑制浓度(50% inhibitory concentration, IC50)较SHP-1-1低,SHP-1-1能较好地抑制IL-6的分泌,SHP-2-1能较好地抑制NO的释放和IL-1β的分泌。瓦尼桑黄中分离得到的两种酸性多糖均能不同程度地抑制LPS诱导的RAW 264.7细胞中NO释放,降低TNF-α、IL-1β和IL-6的水平,减轻炎症损伤,发挥抗炎作用。见图6、表2。

表2 SHP-1-1和SHP-2-1对LPS诱导的RAW264.7细胞释放的NO及分泌的炎症细胞因子的IC50值比较
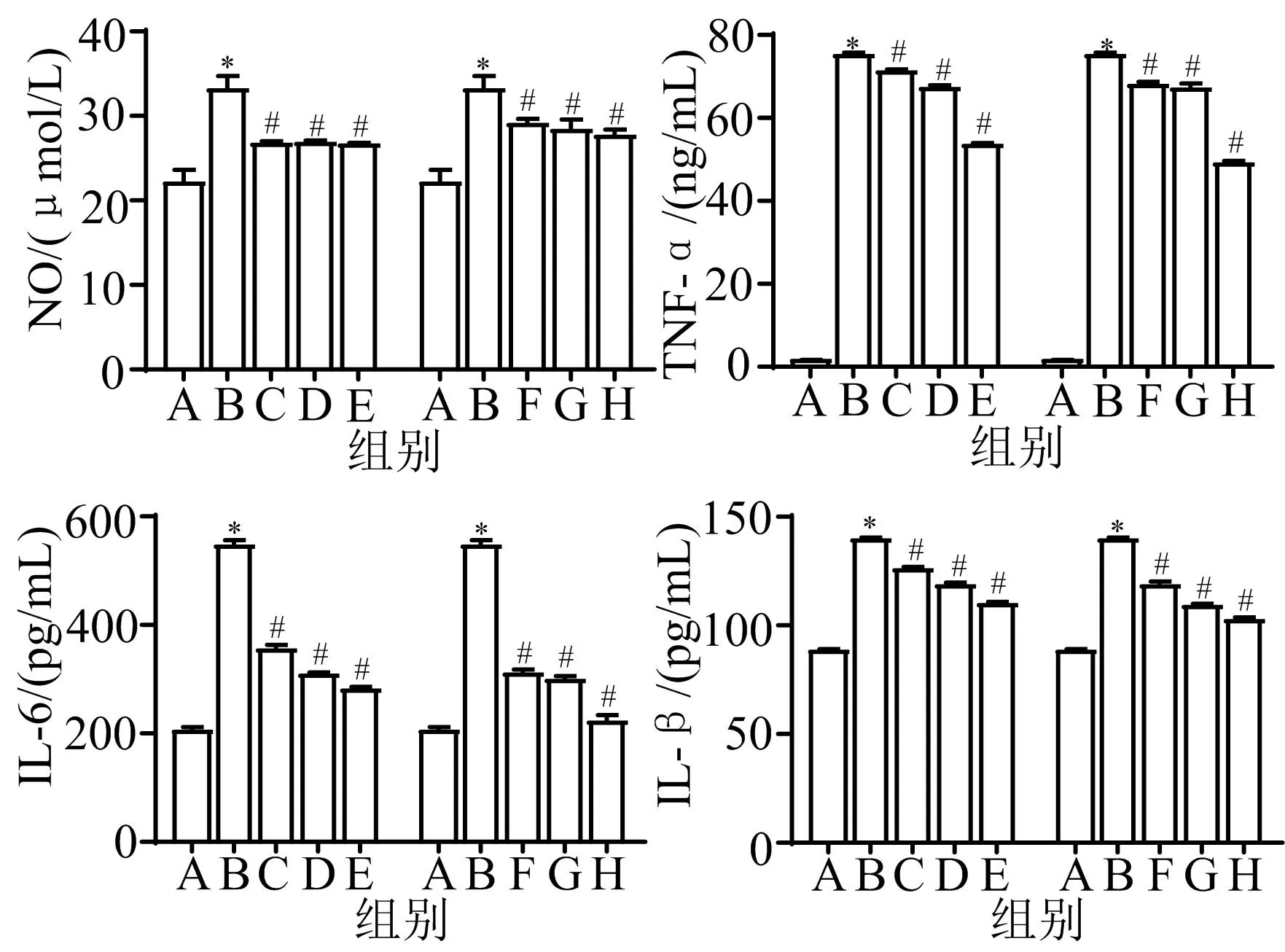
注:A.正常组;B.模型组;C.25 μg/mL SHP-1-1组;D.50 μg/mL SHP-1-1组;E.100 μg/mL SHP-1-1组;F.25 μg/mL SHP-2-1组;G.50 μg/mL LPS+SHP-2-1组;H.100 μg/mL SHP-2-1组;与正常组比较,*P<0.05;与模型组比较,#P<0.05
4 讨论

本实验选用LPS诱导RAW264.7巨噬细胞为炎症模型,评价桑黄酸性多糖SHP-1-1和SHP-2-1的体外抗炎作用。SHP-1-1和SHP-2-1在安全浓度内均能降低LPS诱导RAW264.7巨噬细胞释放的NO含量,抑制TNF-α、IL-6及IL-1β的分泌,表现出良好的抗炎活性。

