药液稀释倍数对威百亩分解产生异硫氰酸甲酯及其消解的影响
陈新华 唐秀军 张毅 方文生 颜冬冬 李园 曹坳程 白庆荣 王秋霞


摘要
種植前施用威百亩进行土壤熏蒸消毒,其分解产生的异硫氰酸甲酯(methyl isothiocyanate, MITC)可有效控制土传病原菌。威百亩以滴灌方式施用更为方便、安全,但在滴灌前的稀释过程中可能会水解产生MITC,MITC继续消解或挥发导致进入土壤的有效成分量减少。因此有必要筛选适宜的威百亩稀释倍数,保证MITC在土壤中分布均匀的同时减少威百亩分解及MITC消解和挥发导致的损失。本文研究了不同pH条件下稀释倍数对威百亩水解产生MITC及MITC消解的影响。结果表明,在中性条件下,由威百亩水解产生的MITC量及其消解速率均随稀释倍数增加而增加;在酸性条件下,稀释100倍时MITC的产生量及消解速率均为最大,稀释50倍时MITC的产生量最低,稀释400倍时MITC消解最慢;在碱性条件下,MITC的产生量随稀释倍数增加而增加,消解速率为稀释1 000倍时最快,稀释100倍时最慢。研究结果对滴灌施用威百亩时田间用水量及威百亩用量均具有指导意义。
关键词
威百亩; 异硫氰酸甲酯; 滴灌施药; 稀释倍数; 消解
中图分类号:
S 482.6
文献标识码: A
DOI: 10.16688/j.zwbh.2023005
Effect of dilution ratio on the amount of metam sodiumproduced methyl isothiocyanate and its dissipation
CHEN Xinhua1, TANG Xiujun2, ZHANG Yi2, FANG Wensheng2, YAN Dongdong2, LI Yuan2,CAO Aocheng2, BAI Qingrong1*, WANG Qiuxia2*
(1. Jilin Agricultural University, Changchun 130033, China; 2. Institute of Plant Protection,
Chinese Academy of Agricultural Sciences, Beijing 100193, China)
Abstract
Preplant soil fumigation with metam sodium can effectively control soilborne pathogens, which is attributed to methyl isothiocyanate (MITC), a degradation product of metam sodium. It is convenient and safe to apply metam sodium by drip irrigation. However, in dilution process before drip irrigation metam sodium may produce MITC through hydrolysis, which will continue to degrade or volatilize, resulting in a decrease of effective components in the soil. Therefore, it is necessary to select a suitable dilution multiple of metam sodium, which can ensure uniform distribution of MITC and reduce its loss by volatilisation or disintegration before being applied in the soil. In this study, the effect of dilution ratio on the amount of metam sodiumproduced methyl isothiocyanate and its dissipation in aqueous solution were investigated under different pH conditions. The results showed that the amount of MITC and its dissipation rate increased with the increase of dilution ratio under neutral conditions. Under acidic conditions, the amount of MITC and its dissipation rate was maximum when diluted 100 times, the minimum amount of MITC occurred at 50 times of dilution, and the slowest dissipation rate was found at 400 times dilution. Under alkaline conditions, the produced MITC increased with the increase of the metam sodium dilution ratio, and the dissipation rate was the fastest when diluted 1 000 times, and was the lowest when diluted 100 times. The results have a guiding significance on how to formulate field water consumption, and application dosage when applying metam sodium by drip irrigation.
Key words
metam sodium; methyl isothiocyanate; drip irrigation; dilution ratio; degradation
土壤熏蒸消毒技术于1869年首次实践应用,熏蒸剂以气体形式在土壤气相中扩散防治土传病害[1]。在过去的几十年里,溴甲烷(bromomethane, MeBr)作为广谱熏蒸剂,广泛应用于农田防治土壤有害生物[2]。但由于溴甲烷破坏臭氧层,1987年《蒙特利尔议定书》呼吁逐步淘汰溴甲烷, 2017年中华人民共和国农业部公告第2552号要求自2019年1月1日起,将含溴甲烷产品的农药登记使用范围变更为“检疫熏蒸处理”,禁止含溴甲烷产品在农业上使用[34]。溴甲烷淘汰后,熏蒸剂威百亩在我国用量逐年增加。
威百亩的活性成分是其一级降解产物异硫氰酸甲酯(MITC)[5]。MITC对大丽轮枝菌Verticillium dahliae[6]、核盘菌Sclerotinia sclerotiorum[7]、腐霉Pythium aphanidermatum[8]、根结线虫(rootknot nematode)[9]、藜Chenopodium album[10]、稗草Echinochloa crusgalli [10]等土壤有害生物均有较好防效。
MITC的饱和蒸汽压相对溴甲烷较低,又易溶于水,以气体形式在土壤中的扩散范围小,所以为了增加MITC在土壤中的分布均匀度,生产中应用其前体物质威百亩或者棉隆。威百亩常用的剂型是35%或42%的水剂,可通过手动或者机动注射装备施药,也可通过滴灌系统或者大水漫灌施药,而采用滴灌系统施药,不需要专门的注射装备,又可在塑料薄膜下完成施药,所以兼具经济及对施药人员安全的优点。
滴灌施药时,为了整田均匀施药,需将威百亩水剂进行稀释,再进行滴灌。在田间,通过滴灌施用威百亩稀释倍数通常在32~850倍[1113]。稀释后的威百亩在水溶液中易发生分解反应产生MITC,而MITC在水中不稳定,易分解成CH3NH2[14]。若威百亩水解速率过快,在滴灌施药过程中威百亩水解产生的MITC可能会通过挥发或者消解而损失,进入土壤中的有效成分就会减少,进而影响防治效果。已有研究表明,滴灌水量和滴灌速度对MITC在土壤中的分布有影响,在滴灌水量45 L/m及滴灌速度1.9~5.0 L/(h·m)时,MITC在供试的砂壤土中分布良好[15]。已有研究表明,滴灌药液浓度大于1 500 mg/kg时才对线虫有效[16],因此为确保对土传病原物的防治效果,威百亩应尽可能以母体形式在土壤中迁移扩散,到达作用土层后分解产生MITC。农药对酸碱度敏感性不同,Ruzo等发现在pH为5、7和9的缓冲液中,威百亩的水解半衰期分别为 24、180 h和 46 h[17]。我国水资源从北到南pH呈现出逐渐降低的特点[18],刘旭艳等[19]对我国12个典型地区10年间降雨、地表水和地下水质分析发现,农田生态系统pH通常在5.55~8.27。本论文依据田间实际情况,研究了在pH 5、7、9条件下稀释50~1 000倍对42%威百亩水剂分解产生MITC及MITC消解的影响,明确稀释倍数和pH对威百亩和MITC水解程度的影响,研究结果可为因地制宜地滴灌施用威百亩时的技术参数制定提供理论支持。
1 材料与方法
1.1 供试药剂及试剂
42%威百亩水剂由江苏利民化学有限公司提供。MITC,分析纯(>98%)购自SigmaAldrich Corporation(St Louis,USA)。色谱级乙酸乙酯(纯度99.7%)和无水硫酸钠分别由北华精细化工有限公司(中国北京)和国药化学试剂有限公司(中国北京)提供。
1.2 仪器与设备
Agilent 气相色谱(6890型)与质谱联用仪(5973型),安捷伦(中国)有限公司;多管涡旋混合仪,杭州米欧仪器有限公司;pH计(雷磁 PHSJ4F型),上海仪电科学仪器股份有限公司。
1.3 试验方法
1.3.1 中性条件下稀释倍数对威百亩转化产生MITC及其消解的影响
在宽颈广口瓶中加入10、20、40、80 mL和200 mL蒸馏水(pH=7),再分别加入0.2 mL 42%威百亩水剂,稀释倍数分别为50、100、200、400、1 000倍(对应的威百亩的初始浓度分别为8 400、4 200、2 100、1 050、420 mg/L)。放入25℃培養箱中3 min、15 min、30 min、1 h、1.5 h、2 h、3 h、4 h、2 d、5 d、11 d、17 d、80 d后,抽取1 mL水样到20 mL顶空瓶中,然后立即加入8 g无水硫酸钠和9 mL乙酸乙酯后盖上装有硅胶垫的铝盖,然后于2 000 r/min转速下振荡30 min。样品静置90 min后用2.5 mL无菌注射器抽取上清液过0.22 μm滤膜至2 mL进样瓶中,待测[20]。
1.3.2 酸性或碱性条件下稀释倍数对威百亩转化产生MITC及其消解的影响
pH=5.0緩冲液的配制:取500 mL 0.1 mol/L的苯二甲酸氢钾溶液,加226 mL 0.1 mol/L氢氧化钠溶液,再用去离子水定容至1 000 mL。
pH=9.0缓冲液的配制:分别取250 mL 0.1 mol/L的硼砂与0.1 mol/L氯化钾溶液,加208 mL 0.1 mol/L氢氧化钠溶液,再用去离子水定容至 1 000 mL。
在宽颈广口瓶中加入10、20、40、80 mL和200 mL上述配制的缓冲溶液(pH=5.0、pH=9.0),在上述宽颈广口瓶中分别加入0.2 mL 42%威百亩水剂,对应的稀释倍数分别为50、100、200、400、1 000倍。放入25℃培养箱中5 min、15 min、30 min、1 h、1.5 h、2 h、3 h、4 h、6 h、3 d、7 d、17 d、34 d后按1.3.1方法制样。
1.3.3 MITC分析方法
气相色谱条件为:载气(He) 流速1.0 mL/min,入口温度250℃。
质谱仪条件如下:离子源和四极杆温度分别设置为230℃和150℃。定性离子为45 m/z和73 m/z,定量离子为73 m/z。
1.3.4 MITC的添加回收率测定
配制10 000 mg/L的MITC母液,用蒸馏水将母液稀释至120、450、2 250、4 500 mg/L,按1.3.1中方法进行提取,每个处理设置5个重复。
1.4 数据分析
用一级降解动力学模型拟合MITC在水体中的消解行为[20],方程如下:
C=C0e-kt
其中,C(mg/kg)表示t时刻水体中MITC浓度,C0(mg/kg)表示MITC在水体中的最高浓度,k(h-1)表示一级消解动力学常数。
MITC的消解半衰期(t1/2)的计算公式如下:
t1/2=0.693/k
MITC消解动力学方程采用Origin 8.0拟合,数据统计分析采用SPSS 17.0软件分析完成,并采用Duncan氏新复极差法进行显著性分析。
威百亩转化为MITC的转化率计算公式如下:
y=X1X2×100%
其中,y(%)表示转化率,X1表示MITC测得实际浓度(mg/kg),X2表示加入威百亩按照碳原子摩尔比1∶1转化为MITC计算所得理论MITC浓度(mg/kg)。
2 结果与分析
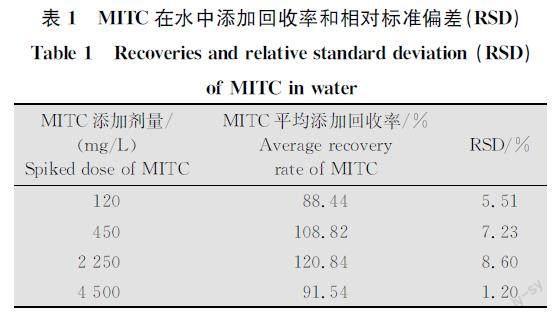
2.1 MITC分析方法的准确度和精确度
对标样的峰面积y与对应质量浓度x(mg/L)进行线性回归分析,在0.5~500 mg/L范围内,R2=0.999 9,MITC在120、450、2 250、4 500 mg/L的添加水平下,MITC添加回收率分别为88.44%、108.82%、120.84%和91.54%, RSD<10%(表1)。
2.2 中性条件下不同稀释倍数对威百亩转化产生MITC的影响
中性条件的不同稀释倍数下,威百亩转化产生MITC的动态变化趋势见图1,从图中可以看出加入威百亩后3 min,即可检测到MITC,这表明威百亩在水体中分解很快。在所有稀释倍数下威百亩转化产生的MITC量均随着时间的推移,呈现先增加而后在250 min后降低的趋势,这表明MITC在水体中可以持续分解。
中性条件下不同稀释倍数威百亩转化产生MITC的峰值、出现时间、转化率见表2。试验结果表明,随着稀释倍数增加,威百亩转化产生MITC的速度和量均增加。从表2中还可以看出,随着稀释倍数的增加威百亩转化产生MITC的比率增加,如从稀释倍数为50倍时的50.61%增加到稀释倍数为400倍时的90.23%;但稀释倍数为1 000倍时,转化率反而低,其原因可能在于高稀释倍数下,产生的MITC消解也快,所以检测的峰值低于稀释倍数为400倍时。
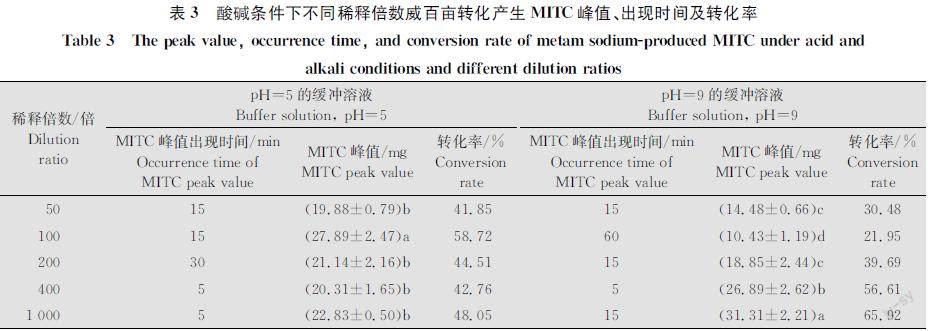
2.3 酸性或碱性条件下不同稀释倍数对威百亩转化产生MITC的影响
从表3中可以看出,在酸性条件下,稀释倍数在100倍时,威百亩分解最快,转化率达到58.72%,虽然其他几个稀释倍数间没有显著性差异,但稀释倍数在400倍和1 000倍时,峰值出现时间更早(加药后5 min)。在碱性条件下,检测到的MITC峰值随着稀释倍数增加而增加,最大转化率是稀释1 000倍时的65.92%。但总体看来,虽然酸性或碱性条件下威百亩的分解率低于在蒸馏水中,但峰值出现时间更早,稀释倍数对其分解依然有影响,尤其是碱性条件下也是稀释倍数越高,分解率越高。
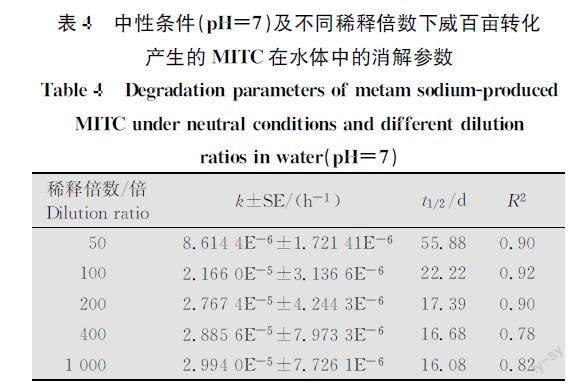
2.4 中性条件下不同稀释倍数对威百亩转化产生的MITC消解的影响
一级降解动力学方程可以较好地拟合威百亩转化产生的MITC在不同稀释倍数下的消解(R2=0.78~0.92),消解参数见表4。从表4中可以看出稀释倍数为50、100、200、400、1 000倍时,MITC消解半衰期分别为55.88、22.22、17.39、16.68 d和16.08 d。上述结果表明:随着稀释倍数的增加,MITC的水解加快,尤其是50倍增加到100倍时,MITC消解速率增加了1.5倍。
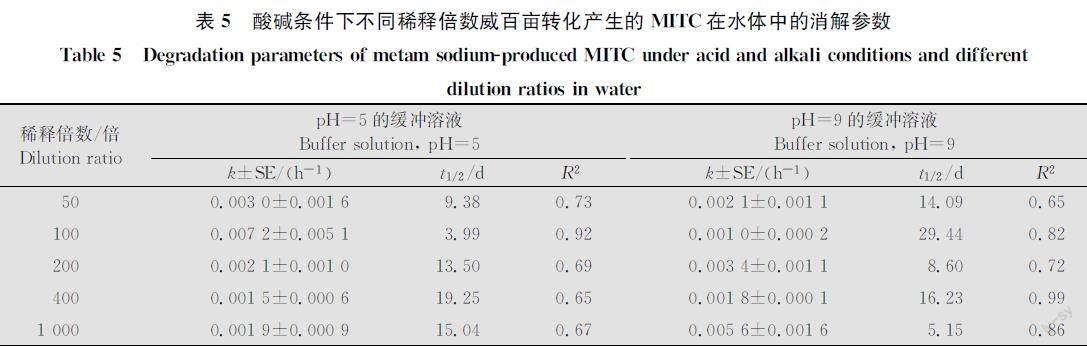
2.5 酸性或碱性条件下不同稀释倍数对威百亩转化产生的MITC消解的影响
從表5数据中可以看出,酸性条件下,MITC在稀释100倍时消解最快,半衰期仅3.99 d;稀释倍数越高消解反而变慢。碱性条件下,是稀释1 000倍的时候消解最快,半衰期为5.15 d。比较3个pH条件,在稀释50倍的时候,pH=7时MITC消解最慢,随着稀释倍数增加差异规律性不显著。但无论是在中性、酸性还是碱性条件下,威百亩均分解较快,MITC消解也较快,所以要减少MITC进入土壤前的损失,就要控制威百亩分解速率。
3 讨论
威百亩在水中的转化途径包括水解和光解,在紫外光下威百亩分解速度显著高于黑暗条件下,通过模型预测,威百亩在盛夏正午阳光下光解半衰期在1 h之内[15]。根据产生的MITC量推算,本试验中威百亩在稀释倍数200倍以上时,稀释后15 min已经分解50%以上,与Draper等[21]的研究相符合。Draper等[21]发现,在避光条件下,水溶液中威百亩初始浓度为530 mg/L时的降解半衰期为50 h,在初始浓度为39 mg/L时降解半衰期为35 h,浓度越低降解越快。本试验中稀释倍数为50、100、200、400、1 000倍时对应的威百亩的初始浓度分别约为8 400、4 200、2 100、1 050、420 mg/L,浓度设置高于Draper试验范围,但降解规律与其研究结果一致,即分解速率随着浓度降低而增加。威百亩降解是一个相对复杂的过程,降解反应存在不同的途径,水解产物间可相互转化[21]。Ruzo等[17]发现在pH 为5、7和9的缓冲液中,威百亩的降解半衰期分别为24、180 h和46 h;在碱性条件下,威百亩水解为MITC 和S元素;在酸性条件下,水解产生MITC、CS2、H2S和CH3NH[14]2。而本研究结果发现威百亩在水中的分解速率很快,其原因可能在于试验是在有光的条件下开展的,威百亩的水解和光解同时发生。Deguigne等[22]发现,在pH=5时威百亩转化产物为CS2(51%)和MITC(39%),这与本试验结果相似。MITC是易挥发性化合物,饱和蒸气压为2.7 kPa(20℃),Smelt等[23]发现20℃下其在水相和气相中的分配比为170,这表明水溶液中威百亩分解产生的MITC量越大,其挥发逃逸量越多,进入土壤的有效成分量越少。
本试验结果表明,威百亩稀释后分解速率较快,产生的MITC可以继续消解,降解半衰期在3~55 d,虽然消解速率慢,但消解的部分也会减弱威百亩防治土传有害生物的效果。Warton等[24]和Verhagen等[25]的研究表明, MITC 在砂壤土中降解半衰期为 9 h,在碱性黏壤土中降解同样迅速;Smelt 等[26]发现pH 为 7.3 时,MITC 的降解半衰期为 0.5 d;赵文等[27]研究发现MITC在20%绝对含水量土壤中降解半衰期为1.2 d,这表明MITC在土壤中降解很快,如果以MITC形式进入土壤,可能在未到达有害生物所在土壤层前就被降解,这将不利于威百亩对土传病原物防治。
理论上减小稀释倍数,可缩短滴灌时间,使得MITC挥发和降解损失减少。但Nelson等[15]发现以较小的滴灌速度1.9 L/(h·m)和5.0 L/(h·m)(用时分别为12 h和4.55 h)滴灌较高水量(45 L/m)时,MITC在土壤中分布优于7.5 L/(h·m)(用时3.03 h)的高滴灌速度或者25 mm的水量时。如果想减少威百亩转化的MITC损失又能保证其在土壤中的均匀分布,建议在滴灌或者浇灌施用威百亩时,先灌清水后再快速施入威百亩,这一步可以减少MITC在进入土壤前的损失;然后继续滴灌清水,这一步可以保证MITC在土壤中的均匀分布。
综上分析,威百亩稀释倍数低,转化产生MITC的速度快,溶解于水中的MITC可挥发逃逸,导致进入土壤中的有效成分低;MITC在土壤中可以继续降解,降解的部分也会影响威百亩对土壤有害生物的防治效果;MITC在土壤中降解速率较快,威百亩施用前转化率高,以MITC形式进入土壤,降解损失大。所以在滴灌或者浇灌应用威百亩时,稀释倍数不应该超过50倍。
4 结论
通过室内水解试验发现,威百亩稀释后可以立刻发生分解反应产生MITC,产生的MITC在水中会继续消解。在中性条件下,威百亩及其分解产生的MITC随着稀释倍数增加分解均加快;在酸性条件下,稀释100倍时威百亩分解最快;在碱性条件下,威百亩的分解随着稀释倍数增加而增加,但MITC消解是在稀释100倍的时候最慢,1 000倍的时候最快。
明确不同酸碱度条件下,稀释倍数对威百亩转化为MITC及对MITC消解的影响对滴灌施用威百亩时田间用水量、滴灌速度及威百亩用量均具有指导意义。威百亩在田间滴灌施药通常在1 d内完成,影响其效果的主要因素是MITC挥发逃逸和进入土壤尚未到达有害生物所在位置发生的降解,因此研究稀释倍数对威百亩降解的影响对田间实际生产具有指导意义。建议在滴灌施用威百亩时,威百亩稀稀释倍数不超过50倍为宜,稀释液避光储存;具体操作时先滴灌清水,再滴药液,然后再滴灌清水,既能减少MITC损失又能保证其在土壤中均匀分布。
参考文献
[1] LEMBRIGHT H W. Soil fumigation: principles and application technology [J]. Journal of Nematology, 1990, 22(4S): 632644.
[2] NOLING J W, BECKER J O. The challenge of research and extension to define and implement alternatives to methyl bromide [J]. Journal of Nematology, 1994, 26(4S): 573586.
[3] ROSSKOPF E N, CHELLEMI D O, KOKALISBURELLE N, et al. Alternatives to methyl bromide: A Florida perspective [J/OL]. Plant Health Progress, 2005, 6(1): 125. DOI: 10.1094/PHP200510270.
[4] 王秋霞, 颜冬冬, 王献礼, 等.土壤熏蒸剂研究进展[J].植物保护学报, 2017, 44(4): 529543.
[5] GERSTL Z, MINGELGRIN U, YARON B. Behavior of Vapam and methylisothiocyanate in soils [J]. Soil Science Society of America Journal, 1977, 41(3): 545548.
[6] TAYLOR R J, PASCHE J S, GUDMESTAD N C. Influence of tillage and method of metam sodium application on distribution and survival of Verticillium dahliae in the soil and the development of Verticillium wilt of potato [J]. American Journal of Potato Research, 2005, 82(6): 451461.
[7] BENYEPHET Y, BITTON S, GREENBERGER A. Control of lettuce drop disease, caused by Sclerotinia sclerotiorum, with methamsodium soil treatment and foliar application of benomyl [J]. Plant Pathology, 1986, 35(2): 146151.
[8] 趙一杰, 谢学文, 傅俊范, 等. 威百亩防治黄瓜苗期猝倒病效果研究[C]∥中国园艺学会 2012 年学术年会论文摘要集, 2012: 137.
[9] 何明明, 费林瑶. 威百亩对设施作物根结线虫病及其他土传病害的防效研究[J]. 湖南农业科学, 2013(17): 8486.
[10]王星懿, 孙振天, 王雪, 等. 35%威百亩水剂对人参田杂草的防除效果及安全性[J]. 农药, 2019, 58(4): 307310.
[11]BROWNE G T, DETAR W R, SANDEN B L, et al. Comparison of drip and sprinkler irrigation systems for applying metam sodium and managing stem rot on potato [J]. Plant Disease, 2002, 86(11): 12111218.
[12]HAAR M J, FENNIMORE S A, AJWA H A, et al. Chloropicrin effect on weed seed viability [J]. Crop Protection, 2003, 22(1): 109115.
[13]PAPIERNIK S K, YATES S R, DUNGAN R S, et al. Effect of surface tarp on emissions and distribution of dripapplied fumigants [J]. Environmental Science & Technology, 2004, 38(16): 42544262.
[14]CROUCHER L, JEWESS P. Metabolic pathways of agrochemicals: part 2: insecticides and fungicides [M]. North Carolina: Royal Society of Chemistry, 2007.
[15]NELSON S D, AJWA H A, TROUT T, et al. Water and methyl isothiocyanate distribution in soil after drip fumigation [J]. Journal of Environmental Quality, 2013, 42(5): 15551564.
[16]NOLING J W. Determining metham sodium lethal dosage for nematodes in grower field microplots [C]∥Annual International Research Conference on Methyl Bromide Alternatives and Emissions Reductions: [proceedings], 2008.
[17]RUZO L O. Physical, chemical and environmental properties of selected chemical alternatives for the preplant use of methyl bromide as soil fumigant [J]. Pest Management Science, 2006, 62(2): 99113.
[18]張心昱, 孙晓敏, 袁国富, 等. 中国生态系统研究网络水体pH和矿化度监测数据初步分析[J]. 地球科学进展, 2009, 24(9): 10421050.
[19]刘旭艳, 张心昱, 袁国富, 等. 近10年中国典型农田生态系统水体pH和矿化度变化特征[J]. 环境化学, 2019, 38(6): 12141222.
[20]DI PRIMO P, GAMLIEL A, AUSTERWEIL M, et al. Accelerated degradation of metamsodium and dazomet in soil: characterization and consequences for pathogen control [J]. Crop Protection, 2003, 22(4): 635646.
[21]DRAPER W M, WAKEHAM D E. Rate constants for metamsodium cleavage and photodecomposition in water [J]. Journal of Agricultural and Food Chemistry, 1993, 41(7): 11291133.
[22]DEGUIGNE M B, LAGARCE L, BOELS D, et al. Metam sodium intoxication: the specific role of degradation productsmethyl isothiocyanate and carbon disulphideas a function of exposure [J]. Clinical Toxicology, 2011, 49(5): 416422.
[23]SMELT J H, LEISTRA M. Conversion of methamsodium to methyl isothiocyanate and basic data on the behaviour of methyl isothiocyanate in soil [J]. Pesticide Science, 1974, 5(4): 401407.
[24]WARTON B, MATTHIESSEN J N, ROPER M M. The soil organisms responsible for the enhanced biodegradation of metham sodium [J]. Biology & Fertility of Soils, 2001, 34(4): 264269.
[25]VERHAGEN C, LEBBINK G, BLOEM J. Enhanced biodegradation of the nematicides 1,3dichloropropene and methylisothiocyanate in a variety of soils [J]. Soil Biology & Biochemistry, 1996, 28(12): 17531756.
[26]SMELT J H, CRUM S J H, TEUNISSEN W. Accelerated transformation of the fumigant methyl isothiocyanate in soil after repeated application of methamsodium [J]. Journal of Environmental Science & Health Part B, 1989, 24(5): 437455.
[27]趙文, 赵一杰, 王惟萍, 等. 实验室条件下威百亩及异硫氰酸甲酯在土壤中的降解特性[J]. 农药学学报, 2013(5): 567573.
(责任编辑:杨明丽)

