磁固相萃取结合超高效液相色谱串联质谱法检测绿茶中19 种有机磷农药残留
郭春丽,余晓峰,韩 芳,贾学颖,雷雨甜,刘会佳,吴 琼,林 童,伊雄海,宋 伟,
(1.合肥海关技术中心,食品安全分析与检测安徽省重点实验室,安徽合肥 230022;2.西宁海关技术中心,青海西宁 810000;3.上海海关动植物与食品检验检疫技术中心,上海 200003)
农药在农业生产中常用于防治虫害,提高农作物产量,延长产品保质期等[1-2]。有机磷类农药是一类含有磷原子的有机酯类化合物的总称,主要用于防治植物病、虫、草害,具有高效、广谱、易降解特性,因而在茶树的种植中被广泛使用[3-4]。朱凤等[3]研究表明因食品中农药残留引发中毒的农药中有机磷农药占比最大,有机磷进入机体会使组织中的乙酰胆碱积累,导致中枢神经系统及胆碱能神经功能异常[5-6],甚至会诱导细胞癌变[7-8]。GB 2763-2021 规定茶叶中大多数有机磷农药的最大残留限量在0.05 mg/kg[9],甚至规定部分高毒性有机磷农药被直接禁用[9-10]。茶叶中有机磷农药残留问题不可轻视,建立高效可靠的前处理方法对保障茶叶质量安全意义重大。
目前,检测有机磷常用的的前处理方法有固相萃取(SPE)[11-12]、固相微萃取(SPME)[13]、液液萃取(LLE)[14-15]、液液微萃取(LLME)[16]、QuEChERS 技术[17]等。但上述方法存在前处理步骤繁琐、耗时长、有机溶剂用量大等不足。有机磷在基质复杂的茶叶中仅痕量存在,净化效果不理想会严重干扰目标物的测定[18]。因此,需要建立一种简单高效,快速且经济安全的前处理方法来富集茶叶样品中的有机磷。
磁固相萃取(MSPE)是将含有目标分析物的待测液中加入具有磁性的吸附剂,经过萃取,将目标物吸附,最后用外加磁场将吸附了目标物的吸附剂从待测溶液中分离的技术。该技术是一种新型前处理技术,具有操作简便、快捷、低成本、易操控等特点,目前被广泛研究[19-21]。石墨烯(G)具有共轭体系,比表面积大,化学稳定性好,可与含有苯环结构的有机分子产生强的π-π键堆积作用[22-24],从而选择性吸附目标物,目前已广泛用于污染物处理中[25-27]。而磁性石墨烯在复杂的食品样品基体以及极性污染物分析中的应用还较少。
本实验结合有机磷农药结构特点及实验室现有农药标品情况,选取19 种有机磷农药为研究对象进行分析考察。将石墨烯与磁性纳米粒子相结合,用化学共沉淀法合成磁性石墨烯,并将磁固相萃取与超高效液相色谱串联质谱结合,建立同时检测绿茶中19 种有机磷农药残留的方法。实验考察了吸附剂用量、萃取时间、样品溶液pH、洗脱剂条件和氯化钠用量对磁固相萃取效率的影响。本方法能避免传统固相萃取方法的时间耗损,检测快速准确,易操控,材料可重复利用,只需要少量的有机溶剂,经济,安全,该技术在复杂样品基质以及极性污染物的富集分离中有很好的参考价值。
1 材料与方法
1.1 材料与仪器
绿茶 购自超市,为4 月份采摘后加工生产,常温储存;石墨 中国Alfa 化学有限公司;氨水(25%~28%)、盐酸(19%)、甲酸、甲醇、丙酮、乙腈、乙酸乙酯 色谱纯,美国Tedia 公司;硫酸铁铵(NH4Fe(SO4)2·12H2O)、硫酸亚铁铵((NH4)2Fe(SO4)2·6H2O)、氯化铁(FeCl3·6H2O)、氯化钠、氢氧化钠、硫酸镁、乙酸钠、乙二醇 分析纯,中国国药集团;实验用水为超纯水 美国Millipore 公司;甲胺磷、乐果、敌百虫、敌敌畏、氧乐果、辛硫磷、哒螨灵、内吸磷、毒死蜱、苯线磷、硫环磷、硫线磷、氯唑磷、杀扑磷、速灭磷、甲拌磷、毒虫畏、乙酰甲胺磷、水胺硫磷标准品,德国Dr.Ehrenstorfer 公司。
Agilent 1290-6460 超高压液相色谱-三重四极杆串联质谱仪 美国Agilent 公司;JSM-6480 LV 扫描电镜 日本电子公司;N-EVAP112 氮吹仪 美国Organomation 公司;KQ2200E 超声波清洗器 昆山市超声仪器有限公司;Buchi-R215 旋转蒸发仪 北京陆德恒泰商贸有限公司;DF 101S 集热式恒温加热磁力搅拌器 上海析牛莱伯仪器有限公司;DZF6020真空干燥箱 上海一恒科技有限公司。
1.2 实验方法
1.2.1 磁性石墨烯的制备 按本实验室[28]和参考文献[29-30]方法制备,采用化学共沉淀法。分别取(NH4)2Fe(SO4)2·6H2O(2.04 g)、NH4Fe(SO4)2·12H2O(3.01 g)和石墨烯(0.6 g)溶于200 mL 超纯水中,在氮气保护下混匀,以100 W,40 kHz 超声20 min,在此过程逐滴加入8 moL/L 氨水,保持pH11~12,缓慢将温度升至50 ℃,在此温度下1300 r/min 搅拌反应1 h。将沉淀物由磁铁收集并用去离子水重复冲洗至中性,在真空下干燥得到黑褐色粉末即为磁性石墨烯(Fe3O4@G)。Fe3O4纳米粒子参照Zhao 等[31]方法制备:称取6.8 g FeCl3·6H2O,18 g 乙酸钠,快速加入250 mL 乙二醇,保持1300 r/min 搅拌反应30 min,充分溶解后将其全部倒入反应釜200 ℃下反应8 h,产物经磁分离后,依次用乙醇、去离子水洗涤3 次,烘干备用。
1.2.2 标准溶液配制 农药标准储备液(100 μg/mL):准确称取10 mg(精确至0.01 mg)标准品于100 mL棕色容量瓶中,用乙腈溶解并定容至刻度,摇匀,4 ℃避光保存。
1.2.3 绿茶样品前处理 提取:参照GB 23200.121-2021[32]的茶叶提取条件并加以优化,将绿茶样品先浸湿后再用乙腈提取有机磷农药。称取1 g(精确至0.01 g)绿茶样品,加入15 mL 水浸湿后涡匀,再加入10 mL 乙腈,涡匀后,以100 W,40 kHz 超声提取10 min,加入4 g 氯化钠,均质后,以8000 r/min 离心5 min。吸取全部上清液于鸡心瓶中,残渣用10 mL乙腈重复提取一次,合并上清液,于旋转蒸发仪上蒸干,用10 mL 乙腈-水(1:9,v/v)复溶。取1.0 mL 上述复溶液于10 mL 容量瓶中,用乙腈-水(1:9,v/v)定容至刻度,备用。
净化:磁固相萃取部分参照刘丽文等[33]实验方法并加以改进。取上述全部溶液加入20 mg Fe3O4@G 吸附剂,涡匀后振荡萃取20 min。将磁铁放试管底部聚集Fe3O4@G 后弃去上清液,加入1 mL 丙酮溶液,涡旋解吸1 min,磁分离后,取全部上清液于另一试管中。重复上述洗脱操作2 次,合并上述解吸液,氮气吹干,随后用200 μL 乙腈-水(1:9,v/v)溶解,供UHPLC-MS/MS 分析。
1.2.4 色谱-质谱条件 色谱-质谱条件参照GB 23200.121-2021[32]的测试条件并加以优化。
1.2.4.1 色谱条件 Agilent Eclipse Proshell 120 C18柱(1.9 μm,100 mm×2.1 mm),流动相A 为2 mmol/L甲酸铵-0.01%甲酸水溶液,B 为2 mmol/L 甲酸铵-0.01%甲酸甲醇溶液,梯度洗脱程序见表1。柱温:40 ℃;进样量10 μL。

表1 19 种有机磷农药梯度洗脱程序Table 1 Gradient elution procedures for 19 organophosphorus pesticides
1.2.4.2 质谱条件 19 种有机磷农药均为ESI+模式;采集方式为多反应监测MRM;干燥器气温度:300 ℃,流速:10 L/min;稍流气温度:300 ℃,流速:11 L/min;雾化气压力:0.28 MPa;电喷雾电压:4.0 kV;毛细管电压:3.0 kV;详细优化参数见表2。
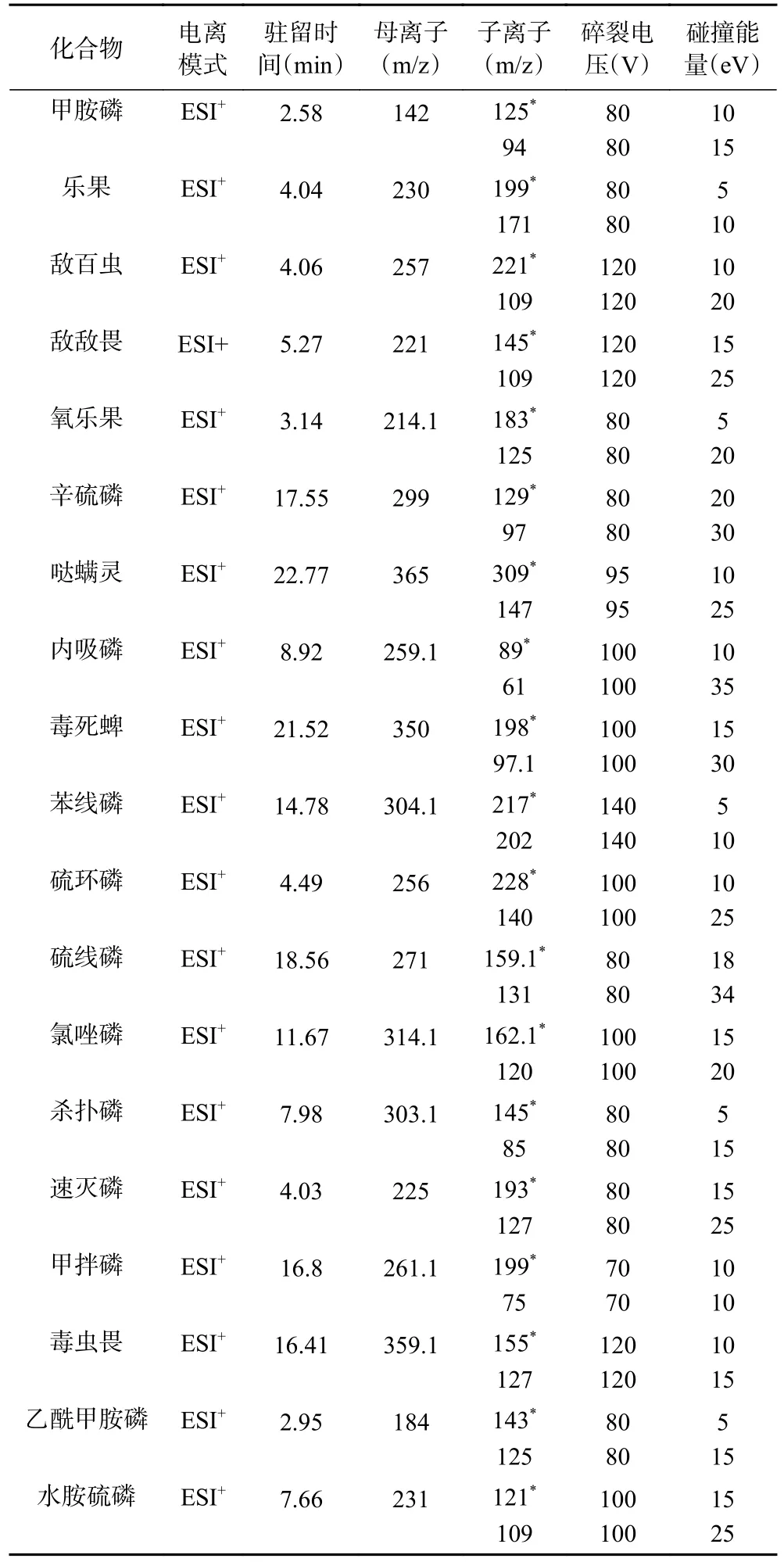
表2 19 种有机磷农药多反应监测模式参数Table 2 Multiple-reaction monitoring (MRM) parameters for 19 organophosphorus pesticides
1.2.5 材料形貌表征 石墨烯磁化前后的形貌,采用SEM 将材料在100000 倍尺度下的形貌进行观察。
1.2.6 萃取性能测试条件 在10 mL 空白样品提取液中加入50 μL 10 μg/mL 的19 种有机磷农药混合标准溶液,使其浓度均为50 μg/L,以回收率为指标,考察Fe3O4@G、G 和Fe3O4对农药的萃取性能,每个实验重复3 次。回收率按式(1)计算。
式中:R 表示萃取回收率,%;Cf表示标曲测得样液中目标物的浓度,μg/L;Vf表示样液最终定容体积,mL;Cq表示加标浓度,μg/L;Vq表示加标体积,mL;F 表示转换系数。
1.2.7 固相萃取优化条件 茶叶中有机磷的提取方法对测定结果至关重要,为达到最佳萃取效果,以10 mL 空白样品提取液中固定每种农药浓度均为50 μg/L,以萃取效率为指标,依据报道[33-34]分别对不同吸附剂用量、萃取时间、溶液pH、解吸溶剂类型和氯化钠用量进行优化,每个实验重复3 次。
吸附剂用量是影响萃取效率的重要参数,吸附剂过少会造成目标物不能被完全吸附,过多会浪费吸附材料。因此实验选取不同质量5.0、10.0、15.0、20.0、40.0、60.0 mg 的Fe3O4@G 材料进行考察。分别在10 mL 空白样品提取液中加入不同量的吸附剂,涡匀振荡吸附20 min 后,进行磁分离,HPLCMS/MS 分析上清液。萃取效率按式(2)计算。
式中:R 表示萃取效率,%;C0表示初始时样液中目标物的浓度,μg/L;Cv表示萃取平衡时标曲测得样液中目标物的浓度,μg/L。
充足的萃取时间是形成动态平衡的关键,磁固相萃取是通过质量传递使目标物在溶液与萃取材料之间形成动态平衡的过程。实验分别考察5、10、15、20、40、60 min 对萃取效率的影响。准确称取40 mg 吸附剂分别加入到10 mL 空白样品提取液中,振荡吸附不同时间后,进行磁分离,HPLCMS/MS 分析上清液。萃取效率按式(2)计算。
样品溶液的pH 影响吸附剂表面的电荷种类、密度及目标物存在状态有着重要的影响,本实验采用甲酸及氨水溶液调节空白样品溶液pH,考察溶液的pH2、3、4、5、6、7、8、9、10、11、12 对有机磷农药萃取回收率的影响。分别准确称取40 mg 吸附剂加入到10 mL 空白样品提取液中,振荡吸附20 min后,进行磁分离,HPLC-MS/MS 分析上清液。萃取效率按式(2)计算。
本实验分别考察四种洗脱有机溶剂,即甲醇、乙腈、丙酮和乙酸乙酯对19 种有机磷农药的洗脱效果。10 mL 空白样品提取液中目标物(固定每种有机磷浓度为50 μg/L)经振荡吸附,磁分离后,弃去上清液,将磁性材料用不同试剂涡旋洗脱,收集全部洗脱液,氮气吹干后,200 μL 乙腈-水(1:9,v/v)溶解,供UHPLC-MS/MS 分析。萃取效率按式(3)计算。
式中:R 表示萃取效率,%;C0表示初始时样液中目标物的浓度,μg/L;V0表示初始时样液的体积,mL;C1表示解吸后标曲测得样液中目标物的浓度,μg/L;V1表示解吸后样液最终定容体积,mL。
在样品前处理中,氯化钠起到盐析作用,使有机相与水相分离,操江飞等[35]研究表明适量的氯化钠更有利于提高蔬果中有机磷回收率。本实验称取1 g 空白绿茶样品,进行加标回收实验,有机磷农药加标水平为100.0 μg/kg,其余前处理步骤按照1.2.3 进行,以回收率为指标,考察氯化钠用量为0.5、1.0、2.0、3.0、4.0、5.0 g 时对盐析的影响。回收率按式(1)计算。
1.3 方法学考察
本实验用乙腈-水(1:9,v/v)溶液配制5~500 μg/L浓度范围的混合有机磷标准溶液,依据1.2.4 色谱-质谱条件进行检测,取不含目标物的空白绿茶样品,按照1.2.3 对样品前处理,采用低中高三个水平进行加标实验,加标水平分别为20.0、40.0、200.0 μg/kg(相当于10、20、100 μg/L),每个水平重复6 次,
1.4 基质效应评价
实际绿茶样品基质复杂,可能含有大量大分子干扰目标物的测定,因此需要评价该实验的基质效应。基质效应(ME)为空白提取液中目标物的峰面积与标准纯样液中目标物峰面积之比[36]。
1.5 实际绿茶样品分析
为验证本研究建立的方法在实际应用中的可靠性,本方法分析20 份绿茶样品,按照GB 2763-2021《食品安全国家标准 食品中农药最大残留限量》[9]与GB 23200.121-2021《食品安全国家标准 植物源性食品中331 种农药及其代谢物残留量的测定 液相色谱-质谱联用法》中茶叶限量的相关规定[32]进行分析。
1.6 数据处理
Agilent MassHunter Workstation Date Acguisition 用于数据采集,Agilent MassHunter Quantitative Analysis 用于数据分析。用WPS Office 计算数据平均值、标准偏差、回收率及相对标准偏差(RSD),使用Origin 85 制图。
2 结果与分析
2.1 石墨烯和磁性石墨烯的表征
石墨烯磁化前后的形貌如石墨烯图(1a)以及Fe3O4@G 图(1b)所示。如图1a 所示,石墨烯具有褶皱的薄纱状片层结构,表面暴露大量的活性位点,为农药吸附提供了大量的空间。从图1b 可以看出,Fe3O4修饰后的石墨烯的基本结构并没有发生改变,仍以薄纱片状存在。石墨烯表面分布大量粒径约为5~50 nm 的Fe3O4纳米粒子,部分纳米粒子稍微有些聚合是由于负载程度已接近饱和的缘故。将Fe3O4纳米粒子修饰在石墨烯上,可能带来以下积极作用:a.Fe3O4是一种常用的MSPE 吸附剂,促进吸附行为[28]。b.Fe3O4提供空间位阻,可有效阻止石墨烯堆叠团聚现象,提高石墨烯在水中的分散性[25-27]。c.Fe3O4被石墨烯夹层包围,可有效减少Fe3O4粒子间团聚和被环境溶液腐蚀的可能,有利于维持其磁性。

图1 石墨烯(a)和磁性石墨烯(b)的扫描电镜图Fig.1 Scanning electron microscope (SEM) images of graphene (a) and magnetic graphene (b)
2.2 材料的农药萃取性能测试
图2 结果表明,Fe3O4@G、G 和Fe3O4对19 种有机磷农药的萃取回收率对分别为89.3%~99.9%、92.3%~105.7%和1.2%~16.5%,说明Fe3O4纳米粒子对19 种有机磷农药吸附作用较弱,石墨烯与19 种有机磷农药之间的吸附作用是萃取过程中的主要作用力。Fe3O4@G 对19 种有机磷农药在萃取过程中可能产生以下若干相互作用力[28]。首先,石墨烯中每个碳原子都含有一个未成键的π电子,可与含有苯环的目标农药形成π-π共轭体系。其次,上述农药结构中可能含有供电子能力的O、N 等,易与Fe3O4@G 结构中大π键形成共用电子对,促进其吸附形成。再次,Fe3O4@G 结构中含有未被还原的羧基基团,也可与农药中电负性强的原子形成氢键作用力。最后,Fe3O4负载在石墨烯表面,可使Fe3O4@G表面带有羟基基团,可能与目标农药化合物中极性基团形成分子间氢键作用力。

图2 Fe3O4@G、G 和Fe3O4 纳米离子对19 种有机磷农药回收率的影响Fig.2 Effect of Fe3O4@G,G and Fe3O4 nanoparticles on the recoveries of the 19 organophosphorus pesticides
为考察不同批次Fe3O4@G 材料吸附性能,实验室对合成3 批次材料进行对比,针对19 种有机磷种农药的萃取回收率均在80%~95%之间,每种农药的相对标准偏差均低于20%,重复性良好。
2.3 磁性固相萃取条件的优化
2.3.1 吸附剂用量对吸附效果的影响 如图3 所示,当Fe3O4@G 用量在5.0~40.0 mg 条件下,前期萃取效率随吸附剂用量的增加而快速升高;当继续增加吸附剂用量,萃取效率基本不变。原因是吸附剂的投加量增加了可利用活性位数量,从而促进了有机磷在Fe3O4@G 上的吸附行为。其中,哒螨灵、毒死蜱、苯线磷、硫环磷和硫线磷最少用量为20.0 mg,其余最少用量均为40.0 mg。为了保证吸附剂的最佳吸附利用率,实验最终确定Fe3O4@G 用量为40.0 mg。

图3 Fe3O4@G 用量对19 种有机磷农药萃取效率的影响Fig.3 Effect of Fe3O4@G amount on extraction efficiency of 19 organophosphorus pesticides
2.3.2 萃取时间对吸附效果的影响 如图4 知,在前10 min 内,有机磷的萃取效率随着时间延长而快速增加;10 min 到20 min,萃取效率随时间缓慢增加;在20 min 时,19 种有机磷的萃取率达到最大,继续延长吸附时间萃取效率没有明显变化。此现象的原因是在反应初期Fe3O4@G 表面有大量未被占据的活性位点,随着反应的进行,剩余可利用的活性位点数量逐渐减少,并且在固液两相中有机磷含量梯度的下降阻碍了Fe3O4@G 的进一步吸附,也影响了有机磷向Fe3O4@G 表面的扩散。因此,将萃取时间定为20 min。

图4 萃取时间对19 种有机磷农药萃取效率的影响Fig.4 Effect of extraction time on extraction efficiency of 19 organophosphorus pesticides
2.3.3 样品溶液pH 的影响 本实验选择溶液pH在2~12 范围对萃取效率的影响(见图5)。其中,溶液的pH 在6~9 范围,敌敌畏萃取效率最佳;溶液的pH 在5~9 范围,甲胺磷、硫线磷和乙酰甲胺磷萃取效率最佳;溶液的pH 在3~10 范围,氧乐果、内吸磷和毒死蜱萃取效率最佳,其余种类的农药溶液的pH在2~12 范围萃取效率均无影响。综上,同时检测绿茶中19 种有机磷农药残留时溶液的pH 在6~9 范围内最佳,绿茶样品经乙腈提取后采用乙腈-水(1:9,v/v)复溶,pH 在7.0 左右,利于19 种有机磷农药的同时萃取,此pH 下萃取效率为92.0%~99.8%。与此同时,考虑到实验操作的简便性,本实验无须调节溶液的pH。

图5 溶液的pH 对19 种有机磷农药萃取效率的影响Fig.5 Effect of pH on extraction efficiency of 19 organophosphorus pesticides
2.3.4 洗脱剂的选择 从图6 可以看出,丙酮和乙腈对19 种目标农药的洗脱效果更佳,乙酸乙酯次之,甲醇相对较差。原因是丙酮沸点低,有机磷的沸点相对较高,萃取吹干过程中沸点低的物质能很好保护沸点高的物质[37]。同时,丙酮可使有机磷更好的溶解,选择丙酮不仅节约氮吹时间,且使有机磷在萃取吹干的过程中损失率降到最低[38],因此选取丙酮作为洗脱剂。

图6 洗脱剂对19 种有机磷农药萃取效率的影响Fig.6 Effect of desorption solvent type on extraction efficiency of 19 organophosphorus pesticides
为将目标分析物从复合物中完全解吸出来,本文优化了洗脱溶剂量,选取丙酮体积分别为1.0、2.0、3.0、5.0、10.0 mL。结果表明当用3.0 mL(1.0 mL×3)丙酮,洗脱复合物时,分析物能被完全解吸。因此选择3.0 mL 丙酮分3 次解吸每次1.0 mL。
2.4 氯化钠用量的选择
结果表明,氯化钠用量0.5~1.0 g 时,氯化钠全部溶解于水中,水相与乙腈相不分离;当氯化钠用量1.0~4.0 g 时,氯化钠全部溶解于水中,水相与乙腈相开始分层,并且随着氯化钠用量的增加,上层分离出的乙腈相增多。由图7 知,当氯化钠用量1.0 g 时,有机磷回收率只有12.3%~35.6%,当氯化钠用量4.0 g时,有机磷回收率在85.8%~95.3%范围;氯化钠用量为4.0~5.0 g 时,氯化钠没有全部溶解,有机磷的回收率基本维持不变。由于氯化钠用量4.0 g 时,整体回收率均优于氯化钠用量1.0 g 时的回收率,故选择氯化钠用量为4.0 g。

图7 氯化钠用量对19 种有机磷农药回收率的影响Fig.7 Effect of sodium chloride dosage on recovery rade of 19 organophosphorus pesticides
2.5 Fe3O4@G 的重复使用性
为了研究Fe3O4@G 吸附剂的重复使用性,按1.2.6 萃取性能测试条件将解吸后的吸附剂重复于有机磷农药的磁性固相萃取实验中,结果表明吸附剂在重复使用15 次之后,Fe3O4@G 对19 种目标农药依然保持良好的萃取能力。
2.6 方法学考察
19 种目标农药线性相关系数均大于0.999。19种目标农药的LOD(S/N=3)为5.0~6.0 μg/kg,LOQ(S/N=10)在15.0~20.0 μg/kg 之间,平均回收率在61.2%~94.9%之间,相对标准偏差RSD(n=6)在2.6%~10.2%之间。由此表明Fe3O4@G 用于绿茶中19 中农药精密度良好,准确度高。具体见表3。

表3 绿茶中19 种农药的线性范围、平均回收率与精密度Table 3 Linear range,average recoveries and relative standard deviation (RSD) of 19 target pesticides in green tea
2.7 基质效应评价
基质效应比较结果如表3 所示,基质中添加三个水平,每个水平重复三次。结果表明,19 种目标农药在空白绿茶基质中的ME 为0.81~0.99 之间,为弱基质抑制效应,因此,本实验可选用溶剂标准溶液外标法进行定量分析。
2.8 实际绿茶样品分析
经分析,在1 份样品中检测到辛硫磷残留,含量为0.04 mg/kg;在1 份样品中检测到哒螨灵残留,含量为0.05 mg/kg;在1 份样品中检测到氧乐果残留,含量为0.025 mg/kg;在1 份样品中检测到毒虫畏残留,含量为0.02 mg/kg;在1 份样品中检测到毒死蜱残留,含量为0.038 mg/kg。其他样品均未检测到上述19 种农药残留。
3 结论
本文采用化学共沉淀法合成磁性石墨烯Fe3O4@G 并成功将其应用于分离富集绿茶中19 种有机磷农药。本实验最佳前处理条件为:复合物用量为40 mg;萃取时间为20 min;氯化钠用量为4 g;洗脱剂为丙酮,洗脱剂用量为3 mL。在最优条件下,方法线性相关系数均大于0.999,19 种有机磷农药的LOD 为5.0~6.0 μg/kg,LOQ 为15.0~20.0 μg/kg,连续6 次重复操作所得相对标准偏差RSD 在2.6%~10.2%之间,在实际样品中有较高的回收率。该方法前处理简单,有机溶剂用量少,适用范围广,材料可重复利用。该技术在复杂样品基质以及极性污染物的富集分离中有很好的参考价值。磁固相萃取是一种新型的样品前处理技术,在本实验中尚存在难以解决的问题:a.需要研究更简便的Fe3O4@G 合成技术;b.尽可能降低本实验的检出限以提高检测准确性与灵敏度。

