强心合剂HPLC 指纹图谱建立及11 种成分测定
高紫薇,吴 磊,林欣荣,陈晓虎*,蒲维娅*
(1.南京中医药大学附属医院,江苏 南京 210029; 2.南京中医药大学第一临床医学院,江苏 南京 210029)
强心合剂是江苏省中医院医疗机构制剂,由国医大师唐蜀华教授根据多年临床经验研制而成[1],在心内科应用多年,由炙黄芪、淡附片、党参、丹参、车前草、玉竹、葶苈子、麦冬8 味中药组成[2],方中黄芪益气升阳,与附子合为君药,共治心衰“虚” 之本; 党参助君药补气功效,丹参凉血活血,消其苦寒之弊,而葶苈子、车前草利水通淋,四者共为臣药; 佐以麦冬、玉竹养阴生津,阴中求阳[3],全方具有加强心肌收缩力、改善舒张功能、减慢心率等作用,主要用于慢性心衰等疾病的治疗[4]。指纹图谱能反映中药复方整体化学信息,使其所含活性成分更直观地呈现出来,从而控制其整体质量[5]。本实验建立强心合剂HPLC 指纹图谱,并同时测定槲皮素-3-O-β-D葡萄糖7-Oβ-D龙胆双糖苷(QGG)、芥子碱硫氰酸盐、芥子酸、大车前苷、毛蕊异黄酮葡萄糖苷、车前草苷D、毛蕊异黄酮、黄芩素、芒刺柄花素、白术内酯Ⅲ、甲基麦冬二氢高异黄酮B 的含量,以期为该方质量控制提供参考。
1 材料
1.1 仪器 安捷伦1260 型高效液相色谱仪,配置DAD 检测器(美国安捷伦公司); BP-211D 型电子分析天平(德国赛多利斯公司); KQ-1000E 型医用超声波清洗仪(昆山市超声仪器有限公司);HH-4 型数显恒温水浴锅(江苏省金坛市荣华仪器制造有限公司); SHZ-DⅢ型循环水式真空泵(巩义市予华仪器有限公司)。
1.2 试剂与药物 槲皮素-3-O-β-D葡萄糖7-O-β-D龙胆双糖苷(QGG)、芥子碱硫氰酸盐、大车前苷、毛蕊异黄酮葡萄糖苷、黄芩素、白术内酯Ⅲ对照品(中国食品药品检定研究院,批号220414、220108、220425、220509、220905、220324); 芥子酸、车前草苷D、毛蕊异黄酮、芒刺柄花素、甲基麦冬二氢高异黄酮B 对照品(江北新区双木实验室检测科技中心,批号 220117、220514、220405、220314、220609)。强心合剂共15 批,编号S1 ~S15,批号20220119、20220130、20220213、20220227、20220310、20220325、20220407、20220418、20220503、20220522),均由江苏省中医院制剂部提供; 各单味药水煎煮液及其阴性制剂均由实验室按制剂工艺制备。8 味饮片经南京中医药大学附属医院药学部专家鉴定为正品,具体见表1。甲醇、乙腈、磷酸为色谱纯; 其余试剂均为分析纯; 水为超纯水。
2 方法与结果
2.1 色谱条件 Agilent Eclipse XDB-C18色谱柱(4.6 mm×250 mm,5 μm); 流动相乙腈(A)-0.01 mol/L 磷酸(B),梯度洗脱(0 ~5 min,2% ~5%A; 5~25 min,5% ~15%A; 25~70 min,15% ~25%A; 70 ~80 min,25% ~40% A; 80 ~90 min,40% ~60% A; 90 ~110 min,60% A); 体积流量1.0 mL/min; 柱温40 ℃; 检测波长230 nm; 进样量10 μL。
2.2 溶液制备
2.2.1 对照品溶液 称取各对照品适量,甲醇制成分别含QGG 0.529 mg/mL、芥子碱硫氰酸盐0.022 mg/mL、芥子酸0.005 mg/mL、大车前苷0.041 mg/mL、毛蕊异黄酮葡萄糖苷 0.050 mg/mL、车前草苷D 0.095 mg/mL、毛蕊异黄酮0.017 mg/mL、黄芩素0.010 mg/mL、芒刺柄花素0.005 mg/mL、白术内酯Ⅲ0.011 mg/mL、甲基麦冬二氢高异黄酮B 0.002 mg/mL 的溶液,0.22 μm微孔滤膜过滤,即得。
2.2.2 供试品溶液 精密量取本品2 mL,加入甲醇2 mL,超声(200 W、40 kHz)处理20 min,取出,静置至室温,用甲醇补足减失的质量,5 000 r/min离心3 min,吸取上清液,0.22 μm 微孔滤膜过滤,取续滤液,即得。
2.2.3 强心合剂制备 按单日处方剂量称取炙黄芪、淡附片、党参、丹参、车前草、玉竹、葶苈子、麦冬共130 g,其中淡附片加10 倍量水先煎15 min,再将药渣和药液与其余7 味饮片合并加到罐中,一煎加5 倍量水浸泡60 min 后煎煮50 min,二煎加4 倍量水煎煮40 min,合并滤液。
2.2.4 单味饮片、阴性样品溶液 按“2.2.3”项下制备工艺制备炙黄芪、淡附片、党参、丹参、车前草、玉竹、葶苈子、麦冬提取液及相关阴性样品,按“2.2.2” 项下方法制备,即得。
2.3 HPLC 指纹图谱建立
2.3.1 精密度试验 取本品 (S1)适量,在“2.1” 项色谱条件下进样测定6 次,以毛蕊异黄酮葡萄糖苷(7 号峰)为参照,测得各共有峰相对峰面积RSD 均小于2.5%,表明仪器精密度良好。
2.3.2 重复性试验 取本品 (S1)适量,按“2.2.2” 项下方法平行制备6 份供试品溶液,在“2.1” 项色谱条件下进样测定,以毛蕊异黄酮葡萄糖苷(7 号峰)为参照,测得各共有峰相对峰面积RSD 均小于2.8%,表明该方法重复性良好。
2.3.3 稳定性试验 取本品(S1)适量,室温下于0、2、4、8、12、24 h 在“2.1” 项色谱条件下进样测定,以毛蕊异黄酮葡萄糖苷(7 号峰)为参照,测得各共有峰相对峰面积RSD 均小于2.7%,表明溶液在24 h 内稳定性良好。
2.3.4 图谱生成 取15 批样品(S1 ~S15),按“2.2.2” 项下方法制备供试品溶液,在“2.1” 项色谱条件下进样测定,将相关数据导入“中药色谱指纹图谱相似度评价系统(2012 版)”,以S1 为参照,采用平均数法,设定时间窗宽度为0.1 min,进行多点矫正、Mark 峰匹配,生成HPLC 指纹图谱、对照图谱(R),共标定20 个共有峰,见图1。

图1 15 批样品HPLC 指纹图谱Fig.1 HPLC fingerprints for fifteen batches of samples
2.3.5 共有峰指认及归属 将对照指纹图谱与对照品保留时间、紫外吸收光谱进行比对,共指认出11 种成分,分别为3 号峰QGG、4 号峰芥子碱硫氰酸盐、5 号峰芥子酸、6 号峰大车前苷、7 号峰毛蕊异黄酮葡萄糖苷、8 号峰车前草苷D、13 号峰毛蕊异黄酮、17 号峰黄芩素、18 号峰芒刺柄花素、19 号峰白术内酯Ⅲ、20 号峰甲基麦冬二氢高异黄酮B,其中毛蕊异黄酮葡萄糖苷分离度较好,峰面积较大,保留时间适中,峰形稳定,并且在所有样品中均存在,故选择其作为参照峰(S),见图2。
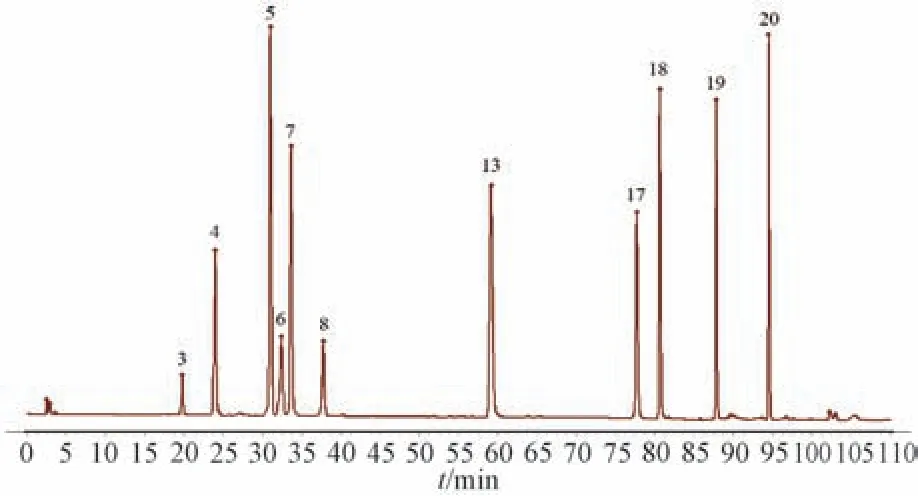
图2 各成分HPLC 色谱图Fig.2 HPLC chromatogram of various constituents
将单味药材及对应阴性样品图谱与样品图谱进行比对,共发现20 个共有峰,见图3。其中,峰7(毛蕊异黄酮葡萄糖苷)、峰13 (毛蕊异黄酮)、峰18 (芒刺柄花素)归属于黄芪,峰19 (白术内酯Ⅲ)归属于党参,峰1~2、10~12、15 ~16 归属于丹参,峰6 (大车前苷)、峰8 (车前草苷D)、峰17 (黄芩素)归属于车前草,峰20 (甲基麦冬二氢高异黄酮B)归属于麦冬,峰3 (QGG)、峰4(芥子碱硫氰酸盐)、峰5 (芥子酸)、峰14 归属于葶苈子,峰9 是丹参、车前草共有成分。

图3 强心合剂特征峰归属Fig.3 Characteristic peak attribution of Qiangxin Mixture
2.3.6 相似度分析 将15 批样品指纹图谱与对照指纹图谱进行比较,计算相似度,结果见表2。由此可知,不同批次样品质量均一稳定,并且所建立的指纹图谱可反映其指纹特征。

表2 15 批样品相似度Tab.2 Similarities of fifteen batches of samples
2.3.7 聚类分析 通过SPSS 26.0 软件对15 批样品进行聚类分析,以20 个共有峰峰面积为变量,平方欧式距离为测量尺度,结果见图4。由此可知,当类间距离小于10 时,各批样品可分为2 类,S2~S4、S8 ~S10、S13 ~S14 为第Ⅰ类,其他批次为第Ⅱ类,表明不同批次样品中各成分含量存在差异,可能与饮片产地、厂家、批次等因素有关,故保持其来源稳定性对强心合剂质量控制具有重要意义。

图4 15 批样品聚类分析树状图Fig.4 Cluster analysis dendrogram of fifteen batches of samples
2.3.8 偏最小二乘法-判别分析(PLS-DA)以20 个共有峰峰面积为变量,采用SIMCA 14.1 软件进行PLS-DA 分析,得分图见图5。由此可知,对X、Y的累积解释能力参数分别为0.735、0.989,预测能力参数Q2为0.944,均大于0.7,表明模型稳定可靠,预测能力强,可用于区分不同批次样品。
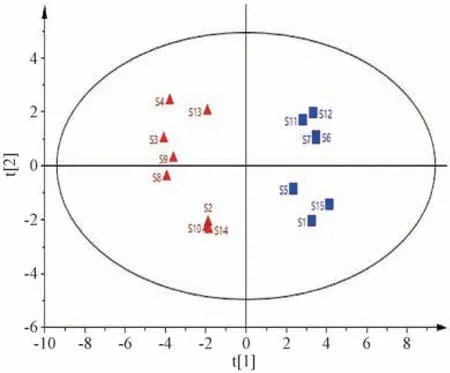
图5 PLS-DA 得分图Fig.5 Score plot for PLS-DA
变量重要性投影(VIP)是基于偏最小二乘回归的一种变量筛选方法[6],可用于评估各共有峰对应主成分对样本分类判别的解释能力,结果见图6。由此可知,各批样品数据均落在95%置信区间内,主要分为2 类,S2 ~S4、S8 ~S10、S13 ~S14为一类,其他批次为一类,与聚类分析结果一致。再以VIP 值>1 为标准筛选主要标志性成分,发现有12 个共有峰符合要求,分别为4 号峰(芥子碱硫氰酸盐)、7 号峰(毛蕊异黄酮葡萄糖苷)、6 号峰(大车前苷)、5 号峰(芥子酸)、1 号峰(未知)、11 号峰(未知)、12 号峰(未知)、2 号峰(未知)、10 号峰(未知)、9 号峰(未知)、13 号峰(毛蕊异黄酮)、14 号峰(未知)。
2.4 各成分含量测定
2.4.1 线性关系考察 取“2.2.1” 项下对照品溶液适量,甲醇逐级稀释,在“2.1” 项色谱条件下进样测定。以对照品峰面积积分值为纵坐标(Y),进样量为横坐标(X)进行回归,结果见表3,可知各成分在各自范围内线性关系良好。

表3 各成分线性关系Tab.3 Linear relationships of various constituents
2.4.2 精密度试验 取“2.2.2” 项下供试品溶液(S1)适量,在“2.1” 项色谱条件下进样测定6 次,测得QGG、芥子碱硫氰酸盐、芥子酸、大车前苷、毛蕊异黄酮葡萄糖苷、车前草苷D、毛蕊异黄酮、黄芩素、芒刺柄花素、白术内酯Ⅲ、甲基麦冬二氢高异黄酮B 峰面积RSD 分别为1.7%、1.4%、2.5%、2.4%、2.4%、1.2%、1.1%、1.0%、1.3%、1.2%、1.0%,表明仪器精密度良好。
2.4.3 重复性试验 取本品 (S1)6 份,按“2.2.2” 项下方法制备供试品溶液,在“2.1” 项色谱条件下进样测定,测得QGG、芥子碱硫氰酸盐、芥子酸、大车前苷、毛蕊异黄酮葡萄糖苷、车前草苷D、毛蕊异黄酮、黄芩素、芒刺柄花素、白术内酯Ⅲ、甲基麦冬二氢高异黄酮B 含量RSD 分别为2.3%、1.2%、2.8%、0.9%、1.2%、0.9%、1.7%、1.2%、1.8%、1.9%、2.4%,表明该方法重复性良好。
2.4.4 稳定性试验 取“2.2.2” 项下供试品溶液(S1)适量,于0、2、4、8、12、24 h 在“2.1” 项色谱条件下进样测定,测得QGG、芥子碱硫氰酸盐、芥子酸、大车前苷、毛蕊异黄酮葡萄糖苷、车前草苷D、毛蕊异黄酮、黄芩素、芒刺柄花素、白术内酯Ⅲ、甲基麦冬二氢高异黄酮B 峰面积RSD 分别为0.6%、1.4%、2.4%、2.9%、1.0%、1.8%、1.2%、2.0%、2.7%、2.8%、0.8%,表明溶液在24 h 内稳定性良好。
2.4.5 加样回收率试验 取各成分含量已知的本品6 份,精密加入对照品溶液适量,按“2.2.2”项下方法制备供试品溶液,在“2.1” 项色谱条件下进样测定,计算回收率。结果,QGG、芥子碱硫氰酸盐、芥子酸、大车前苷、毛蕊异黄酮葡萄糖苷、车前草苷D、毛蕊异黄酮、黄芩素、芒刺柄花素、白术内酯Ⅲ、甲基麦冬二氢高异黄酮B 平均加样回收率分别为101.52%、98.47%、101.56%、101.09%、102.85%、100.68%、99.81%、101.41%、101.22%、100.89%、99.58%,RSD 分别为1.05%、1.25%、1.11%、1.51%、0.76%、1.16%、1.29%、0.87%、1.39%、0.48%、1.74%。
2.4.6 样品含量测定 取 15 批样品,按“2.2.2” 项下方法制备供试品溶液,分别精密吸取10 μL,在“2.1” 项色谱条件下进样测定,计算含量,结果见表4。

表4 各成分含量测定结果(μg/mL)Tab.4 Results of content determination of various constituents (μg/mL)
3 讨论
本实验通过切换不同检测波长 (205、230、260、280、310 nm)发现,11 种成分在230 nm 左右处均有较好吸收,并且强心合剂在该波长下信息丰富。另外,柱温对芥子酸、大车前苷、毛蕊异黄酮葡萄糖苷分离度均有影响,故本实验对不同柱温(30、40 ℃)进行考察,发现40 ℃时各成分目标峰与其他色谱峰的分离情况均较理想。最终,选择230 nm 作为检测波长,40 ℃作为柱温。
强心合剂按照传统工艺进行制备时,所煎煮出的成分大多能溶于水,故本实验对水溶性成分进行研究,包括毛蕊异黄酮、党参炔苷、苯甲酰乌头原碱、丹酚酸B 等20 种[7-20],最终鉴定出11 种,分别为QGG、芥子碱硫氰酸盐、芥子酸、大车前苷、毛蕊异黄酮葡萄糖苷、车前草苷D、毛蕊异黄酮、黄芩素、芒刺柄花素、白术内酯Ⅲ、甲基麦冬二氢高异黄酮B,故将其作为指标成分。
然后,建立了15 批强心合剂HPLC 指纹图谱,发现有20 个共有峰,鉴定出11 个。相似度分析结果表明,不同批次样品之间存在一些差异,但均大于0.93,表明其质量较稳定。根据聚类分析、PLS-DA 分析结果,可将各批样品大致分为2 类,其中导致批次差异的成分有12 种,鉴定出5 种,分别为毛蕊异黄酮、毛蕊异黄酮葡萄糖苷、芥子酸、芥子碱硫氰酸盐、大车前苷,故今后在生产工艺中可通过严格控制其含量来监管全方质量,从而使后者更稳定安全。
4 结论
本实验建立强心合剂HPLC 指纹图谱,并同时测定QGG、芥子碱硫氰酸盐、芥子酸、大车前苷、毛蕊异黄酮葡萄糖苷、车前草苷D、毛蕊异黄酮、黄芩素、芒刺柄花素、白术内酯Ⅲ、甲基麦冬二氢高异黄酮B 的含量,该方法稳定可靠,可较全面地反映该方质量,从而为其质量控制奠定基础。

