生物质水热液化研究进展
张洪伟, 张顺元, 张克江,2*
(1.兰州交通大学 环境与市政工程学院,甘肃 兰州 730000; 2.艾伯塔(成都)环境技术研究院,四川 成都 610000)
目前在各种可利用的再生能源中核能和水电具有潜在的生态环境风险,风能、太阳能、地热能受区域限制,而生物质能以其可再生性、丰富性等特点受到了广泛关注。生物质能的转化主要包括热化学转化与生物化学转化两种方式。与生物化学转化相比,热化学转化克服了生物质在发酵过程中存在的反应时间长、转化效率低、产品提纯能耗高等缺点[1]。热化学转化包括直接燃烧、热解、液化等[2-4]。直接燃烧技术存在热利用效率低且在燃烧过程中会产生大量硫化物和氮氧化物以及粉尘污染等问题[5]。热解技术往往需要在热解前将自然状态下的高含水率生物质进行预先脱水干燥处理[6-7]。水热液化技术是在高温高压(200~350 ℃、 5~25 MPa)下,以水为溶剂,充分利用水在超临界或亚临界状态下的特性将生物质中的大分子物质通过水解、脱羧、脱氨基、再聚合等一系列反应最终生成生物油、水相产物、气体和固体残渣[8-10]。相较于热解,水热液化可处理高含水率生物质,无需脱水等高耗能环节,极具产业化应用价值,成为国内外研究热点。生物质是一种丰富的可再生能源,通常由碳、氢和氧衍生的有机物质组成。这些物质可分为草本植物、木本植物、水生植物及各种有机废物,其通常是有机物和少量无机物的混合物,总体上由纤维素、半纤维素、木质素、脂质及蛋白质组成[11]。通常情况下,绝大多数生物质脂质含量较低,纤维素、半纤维素和蛋白质含量较高[12]。本文从生物质组分及其水热转化的路径综述了纤维素、半纤维素、木质素、脂质和蛋白质的水热转化情况,并就水热液化过程的间歇式反应器和连续式反应器进行详细介绍,全面叙述了生物质水热液化研究的进展。
1 生物质水热液化的发展历程
20世纪20年代德国恩斯特·贝尔教授开展了首次生物质水热液化技术的研究,结果表明:在水热热化和碱催化剂的条件下,由生物质生产生物原油是可行的。自此,生物质水热液化技术逐渐被科研人员应用。1970年美国石油危机爆发后,美国能源部制订了一系列开发生物质能源的计划,开始了对生物质水热液化技术的系列研究。20世纪70年代初期,美国匹兹堡能源中心(PERC)进行了开创性的生物质高压液化研究。PERC工艺是将木材与蔥油的混合浆液在300~370 ℃,25 MPa的条件下反应20~40 min,使其转化为生物油。浆液中木材质量为7%~10%,以Na2CO3为催化剂,并向反应体系中添加体积比3∶2的CO和H2的混合还原性气体以降低产品中的含氧量。该工艺被美国奥尔巴尼工厂试验时发现基质质量分数高于10%的浆液(进入反应器的浆液含有接近90%的循环油)很难向反应器输送,在运行测试期间(572 h),总共生产了5 000 kg以上的生物油,生物油含氧量为12.3%,高位热值为34.52 MJ/kg[13]。
由于在PERC工艺中,进入反应器的物料只有10%~20%是新鲜木材,其余的为循环油,因此该工艺需要大量回收循环油,为了减少循环油回收量,美国劳伦斯伯克利实验室(LBL)建议进行“一次性”工艺改造,将生物质作为水溶液而非油浆送入反应器。LBL工艺是在木材液化之前进行预处理,即将木材在180 ℃,pH值为1.8的条件下预处理45 min,从而达到软化木质纤维的目的。其后的反应流程大致与PERC工艺一致。在pH值的调节过程中,由于基质的pH值较低,因此需要添加大量的Na2CO3催化剂。LBL工艺虽然能显著降低循环油的回收量,但生物油产量较低且产生大量高浓度的有机废水,因此,该项目于1983年末被中止[13-14]。
生物质水热液化的早期研究以木材的液化为主,随着时间的推移,研究者们也开始考虑其他类型的生物质,如废弃植物材料、能源作物等。自2009年开始,人们对藻类水热液化进行了大量研究,以探究微藻、大型藻类和蓝藻生产生物油的机理[15]。Gai等[16]对蛋白核小球藻(CP)和稻壳(RH)在亚临界水中进行了共水热液化,分析了液化温度、停留时间、固体浓度和CP/RH质量比对生物油生产工艺的影响。Kiran等[17]研究了在亚临界水条件下使用高压间歇式反应器对微藻进行水热液化生产生物油并分析了生物油的组成,得出了藻类生物原油主要由呋喃、苯酚、酸和酯及其衍生物组成。此外,还发现通过提高温度可以提高生物油产率。这是聚合反应将小分子物质转化为大分子物质的结果。Toor等[18]在亚临界水条件(220~375 ℃,2~25.5 MPa)下,对湿藻进行了水热液化研究,探索了从湿藻中提取脂质、保存藻类固体残渣中的营养物质以及回收藻类培养的工业废水的可行性,证明了在水热液化过程中藻类固体残留物含有高水平的蛋白质。
水热液化反应机理的探明对于生产高质量的生物原油和高价值的化学品、设计和开发高效的反应器至关重要。目前,尽管许多研究人员如Balat[19]、Peterson[20]、Hietala[21]等多年来一直致力于此研究,但对于生物质水热液化机理的了解仍显不足。通常水热液化过程中,生物质首先通过水解分解为小分子物质,然后通过脱水、脱氢、脱氧和脱羧反应进一步降解为更小分子的物质,最后通过聚合反应合成一些较为复杂的化合物。在聚合过程中生成的产物一般含有酸、醇、醛、酯、酮、酚和其他芳香化合物[22]。由于基质和水热液化产物的多样性以及复杂的中间反应,生物质水热液化反应的确切机理或转化途径仍不清楚。此外,生物质水热液化目前处于实验室中试规模向工业化规模的过渡状态,这使得对其机理的研究更加迫切。
2 生物质组分及水热转化路径
2.1 纤维素
纤维素是自然界含量最多、分布最广的天然有机聚合物,年产量预计可达1.5×1012吨,被认为是取之不尽用之不竭的生物质原料来源[23]。纤维素的通式为(C6H10O5)n,是一种具有高聚合度、高分子质量的长链多糖,由D-吡喃葡萄糖单元以β-1,4糖苷键组成。纤维素在常温下难溶于水,但在302 ℃时可以部分溶解在亚临界水中,在330 ℃时完全溶解。在亚/超临界水中,纤维素首先降解为低聚糖和单糖,继续升高温度,单糖解聚为呋喃衍生物,并最终产生醛和小分子酸[24]。纤维素因其结构中β-1,4葡聚糖链通过链间和链内的氢键紧密结合,形成具有刚性结构的微纤丝,所以不溶于大多数有机溶剂[25]。
纤维素在水热液化过程中可能的转化路径见图1。首先,纤维素在亚临界水中被水解为可溶性和不溶性的葡萄糖。其次,葡萄糖异构化为果糖并通过离子机制进一步分解为5-羟甲基糠醛(5-HMF)及有机酸。5-HMF不仅可以与乙酰丙酸、甲酸或三羟基苯反应,而且自身可能发生聚合反应并生成聚呋喃中间体。此外,纤维素亦可直接通过水热降解为碳氢化合物,但碳氢化合物的结构因反应底物和反应条件而异[26],如Sevilla等[27]提出由芳香化合物所组成的碳氢微球的核-壳模型结构,该碳氢化合物结构核心内部为疏水性芳香化合物,外壳由亲水性、高度氧化性的芳香化合物构成,以及Falco等[26]提出了富呋喃结构。
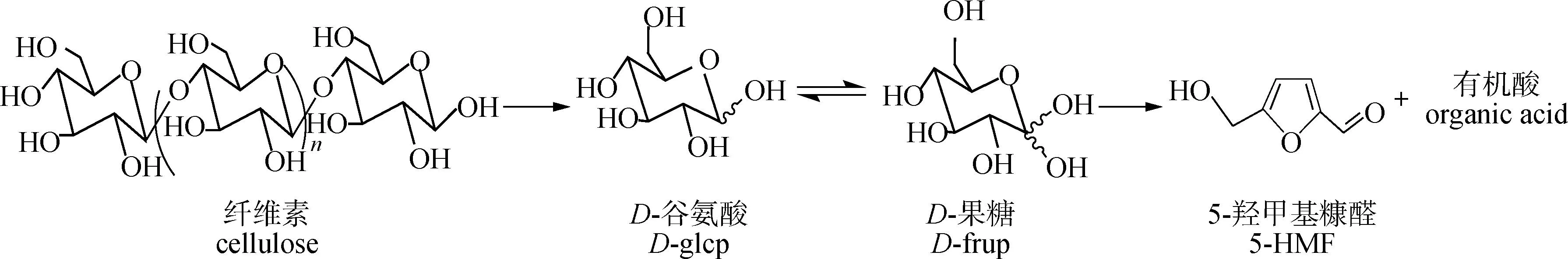
图1 纤维素水热降解主要途径
Möller等[28]研究了纤维素在亚临界水中的水热液化,发现纤维素首先水解为葡萄糖,然后在180 ℃时降解为羟甲基糠醛。Gao等[29]检测到200 ℃时由纤维素制得的生物原油中的主要化合物为4-羟基-4-甲基-2-戊酮和羟甲基糠醛,而羟甲基糠醛在250 ℃时水合转化为乙酰丙酸,随着温度升高至300 ℃,生物油粗相中的化合物以1,4-苯并二恶烷-6-甲醛、苯甲醛、 2,4,5-三甲基为主。当反应温度升至350 ℃时,生物油的成分变得更加复杂,还产生了许多稠合杂环、六杂环和五元杂环化合物。Yin等[30]研究发现:纤维素水热液化反应体系的酸碱性对生物油的组成有很大的影响。在酸性和中性条件下,生物油的主要成分为5-羟甲基糠醛(HMF);在碱性条件下,主要化合物变成C2~C5羧酸。Xu等[31]在氨存在的条件下对纤维素进行了水热液化,发现反应温度的升高和时间的延长可以促进纤维素的转化,并减少固体残留物的量,以及反应温度对固体残留物形成的影响大于反应时间,此外还提出了纤维素在NH3·H2O水热液化过程中形成N-杂环化合物的可能反应途径。Cao等[32]研究发现:催化剂中的过渡金属硫酸盐可以改变纤维素水热液化过程中葡萄糖的选择性,并促进葡萄糖转化为乳酸、乙酰丙酸和甲酸等产物,如Zn2+和Ni2+促进葡萄糖转化为乳酸;Cu2+和Fe3+在高温下促进葡萄糖转化为乙酰丙酸和甲酸。Fraga等[33]提出了一个量化主要反应类型对液化机理贡献的模型,并指出脱水反应是纤维素水热液化的主要反应类型,占总反应的86.2%。
2.2 半纤维素
半纤维素类似于纤维素,也是由基本糖单元构成的高聚物,但其聚合度低于纤维素。半纤维素主链通常由戊糖(如木聚糖)、甘露糖、葡萄糖的交替物(甘露聚糖或葡甘聚糖)、半乳聚糖等组成。值得注意的是,所有半纤维素都有侧链,并影响其在溶剂中的溶解度[34]。植物中半纤维素约占20%~40%,其组分因植物类型的不同而有较大的差异。草本半纤维素主要由木聚糖构成,木本半纤维素则富含甘露聚糖、葡聚糖和半乳聚糖[25]。在谷物秸秆中,半纤维素与纤维素形成氢键,与木质素形成共价键(主要是α-苄基醚键),与乙酰基和羟基肉桂酸形成酯键[35]。Sasaki等[36]提出了D-木糖在360 ℃的亚临界水中分解的主要途径,如图2所示。D-木糖的初级分解有两种反应途径:第一种途径为D-木糖通过反羟醛缩合反应生成乙醇醛和甘油醛,甘油醛经酮-烯醇互变异构转化为二羟基丙酮,或通过脱水反应生成丙酮酸;第二种途径为D-木糖通过脱水反应生成2-糠醛。

图2 亚临界水中D-木糖分解的主要反应路径[36]
Möller等[37]以木糖及其聚合物木聚糖作为半纤维素模型化合物,研究了在160~240 ℃和5~120 min下模型化合物转化为糠醛的反应。木聚糖的转化需要较低的温度(160~180 ℃)以促进聚合物的水解,产生木糖作为糠醛前体。木糖在转化为糠醛的过程中主要副产物为甲酸、二羟基丙酮(通过反羟醛反应形成)和羟基丙酮。此外,在水热液化期间,Zn2+和Ni2+对木糖转化为乳酸表现出明显的影响[32]。Yoon等[38]在180~220 ℃下对郁金香中木聚糖水解反应进行了动力学分析,并研究发现降低反应温度和缩短反应时间可以提高木聚糖转化率和低聚木糖产量。此外半纤维素的其他单糖在水热条件下的液化机制相似,如葡萄糖、果糖、甘露糖和半乳糖的主要液化产物均是乙醇醛、甘油醛和糠醛[39]。Concepción等[40]研究发现:水热液化产物中的糠醛主要通过吡喃糖型木糖的转化产生,而乳酸、甲酸、甘油醛和丙酮醛等降解产物则通过木糖的开环转化产生。
2.3 木质素
木质素主要是由苯基丙烷单元通过C—C和C—O—C键连接而成的无定形、高复杂度芳香聚合物,是自然界中储量仅次于纤维素的第二大生物质资源。木质素具有非晶态无序结构,主要由反香豆醇、松柏醇、芥子醇3种单体构成[41]。其中,松柏醇是软木木质素的主要单体,松柏醇和芥子醇为硬木木质素的主要单体,反香豆醇为软木木质素和硬木木质素的次要单体[42]。一般情况下,木质素可以根据其结构元素分为3类:由紫丁香基丙烷结构单体聚合而成的紫丁香基木质素,由愈创木基丙烷结构单体聚合而成的愈创木基木质素和由对-羟基苯基丙烷结构单体聚合而成的对-羟基苯基木质素[43]。木质素相对耐化学及酶降解,在水热液化过程中,木质素中的醚键会水解形成各种酚,但苯环在水解过程中是稳定存在的[44]。
木质素在水热液化过程中的分解主要可分为三步:1) 水解和裂解C—C键和醚键;2) 脱甲基氧化;3) 烷基化[45]。水解在木质素的水热液化过程中起着至关重要的作用,酚类化合物是木质素的主要水解产物。Kang等[45]检测到木质素水热液化后的产物中酚类化合物的量超过50%。有机酸、醇、酯等化合物在木质素的水热液化产物中也被检出,有机酸和醇可能是由木质素丙基侧链的分解产生的,且可能发生酯化反应产生酯。此外,水热条件下温度的升高会增强愈创木酚的脱甲氧基化,形成邻苯二酚和苯酚[46]。
Barbier等[47]研究发现:木质素在370~390 ℃的亚/超临界状态下,裂解反应和缩合反应同时发生,且二者处于竞争状态。在木质素的水热处理中观察到,芳香环通常不受水热反应的影响,但其取代基与此相反,醚键比C—C键更容易断裂。这一结论与Siskin和Ehara研究结果一致[48-49]。Nagel等[50]系统探索了β-O-4木质素二聚体在175 ℃、不同氢氧化物和碳酸盐浓度下的水热分解,发现弱碱性条件能有效地裂解β-O-4键,其中主要产物为愈创木酚,次要产物为香兰素和乙酰香兰素,提出了键断裂的分子内取代、双分子消除和分子间取代机制,并首次表明β-O-4木质素二聚体水热处理中产生了香兰素。此外,确定了β-O-4木质素二聚体分解的主要途径:在中性条件下,首先形成醌甲酰胺,然后再均解;在碱性条件下转化为稳定的乙烯基醚和高度不稳定的高香兰素。Lui等[51]利用木质素模型化合物阐明了水热条件下α-O-4芳醚键的反应途径:木质素中的α-O-4键经过催化水解,在亚临界水中的主要产物为酚类和链烯苯衍生物,且α-碳上的烷基和苯环上的甲氧基可以显著提高天然木质素中α-O-4键的转化率。
2.4 脂质
脂质是一种非极性有机化合物,主要由脂肪酸、甘油以及自然界中疏水性膜的特定成分组成,在室温下不溶于水。生物质中的脂质主要以三酰甘油酯(TAG)的形式存在,即脂肪酸和甘油三酯[52]。在亚临界条件下,水的介电常数显著降低,具有更大的溶解度[2],在没有催化剂的条件下,脂质很容易被水解为长链脂肪酸和甘油[53]。甘油脱水可进一步生成醇类和醛类,同时长链脂肪酸部分转化为长链烃。长链脂肪酸中的羟基可以与蛋白质水解产生的氨基酸脱氨产生的氨反应,生成脂肪胺类化合物。此外,一定量的长链脂肪酸与脱胺后的氨基酸反应生成酯类。
在水热液化过程中,甘油不会以油相的形式存在,而是转化为水溶性化合物。Lehr等[54]研究发现:在360 ℃,34 MPa和以ZnSO4为催化剂的条件下,甘油可以转化为丙烯醛。Bühler等[52]得出:在亚临界水中甘油降解的主要产物为甲醇、乙醛、丙醛、丙烯醛、烯丙醇、乙醇、甲醛、一氧化碳、二氧化碳和氢气。脂肪酸具有相对较高的热稳定性,在亚临界水中相对稳定[55-56]。King等[55]在330~340 ℃,13.1 MPa的亚临界水中实现了豆油的快速水解,在10~15 min内,游离脂肪酸产率达到90%~100%。但脂肪酸在超临界状态下会通过脱羧生成具有优异燃料性能的长链烃。Chen等[57]在400 ℃密闭系统下制备的植物油液化产物中发现大量C8~C18烯烃和少量C7~C17烷烃,大多数碳氢化合物是不饱和的,这可能是由植物油的氢含量不足造成的。Watanabe等[58]将硬脂酸(C17H35COOH)在400 ℃、 25 MPa的超临界水中处理30 min,其转化率仅为2%,主要产物为烯烃,然而,在反应体系中加入碱金属氢氧化物(NaOH和KOH),增强了硬脂酸的脱羧作用,烷烃产率达到了32%。由此可见在碱性条件下,脂质主要的分解机制是脂肪酸的脱羧。
2.5 蛋白质
蛋白质是微生物或藻类生物质的主要组分之一。微藻含蛋白质量约为43%,远高于大型藻类(15%)。同种藻类的组分因生长环境的不同而差异显著,如微绿球藻含蛋白质量为13%~63%,含脂质量为18%~55%。蛋白质是由一条或多条肽链经过盘曲折叠形成的具有一定空间结构的物质。这些肽链是氨基酸的聚合物,具有高度异质性。氨基酸之间的结构键为肽键,即氨基酸的羧基和胺基之间的酰胺键[44]。相较于纤维素和淀粉中的糖苷键,肽键的结构更稳定,只有在230 ℃左右才会发生缓慢水解[59-60]。在水热液化过程中,蛋白质水解速率非常快,肽键很容易断裂,并产生氨基酸。作为蛋白质的主要组成部分,氨基酸由于其侧链性质的不同而具有异质性,但都具有相同的肽骨架。因此,在水热条件下,所有氨基酸都会经历类似的脱羧和脱氨基反应,脱氨基生成氨和有机酸,脱羧基生成碳酸和胺[44]。这两种反应同时发生,但它们之间也会存在竞争[9]。
Sato等[61]研究发现:脱氨/脱羧的敏感性因底物以及反应介质的pH值而异。脱氨/脱羧发生的概率比因氨基酸的类型而不同。绝大多数氨基酸都发生这2种反应,但天冬氨酸主要发生脱氨反应。这可能是因为与其他氨基酸溶液(丙氨酸、亮氨酸、苯丙氨酸和甘氨酸,pH值5.5~6)相比,天冬氨酸溶液的初始pH值较低,仅为1.8。Alargov等[62]研究了在水热条件下温度对甘氨酸行为的影响。结果表明:氨基酸的脱羧在高温下是有利的,而脱氨反应在低温下发生。Li等[63]研究了丙氨酸在亚/超临界水中的分解,发现:增加丙氨酸的反应物浓度促进了脱羧反应,而不是脱氨反应。蛋白质的水热液化过程中,也伴随着其他反应的进行,如脱水、脱氢以及环化反应。Chen等[64]研究发现:亮氨酸、精氨酸、谷氨酸和天冬氨酸可以通过环化反应生成吡啶,而吡咯来自亮氨酸或脯氨酸的脱羧或脱氢反应。
3 水热液化反应器
3.1 间歇式反应器
与连续式反应器相比,间歇式反应器更容易控制和监测反应过程中的工艺参数[13],因此,间歇式反应器为研究者们的首先选择。间歇式反应器可以采用不可泵送的高含固率的基质,从而使其在反应过程中不会出现诸如堵塞等在连续式反应器中存在的问题。此外,间歇式反应器的基质在反应过程中更易保持均匀。然而,为了实现更高的加热速率和更大的液化产量,间歇式反应器需要配备大功率的搅拌器和加热装置。标准间歇式反应器中的高斜升时间会加剧再聚合反应的发生,从而导致生物油产量降低[65]。一种全尺寸间歇式水热液化反应器如图3所示。
1.进料箱 feeding box; 2.高压进料泵 high pressure feed pump; 3.热交换器 heat exchanger; 4.阀门 valve; 5.间歇反应器
Gundupalli等[66]采用高压搅拌间歇式反应器对椰壳进行亚临界水处理,合成轻质油、原油、天然气和生物炭,该高压搅拌间歇式反应器由不锈钢容器(SS316)组成,设计承受35 MPa的压力和500 ℃的温度。在整个研究过程中,反应器固体负荷保持在10%,搅拌器以150 r/min运行来均匀分配热量,通过向反应器内的SS盘管泵入冷水来实现反应器冷却至室温。Montero等[67]在高温高压间歇式反应器中对微藻进行低温湿法预处理,以降低最终生物原油中氮和氧含量,该高温高压间歇式反应器采用来自美国Autoclave Engineers公司的E010SS 100 mL ezeseal 316SS,带有气体进出口连接、热电偶和冷却盘管,反应器用氮气密封和净化,并使用电加热夹套加热。Fan等[68]探究了污泥间歇水热液化的高附加值产品,其中高压灭菌器由1.4571 Ti不锈钢制成,可承受高达40 MPa的压力和400 ℃的最高温度。间歇式生物原油中氮含量较高,说明在加热和冷却过程中,中间体之间的相互作用和螯合作用增强,导致含氮化合物增多。
3.2 连续式反应器
在大多数间歇式反应过程中,通常通过加热反应物来获得压力,以及使用惰性气体对反应器进行预加压。高压增加了惰性气体在亚/超临界水中的溶解度,从而使预加压的影响越来越小。而在连续反应器中,压力和温度可以单独控制。另外,间歇式反应器的工业应用通常更适用于含固率高、生产数量少和附加值高的产品。对于水热液化生产燃料,因燃料生产量大,如何优化工艺系统控制和减少能耗是确定采用何种反应器的关键。因此大规模生产一般在连续式反应器中实现。
Anastasakis等[69]研究发现:连续式水热液化反应器的热回收率可达66.5%~79.9%。相较于间歇式反应器,连续式反应器升温速率更快,可达100 ℃/min[69],甚至可达200~400 ℃/min[70]。高效的升温速率导致连续式水热液化反应器具有较高的生物原油产量[71-73],并可显著减小反应器的体积。由于生物质的液化一般采用较高的温度和压力,反应器的材质一般采用耐高温、耐腐蚀的特种合金材料,因此,较小的反应器体积也可以大幅降低系统的投资。
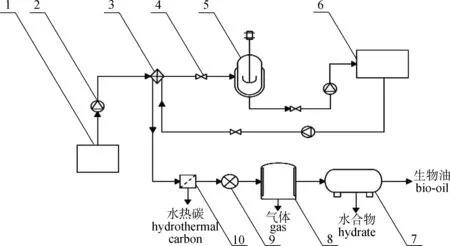
近年来,世界范围内建立了许多不同规模的连续式示范装置,从小的实验室规模到更大规模的工业化应用[74]。美国太平洋西北国家实验室(PNNL)建立了一种连续式水热液化反应器,包括一个连续流搅拌罐反应器和一个水平管式反应器[75-77]。该系统已用于微藻[78]、大型藻类[77]、食物垃圾[75]以及污水污泥[76,79]的水热液化研究,其主要由容量为210 mL的卧式预热器以及容量为415 mL的带搅拌的槽式反应器组成。槽式反应器包括用于保持浆料温度的卧式油夹套反应器和用于在反应条件下去除固体的高温压力过滤器。系统的总体积约为1.6 L,并且以1~2.1 L/h空速运行。澳大利亚悉尼大学设计了一种中试规模的连续式水热液化系统,如图4所示[80]。在该系统中,加压浆料在进入加热器之前在两个热交换器中被预热,加热器由4个浸没在流化床中的不锈钢盘管组成,进入热交换器的浆液被冷却至170 ℃并减压至0.1 MPa,加热器(4个盘管)的总体积约为2 L,通过使用纯水及水和有机溶剂的混合物,证明了该系统适用于微藻和大型藻类。该系统可在超临界(450 ℃和35 MPa)条件下运行[81]。上述2种反应器,均可在亚临界条件(约350 ℃和20 MPa)下运行。

1.生物质浆料罐 biomass slurry tank; 2.阀门 valve; 3.低压螺杆泵 low pressure screw pump; 4.高压进料泵 high pressure feed pump;5.压力控制阀 pressure control valve; 6、 8、 9.热交换器heat exchanger; 7.加热器 heater; 10.减压阀pressure reducing value; 11.气液分离罐 gas-liquid separation tank
4 总结与展望
生物质水热液化由于其良好的转化效果与经济性,已成为利用生物质的首要选择。但在生物质水热液化研究过程中,仍存在一些亟待解决的问题:1) 既有的研究成果基本聚焦于单一的生物质组分在亚/超临界状态下转化过程的分析。生物质中不同组分在相同的水热液化条件下其转化过程是否会相互影响及其影响的机理和转化路径,目前并不清楚; 2) 生物质组分在亚临界或超临界水热液化条件下的反应动力学研究尚未可知; 3) 对大多数生物质原料水热液化的研究仅限于模型化合物的分析,相较于真实生物质具有一定的差异性; 4) 在生物质水热液化过程中,如何得到特定的反应产物,如液化生产液态肥或生物质柴油等; 5) 目前绝大多数生物质水热液化的研究仅限于实验室规模或中试规模,距工业化放大生产还有一定的距离。尽管目前这项具有前景的技术已经取得了长足的进步,但仍有很大的发展空间。随着生物质水热液化技术的研究逐步成熟,上述问题将会逐一解决,在不远的未来将可能在不改变当前燃料利用基础设施的情况下,最大限度地减少对化石燃料的依赖。

