宫颈浸润性复层产黏液性癌1例临床病理分析
李 君 刘 莎
湖北省钟祥市人民医院病理科 431900
宫颈复层产黏液上皮内病变(Stratified mucin-producing intraepithelial lesion,SMILE)由Park等[1]于2000年首次报道,遂后报道非常少,直至2014年第4版WHO女性生殖系统肿瘤分类把SMILE归属于宫颈原位腺癌(AIS)的一种亚型[2]。宫颈浸润性复层产黏液性癌(Invasive stratifiedmucin-producing carcinoma,ISMC)是一种少见的宫颈浸润性癌,由Lastra等[3]于2016年首次报道并命名,与SMILE具有相同的形态学特征,被认为是SMILE的浸润模式。由于ISMC少见,目前对其认识尚不足,本文现报道1例ISMC,并结合文献复习,探讨其临床病理学特征、免疫组化、鉴别诊断及预后,以提高临床病理医师对该疾病的认识。
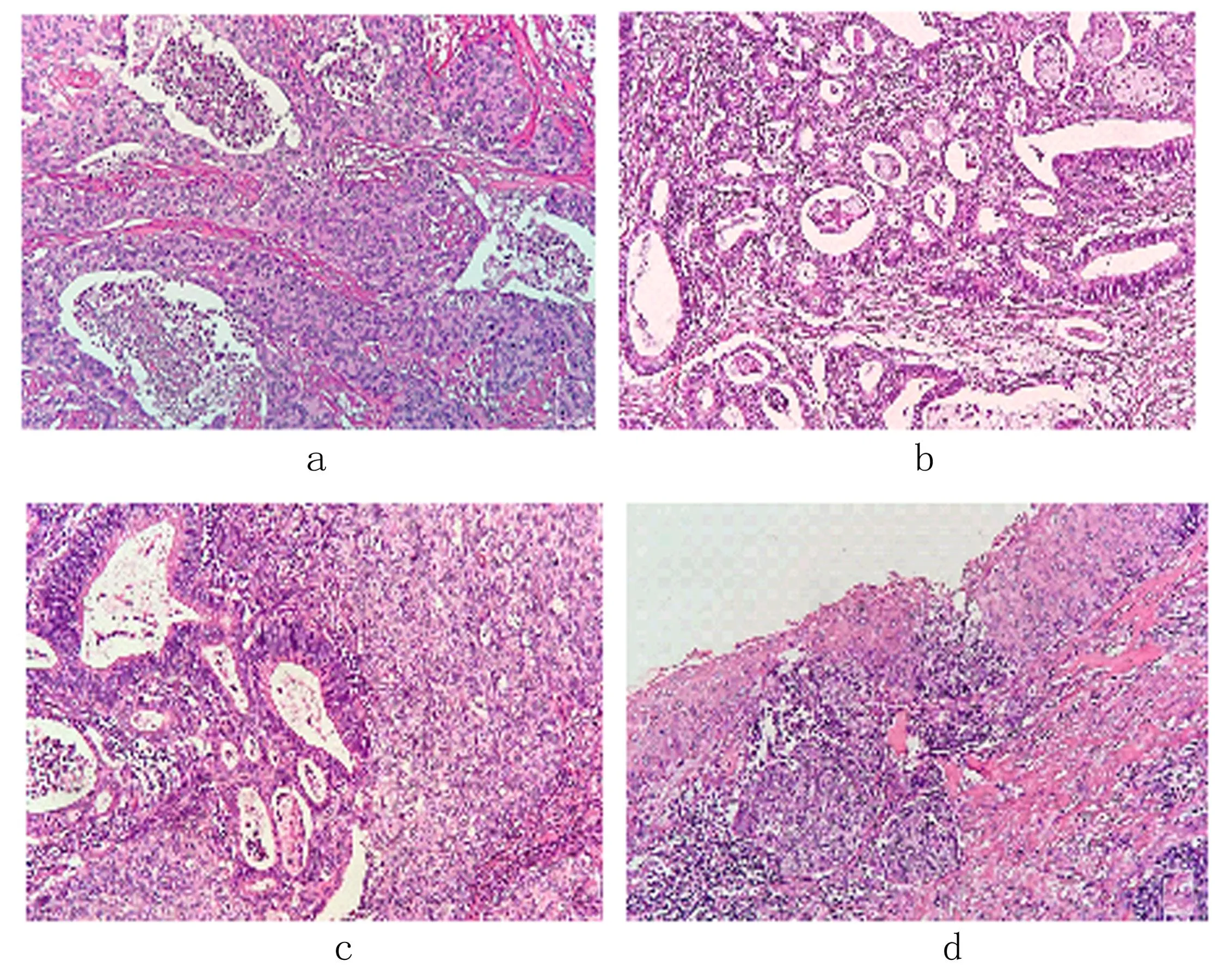
图1 ISMC病理检查
1 病例资料
患者女,60岁,绝经8年,阴道不规则出血半个月,量多,色红。外院彩超示宫颈内可见大小2.9cm×2.6cm低回声团,内见丰富血流信号。TCT示非典型鳞状上皮细胞、意义不明确,HPV示高危型18型阳性。于我院门诊行阴道镜检查+宫颈活检及宫颈管诊刮术,病理诊断为宫颈鳞状细胞癌。后入院治疗,于2022年6月7日行腹腔镜下广泛全子宫+双侧附件切除+盆腔淋巴结清扫术。术中见宫颈后壁可见大小约3cm×2cm病灶,近宫颈内口,宫体正常大小,双侧附件外观正常,双侧盆腔淋巴结未见明显肿大。
2 病理检查
巨检:子宫大小9cm×4cm×3cm,宫颈管后壁近宫颈内口处可见隆起肿块,大小约3.5cm×2cm×0.5cm,切面灰白、实性、质中,侵及肌层,未突破外膜,宫颈外口黏膜光滑,双侧附件外观正常。镜检:术前宫颈活检样本见肿瘤细胞呈实性片块状排列,细胞较大,胞质丰富,嗜碱性,异型明显,核分裂多见,未见明显角化及细胞间桥,活检病理诊断为宫颈鳞状细胞癌。根治术后样本肿瘤组织形态具有多样性,肿瘤细胞大多呈实性片状、巢团状分布;癌巢基底部细胞部分呈栅栏状排列,巢内见大量中性粒细胞(见图1a);部分区域肿瘤细胞形成筛孔状,胞质内含大量黏液,可见黏液湖形成(见图1b);间质纤维增生部分形成分隔,伴玻璃样变性。肿瘤细胞核大小不一,圆形或卵圆形,染色质粗颗粒状,可见核仁,核分裂和凋亡小体易见。少数区域呈典型的高—中分化普通型腺癌结构(占10%)(见图1c),可见小片状HSIL与SMILE共存区域,局灶SMILE突破基底膜向下浸润,与ISMC形成过度(见图1d)。术后再次查阅活检样本切片,可见局部癌巢基底部肿瘤细胞呈栅栏状排列,巢内中性粒细胞浸润,高倍镜下见小片状黏液分泌病灶。由于活检样本局限性及对ISMC认识不足,造成误诊。免疫组化:肿瘤细胞p16(见图1e)、CK8/18(见图1f)、CEA、EMA弥漫强阳性,CK5/6局灶阳性(见图1g)、p63、p40均阴性,Ki67增殖指数较高(ISMC区域约80%、普通型腺癌区域约70%)。特殊染色:对术前活检标本加做PAS染色,可见实性和小片状黏液区PAS染色(+),根治术后样本PAS染色(+)(见图1h)。人乳头瘤病毒(HPV)DNA基因分型检测:HPV18阳性。根治术后样本病理诊断:宫颈浸润性复层产黏液性癌(ISMC),癌组织侵犯宫颈纤维肌壁近全层(>2/3)局部区域合并高—中分化腺癌(约占8%),并见小灶鳞状上皮高级别上皮内病变(HSIL)及SMILE,可见脉管内癌栓,未见明确神经侵犯。双侧盆腔淋巴结未见转移癌。FIGO分期:ⅠB1。
3 讨论
关于宫颈浸润性复层产黏液性癌(ISMC)相关报道较少,临床认识尚不足。查阅国内外相关文献,截至目前共报道病例70余例,且多为个案报道。ISMC患者的发病年龄为29~66岁,其临床表现多为异常阴道出血、接触性出血,少数患者无症状经体检发现。ISMC大小不等,肿瘤最大径0.8~7.5cm,大多呈息肉状外生性生长。
ISMC目前被认为是SMILE的浸润性病变,两者具有相似的组织学特点,典型的特征是复层、未成熟的上皮细胞,多数上皮细胞浆内可见不等的黏蛋白。本例样本中可见小片状HSIL与SMILE共存区域,局灶SMILE突破基底膜向下浸润,形成SMILE与ISMC的过度区域,从组织学上为SMILE微浸润或早期浸润提供有力证据,支持ISMC是SMILE的浸润性病变。
ISMC可以单纯性形态发生,也可以混合性模式存在。混合性成分以普通型腺癌、鳞状细胞癌常见,部分学者报道少见成分包括腺样基底细胞癌[4]和小细胞神经内分泌癌[5]。混合性ISMC组织结构具有多样性,瘤细胞大多呈巢团状、实性片状排列,可见腺样及筛孔状结构。实性巢状结构周围细胞排列呈栅栏状,巢内细胞呈分层状、无极向排列。肿瘤细胞圆形或卵圆形,胞质丰富,嗜碱性,可见核仁,核分裂象易见。癌巢内可见不同比例的黏液细胞分布,并可见多量中性粒细胞浸润,间质促纤维组织增生,肿瘤内砂粒体钙化 。由于ISMC组织形态多样性,术前活检样本很难准确诊断,Lin等[6]报道病例中,仅有40%的活检标本被正确诊断。本文报道病例由于活检标本局限性及对ISMC认识不足,误诊为鳞状细胞癌。因此,需要积累更多的病例,加强对ISMC形态学的认识,提高病理诊断准确性。
免疫表型上,肿瘤细胞弥漫表达p16、CK7,同时Ki-67 增殖指数较高。p63、CK5/6、p40 阴性或基底部细胞局灶阳性。PAS染色可显示肿瘤细胞胞质中的黏液。研究[6-7]报道的病例,均为高危HPV阳性,主要是HPV18型,提示ISMC病变与高危型HPV感染密切相关。
鉴别诊断:(1)黏液表皮样癌:类似唾液腺发生的黏液表皮样癌,包括3种特征性细胞: 表皮样/鳞状细胞、黏液分泌细胞和中间型细胞,缺乏腺样结构。黏液细胞通常位于鳞状细胞癌巢中央,PAS染色阳性。黏液表皮样癌中无原位癌成分,少许中性粒细胞及凋亡碎片,可见ISMC相鉴别。(2)腺样基底细胞癌:罕见于宫颈,常见于绝经后女性,肿瘤由一致的基底样小细胞组成,排列呈小巢状,癌巢周围细胞呈栅栏状排列,与ISMA形态相似。腺样基底细胞癌内无黏液细胞,PAS染色(-)。免疫组化显示基底细胞标志物p63、p40阳性,而ISMC免疫组化p63、p40多阴性,有助于鉴别。(3)毛玻璃细胞癌:是一种分化差的腺鳞癌,肿瘤细胞排列呈实性巢状,可形成微小腺管状结构。细胞多边形,胞膜清楚,胞质丰富,嗜酸性,可见显著的核仁,间质中可见嗜酸性粒细胞和浆细胞浸润,常混合有鳞癌、腺癌等成分。PAS 染色显示胞质阴性,胞膜阳性,可与ISMC鉴别。(4)鳞状细胞癌:鳞状细胞癌中可能存在分散的产黏液的细胞,与ISMC的区别在于,肿瘤细胞呈多边形,具有细胞间桥和角化珠,肿瘤细胞弥漫性表达CK5/6、p63和p40;而ISMC均阴性。
相关报道,ISMC与普通型宫颈腺癌相比,可能更具侵袭性,预后更差,并且有很大的远处转移疾病风险,尤其是肺部。Lastra等[3]报道的8例ISMC,5例获得随访,2例患者分别随访9个月及36个月后发现肺转移,1例患者1.5个月后因盆腔广泛转移死亡。Horn等[7]报道的11例患者中有7例在随访6周~36个月后出现复发或转移,5例患者死于该疾病,提示ISMC预后不佳。本例患者病检提示脉管内瘤栓,随访11个月未复发,目前仍在随访中。由于ISMC罕见,因此需要积累更多的病例及更长时间判断其预后。

