下肢动脉硬化闭塞症并发重度肢体缺血性坏疽伴感染患者血管腔内介入术后截肢风险预测模型的构建
李树森,姚书格,吴广迎,张雪峰,刘皓
邢台医专第二附属医院介入血管外科,河北邢台 054000
下肢动脉硬化闭塞症(ASD)是指动脉硬化造成下肢血管狭窄或闭塞,并引起肢体发冷、疼痛,甚至溃疡、坏死等一系列慢性缺血性疾病。ASD 并发重度肢体缺血性坏疽伴感染的发生率为5%~10%[1-2]。目前ASD 的治疗主要通过改善循环、适当运动等改善患者的生活质量,严重缺血者可通过血管腔内介入治疗进行干预,以降低截肢率[3]。但对于已经并发重度肢体缺血性坏疽伴感染的ASD 患者,即使行血管腔内介入治疗,术后仍有较高的截肢率。因此,了解影响介入治疗后截肢的危险因素,对指导临床治疗有重要意义。本研究通过探讨并发重度肢体缺血性坏疽伴感染的ASD 患者血管腔内介入术后截肢的影响因素,建立术后截肢风险预测模型,旨在为临床治疗提供参考。
1 资料与方法
1.1 临床资料 选择2019 年1 月—2022 年1 月我院收治的106 例并发足部重度肢体缺血性坏疽伴感染的ASD患者,男72例、女34例,年龄18~76(63.1 ±5.3)岁。纳入标准:年龄≥18 岁;ASD 的诊断符合《下肢动脉硬化闭塞症诊治指南》中的标准[4],下肢动脉缺血卢瑟福分级5~6 级;感染的诊断参照Wagner分级[5];截肢组均为单肢截肢。排除标准:已使用抗菌药物;精神异常或认知功能异常;临床资料不完整。患者均行血管腔内介入手术治疗,术后随访1 年,根据是否截肢将患者分为截肢组与非截肢组。本研究经过我院医学伦理委员会审核,患者均自愿参与并签署知情同意书。
1.2 术后截肢影响因素收集 ①临床资料:包括性别、年龄、病程、身体质量指数(BMI)、踝肱指数(ABI)、基础疾病(糖尿病、高血压、冠心病等)、吸烟及饮酒情况等。ABI 检测方法:患者仰卧,用12 cm × 40 cm 气袖分别置于双侧踝部及上臂,用多普勒听诊器协助测量足背或胫前动脉、胫后动脉以及肱动脉收缩压,两者之比即为ABI。②实验室指标:于介入术前采集患者静脉血,使用血细胞分析仪检测白细胞(WBC)、血小板(PLT),计算中性粒细胞/淋巴细胞比值(NLR)、血小板/淋巴细胞比值(PLR);使用全自动生化仪检测空腹血糖(FPG)、血红蛋白(Hb)、白蛋白(Alb),免疫荧光干式定量法检测血清C反应蛋白(CRP),ELISA法检测血清降钙素原(PCT)。③感染程度:参照Wagner 分级。穿透性溃疡,并发软组织感染(红肿热痛及流脓),但无脓肿及骨髓感染为轻度;深部溃疡,并发深部脓肿或骨髓感染,但生命体征平稳为中度;缺血性溃疡,并发全身脓毒血症,生命体征不平稳为重度。④病原菌:采集患者感染部位渗出液,使用全自动微生物分析系统(梅里埃)ATB Compact 进行病原菌分析。质控标准:以肺炎克雷伯菌ATCC700603 作为阳性对照,大肠埃希菌ATCC25922作为阴性对照。
1.3 术后截肢预测模型建立 采用联合应用ROC理论模式(即LogP 模式),根据筛选出的危险因素和回归系数建立风险预测模型。
1.4 统计学方法 采用SPSS23.0 统计软件。计量资料采用单样本K-S 检验变量是否符合正态分布,符合正态分布且方差齐的计量资料以±s表示,组间比较采用LSD-t检验;计数资料以例(%)表示,组间比较采用χ2检验。影响因素分析采用多因素非条件Logistic 回归,采用逐步后退法进行变量的选择和剔除。对影响术后截肢的危险因素绘制受试者工作特征(ROC)曲线,根据曲线下面积(AUC)分析预测模型的预测价值。P<0.05 为差异有统计学意义。
2 结果
2.1 两组术后截肢影响因素比较
2.1.1 两组临床资料比较 截肢组20例,男12例、女8 例,年龄(63.3 ± 5.45)岁,病程(60.16 ± 12.54)d,BMI(23.64 ± 1.11)kg/m2,合并糖尿病14例、高血压7例、冠心病2例,吸烟10例、饮酒2例,卢瑟福分级5级7例、6级13例,ABI为0.51 ± 0.11;非截肢组86例,男60 例、女26 例,年龄(63.1 ± 5.55)岁,病程(60.22 ±14.12)d,BMI(23.23 ± 1.31)kg/m2,合并糖尿病36例、高血压20例、冠心病10例,吸烟24例、饮酒10例,卢瑟福分级5级56例、6级30例,ABI为0.78 ± 0.10。截肢组年龄、ABI及合并糖尿病、卢瑟福6 级、吸烟比例均高于非截肢组(P<0.05 或<0.01)。
2.1.2 两组实验室指标比较 截肢组WBC、NLR、PLR、CRP、PCT高于非截肢组,Alb、Hb低于非截肢组(P<0.05或<0.01)。见表1。
表1 两组实验室指标比较(± s)

表1 两组实验室指标比较(± s)
注:与截肢组比较,*P<0.05,**P<0.01。
?
2.1.3 两组感染程度比较 截肢组感染程度轻度2 例、中度6 例、重度12 例,非截肢组感染程度轻度56 例、中度25 例、重度5 例,截肢组重度感染比例高于非截肢组(P<0.05)。
2.1.4 两组病原菌分布比较 106 例患者感染部位渗出液样本中共检出148 株病原菌,其中截肢组34株、非截肢组114株。截肢组奇异变形菌、大肠埃希菌检出率高于非截肢组,非截肢组铜绿假单胞菌、金黄色葡萄球菌检出率高于截肢组(P均<0.05)。见表2。

表2 两组病原菌分布比较[株(%)]
2.2 ASD 并发重度肢体缺血性坏疽伴感染患者血管腔内介入术后截肢的影响因素分析结果 多因素Logistic 回归分析结果显示,合并糖尿病、卢瑟福分级6级、重度感染、ABI降低、感染病原菌为奇异变形菌、Alb 及Hb 水平降低是ASD 并发重度肢体缺血性坏疽伴感染患者血管腔内介入术后截肢的危险因素(P均<0.05)。见表3。
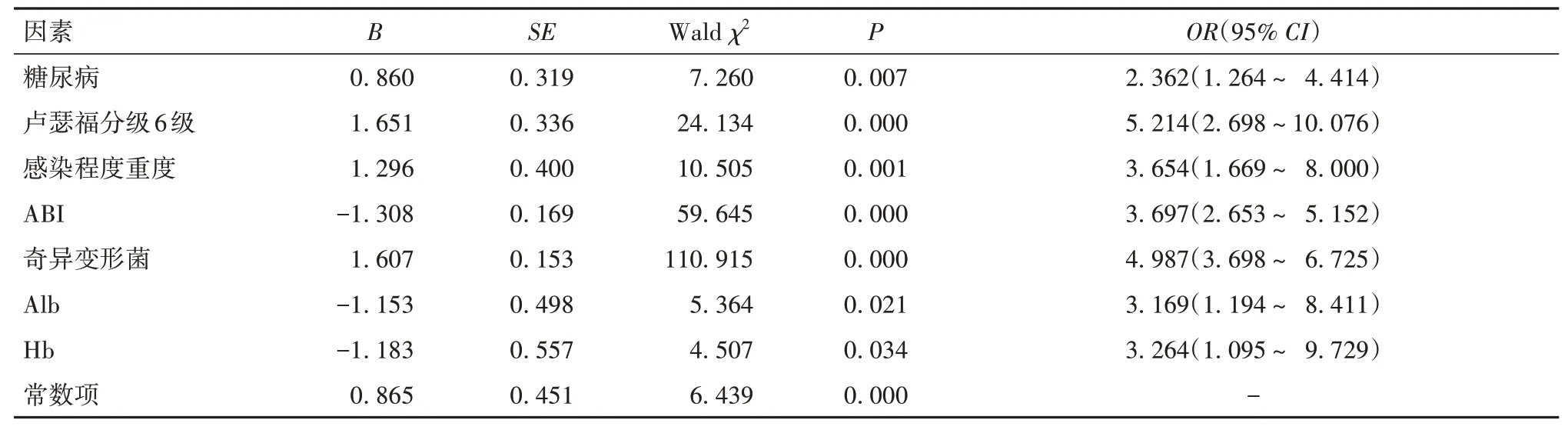
表3 影响ASD并发足部重度肢体缺血性坏疽伴感染患者截肢的多因素Logistic回归分析结果
2.3 ASD 并发重度肢体缺血性坏疽伴感染患者血管腔内介入术后截肢预测模型的构建结果及其预测价值 以多因素Logistic 回归筛选出的危险因素构建预测模型为0.865+0.860×糖尿病+1.651×卢瑟福6 级+1.296×重度感染-1.308×ABI+1.607×奇异变形菌-1.153×Alb-1.183×Hb。该模型预测术后截肢的AUC 为0.904(0.824~0.982),敏感度为94.0%,特异度为87.4%。见图1。
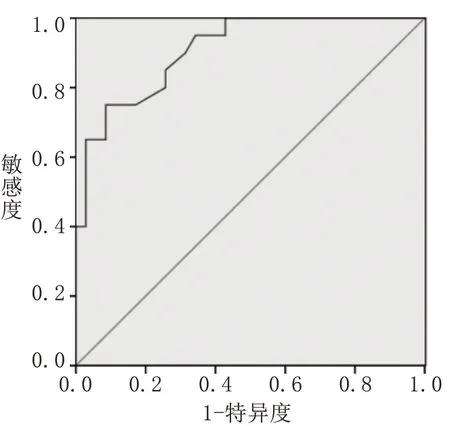
图1 预测模型预测术后截肢的ROC曲线
3 讨论
血管腔内介入治疗可显著降低ASD 患者的截肢率,但对于已经并发足部重度肢体缺血性坏疽伴感染的患者,介入术后截肢率仍比较高。本研究结果显示,并发足部重度肢体缺血性坏疽伴感染的ASD 患者行血管腔内介入术后随访1 年,截肢率为18.9%。分析其原因可能是由于ASD已存在下肢血管动脉硬化,并发重度肢体缺血性坏疽伴感染者多为Wagner 分级为2 级以上者,该类患者可能已存在神经病变,因此即使通过腔内介入治疗改善了血液循环,但神经损伤后神经营养障碍不易恢复[6],随着时间延长,感染症状会复发或进一步加重,最终导致截肢。临床上了解并发足部重度肢体缺血性坏疽伴感染的ASD 患者血管腔内介入术后截肢发生的危险因素,可以提前给予必要的干预,以减少该疾病发生风险或降低其严重程度。
本研究结果显示,截肢组年龄、ABI、合并糖尿病、卢瑟福6 级、吸烟史比例高于非截肢组;截肢组炎症因子WBC、NLR、PLR、CRP、PCT 高于非截肢组,营养指标Alb、Hb 低于非截肢组;截肢组重度感染比例高于非截肢组;两组病原菌分布亦存在差异。多因素Logistic 回归分析发现,合并糖尿病、卢瑟福分级6级、重度感染、ABI低、病原菌为奇异变形菌、Alb 及Hb 水平降低是ASD 并发足部重度肢体缺血性坏疽伴感染患者截肢的危险因素。糖尿病患者本身可能已经存在下肢微血管病变,甚至已经并发糖尿病足,而介入术仅能改善大血管病变,微循环障碍会严重降低介入手术的临床获益[7]。此外糖尿病患者多存在胰岛素抵抗,对于重度肢体缺血性坏疽伴感染患者,胰岛素抵抗与机体炎症反应之间不仅相互促进,且可以共同促进血小板聚集与活化,增加术后血栓形成[8]。卢瑟福6 级及重度感染者多为全身性感染,该类患者常常存在生命体征不稳定,容易出现感染性休克,因此介入术后由于血容易不足亦不能有效改善坏疽组织的血液循环,保证侧支循环的有效建立[9-10]。ABI 与下肢血液供应呈正相关,有研究认为,ABI 不会影响ASD 血管腔内介入治疗成功率[11],但对于并发重度肢体缺血性坏疽伴感染的ASD 患者,远期生存率及保肢率会降低,提示ABI降低会增加ASD 并发重度肢体缺血性坏疽伴感染患者介入术后截肢风险。张杉杉等[12]报道,Wagner 3~5 级的下肢重度肢体缺血性坏疽伴感染者奇异变形菌感染率明显高于Wagner 1~2 级者。因此,了解病原菌分布对指导临床早期使用抗菌药物有重要意义,但病原菌增加介入术后截肢风险的机制尚不明确,可能与奇异变形菌为厌氧菌,其产生的前列环素具有强烈的缩血管作用有关[13]。重度肢体缺血性坏疽伴感染的恢复需要充足的营养支持,机体营养状况差感染不易控制、机体免疫力进一步降低形成恶性循环[14-15]。Alb、Hb是机体营养状况的主要评估指标[16],其水平越低,感染越重,即使介入手术改善血液循环,随着时间延长,皮肤、肌肉等组织缺乏足够营养支持,坏疽不易愈合甚至加重,最终因挽救生命而截肢。
本研究根据ASD 并发足部重度肢体缺血性坏疽伴感染患者血管腔内介入术后截肢的各项危险因素构建预测模型,结果显示,该预测模型的AUC 为0.909,灵敏度为94.0%,特异度为87.4%,提示该预测模型对ASD 并发足部重度肢体缺血性坏疽伴感染患者血管腔内介入术后截肢有较高的预测价值,临床上可进行多项指标联合预测以提高临床应用价值。
综上所述,ASD 并发重度肢体缺血性坏疽伴感染患者血管腔内介入术后仍有较高截肢率,糖尿病、重度感染、ABI<0.52、奇异变形菌等可显著增加术后截肢风险,由上述危险因素构建的预测模型对ASD并发重度肢体缺血性坏疽伴感染患者血管腔内介入术后截肢有较高的预测价值。

