高效液相色谱-串联质谱法测定牛组织中马波沙星残留方法的研究
贾兴,黄凯,李红园★,耿智霞,瞿红颖,刘静,宋婷婷,邓彦宏
(1.河北远征药业有限公司,河北石家庄 050041;2.河北省兽药技术创新中心,河北石家庄 050041;3.石家庄市兽药技术创新中心,河北石家庄 050041;4.吉林大学动物医学学院,吉林长春 130000)
1 引言
近年来, 喹诺酮药物长期使用导致动物产生耐药性[1-3]。 马波沙星是动物专用的氟喹诺酮类抗菌药,在欧盟、新西兰等国家应用广泛,用于治疗猪乳房炎-子宫炎-无乳综合征(MMA)以及牛的呼吸道感染和由大肠杆菌引起的乳腺炎[4]。马波沙星在体内吸收迅速,分布广泛,生物利用度高,具有抗菌谱广、活性强等诸多优点,对革兰氏阳性菌、革兰氏阴性菌及支原体都具有很强的抗菌活性[5]。 国内批准的马波沙星注射液可用于猪的临床疾病的治疗,仅有法国诗华进口注册的马波沙星注射液课用于靶动物牛。 本试验建立了一种高效液相色谱-串联质谱测定马波沙星的检测方法,可用于牛组织中马波沙星残留量的检测。
2 材料与方法
2.1 仪器与设备
液相色谱-串联质谱仪(岛津,LCMS-8045);电子天平(赛多利斯,QUINTIX125D-1CN);高速组织均质机 (安徽博进化工机械有限公司,BRS500);台式冷冻离心机(长沙湘仪离心机仪器有限公司,H1850R);旋涡混合器(其林贝尔,XW-80A);旋转蒸发仪(上海亚荣,RE-52AA)。
2.2 药品与试剂
马波沙星标准物质(批号H0801511,中国兽医药品监察所);乙腈(色谱纯,Fisher 公司);甲醇(色谱纯,Fisher 公司);甲酸(色谱纯,Merck);水(GB/T 6682 规定的一级水);其他试剂均为国产分析纯。
2.3 试液配制
2.3.1 标准储备溶液 取马波沙星标准品10毫克,精密称定,用乙腈溶解并定容于50 毫升棕色容量瓶中,置冰箱中避光保存。
2.3.2 标准中间溶液 精密量取马波沙星储备溶液5 毫升于100 毫升棕色容量瓶中, 用乙腈溶液溶解并定容至刻度,置冰箱中避光保存。
2.3.3 样品溶解液 乙腈溶液+0.1%甲酸的水溶液。
2.3.4 空白样品基质溶液 采用不含待测组分的空白样品制备。
2.4 方法
2.4.1 样品前处理
取组织样品约20 克,完全切碎后经高速均质机捣碎,用四分法缩分出适量试样,称取2 克试样(冷冻试样应解冻至室温),加乙腈-10%三氯乙酸溶液10 毫升,10000 转/分钟匀浆3 分钟, 用样品提取液5 毫升洗刀头和匀浆杯,合并样液,漩涡30 秒,4℃条件下10000 转/分离心6 分钟,上清液用10 毫升水稀释备用。
SPE 柱经甲醇3 毫升活化, 水3 毫升平衡。将备用液过柱,样液过柱速度约为1 毫升/分钟。经10%甲醇3 毫升淋洗,负压抽干,甲醇3 毫升洗脱,抽干。洗脱液于60℃氮气流吹干,用1.0 毫升乙腈-0.1%甲酸水溶液溶解残渣, 混匀,4℃条件下12000 转/分离心6 分钟, 取适量溶液经0.22 微米滤膜过滤至样品瓶中,供液相色谱-串联质谱仪测定。
2.4.2 液相色谱条件
色谱柱为C18(125×2.0 毫米,3.0 微米);流动相:0.1%甲酸/乙腈溶液+0.1%甲酸/水溶液,梯度洗脱(梯度洗脱时间表见表1); 流速:0.3 毫升/分;柱温:30℃;进样量:20 微升。

表1 液相色谱梯度洗脱条件
2.4.3 质谱条件
离子源:电喷雾离子源;扫描方式:正离子扫描; 检测方式: 多反应监测 (MRM);DL 温度:350℃; 检测器电压:2.0 千伏; 加热器流量:600升/小时;雾化气流量:500 升/小时;干燥气流量:500 升/小时;MRM 参数(见表2)。

表2 MRM 参数列表
2.5 方法确证
2.5.1 特异性
分析不同来源空白牛组织(牛肌肉、肝脏、肾脏、脂肪)样品(n=20),观察在药峰出现的区域是否有干扰信号。
2.5.2 标准曲线
分别设置6 个不同浓度的标准工作溶液,依次为5、10、20、50、100 和200 纳克/毫升,依据设定浓度加入标准品,将所得峰面积为纵坐标,以相应的浓度为横坐标绘制基质标准曲线,得到相应的基质标准曲线方程与相关系数。
2.5.3 方法的准确度与精密度
通过添加回收试验验证方法的准确度与精密度,分别用回收率和变异系数表示准确度和精密度。 选择以10、50、100 纳克/毫升进行添加回收。每批3 个不同浓度,每个浓度5 个平行样品,重复3 批,分别计算回收率、批内变异系数和批间变异系数。
3 试验结果
3.1 特异性
在上述色谱工作条件下, 分析不同来源的空白牛肌肉、肝脏、肾脏、脂肪组织样品,目标化合物的保留时间附近没有杂质干扰,马波沙星的色谱峰保留时间为4.0 分钟左右。
3.2 重复性
选择10 纳克/毫升浓度做重复性实验,每个组织样品重复测6 次。 得到牛肌肉组织中马波沙星含量测定重复性保留时间RSD 值为1.265%,峰面积的RSD 值为2.290%;牛肝脏组织中马波沙星含量测定重复性保留时间RSD 值为0.264%,峰面积的RSD 值为0.806%;牛肾脏组织中马波沙星含量测定重复性保留时间RSD值为0.138%,峰面积的RSD 值为0.658%;牛脂肪组织中马波沙星含量测定重复性保留时间RSD 值为0.117%,峰面积的RSD 值为2.279%。均小于5%。 系统适应性良好。
3.3 测定低限
测得牛奶中马波沙星的测定低限为10.0 微克/千克。
3.4 线性范围
在10~200 纳克/毫升的浓度范围内,方法的线性关系良好,牛肌肉组织、肝脏组织、肾脏组织、 脂肪组织基质标准曲线的相关系数 (R)≥0.999,标准曲线回归方程如表3 所示。

表3 基质标准曲线回归方程及相关系数
3.5 准确度和精密度
马波沙星的添加回收率和精密度见表4 和表5。 从表4、表5 中可得出,牛肌肉组织中在10、50、100 纳克/毫升浓度的回收率在77.1%~101.4%;批内变异系数均小于2.16%,批间变异系数均小于9.77%;牛肝脏组织中在10、50、100纳克/毫升浓度的回收率在81.2%~100.3%;批内变异系数均小于2.01%, 批间变异系数均小于2.29%;牛肾脏组织中在10、50、100 纳克/毫升浓度的回收率在83.8%~97.0%;批内变异系数均小于1.41%,批间变异系数均小于3.80%;牛脂肪组织中在10、50、100 纳克/毫升浓度的回收率在80.3%~107.6%;批内变异系数均小于5.63%,批间变异系数均小于11.53%。
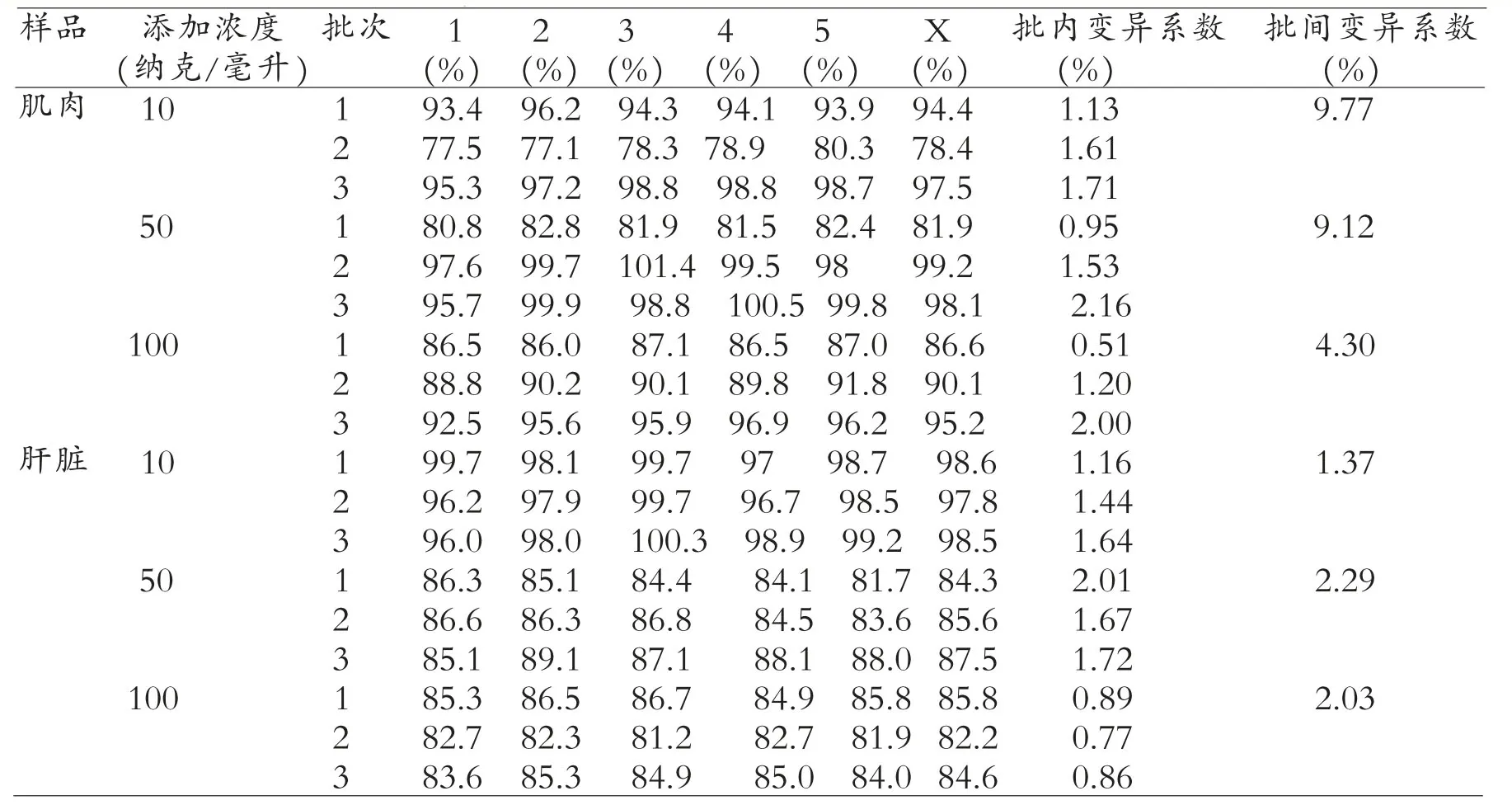
表4 不同批次牛肌肉、肝脏组织样品中添加马波沙星的回收率和变异系数
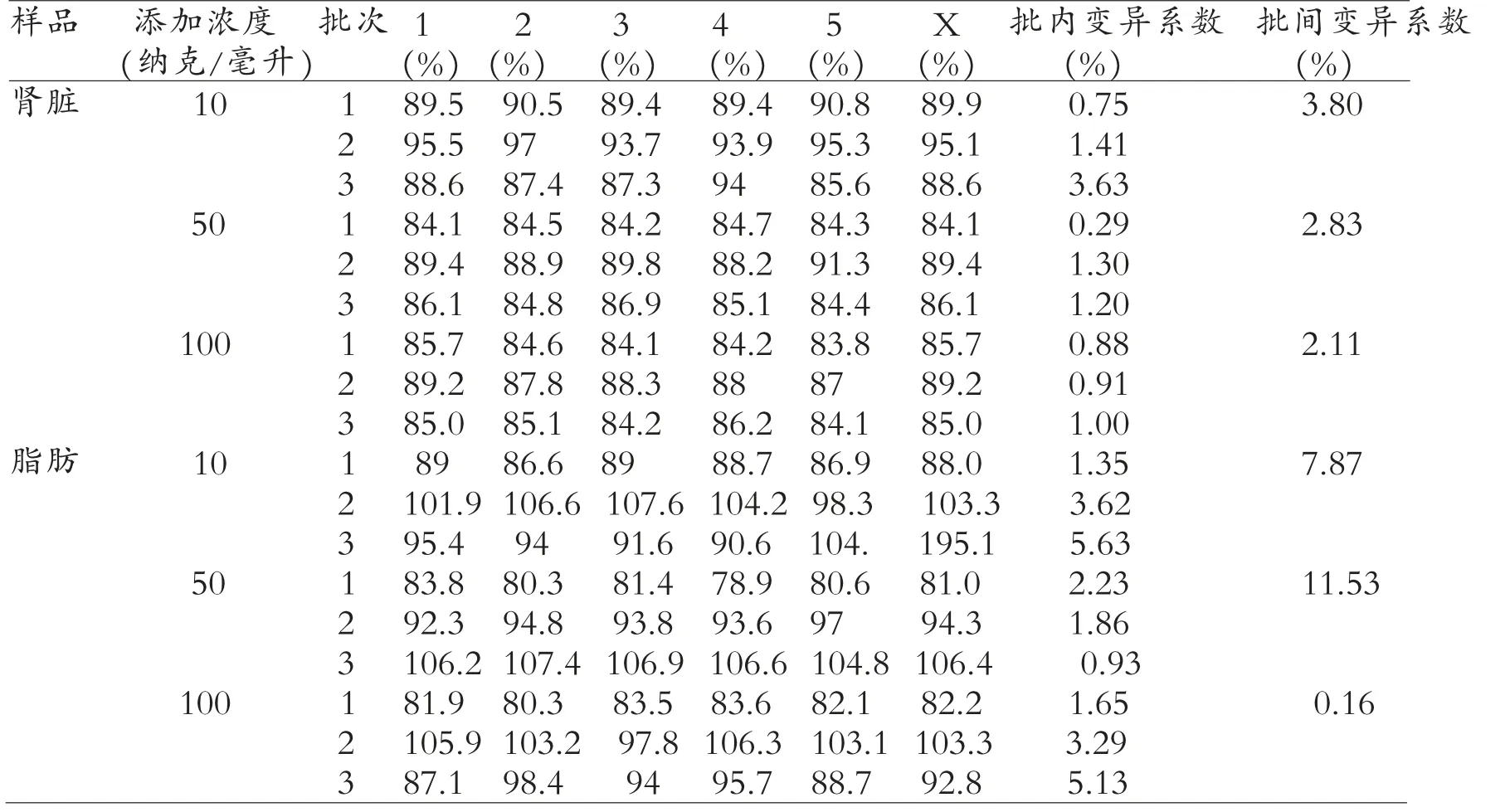
表5 不同批次牛肾脏、脂肪组织样品中添加马波沙星的回收率和变异系数
4 讨论
近年来,随着氟喹诺酮类药物的普遍使用,其残留检测技术已被国内外广泛研究,目前的检测方法主要包括高效液相色谱法、 液相色谱/串联质谱法、毛细管电泳法、酶联免疫法等[6]。 本实验建立了牛肌肉、肝脏、肾脏、脂肪组织中马波沙星残留液相色谱-串联质谱测定方法,方法专属性良好,空白基质中目标化合物的保留时间附近没有杂质干扰。 方法在牛肌肉、肝脏、肾脏、脂肪组织中的测定低限可设定为10.0 微克/千克;基质标准曲线范围为10~200 纳克/毫升, 相关系数>0.998;在牛的肌肉、肝脏、肾脏及脂肪组织样品中, 马波沙星在10、50、100 纳克/毫升浓度的平均回收率在70%~120%, 批内变异系数CV≤10% , 批间变异系数 CV ≤15%。 结果表明该方法的重复性、 灵敏度、线性范围、准确度、精密度能够满足残留检测要求。
5 结论
本研究针对新兽药马波沙星注射液应用后在牛组织中的残量检测,建立了高效液相-串联质谱法。 该方法可用于检测牛肌肉、 肝脏、肾脏及脂肪等多种组织中马波沙星药物的残留量,并且经试验研究验证,该方法的灵敏度、准确度与精密度均良好。
(支持项目: 河北省省级科技计划资助(21322601D))

