MECT联合帕罗西汀治疗抑郁症伴失眠患者的疗效及对血清神经递质的影响
闫美丽,廖飞文
(湖北科技学院附属第二医院,湖北 咸宁 437100)
抑郁症是常见的精神致残性疾病,患者主要特征表现为持久性心境低落和兴趣缺失,并可伴随失眠症状[1]。随着人们生活方式的改变及社会生活压力的增大,抑郁伴失眠的发病率逐年递增,给社会造成极大的疾病负担。目前,对于抑郁症伴失眠患者,临床主要应用抗抑郁药联合安眠药进行干预,帕罗西汀是临床常用药物,虽可有效减轻抑郁症状和睡眠障碍,但效果有限,同时存在明显副作用[2],故需要探寻新的干预手段。无抽搐电休克(MECT)是一种无创神经调控治疗方法,通过对大脑皮质实施强脉冲式电刺激以诱发脑区癫痫发作,从而发挥抗抑郁作用[3]。目前,关于MECT对抑郁症伴失眠患者的疗效尚缺乏研究报道。本研究旨在探讨在帕罗西汀治疗基础上MECT对抑郁症伴失眠患者的增效作用。
1 资料与方法
1.1 一般资料
选取2021年7月至2022年6月在本院接受治疗的抑郁症伴失眠患者80例。纳入标准:①确诊为抑郁症,参照《国际疾病分类(第10版)》[4]中相关标准;②年龄为18~60岁;③汉密尔顿抑郁量表(HAMD)-17评分≥17分;④伴有睡眠障碍,匹兹堡睡眠质量指数(PSQI)≥7分;⑤能够正常沟通交流。排除标准:①伴有其他类型精神障碍如精神分裂症、双相障碍者;②伴有脑器质性疾病者;③存在严重躯体疾病者;④体内存在金属植入物者;⑤孕妇或处于哺乳期者。采用随机信封法将入组对象分为两组:对照组与MECT组,每组40例。两组一般资料无统计学差异(P>0.05),见表1。本研究符合伦理并获得伦理审批,患者入组时对研究充分知情并签署知情同意书。

表1 两组一般资料比较
1.2 治疗方法
对照组予以帕罗西汀(批号:0000047022;生产单位:浙江华海药业股份有限公司)口服,剂量为20 mg/d,在早餐时服用,持续治疗4周。在对照组基础上,MECT组实施MECT治疗,采用电抽搐治疗仪(美国Somatics Thymatron公司),以双额叶作为治疗部位,刺激强度根据最大电荷量的5%增量予以调节,脉冲宽度为0.5ms。共进行6次MECT治疗,第1周连续进行3次(1次/d),后3周,每周1次。
1.3 观察指标
(1)临床症状评分:于治疗前和治疗4周后,由同一名对分组情况不知情的专科医师对患者临床症状进行评估,行HAMD-17量表[5]和PSQI量表[6]测评,HAMA-17评分越高意味着患者抑郁症状越严重,PSQI量表评分越高,说明患者睡眠越差。
(2)血清神经递质及脑源性神经营养因子(BDNF):于治疗前和治疗4周后,采集患者外周静脉血5mL,离心(3000r/min,离心半径为15cm)10min,获得血清,采用酶联免疫吸附法进行5-羟色胺(5-HT)、去甲肾上腺素(NE)和BDNF的测定,5-HT、NE试剂盒为上海酶联生物科技有限公司产品,BDNF试剂盒为美国ADL公司产品。
(3)安全性:记录两组治疗期间不良反应情况。
1.4 疗效评价
参照文献[7],根据HAMD-17减分率进行疗效评价。临床痊愈:HAMD-17减分率不低于75%;显效:HAMD-17减分率不低于50%,但也未达到75%;有效:HAMD-17减分率不低于30%,但未达到50%;无效:HAMD减分率不足30%。HAMD-17减分率=(HAMD-17治疗前-HAMD-17治疗后)/HAMD-17治疗前×100%。将临床痊愈、显效、有效合计为总有效,计算总有效率。
1.5 统计学方法
2 结 果
2.1 临床疗效
与对照组比较,MECT组总有效率提高,差异显著(P<0.05)。见表2。
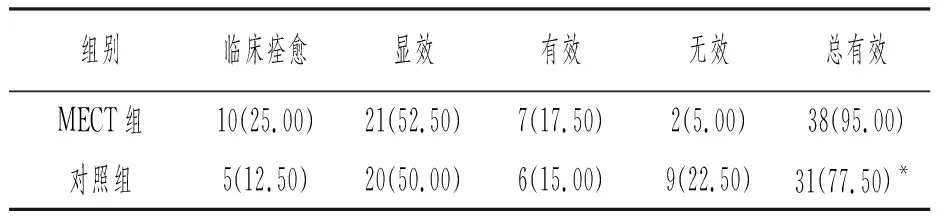
表2 两组临床疗效比较[n=40,n(%)]
2.2 HAMD-17评分和PSQI评分
治疗前,两组HAMD-17和PSQI评分无统计学差异(P>0.05)。治疗后,两组HAMD-17和PSQI评分与治疗前相比均降低(P<0.05),组间对比,MECT组以上评分更低(P<0.05)。见表3。
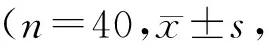
表3 两组临床症状评分比较分)
2.3 血清神经递质和BDNF水平
治疗前,两组血清NE、5-HT和BDNF无统计学差异(P>0.05)。治疗后,两组NE、5-HT和BDNF与治疗前相比均增高(P<0.05),组间对比,MECT组以上指标更高(P<0.05)。见表4。

表4 两组血清神经递质和BDNF比较
2.4 安全性
两组不良反应发生率分别为15.00%、10.00%,组间无统计学差异(P>0.05)。见表5。

表5 两组不良反应比较[n=40,n(%)]
3 讨 论
抑郁症是危害人类身心健康的常见精神疾病,具有患病率高、病程长的特点,给家庭及社会造成巨大负担。抑郁症可伴发失眠症状,失眠又会加重抑郁,形成恶性循环。当前阶段,药物仍是抑郁症的主要干预手段,帕罗西汀作为选择性5-羟色胺再摄取抑制剂(SSRI)的代表药物,能够通过抑制5-HT的重吸收,使神经突能间隙内5-HT含量增高,从而起到缓解抑郁症状的作用,在临床上备受认可。但实践显示[8-9],帕罗西汀对睡眠障碍的改善作用依赖于症状缓解,且用药早期甚至可能导致失眠症状加重。因此,探寻抑郁症伴失眠的非药物治疗手段尤为必要。近年来,随着对精神疾病神经生物学研究的深入,无创脑刺激技术(NIBS)在精神疾病领域日益受到关注。
MECT是一种较为成熟的NIBS,通过予以特定脑区高频强脉冲持续刺激,引发癫痫活动,从而发挥神经调节和抗抑郁作用[10]。MECT治疗抑郁症的神经调控机制可能在于,其能够调控患者默认网络功能连接异常[11]。已有研究显示[12],MECT对抑郁症患者的症状有明显改善作用。但目前抑郁症伴失眠患者药物治疗联合MECT的研究报道尚少。本研究结果显示,与对照组比较,MECT组总有效率提高,且治疗后HAMD-17和PSQI评分下降,表明MECT联合帕罗西汀治疗抑郁症疗效显著,能够更好地缓解患者抑郁症状,改善患者睡眠症状。
抑郁症的发病机制复杂且尚未完全明确,单胺类神经递质表达失衡是其中重要的病理生理改变。5-HT、NE等神经递质的表达下降与抑郁症发生有关,对单胺类神经递质表达的调控是抗抑郁治疗的关键靶点[13]。并且5-HT被称之为“致眠因子”,其参与着睡眠-觉醒机制,对慢波睡眠有着重要维持作用[14]。研究显示[15],抑郁症患者血清5-HT、NE水平能够反映患者病情严重程度,与HAMD-17和PSQI评分存在负相关关系。BDNF是反映神经可塑性的重要生物标志物,在抑郁症的病理过程中有着重要作用,且与抗抑郁药物的作用机制存在相关性[16]。抑郁症患者BDNF显著降低,抗抑郁治疗可上调患者BDNF表达,且BDNF可作为抗抑郁疗效的预测指标[17]。本研究结果显示,MECT联合帕罗西汀治疗能够更显著上调患者血清5-HT、NE和BDNF表达,这可能是发挥治疗作用的重要原因。本研究中,两组不良反应无统计学差异,说明联合治疗安全性良好。
总之,MECT联合帕罗西汀治疗抑郁症伴失眠能够上调患者血清神经递质及BDNF表达,更好地缓解抑郁症状,改善患者睡眠,提高临床疗效,且不会明显增加不良反应。

