基于稀土掺杂上转换纳米材料NaYF4:Yb,Er@TGA直接对金属离子进行定量分析的方法探究*
白安琪,彭孔浩,罗利霞,2,崔茹慧,岳晓梅,李淑荣,2,冀 华,2,孟佩俊,2
(1.包头医学院公共卫生学院,内蒙古 包头 014040;2.内蒙古自治区卫生检测与评价工程技术中心)
金属元素不仅是构成人体组织的重要成分,而且参与机体的正常新陈代谢活动,可以说没有金属离子的存在就没有生命活动的正常运行。即使是人体必需金属元素,也有一个合理的范围,过多或过少摄入均不利于人体健康。例如,Mg2+摄入过量会导致镁中毒,引起低血压、恶心、呕吐、面部潮红、肠梗阻、抑郁、意识模糊和嗜睡等症状[1];而Mg2+摄入过少会导致2型糖尿病、心血管疾病、心律失常以及一般肌肉和神经系统问题[2]。过量的Fe3+会促进芬顿反应产生羟基自由基和其他活性氧,从而破坏脂质、DNA和其他细胞成分[3];Fe3+摄入不足会使红细胞的产生受损,从而导致贫血[4]。Ca2+过量可能会加速血管和软组织钙化;Ca2+缺乏可能导致过度的骨质流失和继发性甲状旁腺功能亢进[5]。
金属离子检测的传统方法主要有络合滴定法[6]、分光光度法、原子吸收光谱法[7]、毛细管电泳法[8]等,虽然这些方法检测准确度高,但也存在一些缺点并不易用于现场快速检测。例如,络合滴定法中铬黑T作为指示剂需在温水浴中进行,否则会影响指示剂变色,此过程操作繁琐;分光光度法准确度低;原子吸收光谱法不能对多种离子进行同时检测分析。因此,构建金属离子的快速、灵敏、准确的检测方法是目前卫生分析检测领域研究的方向之一。
稀土掺杂上转换纳米材料(rare earth elements upconversion nanoparticles,REEs-UCNPs)作为一种新型荧光纳米材料引起人们广泛关注,它是由激活剂、敏化剂和基质组成,其中荧光效率最高的是NaYF4:Yb,Er。在近红外光激发下因其具有独特的光学性质、组织穿透能力深、对生物组织无损伤、抗干扰能力强等优势,成功应用于细胞成像、组织成像、生物检测、药物治疗等方面[9-10]。2020年,Liu等[11]基于NaY/GdF4:Yb,Er和柠檬酸修饰银纳米粒子(Cit-AgNPs),建立了一种灵敏、选择性检测Cr3+荧光分析方法,在0.5~40 μM浓度范围内,荧光呈线性下降,检测限为34 nM。同年,Wang等[12]基于NaYF4:Yb,Er@NaYF4和AuNPs之间的荧光共振能量转移构建了用于特异性检测污染水中的Pb2+的传感器,在0~50 nM之间具有显著的线性关系,检测限为4.1 nM。
本研究采用溶剂热法制备了NaYF4:Yb,Er,并用巯基乙酸对其进行表面修饰形成亲水性的纳米材料NaYF4:Yb,Er@TGA。通过测量不同金属离子对NaYF4:Yb,Er@TGA荧光强度的影响,筛选能够引起NaYF4:Yb,Er@TGA荧光强度增强或下降,且与金属离子浓度呈线性关系的金属离子类型,进而构建基于REEs-UCNPs荧光增强或猝灭机制实现对金属离子快速、灵敏、准确的检测新方法,拓展金属离子检测手段。
1 材料与方法
1.1实验仪器与试剂 SZCL-2数显智能控温磁力搅拌器(巩义市寻华仪器有限公司);C-MAGHS4S25磁力搅拌器(巩义市予华仪器有限责任公司);DLSB Series低温冷却液循环泵(郑州长域科工贸有限公司);FA2004电子分析天平(天津天马仪器厂);TDZ4-WS低速自动平衡离心机(长沙湘仪离心机仪器公司);KQ-300DE型数控超声波清洗器(昆山市超声仪器公司);移液枪(上海求精生化试剂有限公司);日立F4600型分子荧光分光光度计(日本岛津公司);MDL-N-980-10W光源。
氧化钇(Y2O3,99.99%)、氧化镱(Yb2O3,99.99%)、氧化铒(Er2O3,99.99%)、油酸(分析纯)、氟化铵(分析纯)、氢氧化钠(分析纯)均购自上海阿拉丁科技生化有限公司;浓盐酸(优级纯)、甲醇(分析纯)、十八烯(>90.0%GC)、无水乙醇(分析纯)、冰乙酸(分析纯)、Ba2+、Ca2+、K+、Se4+、Sr2+、Zn2+、Fe3+、Sn4+、Cr3+、Pb2+、Mn2+、Cu2+、Mg2+、Cd2+标准贮备液(1.00 mg/mL)均购自天津市凯通化学试剂有限公司;巯基乙酸(TGA,>98%,上海麦克林科技生化有限公司);无水乙酸钠(分析纯,中国医药公司北京公司经销);磷酸二氢钠(分析纯,北京红星化工厂);磷酸氢二钠(分析纯,北京精求化工有限责任公司),娃哈哈纯净水(纯水)。
1.2不同pH值的乙酸-乙酸钠缓冲溶液和磷酸缓冲溶液的配制
1.2.1乙酸-乙酸钠缓冲溶液的配制 称取0.41 g无水乙酸钠,并溶于适量纯水,定容至25.00 mL,即得浓度为0.20 mol/L的乙酸钠溶液;吸取0.45 mL冰乙酸于25 mL容量瓶中,用纯水定容,即得浓度为0.30 mol/L的冰乙酸溶液;再分别吸取0.20 mol/L的乙酸钠溶液1.20、5.90、9.40 mL和0.30 mol/L的冰乙酸溶液8.80、4.10、0.60 mL,分别混合配制pH值分别为3.8、4.8、5.8的乙酸-乙酸钠缓冲溶液,放置备用。
1.2.2磷酸缓冲溶液的配制 分别称取2.84 g Na2HPO4和2.4 g NaH2PO4,用适量纯水溶解,分别转移到100 mL容量瓶中,用纯水定容,即得浓度为0.20 mol/L的Na2HPO4溶液和0.30 mol/L的NaH2PO4溶液。再分别吸取0.20 mol/L的Na2HPO4溶液12.30、61.00、94.70 mL和0.30 mol/L的NaH2PO4溶液87.70、39.00、5.30 mL,分别混合配制pH值为6.0、7.0、8.0的磷酸缓冲溶液,放置备用。
1.3稀土氯化物(LnCl3)的制备 分别准确称取一定量的Y2O3、Yb2O3、Er2O3于烧杯中,分别加入体积分数为50%的盐酸水溶液,加热使其充分溶解,并将溶剂挥发,制得稀土氯化物固体。用适量甲醇分别将上述三种稀土氯化物固体溶解并定容,制备成稀土氯化物甲醇溶液,分别为:0.48 mol/mL YCl3、0.18 mol/mL YbCl3、0.01 mol/mL ErCl3。
1.4NaYF4:Yb,Er的合成、表面修饰及表征 吸取1.625 mL YCl3,1.111 mL YbCl3,2.000 mL ErCl3,8.00 mL油酸,18.00 mL十八烯,依次加入三口烧瓶中。在三口烧瓶中放入磁珠,置于电热套式控温磁力搅拌器中,快速升温至160 ℃,保持30 min,形成浅黄色透明溶液。冷却至室温,逐滴加入10.00 mL溶有0.103 5 g氢氧化钠和0.148 2 g氟化铵的甲醇溶液,搅拌30 min。快速升温到100 ℃,保持30 min。最后将体系快速升温至300 ℃,通氩气,冷凝回流1.5 h,得到OA-NaYF4:Yb,Er。
取一定量的OA-NaYF4:Yb,Er,加入无水乙醇,离心10 min,去上清,在沉淀中加入一定量巯基乙酸和乙醇溶液充分混匀超声1 h后,离心,最后去上清将沉淀溶于与所取原液等体积的纯水中,备用。采用激发光波长为980 nm,荧光波长扫描范围为400~800 nm,扫描速度为1 200 nm/min的荧光分光光度计对合成的NaYF4:Yb,Er@TGA进行发射光谱表征;采用最大加速电压为200 kV的日本电子JEM 2100F型透射电子显微镜对NaYF4:Yb,Er@TGA的形貌、粒径等进行表征;采用日本理学Smartlab 9型X-射线多晶衍射仪对NaYF4:Yb,Er@TGA结构进行表征。
1.5NaYF4:Yb,Er@TGA稳定性测定 分别取一定体积的NaYF4:Yb,Er@TGA水溶液于6支离心管中,再各加入pH值为6.0、7.0、8.0的磷酸盐缓冲溶液和pH值为3.8、4.8、5.8的乙酸-乙酸钠缓冲体系,混匀。每日定时检测其荧光强度,以时间为横坐标、荧光强度为纵坐标绘制荧光强度随时间变化曲线,探究缓冲液类型和pH值对NaYF4:Yb,Er@TGA稳定性的影响。
1.6不同金属离子对NaYF4:Yb,Er@TGA荧光强度的影响及方法学性能评价 分别吸取一定体积的Sn4+、Cr3+、Pb2+、Mn2+、Cu2+、Mg2+、Cd2+、Ba2+、Ca2+、K+、Se4+、Sr2+、Zn2+、Fe3+标准贮备液(浓度均为1.00 mg/mL),用纯水分别配制成浓度均为0.25 mg/mL的不同金属离子标准应用液。针对不同金属离子,分别取8支2.00 mL离心管,分别加入一定体积的不同金属离子的标准应用液和100 μL的NaYF4:Yb,Er@TGA水溶液,用纯水定容至2.00 mL,混匀,不同金属离子的浓度均分别为0.00、1.00、2.00、3.00、4.00、5.00、6.00、7.00 μg/mL。用分子荧光分光光度计检测其荧光强度。以金属离子浓度为横坐标,荧光强度为纵坐标,绘制荧光强度随不同金属离子浓度变化曲线图,探究不同金属离子对NaYF4:Yb,Er@TGA荧光强度的影响。对于金属离子浓度与NaYF4:Yb,Er@TGA荧光强度呈良好线性关系的金属离子,进一步计算线性方程,并进行方法学性能评价。方法检出限按照L=3Sb/S计算(Sb—空白溶液多次测定值的标准偏差,S为上述标准曲线的斜率)。通过对上述符合要求的5.00 μg/mL的金属离子溶液连续测定9次荧光强度,计算相对标准偏差(RSD),进行精密度评价。在上述符合要求的2.00、5.00 μg/mL的金属离子溶液体系中,再分别加入16、40 μL的相应金属离子标准应用液,在相同条件下,测定荧光强度,从标准曲线上对应其浓度,计算加标回收率,进行准确度评价。
2 结果
2.1NaYF4:Yb,Er@TGA的表征 本研究合成的NaYF4:Yb,Er@TGA分子荧光光谱图如图1。与贺璐[13]用溶剂热法制备的纳米材料荧光光谱图对比,峰形一致且在543 nm处出现特征峰,表明本研究通过溶剂热法成功合成了荧光强度较高的NaYF4:Yb,Er@TGA。
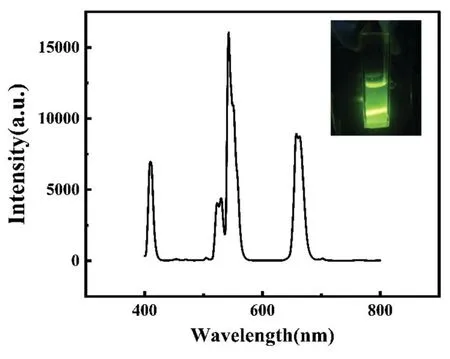
图1 NaYF4:Yb,Er@TGA的荧光光谱图(λex=980 nm)
NaYF4:Yb,Er@TGA的TEM和XRD表征结果如图2,NaYF4:Yb,Er@TGA粒径约30 nm的六边形,形貌大小均一、粒度均一,分散性良好,其衍射峰位置与NaYF4的标准卡片JCPDS No.28-1192相匹配,属于六方晶型。
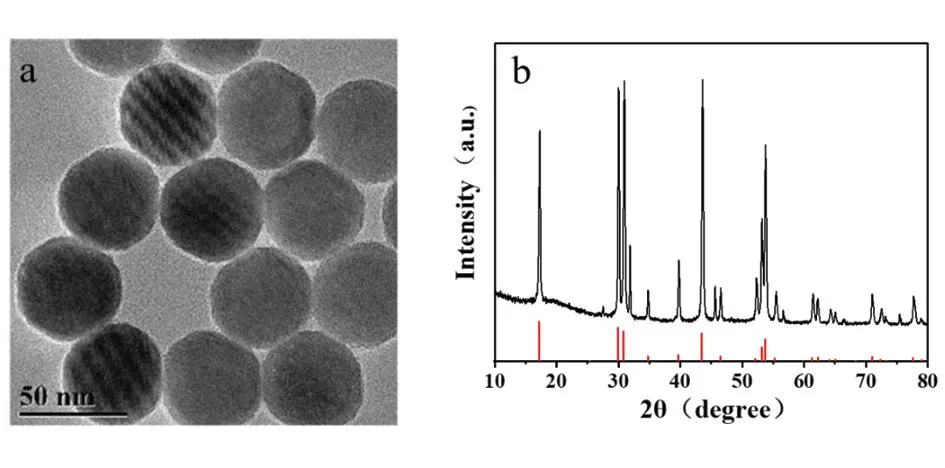
图2 NaYF4:Yb,Er@TGA的TEM图(a)和XRD图(b)
2.2NaYF4:Yb,Er@TGA的稳定性 不同pH值磷酸盐缓冲溶中的NaYF4:Yb,Er@TGA最大荧光强度-时间曲线变化趋势如图3a所示。从图中可以看出,NaYF4:Yb,Er@TGA在不同pH的磷酸盐缓冲溶液(pH =6.0、pH =7.0和pH =8.0)的第1~10天荧光强度逐渐减小,表明NaYF4:Yb,Er@TGA逐渐降解;第11-20天,NaYF4:Yb,Er@TGA溶液荧光强度变化逐渐减慢,表明NaYF4:Yb,Er@TGA的降解速率减小。
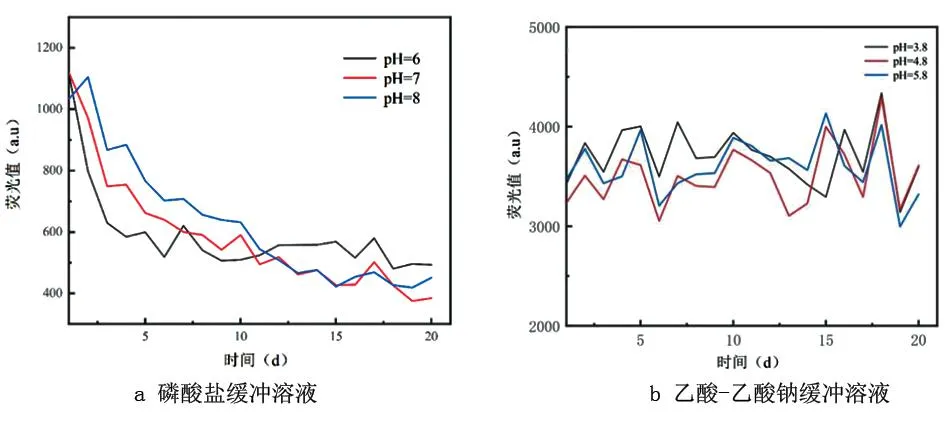
图3 不同缓冲溶液中NaYF4:Yb,Er@TGA最大荧光强度-时间曲线图
不同pH值乙酸-乙酸钠缓冲溶中的NaYF4:Yb,Er@TGA最大荧光强度-时间曲线变化趋势如图3b所示。从图中可以看出,随着时间的增加,NaYF4:Yb,Er@TGA在不同pH的乙酸-乙酸钠缓冲溶液(pH=3.8、pH=4.8和pH=5.8)中荧光强度基本稳定,表明本研究合成的NaYF4:Yb,Er@TGA在pH为3.8、4.8和5.8的乙酸-乙酸钠缓冲溶液中是较稳定的。
2.3不同金属离子对NaYF4:Yb,Er@TGA荧光强度的影响 NaYF4:Yb,Er@TGA荧光强度随不同金属离子浓度变化曲线图如图4(a-f)所示。
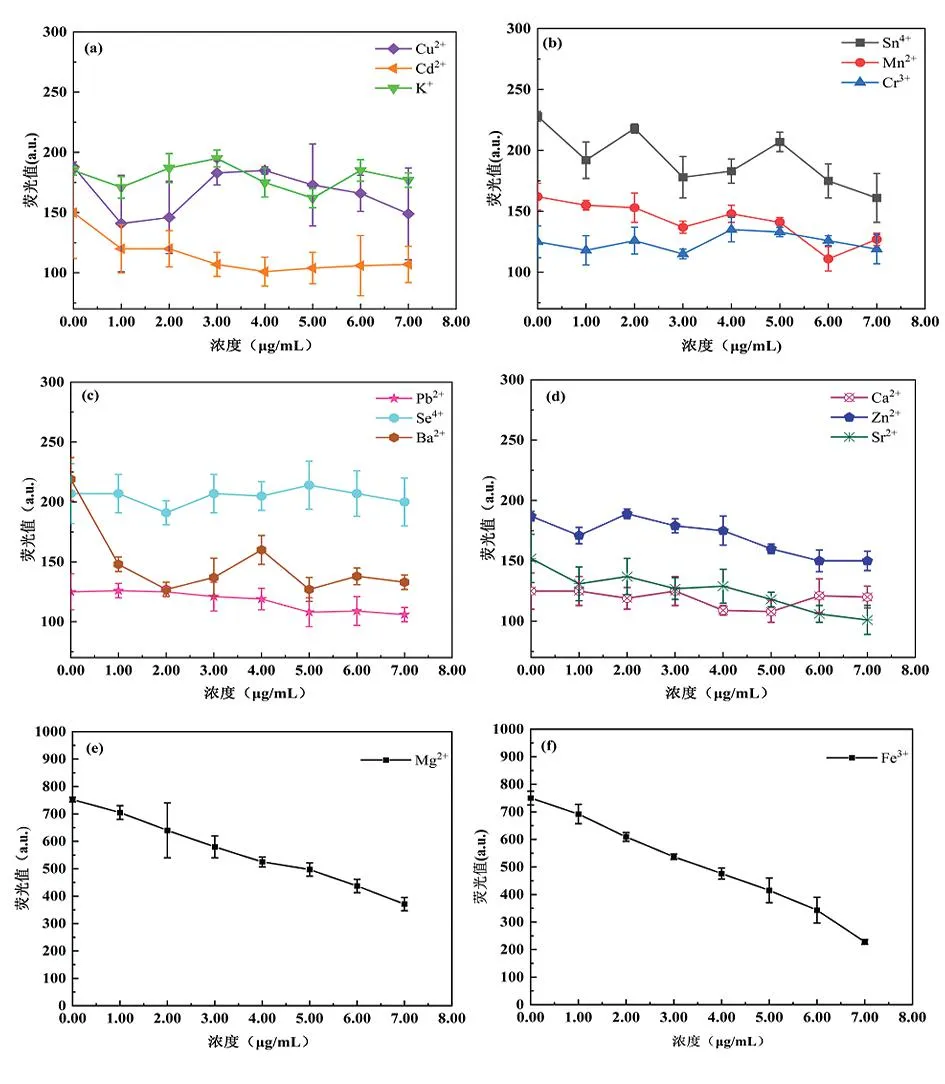
图4 NaYF4:Yb,Er@TGA荧光强度随Cu2+、Cd2+、K+(a)、Sn4+、Mn2+、Cr3+(b)、Pb2+、Se4+、Ba2+(c)、Ca2+、Zn2+、Sr2+(d)、Mg2+(e)、Fe3+(f)浓度变化曲线图
2.4Mg2+、Fe3+定量分析方法建立与评价 由图4(a-f)可以看出,基于NaYF4:Yb,Er@TGA实现对样品中Mg2+、Fe3+进行定量检测的方法性能评价结果如表1所示。金属离子Mg2+、Fe3+分别在浓度为0~7.00 μg/mL、0~6.00 μg/mL浓度范围内与NaYF4:Yb,Er@TGA荧光强度呈现良好的线性关系,其标准曲线方程的线性系数分别为0.992 4、0.998 2,检出限分别为1.79、1.30 μg/mL,加标回收率分别为95.5%~98.8%、92.5%~97.8%,方法相对标准偏差分别为4.05%、8.18%。

表1 方法学性能评价
3 讨论
本研究在最优条件下采用溶剂热法合成的稀土掺杂上转换纳米材料NaYF4:Yb,Er呈六方晶型,粒径约30 nm,形貌均一,发光强度较高且分散性好。制备的NaYF4:Yb,Er在980 nm激发下发射出绿色上转换荧光,分别在410、524、543和654 nm具有发射峰,分别对应于Er3+的辐射跃迁过程:2H9/2→4I15/2、2H11/2→4I15/2、4S3/2→4I15/2和4F9/2→4I15/2,与丁明烨、王倩等[14-15]报道一致。经巯基乙酸修饰后转化为亲水性纳米材料NaYF4:Yb,Er@TGA。稳定性研究结果表明,NaYF4:Yb,Er@TGA在磷酸盐缓冲溶液(pH=6~8)中稳定性较差,而在乙酸-乙酸钠缓冲液(pH=3.8~5.8)中稳定性较好,这可能与NaYF4:Yb,Er@TGA的表面修饰基团(巯基乙酸)与乙酸、乙酸钠结构相似,相容性较好有关。
通过测量Cu2+、Cd2+、K+、Sn4+、Mn2+、Cr3+、Pb2+、Se4+、Ba2+、Ca2+、Zn2+、Sr2+、Mg2+、Fe3+等14种金属离子对NaYF4:Yb,Er@TGA荧光强度的影响,Sn4+、Cu2+、Mn2+、Cr3+、Cd2+、Pb2+、Ca2+、K+、Se4+离子在0.00~7.00 μg/mL浓度范围内对NaYF4:Yb,Er@TGA的荧光强度影响较小;当Ba2+浓度在0.00~2.00 μg/mL范围内,NaYF4:Yb,Er@TGA的荧光强度随着浓度增大而降低,Ba2+浓度增加至7.00 μg/mL时,对NaYF4:Yb,Er@TGA的荧光强度影响较小;Zn2+浓度在2.00~6.00 μg/mL时,NaYF4:Yb,Er@TGA的荧光强度随Zn2+浓度增大而降低,NaYF4:Yb,Er@TGA的荧光强度与Zn2+浓度之间具有一定的线性关系(R2=0.947 2),但灵敏度较差,不适合做定量分析;Sr2+浓度与NaYF4:Yb,Er@TGA的荧光强度之间存在一定的线性相关性(R2=0.937 5),但灵敏度低,同样不适合做定量分析。
NaYF4:Yb,Er@TGA的荧光强度随Mg2+、Fe3+浓度的增加而降低,且在一定浓度范围内Mg2+、Fe3+浓度与NaYF4:Yb,Er@TGA的荧光强度呈良好的线性关系。基于上述结果,NaYF4:Yb,Er@TGA对Mg2+、Fe3+的荧光响应具有一定的选择性,进而初步建立了基于稀土掺杂上转换纳米材料NaYF4:Yb,Er@TGA直接对Mg2+和Fe3+进行定量分析的检测方法。方法学性能评价结果表明,在Mg2+和Fe3+浓度分别为0~7.00 μg/mL、0~6.00 μg/mL范围内,方法线性关系良好,检出限低、准确度较高、精密度较好,为后续进行实际样品中Mg2+和Fe3+定量分析奠定了坚实基础。

