葡萄糖目标范围内时间在胰岛素周制剂中的评价与临床启发
秦贵军
郑州大学第一附属医院,河南 郑州 450052
葡萄糖目标范围内时间(time in range,TIR)或称葡萄糖达标时间百分比,是指24 h 内葡萄糖在目标范围内的时间或其所占的百分比,是临床上评估血糖控制的新指标,可通过持续葡萄糖监测(continuous glucose monitoring,CGM)数据计算获得。近来,国内外指南对于CGM 和TIR 的指导也越来越精细化。《中国2 型糖尿病防治指南(2020年版)》[1]指出“TIR 应纳入血糖控制目标”。2022版《ADA/EASD:2 型糖尿病高血糖管理共识》[2]指出“使用胰岛素治疗的2 型糖尿病(T2DM)患者,应该使用CGM 进行血糖监测”。2023 年ADA《糖尿病诊疗标准》也针对不同胰岛素治疗方案的1 型糖尿病(T1DM)和2 型糖尿病(T2DM)患者,应用CGM 进行了指导,并强调患者可以从动态血糖监测中获益[3]。因此,TIR 作为CGM 系统所提供的关键血糖信息,已成为血糖管理的重要指标,也有助于更全面地评估降糖药物的疗效和安全性。本研究就从TIR 角度,简述TIR 对于糖尿病管理的重要意义,并通过胰岛素周制剂依柯胰岛素(insulin icodec)3 期临床研究ONWARDS 系列研究中的TIR数据,来探索如何通过TIR 评估依柯胰岛素的血糖控制效果和安全性以及其带来的临床启发。
1 TIR 对于糖尿病管理具有重要意义
血糖监测是糖尿病管理的重要组成部分,血糖监测结果有助于糖尿病患者血糖控制情况的评估及降糖治疗方案的调整。持续葡萄糖监测是指通过葡萄糖感应器连续监测皮下组织间液葡萄糖浓度的技术,提供连续、全天血糖信息。2017 年《CGM 临床应用国际专家共识》[4]推荐TIR,葡萄糖高于目标范围时间(time above range,TAR),葡萄糖低于目标范围时间(time below range,TBR)作为CGM的关键报告参数,分别反映血糖控制良好、高血糖和低血糖情况。
TIR 指葡萄糖水平在目标范围内(通常为3.9~10.0 mmol/L,或为3.9~7.8 mmol/L)的时间或其所占的百分比(%)[4]。多项研究[5-7]显示,TIR 与HbA1c 的水平、糖尿病微血管病变、糖尿病大血管病变、全因死亡及心血管死亡密切相关。SWITCH PRO 事后分析[8]显示TIR 与HbA1c 呈线性负相关,且在HbA1c 基线较高的亚组(HbA1c ≥7.5%)TIR与HbA1c 的相关性更强。DEVOTE 研究事后分析[9]显示TIR>70%相较于TIR ≤70%的患者,主要心血管不良事件(major adverse cardiovascular events,MACE)发生风险减少27%[HR:0.73,95%CI:(0.59,0.90)]。来自国际及中国的研究数据[5-7]显示TIR每降低10%与糖尿病视网膜病变、微量蛋白尿、糖尿病周围神经病变、全因死亡和脑血管疾病死亡风险增高密切相关。
众多国内外指南及专家共识提出将TIR 作为血糖控制目标[1-3]。2023 ADA《糖尿病诊疗标准》[3]指出,对于大多数非妊娠成人糖尿病患者控制目标为TIR>70%(血糖3.9~10.0 mmol/L)、TBR(血糖<3.9 mmol/L)<4%、TBR(血糖<3.0 mmol/L)<1%。对于虚弱或低血糖风险高的患者,建议TIR>50%,TBR<1%。
2 胰岛素周制剂-依柯胰岛素的研发源于临床未被满足的需求
胰岛素自问世至今已经历逾百年的发展历程,在糖尿病治疗中发挥着重要作用。自1936 年首个基础胰岛素被研发出来,基础胰岛素历经了数次更新迭代,疗效和安全性逐步提高,但仍需要每日注射。糖尿病患者更希望减少胰岛素的注射次数,对于每日注射的担忧和治疗依从性差是导致很多糖尿病患者血糖控制不佳的重要因素[10-11]。若基础胰岛素能每周注射一次,可以预测其将具有使用更方便,治疗依从性更好,改善治疗持续性,并提高患者的生活质量的潜能[12-13]。
目前全球在研的胰岛素周制剂包括依柯胰岛素(诺和诺德研发,已完成3 a 期临床试验,目前在上市申请中)和insulin-Fc efsitora alfa(礼来研发,尚在临床试验阶段)[14]。依柯胰岛素将人胰岛素的分子结构进行2 项特殊分子设计:(1)去除了人胰岛素B 链第30 位氨基酸苏氨酸,在B 链第29 位的赖氨酸处通过寡聚乙二醇(OEG)γ-L-谷氨酸连接了20 碳-脂肪酸侧链;(2)将人胰岛素分子进行了3 处氨基酸替换,即将A 链14 位的酪氨酸替换为谷氨酸(A14E),B 链16 位的酪氨酸替换为组氨酸(B16H),B 链25 位的苯丙氨酸替换为组氨酸(B25H)。通过2 项关键的生物技术:与白蛋白强效、可逆的结合,以及胰岛素受体介导的清除减慢,实现了依柯胰岛素半衰期的极大延长。皮下注射后,依柯胰岛素能够从白蛋白结合储库中缓慢、持续地释放活性胰岛素,如“涓涓细流”作用于靶器官和组织[15-16]。药代动力学研究[17]显示,依柯胰岛素在人体内半衰期可长达196 h,药效动力学研究显示,依柯胰岛素每周1 次皮下注射,降糖效果在1周内日间分布接近平均,3~4 周后可达稳态。
依柯胰岛素3 期临床试验ONWARDS 系列研究[18-19]是一项全面的全球3 期临床项目,包含6项临床研究,纳入超过4 200 例糖尿病患者,评估了依柯胰岛素在不同患者人群、与不同的基础胰岛素日制剂比较、用于不同治疗方案的长期使用的疗效和安全性。同时在ONWARDS 1/2/4/6 中均使用了CGM 评估血糖控制情况,为全面地评估依柯胰岛素的降糖疗效和安全性提供了进一步的证据,以下重点介绍已公布的ONWARDS 1/2/4 主要研究结果及TIR 数据[20-25]。
3 ONWARDS 研究中,通过TIR 等相关CGM 数据评估依柯胰岛素的疗效和安全性概览
3.1 ONWARDS 1:在既往未使用胰岛素的T2DM 患者中评估依柯胰岛素的疗效和安全性
ONWARDS 1 是一项随机、开放标签、治疗达标、双盲CGM、3 a 期临床研究,研究纳入984 例未使用胰岛素治疗的2 型糖尿病患者,患者年龄≥18 岁,HbA1c 7%~11%,按1∶1 比例随机分为依柯胰岛素组和甘精胰岛素U100 组,进行为期78周试验(包括52 周的主要试验期和26 周的延长期),外加5 周的随访期。研究主要终点为HbA1c水平自基线到第52 周的变化。次要终点为48~52 周时TIR(3.9~10.0 mmol/L)的时间百分比,第52 周时空腹血糖相对于基线的变化,2 级低血糖(临床显著低血糖,血糖<3.0 mmol/L)和3 级低血糖(严重低血糖,需要外部援助才能恢复)的发作次数等。ONWARDS 1 研究的最新数据于2023 ADA 年会发布,全文同步发表于《新英格兰医学杂志》[20],研究结果显示:52 周时,主要终点HbA1c 平均下降幅度依柯胰岛素组大于甘精胰岛素U100 组(-1.55%vs-1.35%),差异有统计学意义,证实了依柯胰岛素相较于甘精胰岛素U100HbA1c 的改善达到了非劣效性(P<0.001)和优效性(P=0.02),至试验延长期78 周时,依柯胰岛素组HbA1c 降幅仍更大(-1.55%vs-1.45%)。并且,依柯胰岛素组HbA1c<7%的达标率优于甘精胰岛素U100 组(52 周:57.6%vs45.4%;78 周:56.8%vs49.1%),依 柯胰岛素组HbA1c<7%且无2 级和3 级低血糖的比例亦优于甘精胰岛素U100 组(52 周:52.6%vs42.6%;78 周:54.5%vs46.4%)。从基线至第52 周及78 周,两组空腹血糖降幅相似(0~52 周:依柯胰岛素组为-3.35 mmol/L,甘精胰岛素U100 组为-3.34 mmol/L,估计治疗差异(estimated treatment difference,ETD)为-0.01 mmol/L[95%CI(-0.27,0.24)];0~78 周:ETD 为-0.04 mmol/L[95%CI(-0.31,0.23)]。两组的2 级低血糖和3 级低血糖事件发生率差异无统计学意义(依柯胰岛素组为0.30 次/年,甘精胰岛素U100 组为0.16次/年,P=0.06)。此外,引人注目的是48~52 周时,依柯胰岛素组的TIR 显著高于甘精胰岛素U100组(71.9%vs66.9%);ETD 4.27%[95%CI(1.92,6.62)],P<0.001。试验延长阶段,74 周~78 周,依柯胰岛素组的TIR 仍更优(70.2%vs64.8%);ETD 4.41%[95%CI(1.92,6.90)],P<0.001。两个时间段的TAR(>10 mmol/L)依柯胰岛素组优于甘精胰岛素U100 组,TBR(<3.0 mmol/L),两组相似且在推荐目标范围内。
3.2 ONWARDS 2/4:既往已经使用胰岛素治疗的T2DM 患者,评估依柯胰岛素的疗效和安全性
ONWARDS 2 研究[21]是一项随 机、开 放标签、治疗达标的3a 期临床研究,研究对象为既往使用基础胰岛素±口服降糖药±胰高糖素样肽-1(glucagon-like peptide-1,GLP-1)受体激动剂皮下注射的T2DM 患者,年龄≥18 岁,HbA1c7.0%~10.0%,随机分为依柯胰岛素组(联合或不联合非胰岛素降糖药物)和德谷胰岛素组(联合或不联合非胰岛素降糖药物),共纳入患者526 例,研究主要终点为26 周时HbA1c 自基线的降幅。研究结果显示,依柯胰岛素胰岛素组与德谷胰岛素组在HbA1c 降幅上达到了非劣效性和优效性(-0.93%vs-0.71%,估计治疗差异-0.22%,95%CI:-0.37~-0.08,非劣效P<0.000 1,优效P=0.002 8。2 级低血糖和3 级低血糖事件发生率两组差异无统计学意义(0.73 次/年vs0.27 次/ 年,P=0.08)。两 组22~26 周时两组TIR、TBR 及TAR 相似,分别为TIR 3.9~10.0 mmol/L(63.1%vs59.5%,P=0.146),TBR<3.0 mmol/L(0.3%vs0.2%,P=0.118),TAR>10.0 mmol/L(35.5%vs39.7%,P=0.083)。依柯胰岛素比德谷胰岛素TIR数值上更高,但差异无统计学意义。
ONWARDS 4 是一项随机、开放标签、治疗达标的3 a 期临床研究[22],研究对象为既往使用基础胰岛素+餐时胰岛素±口服降糖药和GLP-1 受体激动剂皮下注射的T2DM 患者,年龄大于等于18 岁,HbA1c 7.0%~10.0%,随机分为依柯胰岛素+门冬胰岛素±非胰岛素降糖药组或甘精胰岛素U100+门冬胰岛素±非胰岛素降糖药组,共纳入患者582 例,进行为期26 周的研究。研究显示,治疗26 周后,依柯胰岛素联合门冬胰岛素组与甘精胰岛素U100 联合门冬胰岛素组在HbA1c 降幅无差异(-1.16%vs-1.18%),达到非劣效性(P<0.001)。2 级低血糖和3级低血糖事件发生率两组无差异(5.64 次/年vs5.62次/年,P=0.93)。两组22~26 周的TIR、TBR、TAR相似:TIR 3.9~10.0 mmol/L(66.9%vs66.4%,P=0.84),TBR<3.0 mmol/L(0.7%vs0.6%,P=0.20),TAR>10.0 mmol/L(30.5%vs31.3%,P=0.68)。
ONWARDS 系列研究除了采用传统的血糖控制指标 HbA1c,还通过血糖控制新指标CGM 重要参数TIR、TBR 及TAR 等全面评估了患者血糖控制情况,结果显示无论既往是否使用胰岛素治疗的T2DM 患者,使用周制剂依柯胰岛素治疗兼具有效性与安全性。
4 依柯胰岛素基于CGM 数据相关事后分析的临床启发
ONWARDS 1/ 2/ 4 研究中通过CGM 数据的事后分析也探讨了针对胰岛素周制剂在临床实践中密切关注的问题。ONWARDS 1 的CGM 数据包括治疗起始期(0~4 周)、研究中期(22~26 周)、主要阶段结束期(48~52 周)、延长阶段结束期(74~78周),事后分析结果显示在未使用胰岛素治疗的T2DM 患者中,依柯胰岛素与基础胰岛素日制剂的低血糖持续时间相似[23],见表1。ONWARDS 2 与ONWARDS 4 研究中的CGM 数据包括转换期(0~4周)、研究结束期(22~26 周)及随访期(27~31 周),事后分析结果显示在已使用胰岛素治疗的T2DM 患者中,依柯胰岛素与基础胰岛素日制剂低血糖持续时间相似[24],见表2。
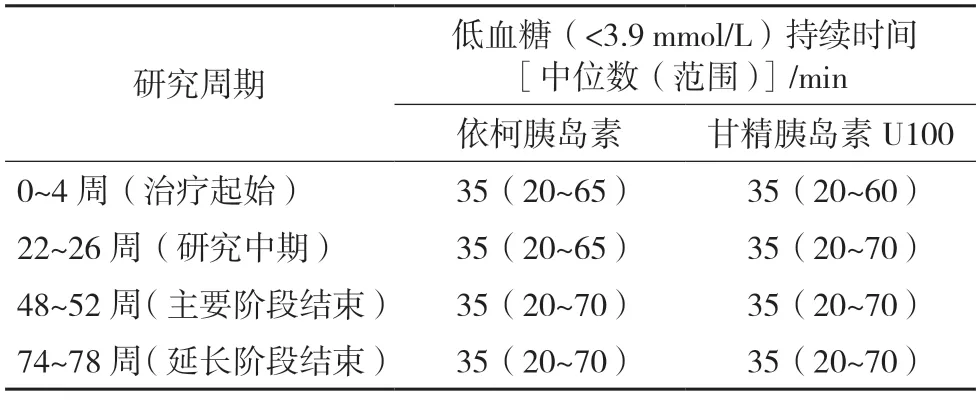
表1 ONWARDS 1研究低血糖持续时间
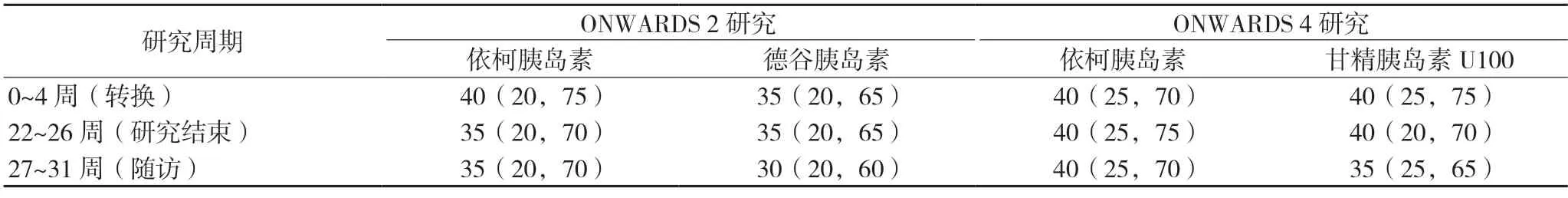
表2 ONWARDS 2和4研究中治疗组的低血糖(<3.9 mmol/L)持续时间[中位数(四分位数)]min
另外一项事后分析重点评估了既往使用过胰岛素治疗的T2DM 患者转换为依柯胰岛素,在转换期的低血糖风险数据,数据来源于ONWARDS 2和ONWARDS 4 研究。结果显示:既往已使用胰岛素治疗的T2DM 患者,转换为依柯胰岛素,在转换期(0~4 周),依柯胰岛素与基础胰岛素日制剂(德谷胰岛素U100 或甘精胰岛素U100 每日一次)的TIR、TBR 与TAR 相似[25],见表3。

表3 ONWARDS 2和4转换期0~4周的CGM
5 结语
TIR 是CGM 评估血糖管理情况的关键指标。在评估胰岛素的疗效与安全性时,越来越多临床试验采用TIR 作为评价的新指标。依柯胰岛素是目前国内外上市进展最为迅速的胰岛素周制剂。ONWARDS 系列3 期临床研究及其事后分析通过TIR 等CGM 指标为全面评估依柯胰岛素的疗效与安全性提供了循证新证,证实依柯胰岛素降糖效果良好,低血糖风险与甘精胰岛素U100 或德谷胰岛素相似。依柯胰岛素每周一次注射,方便患者使用,这必将减少胰岛素起始使用的困难,提高患者依从性,让更多接受胰岛素治疗的患者获益。

