全自动酶免分析仪与自动核酸纯化仪在基层血站的应用效果探究
双莉华 范彩霞 黄康 吴晨 抚州市中心血站质管科 (江西 抚州 344000)
内容提要: 目的:探究分析在基层血站全自动酶免分析仪与自动核酸纯化仪的运用价值。方法:选取2020年1月~2022年12月某基层血站无偿献血样本共计76528例,其中,2020年检测总数为24407例,2021年检测总数为25709例,2022年检测总数为26412例,使用全自动酶免分析仪与自动核酸纯化仪,首先实施酶免检测,如若检验结果为阳性直接判定,对于特殊样本,实施酶免检测与核酸并行检测,观察分析在乙型肝炎病毒检测、丙型肝炎病毒检测、艾滋病毒检测、梅毒检测中不合格情况。结果:①分析2020年~2022年酶免检测结果,在2020年,乙型肝炎阳性病毒检出率最高达到0.37%,梅毒病毒阳性检出率0.33%次之;在2021年,乙型肝炎病毒阳性检出率最高达到0.40%,梅毒病毒阳性检出率0.14%次之;在2022年,乙型肝炎病毒阳性检出率达到0.33%,梅毒病毒阳性检出率0.11%次之。②2020年核酸检测共检测出乙型肝炎阳性数51例,阳性率0.21%;2021年共检测出乙型肝炎阳性数33例,阳性率0.13%,人类免疫缺陷病毒阳性数1例,阳性率0.004%;2022年共检测出乙型肝炎阳性数42例,阳性率0.16%。结论:利用全自动酶免分析仪与自动核酸纯化仪,进行核酸检测和免疫检测平行筛查,能够发挥优势互补的作用,可降低输血传播疾病残余风险,有效控制输血传播的病毒性疾病,为输血者提供安全保障。
随着我国公益事业快速发展,社会大众的公益观念稳步提升,无偿献血得到国家政策的大力支持,促使自愿无偿献血志愿者数量逐渐增加[1]。无偿献血为临床输血提供宝贵的血液资源,为了提高临床输血的安全性,要严格筛查血液样本,以便第一时间发现不符合标准的血液产品,确保血液质量,以降低输血过程中出现的不良输血事件[2]。过去基层血站对血液筛查主要利用血清酶联免疫吸附方法进行检验,能够及时检出乙型肝炎病毒、丙型肝炎病毒、艾滋病病毒、梅毒病毒等,但是也无法将弱阳性、灰区样本有效排出。在血液检验中,核酸检测运用更加普遍,有较高的敏感性,能够及时发现弱阳性、灰区样本,保证血液筛查的有效性[3]。为了提高基层血站血液筛查的有效性,现对全自动酶免分析仪与自动核酸纯化仪的运用价值展开如下汇报。

表1.2020年~2022年酶免检测结果(n/%)
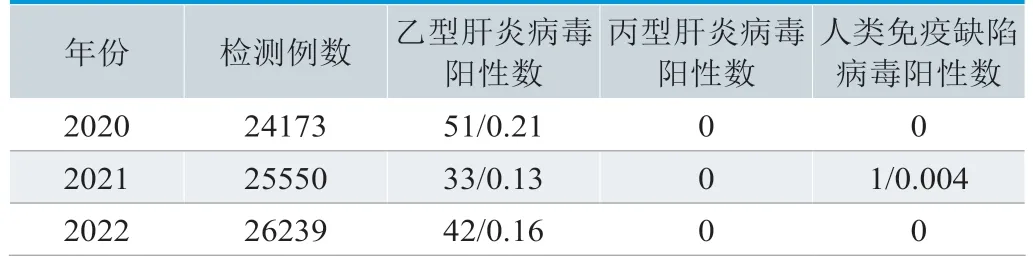
表2.2020年~2022年核酸检测结果(n/%)
1.资料与方法
1.1 一般资料
选取2020年1月~2022年12月某基层血站无偿献血样本共计76528例,其中,2020年检测总数为24407例,2021年检测总数为25709例,2022年检测总数为26412例,每份血液样本5mL。其中,38744例为男性,37784例为女性,年龄18~60岁,平均(34.42±3.21)岁。
纳入标准:①全部献血者均满足GB18467-2011献血者健康检查要求;②全部献血者均为无偿献血。排除标准:①排除难以配合献血工作的献血者;②排除存在凝血功能障碍的献血者。
仪器设备:①酶免检测。Uranus AE150全自动酶免仪(产地:深圳爱康公司)或EVO ELISA200(产地:瑞士帝肯公司)。②核酸检测。ChiTas-BSS1200自动核酸纯化仪(产地:苏州新波生物公司)和ABI-7500实时荧光定量PCR扩增仪(产地:爱普拜斯生物公司)或cobass201全自动核酸血液筛查系统(产地:罗氏有限公司),DL-42M医用低温离心机(产地:湖南平凡科技公司)。
检测试剂:①酶免检测试剂厂家:厦门新创所提供的HBsAg、HCV抗体、HIV抗体和TP检测试剂,另一厂家由北京万泰提供的HBsAg、TP检测试剂以及珠海丽珠提供的HCV抗体、HIV抗体检测试剂。②核酸检测试剂厂家:上海浩源生物科技有限公司、罗氏诊断产品有限公司。
1.2 方法
根据试验的技术要求,采用相应类型的真空采血管本在血液采集完成后从血袋血液中留取分别留取1管5~6mL血液标本,用于酶免和核酸检测。酶免检测标本3000r/min离心15min;核酸检测标本在采集后4h之内宜采用水平离心机进行离心,离心力为1500~1800g,在低温条件下离心20min。一般情况下,本血站采取血清学与核酸顺序检测模式进行检测,如若酶免检验结果呈阳性,直接判定为不合格,将酶免检测为合格的标本再进行核酸检测,检测为有反应的判为不合格。如若遇到特殊标本,例如机采献血样本或者因血库血液库存量比较少的情况下,则采取血清学与核酸并行检测模式,将血液标本同时进行酶免检测与核酸检测,酶免检测和核酸检测均阴性的或无反应的判为合格。
1.3 观察指标
严格按照检测试剂以及仪器操作说明书进行操作,利用ELISA检测技术对血液样本进行乙型肝炎表面抗原、丙型肝炎抗体、艾滋病病毒和梅毒抗体的检测,利用核酸检测技术对血液样本进行HBV/HCV/HIV核酸联合检测,分析检测结果。
2.结果
2.1 2020年~2022年酶免检测结果分析酶免检测结果分析
经过酶免检测,2020年共检出乙型肝炎阳性数91例(阳性率0.37%),丙型感染阳性数19例(阳性率0.08%),人类免疫缺陷病毒阳性数14例(阳性率0.06%),梅毒阳性数81例(阳性率0.33%);2021年共检出乙型肝炎阳性数104例(阳性率0.40%),丙型感染阳性数15例(阳性率0.06%),人类免疫缺陷病毒阳性数15例(阳性率0.06%),梅毒阳性数36例(阳性率0.14%);2022年共检出乙型肝炎阳性数87例(阳性率0.33%),丙型感染阳性数17例(阳性率0.06%),人类免疫缺陷病毒阳性数13例(阳性率0.05%),梅毒阳性数29例(阳性率0.11%),见表1。
2.2 2020年~2022年核酸检测结果分析
经过核酸检测,2020年共检测出乙型肝炎阳性数51例,阳性率0.21%;2021年共检测出乙型肝炎阳性数33例,阳性率0.13%,人类免疫缺陷阳性数1例,阳性率0.004%;2022年共检测出乙型肝炎阳性数42例,阳性率0.16%,见表2。
3.讨论
无偿献血主要针对志愿者在自愿、无偿的条件下自行捐献适量血液的一种行为,在无偿献血中获得血液资源是临床输血的主要来源渠道,可在不同疾病治疗中合理使用[4,5]。在无偿献血者血液样本收集完毕后,为了提高临床输血的安全性,保证血液的质量,需要对血液样本开展输血传播病原体进行系统检查,以便第一时间发现受到污染的血液样本,保证临床输血安全可靠,以免造成血液资源的浪费,防止临床输血过程中出现不良输血事件[6]。由此可见,重视基层血站血液样本筛查检验工作非常关键。
患者在输血治疗期间,血液质量安全作为确保临床治疗效果的前提条件,而血液安全问题,在基层血站工作中最为重要。对血液样本进行安全筛查,作为确保血液安全性的有效方法,也是临床预防血液传播传染病疾病的有效手段。当前,在临床血液筛查过程中,利用酶免检验和核酸检验方式。其中,酶免检验主要以抗体、抗原检测为主,但是病毒抗体和抗原容易出现蛋白结构变异,导致病毒在窗口期容易对检验结果带来影响,从而出现误检、漏检的问题[7,8]。病毒窗口期主要针对被病毒感染到此种病毒可能被某一种检验方式筛查、检出的一段时间,且处于窗口期的病毒难以被及时检出,且存在传染性。然而,核酸检验的灵敏度与特异性都比较高,在血液样本检验过程中,即使样本含有少许病毒核酸,也能及时被检出,使免疫检测中的病毒窗口期进一步缩短。根据相关研究发现,核酸检测能够使乙型肝炎病毒、丙型肝炎病毒、艾滋病毒的平均感染窗口期缩短,且核酸检测能进一步避免病毒变异、隐性感染情况等,有效解决临床误检、漏检的问题[9]。
为了提高血液样本筛查的有效性,合理运用先进的全自动酶免分析仪器、自动核酸纯化仪器,展开酶免检测与核酸检测,一般情况下,采取血清学与核酸顺序检测模式进行检测,如若酶免检验结果呈阳性,直接判定为不合格,将酶免检测为合格的标本再进行核酸检测,检测为有反应的判为不合格。如若遇到特殊标本,例如机采献血样本或者因血库血液库存量比较少的情况下,则采取血清学与核酸并行检测模式,将血液标本同时进行酶免检测与核酸检测,酶免检测和核酸检测均阴性的或无反应的判为合格。本次研究结果显示:①分析2020年~2022年酶免检测结果,在2020年,乙型肝炎阳性病毒检出率最高达到0.37%,梅毒病毒阳性检出率0.33%次之;在2021年,乙型肝炎病毒阳性率最高达到0.40%,梅毒病毒阳性率0.14%次之;在2022年,乙型肝炎病毒阳性率达到0.33%,梅毒病毒阳性检出率0.11%次之。②2020 年共检测出乙型肝炎阳性数51 例,阳性率0.21%;2021年共检测出乙型肝炎阳性数33例,阳性率0.13%,人类免疫缺陷病毒阳性数1例,阳性率0.004%;2022年共检测出乙型肝炎阳性数42例,阳性率0.16%。由此可见,在基层血站血液样本检测过程中,借助全自动酶免分析设备、自动核酸纯化设备,展开酶免检测后,对特殊血液样本进行核酸检测,能够及时检出假阴性样本,提高血液检验的有效性,保障临床输血安全可靠。然而,出现假阳性样本的原因主要包括以下几点:①实验室操作者没有根据试剂要求和仪器要求实施检验,促使血液样本检验结果为阳性;②血液样本在运输至实验室中储存不当,核酸物质由于储存环境温度比较高、运输时间比较长等外界因素影响而出现分解现象[10];③血液样本在抽取过程中,病毒浓度比较低,难以及时判定;④在血液样本留存确认环节中,因病毒颗粒处于血浆内的泊松分布,使病毒浓度分布不均匀,留取样本病毒浓度比较低,无法及时检出。
综上所述,血液检验容易受诸多因素的干扰,导致血液检验容易存在误检、漏检的可能性。然而,借助先进的全自动酶免分析系统、自动核酸纯化系统,做好酶免检验与核酸检验工作,能够使病毒窗口期缩短,提高阳性检出率,为临床用血与治疗干预提供可靠的输血保障。为此,各个基层血站建议推广全自动酶免分析系统、自动核酸纯化系统的临床应用,在检测过程中规范操作标准,才能确保基层血站血液质量符合标准。

