高纯纳米氧化铁的制备
吴文军,韩 召,张福元,刘鹏飞,李 杰
(安徽工业大学 冶金工程学院,安徽 马鞍山 243032)
氧化铁是一种具有广泛应用的无机非金属物质,外观为红色或红棕色粉末,通常将质量分数>99.5%的氧化铁称为高纯氧化铁。高纯纳米氧化铁具有优异的光学、电学、吸附、催化和磁化特性,因此被广泛地应用于传感器、催化剂、生物医药等和光催化领域等[1-4]。
高纯纳米氧化铁中仍旧包含多种杂质离子,其中,Ca2+、Mg2+等杂质离子是影响其颜色、微观形貌和综合性能的主要因素;Al3+、Si4+等杂质离子会影响铁氧体的显微结构和电磁性能;氧化铁中的Mn2+等重金属离子的含量在生物医药领域也有严格的要求[5]。在铁氧体磁芯中,当氧化铁的质量分数误差达到0.1%时,就会对磁芯的磁性产生很大影响,同时,氧化铁粉体的粒径较小时,可压缩性能更好,并有利于制备尺度较小的铁磁体[6]。高纯纳米氧化铁还有去除硫化氢的功能,氧化铁中所含杂质越少,脱硫性能就越好[7]。综上所述,不同应用领域均对高纯纳米氧化铁提出了高纯度、小粒径和窄粒度分布的苛刻要求。
制备纳米氧化铁的方法主要有水热法、溶剂热法、溶胶凝胶法、液相沉淀法、模板法、物理溅射法、脉冲激光沉积法、电子束蒸发法等[8-11]。余旺等[12]以硫酸亚铁(Fe2SO4)为原料,通过重结晶后的水热反应合成了质量分数为98.8%、粒径为580 nm的纳米氧化铁。焦建国[13]利用水热法制备出了羟基氧化铁(FeOOH),在温度为400 ℃时煅烧制得氧化铁纳米棒。郝素菊等[14]以九水合硝酸铁(Fe(NO3)3·9H2O)为原料,以尿素为沉淀剂,用热解前驱体法制得球状纳米氧化铁。目前,关于制备的纳米氧化铁的研究对纯度的关注度较低,导致其制备的纯度较低,主要原因是未对实验中所使用的铁源进行提纯处理,水热法制备难以完全去除氧化铁中剩余的铵根离子和硫酸根离子,因此,需要寻找一种操作简单有效的制备高纯纳米氧化铁的方法。
为了制备高纯纳米氧化铁,本文中首先采用重结晶法去除硫酸亚铁中Ca2+、Mg2+、Mn2+等杂质离子,采用氟化铵沉淀进一步去除硫酸亚铁中的Ca2+、Mg2+杂质离子,然后使用过氧化氢氧化法、氨水沉淀法对硫酸亚铁进行沉淀制得羟基氧化铁,接着采用调浆法和超声法洗涤羟基氧化铁制得前驱体,最后焙烧前驱体制得高纯纳米氧化铁;使用仪器和设备分析高纯纳米氧化铁的颗粒形貌、粒径分布和杂质离子的质量浓度,对制得的高纯纳米氧化铁产品进行验证。
1 方法
1.1 试剂材料和仪器设备
试剂材料:七水合硫酸亚铁(分析纯,上海泰坦科技股份有限公司); 过氧化氢(分析纯,国药集团化学试剂有限公司); 硫酸(分析纯,国药集团化学试剂有限公司); 氨水(分析纯,国药集团化学试剂有限公司); 氟化铵(分析纯,国药集团化学试剂有限公司)。
设备:HK2000ULT型超低温循环恒温槽(杭州三浦精密仪器公司); TL1200型卧式管式炉(南京亚玥五金机电有限公司); DK-8D型数显恒温水浴锅(金坛西城新瑞仪器厂); DHG-9145A型真空干燥箱(上海一恒科学仪器有限公司); F-12080型超声波清洗机(深圳市洁盟清洗设备有限公司)。
仪器:ICE-3000型原子吸收光谱仪(赛默飞世尔公司),LCMS-8040型电感耦合等离子体原子发射光谱仪(日本岛津公司),Rigaku Uitlmal V型X射线衍射仪(日本理学公司),Apreo 2型场发射扫描电子显微镜(赛默飞世尔公司),90Plus型纳米激光粒度仪(布鲁克海文公司),CT-20型笔式电导率仪(上海力辰仪器科技有限公司)。
利用电感耦合等离子体原子发射光谱仪检测七水合硫酸亚铁配置的溶液,硫酸亚铁溶液中的主要杂质离子Ca2+、Mg2+、Mn2+的初始质量浓度分别为161、128、91 mg/L。
1.2 制备
制备高纯纳米氧化铁的工艺流程图如图1所示。由图可知,首先,利用重结晶法一次提纯硫酸亚铁,将饱和硫酸亚铁溶液放入低温循环恒温槽中进行结晶,去除杂质后制得硫酸亚铁晶体,重复结晶步骤直到纯度达到要求; 其次,通过氟化铵沉淀进行二次提纯硫酸亚铁,先将初次提纯后的硫酸亚铁晶体配置为溶液,再向硫酸亚铁溶液中加入氟化铵和氨水,沉淀后再次去除杂质制得纯净硫酸亚铁溶液; 最后,向纯净硫酸亚铁溶液中加入过氧化氢进行氧化,并通过氨水沉淀制得羟基氧化铁,再对羟基氧化铁通过调浆法、超声洗涤法进一步去除杂质制得氧化铁前驱体,氧化铁前驱体经焙烧后制得高纯纳米氧化铁。
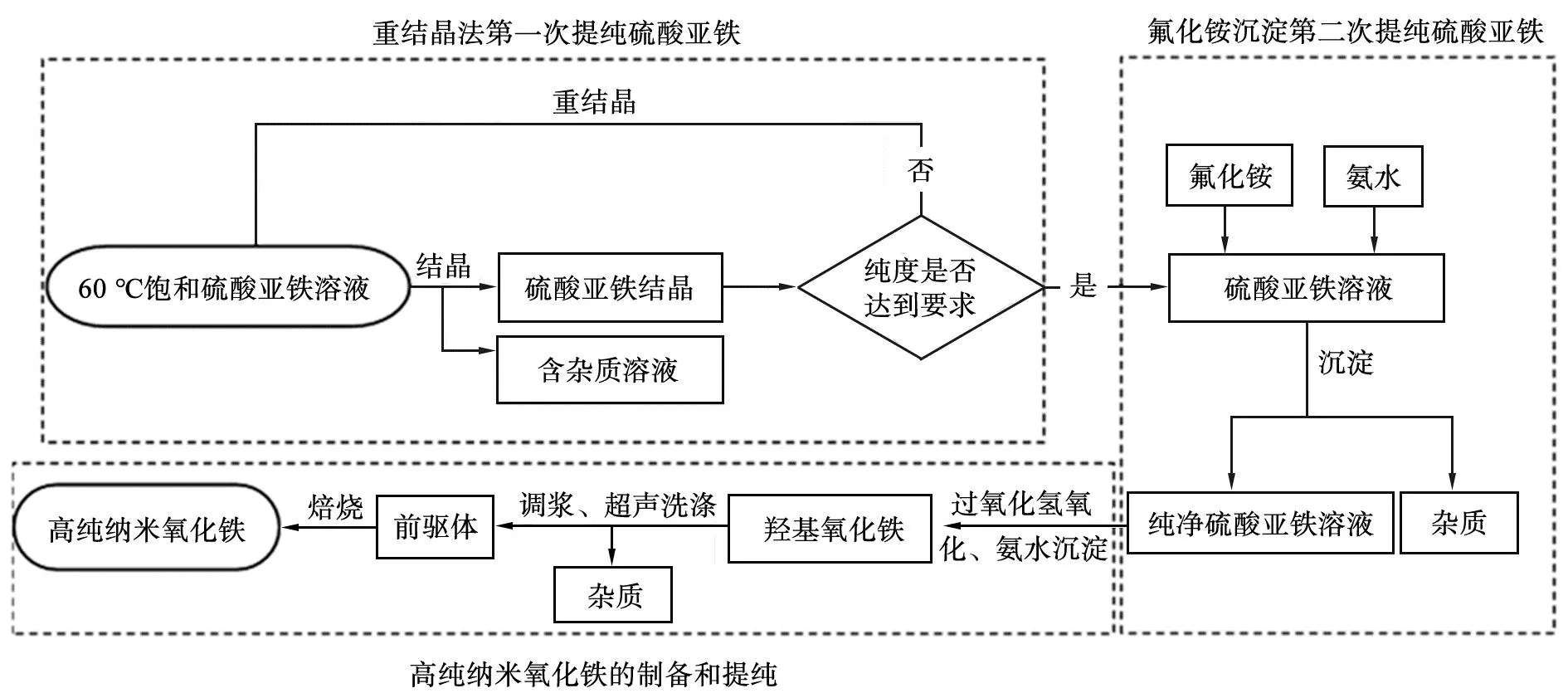
图1 制备高纯纳米氧化铁的工艺流程图
1.2.1 重结晶法第一次提纯硫酸亚铁
将60 ℃时饱和硫酸亚铁溶液放入低温循环水槽中,以不同的降温速率进行降温(直接放入结晶温度降温和降温速率为2 ℃/h),使得溶液的降低至不同的结晶温度(结晶温度为5~30 ℃),使得硫酸亚铁第一次结晶,待结晶稳定后,进行抽滤处理制得硫酸亚铁结晶体;整个结晶过程重复5次。
1.2.2 氟化铵沉淀第二次提纯硫酸亚铁
将上一步制备的硫酸亚铁结晶配置成Fe2+质量浓度为60 g/L溶液,加入稀氨水调节pH为2.5~8时,加入能使Ca2+、Mg2+完全沉淀的过量系数为1~15的氟化铵,在不同温度(分别为20~60 ℃)反应1 h后,将硫酸亚铁液体通过孔径为0.45 μm的滤膜过滤制得纯净硫酸亚铁溶液。
1.2.3 高纯纳米氧化铁的制备和提纯
向除杂后的硫酸亚铁溶液加入质量分数为10%的过氧化氢,将硫酸亚铁进行氧化;待溶液完全氧化后,加入稀氨水调节硫酸铁溶液的pH至6.5,制得羟基氧化铁沉淀;收集沉淀物,置入烧杯后重复加入去离子水,调浆洗涤沉淀物,直到过滤后滤液的总溶解固体值维持稳定;将溶液放入超声清洗器中继续清洗,记录不同洗涤时间和次数时的滤液总溶解固体值,直到总溶解固体值不再发生改变,固液分离后制得最终产物的前驱体;将前驱体放入真空干燥箱中烘干,干燥后将前驱体放入管式炉焙烧,在温度为500~800 ℃的空气中焙烧2 h,制得高纯纳米氧化铁。在制备过程中,过氧化氢氧化硫酸亚铁、氨水沉淀、焙烧氢氧化铁时发生的化学反应的方程式分别为

(1)

(2)

(3)
1.3 物相分析
使用原子吸收光谱仪、电感耦合等离子体原子发射光谱仪分析硫酸亚铁溶液和高纯纳米氧化铁中的离子质量浓度;针对最终产物高纯纳米氧化铁,使用X射线衍射仪分析物相组成,使用场发射扫描电子显微镜分析颗粒形貌,使用纳米激光粒度仪分析粒径分布。
2 结果与讨论
2.1 重结晶法
硫酸亚铁的溶解度在温度为60 ℃时最大,选取硫酸亚铁饱和溶液为初始溶液。随着温度的下降,硫酸亚铁的溶解度快速减小,当温度约为0 ℃时,硫酸亚铁溶液到达冰点,故结晶温度应大于0 ℃。不同结晶温度条件下硫酸亚铁晶体中杂质离子的质量浓度如图2所示。由图可知,硫酸亚铁晶体中Ca2+、Mg2+、Mn2+离子的质量浓度随着结晶温度的降低而减小,这是因为,温度较低时,杂质离子的动能较小,富集速度较慢,此时硫酸亚铁结晶中富集的杂质减少; 当结晶温度低于10 ℃时,硫酸亚铁晶体中3种杂质离子的质量浓度均较小,杂质 Ca2+、Mg2+、Mn2+的质量浓度分别34、33、15 mg/L。综上,饱和硫酸亚铁溶液的结晶温度选为10 ℃。

图2 不同结晶温度下硫酸亚铁晶体中杂质离子的质量浓度
为了研究降温速率对硫酸亚铁晶体中各杂质离子质量浓度的影响,配置好温度为60 ℃的饱和硫酸亚铁溶液后,分别按照快速降温(直接放入温度为10 ℃的冷却槽中)和缓慢降温(降温速率为2 ℃/h)的方法,将溶液温度调节至结晶温度10 ℃,然后进行实验,检测硫酸亚铁晶体中杂质离子的质量浓度。不同降温速率下硫酸亚铁晶体中各杂质离子的质量浓度如图3所示。由图可知,硫酸亚铁晶体中质量浓度从大到小的杂质离子依次为Ca2+、Mg2+、Mn2+,缓慢降温时Ca2+、Mg2+、Mn2+的质量浓度分别为36、35、13 mg/L,快速降温时Ca2+、Mg2+、Mn2+的质量浓度分别为43、32、12 mg/L;对同一种离子而言,缓慢降温和快速降温对硫酸亚铁晶体中杂质离子的质量浓度的影响并不明显,这是因为,无机物离子的性质与硫酸亚铁的差异较小,在结晶过程中,部分杂质离子被夹杂在晶体内部,难以通过1次重结晶过程去除杂质离子。综上,选取快速降温法进行重结晶。
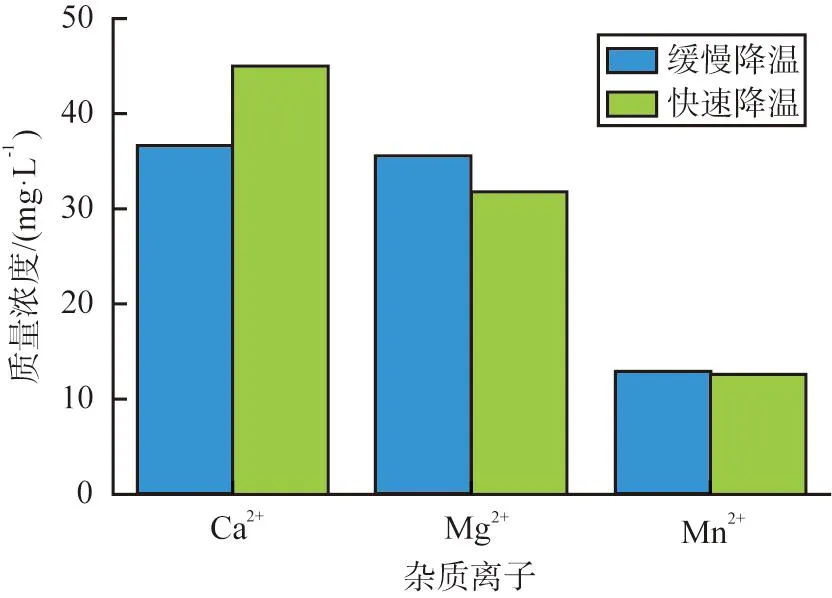
图3 不同降温速率下硫酸亚铁晶体中杂质离子的质量浓度
重结晶次数对硫酸亚铁晶体中杂质离子质量浓度影响如图4所示。由图可知,第2次重结晶时,硫酸亚铁中Ca2+、Mg2+、Mn2+的质量浓度分别从161、128、91 mg/L减小到20、16、6 mg/L,结晶提纯效果明显;随着重结晶次数的继续增加,杂质离子的质量浓度的减小幅度逐渐变缓,每次重结晶的回收率在60%左右,硫酸亚铁中的3种杂质离子的质量浓度逐渐趋于0,可见重复结晶能够有效地去除硫酸亚铁晶体的杂质[15]。综上,重结晶次数控制在2次较为合适。

图4 重结晶次数对硫酸亚铁晶体中杂质离子的质量浓度影响
2.2 氟化铵沉淀
氟化铵去除杂质时硫酸亚铁溶液pH对杂质离子质量浓度的影响如图5所示。由图可见,随着硫酸亚铁溶液pH的增大,Ca2+、Mg2+的质量浓度减小,Ca2+、Mg2+分别形成CaF2、MgF2沉淀物;当pH为6时,硫酸亚铁溶液中Ca2+、Mg2+的质量浓度为11.5、7.0 mg/L,当pH>7,溶液中生成较多FeOOH沉淀物。当溶液pH为4时,Ca2+、Mg2+的去除率存在一个最低点,原因是溶液pH为3.5~4时会形成[MFn]2-n配合离子(M为Ca2+、Mg2+等杂质离子),部分CaF2、MgF2沉淀物会重新溶解,导致Ca2+、Mg2+在溶液中质量浓度的减小趋势减缓[16-17]。综上所述,采用氟化铵去除杂质时,选取硫酸亚铁溶液pH为6。
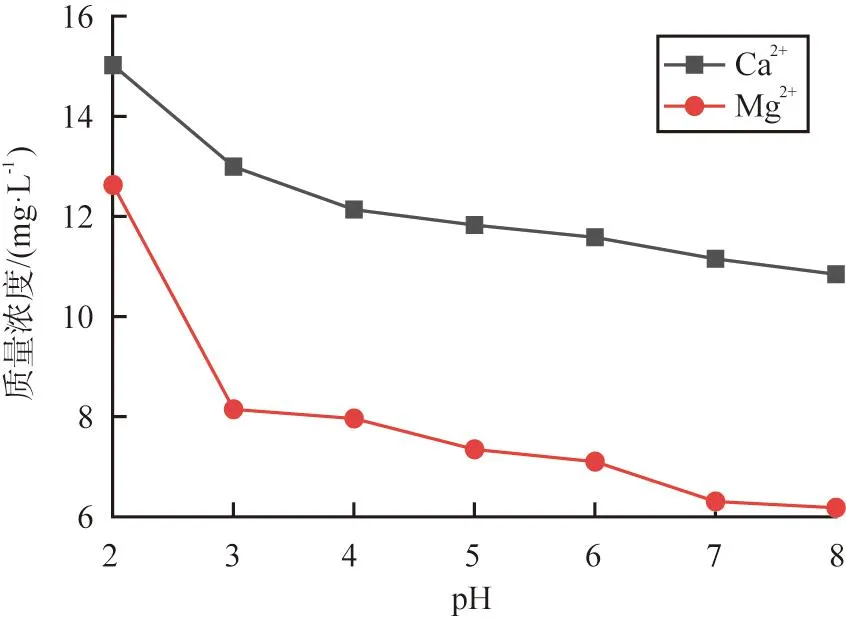
图5 氟化铵去除杂质时硫酸亚铁溶液pH对杂质离子质量浓度的影响
氟化铵去除杂质时,反应温度对杂质离子质量浓度的影响如图6所示。由图可见,在温度为30 ℃时,硫酸亚铁溶液中 Ca2+、Mg2+质量浓度分别为11.5、6.7 mg/L;在温度高于40 ℃时,大部分FeOOH沉淀物从溶液中去除,Ca2+、Mg2+在硫酸亚铁溶液中质量浓度相对增大。综上所述,采用氟化铵去除杂质时,需控制反应温度为30 ℃。
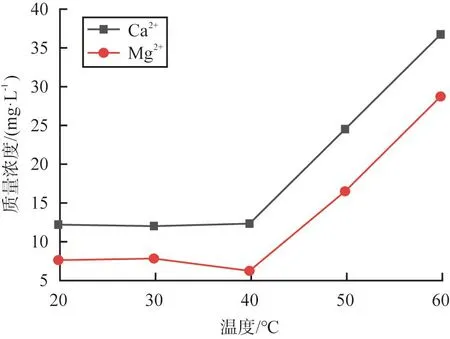
图6 氟化铵去除杂质时反应温度对杂质离子的质量浓度的影响
氟化铵过量系数为1时,氟化铵可与硫酸亚铁溶液中的Ca2+、Mg2+完全反应,将氟化铵过量系数设为1~15,氟化铵过量系数对杂质离子的质量浓度的影响如图7所示。由图可见,随着氟化铵过量系数的增大,溶液中Ca2+、Mg2+质量浓度逐渐减小; 当氟化铵过量系数为5时,硫酸亚铁溶液中 Ca2+、Mg2+的质量浓度为10.4、6.5 mg/L;当氟化铵过量系数大于5时,Ca2+、Mg2+质量浓度减小趋势减缓。因为CaF2、MgF2、FeF2的沉淀溶解平衡常数分别为2.7×10-11、6.4×10-9、2.36×10-6,硫酸亚铁溶液中的3种离子的沉淀顺序依次为Ca2+、Mg2+、Fe2+。过量的F-和溶液中硫酸亚铁溶液中少部分的Fe2+反应,以FeF2沉淀物形式从溶液中去除,但添加过多的氟化铵仍可能引入额外杂质。综上所述,氟化铵过量系数选择为5。
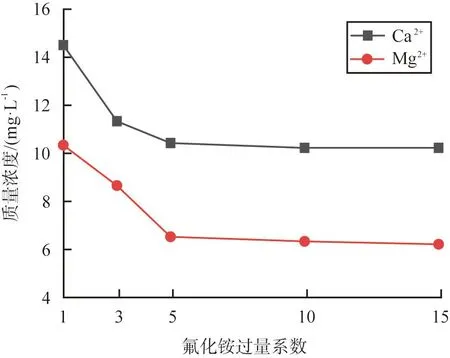
图7 氟化铵过量系数对杂质离子的质量浓度的影响
2.3 调浆洗涤法和超声洗涤法
羟基氧化铁中的铵根离子和硫酸根离子的质量浓度随着调浆洗涤次数的变化如图8所示。由图可知,随着调浆洗涤次数的增多,固液分离后的滤液中,羟基氧化铁中的铵根离子和硫酸根离子的质量浓度逐渐减小,从3 500 mg/L减小至18 mg/L,说明重复洗涤对于铵根离子和硫酸根离子有着较好的去除效果,重复8次调浆洗涤后能够有效去除羟基氧化铁中的铵根离子和硫酸根离子。

图8 铵根离子和硫酸根离子的质量浓度随着调浆洗涤次数的变化
羟基氧化铁中的铵根离子和硫酸根离子的质量浓度随超声洗涤时间的变化如图9所示。由图可见,超声洗涤1次时,在洗涤时间20 min内,羟基氧化铁中的铵根离子和硫酸根离子的质量浓度急剧增大至25 mg/L,洗涤时间为30~60 min时,铵根离子和硫酸根离子的质量浓度变化不大; 重复3次超声洗涤后,铵根离子和硫酸根离子的质量浓度约为17 mg/L,较为稳定。在超声辅助洗涤时,粉体的分散性增强,溶液中生产大量的空化气泡有助于破碎团聚物,使羟基氧化铁沉淀物中夹杂的铵根离子和硫酸根离子溶解在溶液中[18]。综上所述,通过3次超声洗涤能够有效去除羟基氧化铁沉淀中铵根离子和硫酸根离子。
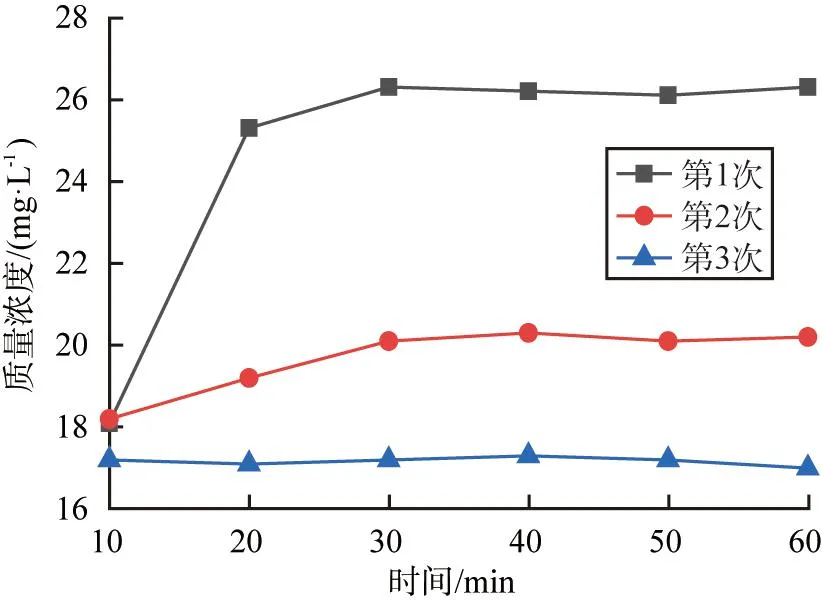
图9 铵根离子和硫酸根离子的质量浓度随超声洗涤时间的变化
2.4 高纯纳米氧化铁的物相分析
不同焙烧温度时的高纯纳米氧化铁的XRD谱图如图10所示。由图可见,在不同温度下焙烧时,衍射峰的位置未发生变化,对应的卡片号为PdfNo.5-637,说明产物均为高纯纳米氧化铁;当焙烧温度为600~800 ℃时,产物结晶度较好。综合考虑各方因素,选取焙烧温度为600 ℃。
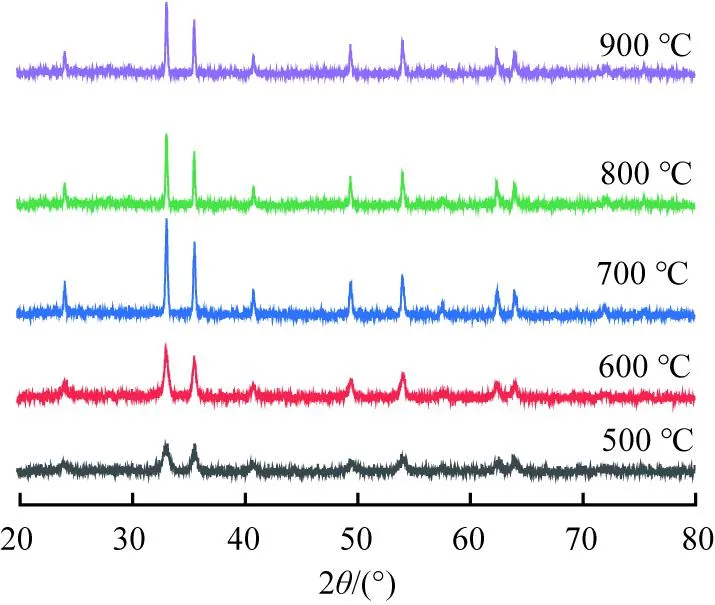
图10 不同焙烧温度时的高纯纳米氧化铁的XRD谱图
采用盐酸溶液溶解在温度为600 ℃时焙烧制得的高纯纳米氧化铁,高纯纳米氧化铁中主要杂质离子质量浓度如表1所示。由表1可知,Ca2+、Si4+的质量浓度分别128、118 mg/L,而Mg2+、Mn2+、Al3+、Zn2+、K+、S2+等杂质离子的质量浓度均小于50 mg/L,总杂质离子质量浓度小于500 mg/L,经换算可知制得的高纯纳米氧化铁中α-Fe2O3的质量分数大于99.95%。

表1 高纯纳米氧化铁中主要杂质离子的质量浓度
不同放大倍数下的高纯纳米氧化铁的SEM图像如图11所示。由图可见,在焙烧温度为600 ℃时,高纯纳米氧化铁均为球形颗粒,形貌均一,粒度为纳米级,颗粒间存在团聚现象,这是因为高纯纳米氧化铁粒子径小,比表面积大,表面能高,容易产生团聚体[19]。

(a)放大倍数为5 000
高纯纳米氧化铁的粒径分布曲线如图12所示。由图可见,氧化铁的中位粒径D50为300 nm,粒径分布较窄。
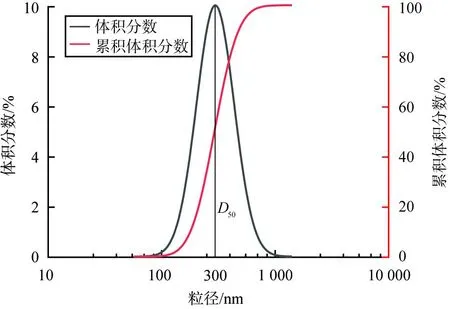
图12 高纯纳米氧化铁的粒径分布曲线
3 结论
在制备高纯纳米氧化铁过程中,首先采用重结晶法去除硫酸亚铁中Ca2+、Mg2+、Mn2+等杂质,采用氟化铵沉淀进一步去除硫酸亚铁中的Ca2+、Mg2+杂质,然后使用过氧化氢氧化法、氨水沉淀法对硫酸亚铁进行沉淀制得羟基氧化铁,采用调浆法和超声法洗涤羟基氧化铁制得前驱体,最后焙烧前驱体制得高纯纳米氧化铁,结论如下:
1)采用重结晶法对硫酸亚铁溶液进行提纯时,饱和硫酸亚铁溶液的结晶温度选为10 ℃,采用快速降温法进行2次重结晶,硫酸亚铁中杂质离子Ca2+、Mg2+、Mn2+的质量浓度分别从161、128、91 mg/L减小为20、16、6 mg/L。
2)采用氟化铵对硫酸亚铁溶液进行提纯时,用稀氨水调节硫酸亚铁溶液pH为6,反应温度设为30 ℃,氟化铵的过量系数设为5,沉淀后硫酸亚铁溶液中Ca2+、Mg2+的质量浓度分别减小为10.4、6.5 mg/L。
3)采用调浆洗涤法和超声洗涤法去除羟基氧化铁中的铵根离子和硫酸根离子,8次调浆洗涤后滤液中铵根离子和硫酸根离子质量浓度从3 500 mg/L减小至18 mg/L,3次超声洗涤后滤液的质量浓度为17 mg/L,趋于稳定。
4)制得的高纯纳米氧化铁为球形颗粒,形貌均匀,中位粒径为300 nm,高纯纳米氧化铁中α-Fe2O3的质量分数大于99.95%。
利益冲突声明(Conflict of Interests)
所有作者声明不存在利益冲突。
All authors disclose no relevant conflict of interests.
作者贡献(Author’s Contributions)
吴文军、韩召和张福元进行了方案设计,吴文军和刘鹏飞参与了论文的写作和修改。所有作者均阅读并同意了最终稿件的提交。
The study was designed by Wu Wenjun、Han Zhao and Zhang Fuyuan.The manuscript was written and revised by Wu Wenjun and Liu Pengfei.All authors have read the last version of paper and consented for submission.

