PLA2G4和ABCC1基因多态性与支气管哮喘患儿孟鲁司特疗效的研究*
任梦洋,魏兵,李令雪,贾京晶,张世楠,尤瑄,支艳杰
(1.惠州市第一妇幼保健院,广东 惠州 516007;2.中国人民解放军北部战区总医院,辽宁沈阳 110016;3.中国医科大学北部战区总医院研究生培养基地,辽宁 沈阳 110016;4.大连医科大学北部战区总医院研究生培养基地,辽宁 沈阳 110016)
支气管哮喘是与可逆性气流阻塞且与支气管高反应相关的慢性炎症病变。全世界有3 亿多人患有支气管哮喘,被认为是儿童最常见的疾病之一,1990年全国城市14 岁以下儿童支气管哮喘的累计患病率为1.09%,2000年为1.97%,2010年为3.02%,20 余年来我国儿童支气管哮喘的患病率呈明显上升趋势[1-4]。支气管哮喘的发病机制很复杂,多为基因和环境因素相互作用,现致病机制仍未明确,对该疾病的治疗也以预防慢性症状、维持肺功能和允许正常的日常活动为主,使患儿达到“无症状”状态[5]。孟鲁司特是最常用的白三烯受体拮抗剂,是目前治疗儿童支气管哮喘的主要药物之一。有研究证明孟鲁司特可显著降低气道高反应性,改善气道重塑,但孟鲁司特疗效有明显的个体差异,其原因除患儿耐药性差异外,还可能与患儿体内白三烯(Leukotriene,LTs)调控及转运基因的多态性有关[6-7]。LTs 是花生四烯酸的水解产物,磷脂酶A2是水解花生四烯酸的关键酶,ATP 结合盒亚家族C 成员1(ATP-binding cassette subfamily C member 1,ABCC1)基因编码的多药耐药相关蛋白1 是内源性物质LTs 的转运蛋白[8-9]。因此推测,调控和转运LTs 的胞浆型磷脂酶A2(recombinant cytosolic phospholipase A2,PLA2G4)基因和ABCC1 基因是影响孟鲁司特疗效发挥的重要因素之一。本研究通过分析PLA2G4 基因和ABCC1 基因多态性与哮喘儿童孟鲁司特疗效的反应性,希望为支气管哮喘患儿提供潜在的药物遗传学标记及用药方案指导。
1 资料与方法
1.1 研究对象
选取2019年3月—2021年9月于中国人民解放军北部战区总医院诊治的121 例支气管哮喘患儿为研究对象。其中,男性80 例,女性41 例;年龄4~9 岁。所有入组儿童为东北地区汉族儿童。纳入标准:①符合中华医学会儿科学分会呼吸学组制订的《儿童支气管哮喘诊断与防治指南(2016年版)》[4]的诊断标准;②1 个月内未全身使用糖皮质激素或免疫调节剂;③能够配合完成肺功能检查和治疗。排除标准:①既往有反复呼吸道感染史;②合并有心血管、肝、肾、内分泌或造血系统等严重原发性疾病及精神病;③对本研究中的药物过敏。本研究经医院医学伦理委员会批准[伦审Y(2020)054 号],所有患儿家属签署知情同意书。
1.2 治疗方法
根据疾病发作时的严重程度,依据《儿童支气管哮喘诊断与防治指南(2016年版)》[4]的治疗方案,给予常规吸氧、雾化平喘、祛痰止咳、抗感染、纠正酸碱平衡等对症治疗。所有患儿睡前口服1次孟鲁司特(顺尔宁,杭州默沙东有限公司,国药准字:J20140167),2~5 岁患儿服用剂量为4 mg,6~14 岁患儿服用剂量为5 mg,1 次/d,连续治疗1 个月。
1.3 基因型检测
抽取受试儿童外周静脉血3 mL 于抗凝管中,置入-80 ℃冰箱冷冻保存备用,提取各样本血细胞基因组DNA 行PCR 扩增,应用Primer 3 软件设计PCR引物(上海生工生物工程股份有限公司),引物序列见表1。反应条件:95 ℃预变性2 min,94 ℃变性20 s,65 ℃退火40 s,72 ℃延伸1.5 min,共35 个循环。PCR 产物纯化后,采用ABI3730XL 测序仪对PLA2G4 基因rs10157410、rs10489409、rs932476 位点和ABCC1 基因rs215066 位点进行基因型检测(上海天昊生物科技有限公司)。

表1 PLA2G4、ABCC1基因各位点的引物序列
1.4 观察指标
1.4.1 肺功能检查治疗前及治疗1 个月后应用肺功能仪(型号:MasterScreen,德国JAEGER 公司)对患儿进行肺通气功能检查,数据均用实测值占预计值百分比表示,纳入指标包含:用力肺活量占预计值百分比(forced vital capacity in predicted,FVC%pred)、第1秒用力呼气容积占预计值百分比(forced expiratory volume in one second in predicted,FEV1%pred)、第1 秒用力呼气容积与用力肺活量比值(forced expiratory volume in one second to forced vital capacity ratio,FEV1/FVC)、最大呼气流量占预计值百分比(maximal expiratory flow in predicted,PEF%pred)、用力呼出50%肺活量时的瞬时流量占预计值百分比(forced expiratory flow at 50% of forced vital capacity in predicted,FEF50%pred)、FEF75%pred。
1.4.2 呼出气一氧化氮(fractional exhaled nitric oxide,FeNO)检查检测仪器为一氧化氮分析仪(型号:NIOX VERO,英国CIRCASSIA 公司),操作参照《儿童肺功能及气道非创伤性炎症指标系列指南(七):呼出气体一氧化氮监测》[10]。所有受试者需在检测前4 h 内禁食酒精类食物,2 h 内禁食含硝酸盐食物、禁食水、避免剧烈运动。测试过程中应保持吸气及呼气连续进行,不可屏气或停顿。
1.4.3 实验室指标分别抽取治疗前和治疗1 个月后患儿空腹静脉血2 mL,采用血细胞分析仪(型号:LH780,德国COULTER 公司)检测嗜酸性粒细胞计数(eosinophil count,EOS),采用酶联免疫吸附试验检测患儿免疫球蛋白E(Immunoglobulin E,IgE)水平,操作严格按照试剂盒说明书进行。
1.5 疗效评价
依据《儿童支气管哮喘诊断与防治指南(2016年版)》[4]对患儿近4 周的哮喘症状进行控制水平分级。评估项目:日间症状(<6 岁,>1 次/周;≥ 6 岁,>2 次/周);夜间因哮喘憋醒或咳嗽;应急缓解药物使用(<6 岁,>1 次/周;≥ 6 岁,>2 次/周);因哮喘出现活动受限。良好控制:无上述各项;部分控制:存在1 或2 项;未控制:存在3 或4 项。
1.6 统计学分析
数据分析采用SPSS 23.0 统计软件。计量资料以均值±标准差(±s)表示,符合正态分布和方差齐性检验的两组比较用t检验、多组比较用单因素方差分析,符合正态分布但不符合方差齐性检验的两组及多组比较用非参数检验;计数资料以构成比(%)表示,比较用χ2检验;等级资料以等级表示,比较用Kruskal-WallisH非参数检验。采用Logistic 回归对PLA2G4 基因与孟鲁司特疗效进行分析。P<0.05 为差异有统计学意义。
2 结果
2.1 PLA2G4、ABCC1 基因各位点不同基因型治疗前后肺功能指标比较
如表2、3所示,PLA2G4 基因rs10157410、rs10489409 和rs932476 位点不同基因型间的肺功能指标治疗前后比较,差异均无统计学意义(P>0.05)。PLA2G4 基因rs10157410 位点GC 和GG 基因型、rs10489409 位点CT 和TT 基因型和rs932476 位点GA 和 AA 基 因 型 的 FEV1%pred、FEV1/FVC、FEF50%pred、FEF75%pred 治疗前后比较,差异均有统计学意义(P<0.05);治疗后较治疗前均升高。此外,PLA2G4 基因rs932476 位点GG 基因型的FEV1/FVC 和FEF75%pred 治疗前后比较,差异有统计学意义(P<0.05);治疗后较治疗前升高。ABCC1 基因rs215066 位点只检测出1 种基因型GG,故不再进行基因型间的肺功能指标分析。孟鲁司特治疗前后ABCC1 基因rs215066 位点GG 基因型的FEV1%pred、FEV1/FVC、FEF50%pred、FEF75%pred 比较,差异均有统计学意义(P<0.05);治疗后较治疗前均升高。
表2 PLA2G4基因各位点不同基因型治疗前后肺功能指标比较 (±s)
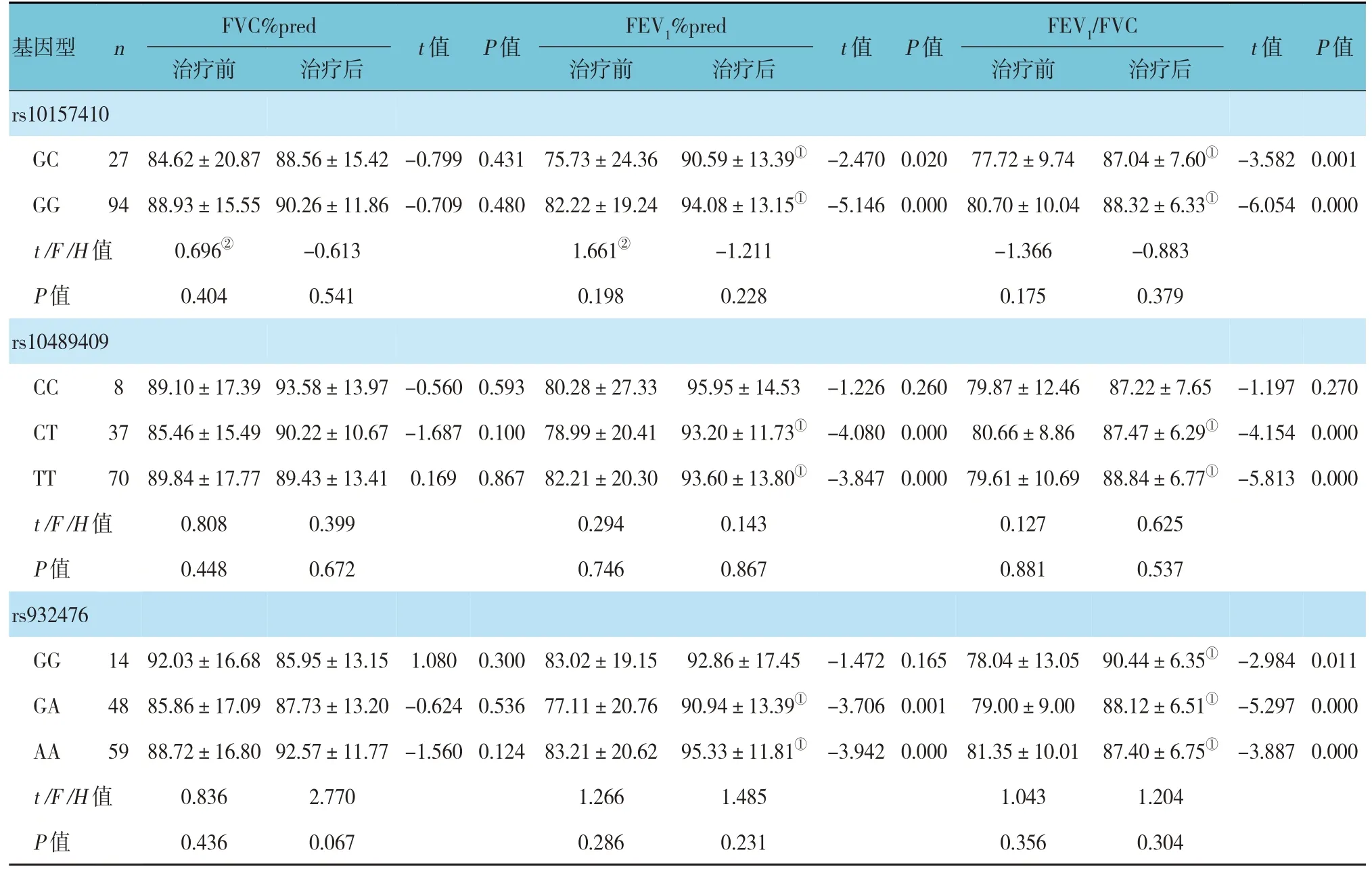
表2 PLA2G4基因各位点不同基因型治疗前后肺功能指标比较 (±s)
基因型n FVC%pred治疗前t 值P 值FEV1%pred治疗前P 值t 值P 值FEV1/FVC治疗前治疗后治疗后rs10157410 GC 27 84.62±20.87 88.56±15.42治疗后-0.799 0.431 75.73±24.36 90.59±13.39①t 值-2.470 0.020 77.72±9.74 87.04±7.60①-3.582 0.001 GG 94 88.93±15.55 90.26±11.86-0.7090.480 82.22±19.24 94.08±13.15①-5.1460.000 80.70±10.04 88.32±6.33①-6.0540.000 t/F/H 值0.696②-0.613 1.661②-1.211-1.366-0.883 P 值rs10489409 0.404 0.541 0.198 0.228 0.175 0.379 CC 8 89.10±17.39 93.58±13.97-0.560 0.593 80.28±27.33 95.95±14.53-1.226 0.260 79.87±12.46 87.22±7.65-1.197 0.270 CT 37 85.46±15.49 90.22±10.67-1.6870.100 78.99±20.41 93.20±11.73①-4.0800.000 80.66±8.86 87.47±6.29①-4.1540.000 TT 70 89.84±17.77 89.43±13.41 0.169 0.867 82.21±20.30 93.60±13.80①-3.847 0.000 79.61±10.69 88.84±6.77①-5.813 0.000 t/F/H 值0.808 0.399 0.294 0.143 0.127 0.625 P 值rs932476 0.448 0.672 0.746 0.867 0.881 0.537 GG 14 92.03±16.68 85.95±13.15 1.080 0.300 83.02±19.15 92.86±17.45-1.4720.165 78.04±13.05 90.44±6.35①-2.9840.011 GA 48 85.86±17.09 87.73±13.20-0.624 0.536 77.11±20.76 90.94±13.39①-3.706 0.001 79.00±9.00 88.12±6.51①-5.297 0.000 AA 59 88.72±16.80 92.57±11.77-1.5600.124 83.21±20.62 95.33±11.81①-3.9420.000 81.35±10.01 87.40±6.75①-3.8870.000 t/F/H 值0.836 2.770 1.266 1.485 1.043 1.204 P 值0.436 0.067 0.286 0.231 0.356 0.304
续表2
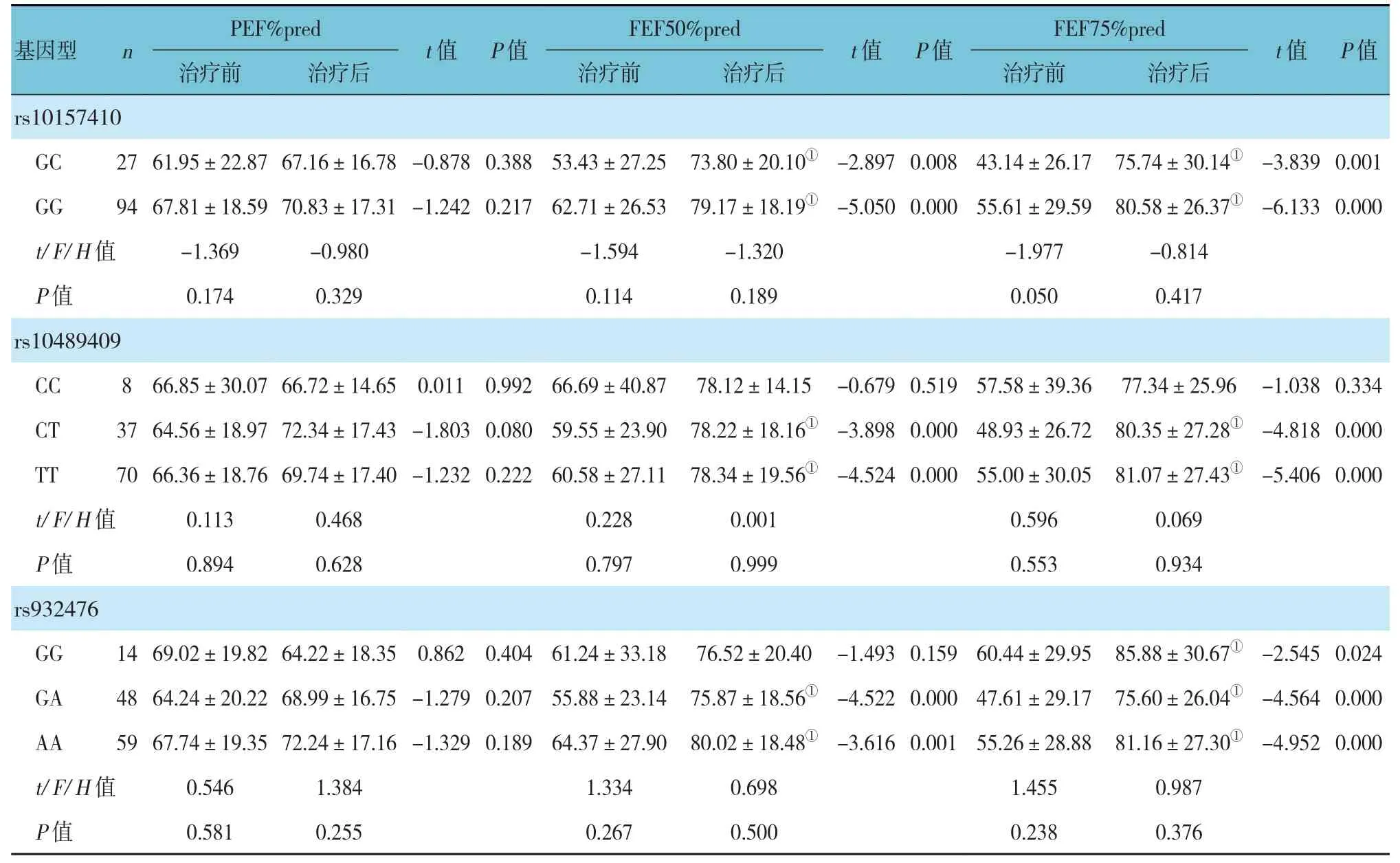
表2 PLA2G4基因各位点不同基因型治疗前后肺功能指标比较 (±s)
注:①与治疗前比较,P<0.05;②为非参数检验H 值。
基因型n PEF%pred治疗前t 值P 值t 值P 值t 值P 值治疗后FEF50%pred治疗前治疗后FEF75%pred治疗前治疗后rs10157410 GC 27 61.95±22.87 67.16±16.78-0.878 0.388 53.43±27.25 73.80±20.10①-2.897 0.008 43.14±26.17 75.74±30.14①-3.839 0.001 GG 94 67.81±18.59 70.83±17.31-1.242 0.217 62.71±26.53 79.17±18.19①-5.050 0.000 55.61±29.59 80.58±26.37①-6.133 0.000 t/F/H 值-1.369-0.980-1.594-1.320-1.977-0.814 P 值rs10489409 0.174 0.329 0.114 0.189 0.050 0.417 CC 8 66.85±30.07 66.72±14.65 0.011 0.992 66.69±40.87 78.12±14.15-0.679 0.519 57.58±39.36 77.34±25.96-1.038 0.334 CT 37 64.56±18.97 72.34±17.43-1.803 0.080 59.55±23.90 78.22±18.16①-3.898 0.000 48.93±26.72 80.35±27.28①-4.818 0.000 TT 70 66.36±18.76 69.74±17.40-1.232 0.222 60.58±27.11 78.34±19.56①-4.524 0.000 55.00±30.05 81.07±27.43①-5.406 0.000 t/F/H 值0.113 0.468 0.228 0.001 0.596 0.069 P 值rs932476 0.894 0.628 0.797 0.999 0.553 0.934 GG 14 69.02±19.82 64.22±18.35 0.862 0.404 61.24±33.18 76.52±20.40-1.493 0.159 60.44±29.95 85.88±30.67①-2.545 0.024 GA 48 64.24±20.22 68.99±16.75-1.279 0.207 55.88±23.14 75.87±18.56①-4.522 0.000 47.61±29.17 75.60±26.04①-4.564 0.000 AA 59 67.74±19.35 72.24±17.16-1.329 0.189 64.37±27.90 80.02±18.48①-3.616 0.001 55.26±28.88 81.16±27.30①-4.952 0.000 t/F/H 值0.546 1.384 1.334 0.698 1.455 0.987 P 值0.581 0.255 0.267 0.500 0.238 0.376
表3 ABCC1基因rs215066位点治疗前后肺功能指标比较 (n=121,±s)
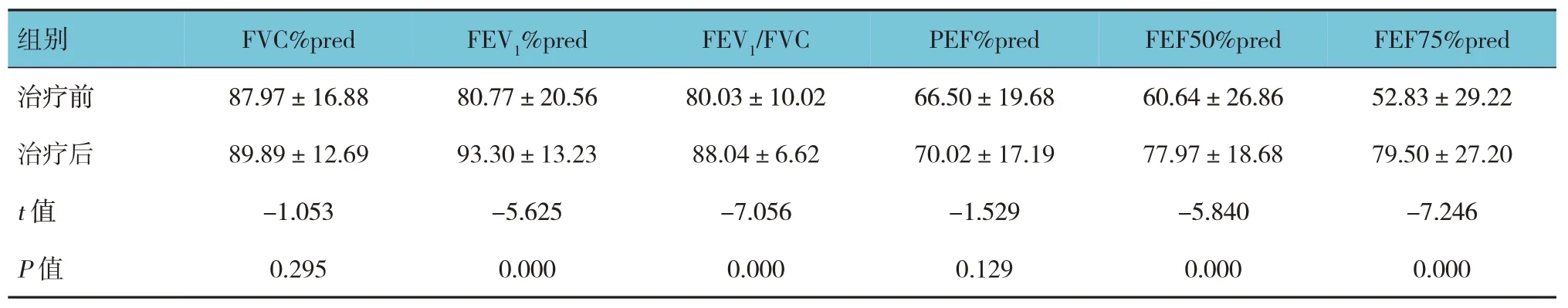
表3 ABCC1基因rs215066位点治疗前后肺功能指标比较 (n=121,±s)
组别FVC%pred FEV1%pred FEV1/FVC PEF%pred FEF50%pred FEF75%pred治疗前治疗后t 值P 值87.97±16.88 89.89±12.69-1.053 0.295 80.77±20.56 93.30±13.23-5.625 0.000 80.03±10.02 88.04±6.62-7.056 0.000 66.50±19.68 70.02±17.19-1.529 0.129 60.64±26.86 77.97±18.68-5.840 0.000 52.83±29.22 79.50±27.20-7.246 0.000
2.2 PLA2G4、ABCC1 基因各位点不同基因型治疗前后炎症指标比较
PLA2G4 基因rs10157410、rs10489409、rs932476位点不同基因型间的炎症指标治疗前后比较,差异均无统计学意义(P>0.05)。治疗前后PLA2G4 基因rs10489409 位点CC 基因型的EOS 比较,差异无统计学意义(P>0.05),PLA2G4、ABCC1 基因各位点不同基因型的炎症指标比较,差异均有统计学意义(P<0.05);治疗后较治疗前改善。见表4。
表4 PLA2G4、ABCC1基因各位点不同基因型治疗前后炎症指标比较 (±s)
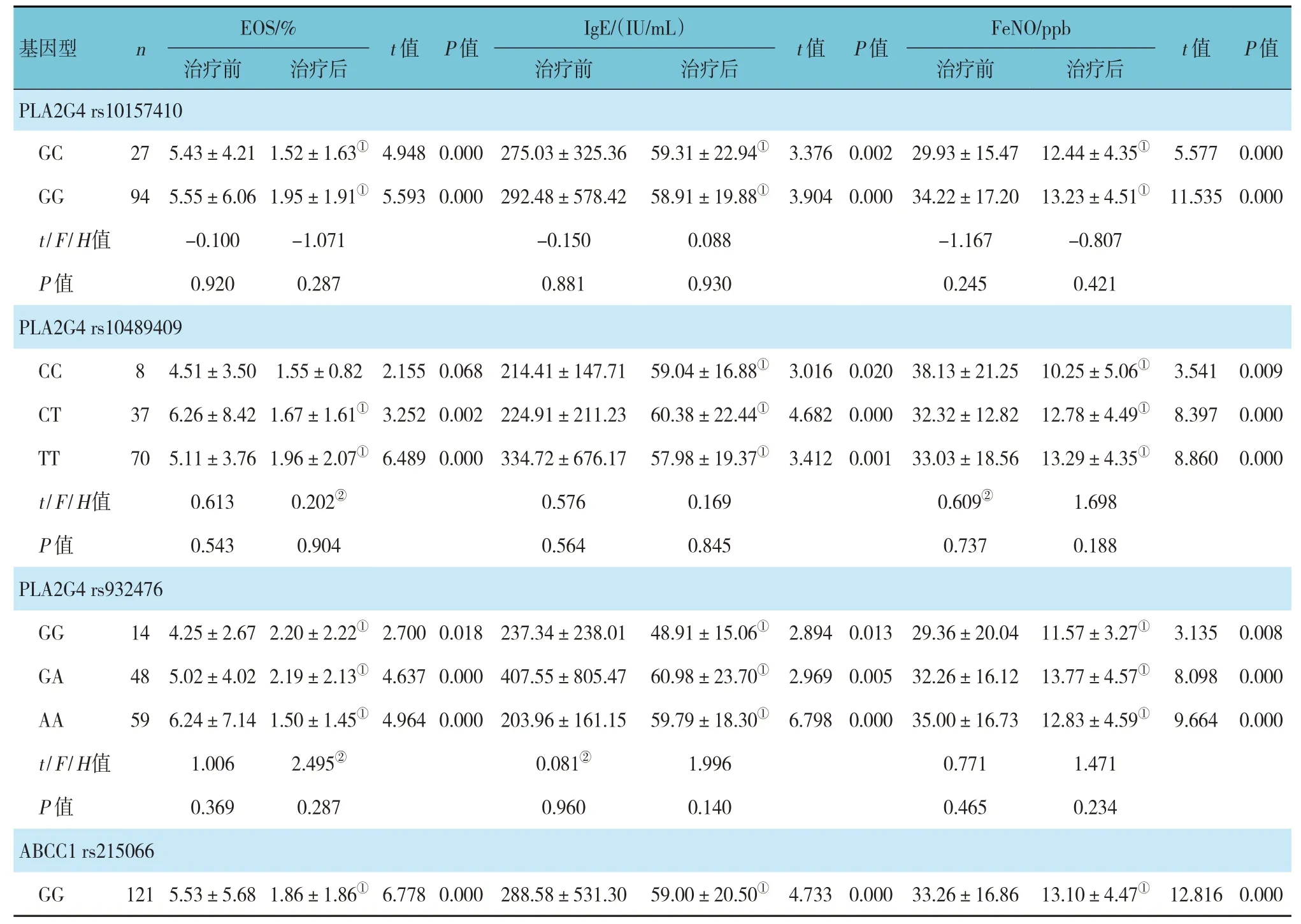
表4 PLA2G4、ABCC1基因各位点不同基因型治疗前后炎症指标比较 (±s)
注:①与治疗前比较,P<0.05;②非参数检验H 值。
基因型n EOS/%治疗前t 值P 值IgE/(IU/mL)治疗前t 值P 值t 值P 值治疗后治疗后FeNO/ppb治疗前治疗后PLA2G4 rs10157410 GC 27 5.43±4.21 1.52±1.63①4.9480.000 275.03±325.36 59.31±22.94①3.376 0.002 29.93±15.47 12.44±4.35①5.577 0.000 GG 94 5.55±6.06 1.95±1.91①5.593 0.000 292.48±578.42 58.91±19.88①3.904 0.000 34.22±17.20 13.23±4.51①11.535 0.000 t/F/H值-0.100-1.071-0.150 0.088-1.167-0.807 P 值PLA2G4 rs10489409 0.920 0.287 0.881 0.930 0.245 0.421 CC 8 4.51±3.50 1.55±0.82 2.155 0.068 214.41±147.71 59.04±16.88①3.016 0.020 38.13±21.25 10.25±5.06①3.541 0.009 CT 37 6.26±8.42 1.67±1.61①3.2520.002 224.91±211.23 60.38±22.44①4.682 0.000 32.32±12.82 12.78±4.49①8.397 0.000 TT 70 5.11±3.76 1.96±2.07①6.489 0.000 334.72±676.17 57.98±19.37①3.412 0.001 33.03±18.56 13.29±4.35①8.860 0.000 t/F/H值0.613 0.202②0.576 0.169 0.609②1.698 P 值PLA2G4 rs932476 0.543 0.904 0.564 0.845 0.737 0.188 GG 14 4.25±2.67 2.20±2.22①2.700 0.018 237.34±238.01 48.91±15.06①2.894 0.013 29.36±20.04 11.57±3.27①3.135 0.008 GA 48 5.02±4.02 2.19±2.13①4.6370.000 407.55±805.47 60.98±23.70①2.969 0.005 32.26±16.12 13.77±4.57①8.098 0.000 AA 59 6.24±7.14 1.50±1.45①4.964 0.000 203.96±161.15 59.79±18.30①6.798 0.000 35.00±16.73 12.83±4.59①9.664 0.000 t/F/H值1.006 2.495②0.081②1.996 0.771 1.471 P 值ABCC1 rs215066 0.369 0.287 0.960 0.140 0.465 0.234 GG 0.000 121 5.53±5.68 1.86±1.86①6.778 0.000 288.58±531.30 59.00±20.50①4.733 0.000 33.26±16.86 13.10±4.47①12.816
2.3 PLA2G4、ABCC1 基因各位点不同基因型的症状控制水平分级及Logistic回归分析
PLA2G4 基因3 个位点的症状控制水平分级比较结果显示,rs10157410 位点和rs932476 位点基因型间的症状控制水平分级比较,差异均有统计学意义(P<0.05);其中rs10157410 位点GC 基因型良好控制比例明显高于GG 基因型,未控制显著低于GG 基因型(P<0.05);rs932476 位点GA 和AA 基因型的良好控制比例与GG 基因型比较,差异有统计学意义(P<0.05)。ABCC1 基因rs215066 位点只检测出1 种基因型,故未做基因型间的症状控制水平分级比较。见表5。
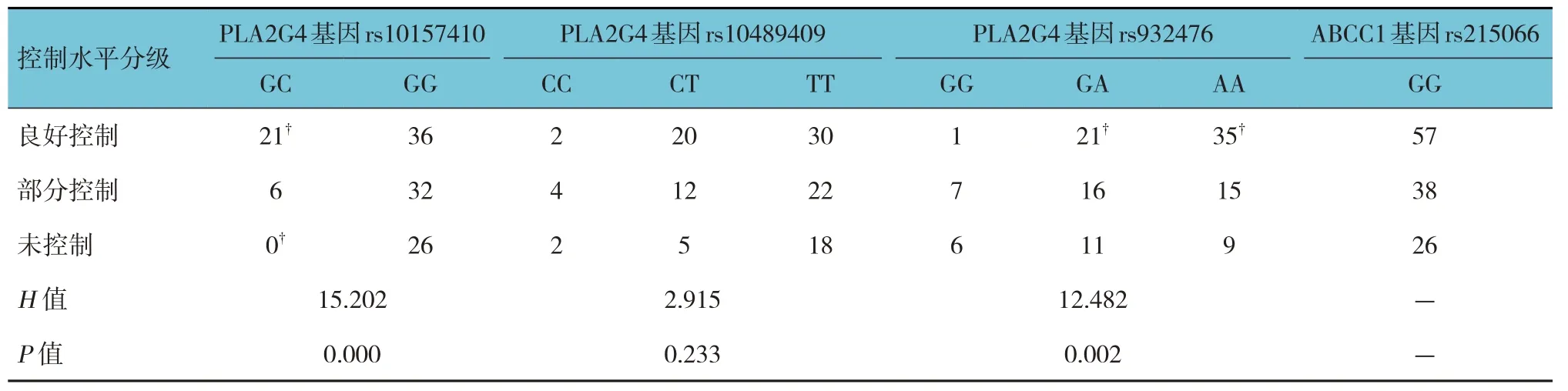
表5 PLA2G4、ABCC1基因各位点不同基因型的症状控制水平分级比较 例
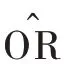
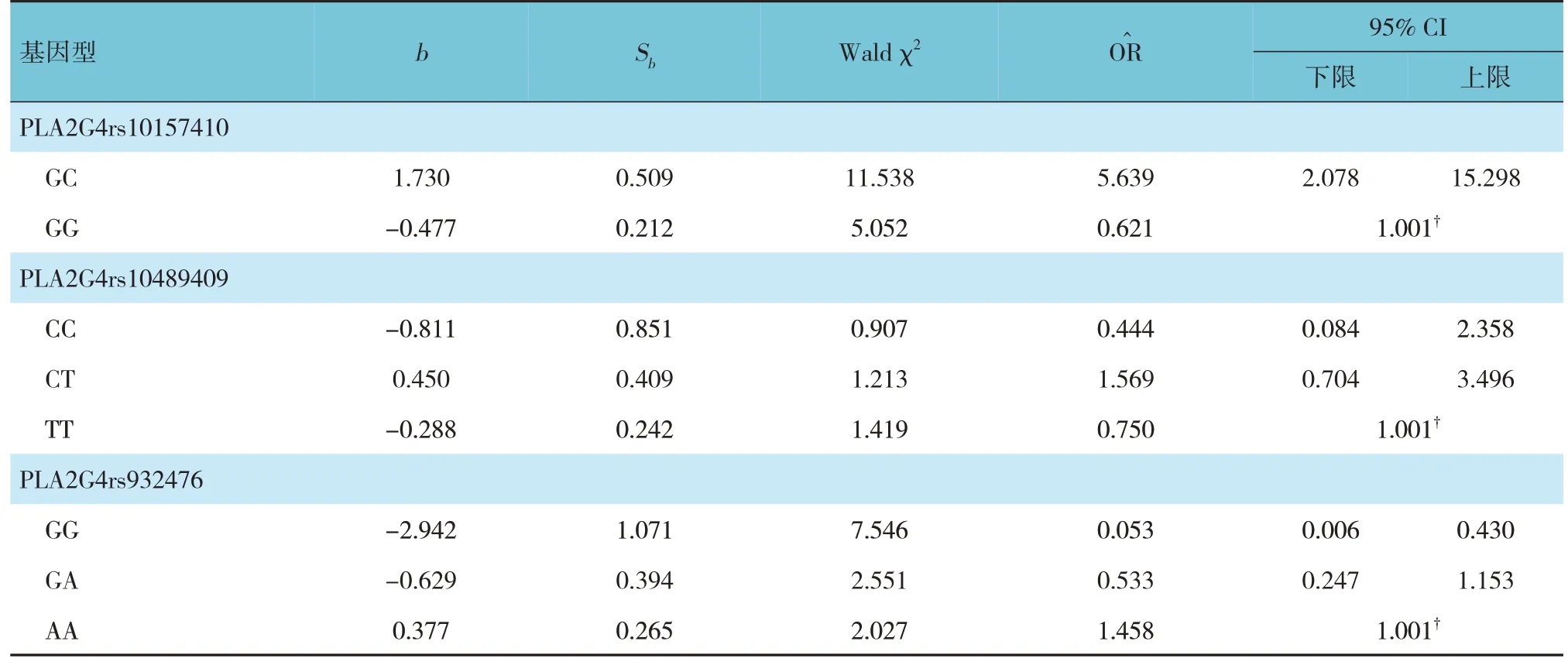
表6 PLA2G4基因各位点不同基因型症状控制水平分级的Logistic回归分析参数
3 讨论
哮喘是儿童最为常见的慢性气道炎症性疾病,治疗目标是有效控制哮喘症状,维持正常的活动水平。迄今为止,尚未发现根治哮喘的治疗方法,频繁的发作和长期的药物治疗严重影响患儿的身心健康,给患儿家庭带来了巨大的经济负担和精神压力[11-12]。目前,在治疗哮喘炎症和缓解气道痉挛方面的药物选择十分有限,部分药物虽能够有效控制症状,但疗效的个体差异性大。基因多态性影响药物靶分子或影响药物代谢从而导致个体对哮喘治疗的差异性,故探寻基因多态性与药物疗效之间的关系具有十分重要的意义。
LTs 是一种能够引起支气管收缩的炎性介质,通过增强炎症细胞反应、支气管收缩力、黏液分泌和气道重塑,从而介导哮喘的发生[13]。PLA2G4基因能够编码磷脂酶A2,水解膜磷脂,释放花生四烯酸,在5-脂加氧酶氧化下生成LTs 等炎性介质,参与气道高反应性[14-15]。因此推测,PLA2G4基因可能与哮喘患儿的肺功能指标和炎症指标密切相关。孟鲁司特作为FDA 批准的LTRA,与白三烯竞争受体,从而阻断白三烯与受体的结合,进而减轻炎症反应和气道高反应性[16]。孟鲁司特具有良好的依从性和有效性,在哮喘的治疗中广泛应用,但受到个体差异的影响,疗效不尽相同。故本研究探讨了哮喘患儿PLA2G4 基因rs10157410、rs10489409 和rs932476 位点突变对肺功能指标、炎症指标及症状控制水平的影响。结果显示与治疗前相比,rs10157410位点GC、GG基因型的FEV1%pred、FEV1/FVC、FEF50%pred、FEF75%pred 肺功能指标及EOS%、IgE、FeNO 炎症指标均有显著改善,提示孟鲁司特能有效缓解GC、GG 基因型哮喘患儿的气道阻塞和气道炎症,但在控制水平分级方面GC基因型良好控制比例明显高于GG 基因型,未控制显著低于GG 基因型,且Logistic 回归分析提示GC基因型是患儿孟鲁司特治疗良好控制的独立影响因素,故认为GC 基因型对孟鲁司特具有更好的反应性。考虑可能与该基因位点编码的磷脂酶A2 介导下产生的白三烯与受体的结合受到了抑制,从而缓解了支气管收缩和气道炎症相关。TREMBLAY等[17]研究了长链n-3 脂肪酸和PLA2G4 基因rs10157410 位点的交互作用,发现补充长链n-3 脂肪酸可导致花生四烯酸减少,从而影响LTs 等炎性介质的产生,与本研究结果一致,国内未发现该位点与哮喘的相关研究。JONG 等[18]通过全基因组关联分析发现PLA2G4 基因rs932476 位点能够激活p38MAPK 通路进而影响肺功能。此外,郭青等[14]研究表明孟鲁司特对该位点AA 型患儿炎症反应的控制及肺功能的改善均优于GG 型,提示该位点多态性可能对孟鲁司特的疗效有一定的影响。本研究结果证实rs932476位点GA、AA基因型的FEV1%pred、FEV1/FVC、FEF50%pred、FEF75%pred 肺功能指标及EOS%、IgE、FeNO 炎症指标相比治疗前改善明显,GA 和AA 基因型良好控制比例显著高于GG 基因型,Logistic 回归分析提示AA 基因型是患儿孟鲁司特治疗良好控制的独立影响因素,综上说明rs932476 位点AA 基因型对孟鲁司特疗效更加显著。
ABCC1 基因编码的MRP1 利用ATP 水解的能量实现底物在细胞内外的跨膜转运,在LTs 转运中具有重要作用,因此推测ABCC1 基因可能与孟鲁司特疗效相关。目前国外关于该基因与孟鲁司特疗效关系的研究较少,国内尚未发现ABCC1 基因与儿童哮喘的相关研究。在一项由577 例美国哮喘患者参加的关于孟鲁司特疗效相关基因的SNPs 与5-脂加氧酶抑制剂关系的研究中检测出ABCC1 基因rs215066 位点有GG、GA 和AA 3 种基因型[19]。本研究受试儿童中只检测出一种GG 基因型,基因型分布与国外分布不同,考虑与样本量较少和人种差异相关。国外研究表明哮喘患者经孟鲁司特治疗后,ABCC1 基因rs215066 位点的FEV1%pred 指标较治疗前显著升高[20]。本研究表明治疗后ABCC1 基因rs215066 位点GG 基因型的FEV1%pred、FEV1/FVC、FEF50%pred、FEF75%pred 肺功能指标和炎症指标均显著改善,提示孟鲁司特对GG 基因型炎症反应的控制及肺功能改善有一定作用。
综上所述,PLA2G4 基因及ABCC1 基因多态性与孟鲁司特疗效有关。其中,PLA2G4 基因rs10157410 位点GC 基因型和rs932476 位点AA 基因型对孟鲁司特疗效具有更好的敏感性,为基因检测指导下的个体化治疗提供参考依据。本研究存在样本量不足及人种、地域单一的问题,未来仍需要大规模、多中心的联合研究。

