妊娠高血压合并急性心肌梗死救治1例并文献复习
金智丽,曾子悦,熊 维,荣 凌,柴玉琼,陈 明,王海蓉,鲁志兵
1. 武汉大学中南医院心内科(武汉 430071)
2. 武汉大学心肌损伤与修复研究所(武汉 430071)
据美国研究报道,过去40 年中妊娠期间急性心肌梗死(acute myocardial infarction,AMI)发生率较低,每10 万例分娩孕产妇中发病4.98 例,孕产妇病死率为5.1%~37%;妊娠期间急性ST段抬高心肌梗死(ST segment elevation myocardial infarction,STEMI)中,16%由冠状动脉自发性夹层所致,21%是非动脉粥样硬化性血栓栓塞所致,29%冠状动脉正常,27%~43%确系冠状动脉粥样硬化所致[1-2]。妊娠高血压时全身小动脉痉挛、血管内皮广泛受损,孕产妇死亡病因的10%~15%与妊娠高血压引发的心血管事件有关[3]。妊娠高血压合并AMI 的救治涉及心血管内科、产科、儿科以及麻醉科等多学科,目前尚无相关专家共识或指南进行指导。本文提供1 例成功救治病案,并检索类似文献进行系统复习,以探讨相关救治策略。本病例报道已获武汉大学中南医院伦理委员会审核批准(批准号:2021075),并征得患者知情同意。
1 病例资料
1.1 基本情况
患者,女,34 岁,孕35 周+4 天待产,因“胸痛18 小时”由外地转诊入院。胸痛为心前区持续性闷痛,当地未做特殊检查与治疗。既往史:35周+4 天孕产妇,产检胎儿正常;有高血压病史2年,最高血压160/100 mmHg,平素口服硝苯地平片降压治疗,自诉血压控制正常;2 年前曾流产一次;中度贫血病史多年,未积极诊治。入院体检:T 36.5℃,P 115 bpm,R 26 bpm,血压(左上臂)157/110 mmHg,(右上臂)162/114 mmHg。端坐位,呼吸急促,全身大汗;双肺底可闻及细湿啰音;腹部膨隆,无压痛及反跳痛;余查体未见明显阳性体征。辅助检查:急诊心电图示“窦性心动过速,II、III、aVF 导联ST 段抬高0.1~0.15 mV”,见图1。
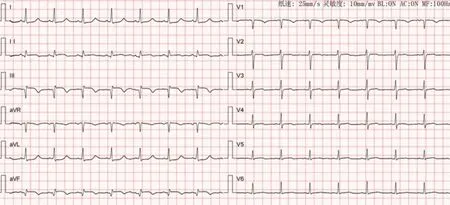
图1 急性ST段抬高型心肌梗死(下壁)Figure 1. Acute ST-segment elevation myocardial infarction (inferior wall)
入院完善检查,床旁超声心动图提示:左室下壁及部分后间隔运动异常(考虑心肌梗死),左室壁肥厚,右心扩大;心包腔少量积液,心包脏壁层分离;液性暗区宽度:左室后壁后方7 mm,心尖部5 mm,右室前壁前5 mm;左冠状动脉瘤样扩张 :内径约1.0 cm,内似可见低回声团;左冠状动脉扩张不排除血栓形成。床旁产科彩超:单活胎,头位。高敏肌钙蛋白>50 000 U/L;脑钠肽248.9 pg/mL↑;血常规分析:血红蛋白77.0 g/L↓(中度贫血),红细胞压积、平均红细胞体积、平均血红蛋白浓度、平均血红蛋白含量均下降;肝功能:天冬氨酸氨基转移酶320 U/L↑,总蛋白53.6 g/L↓,白蛋白23.5 g/L↓,球蛋白30.1 g/L↑;凝血功能:凝血酶原时间活动度153%↑,纤维蛋白原-C 544 mg/dL↑;铁、铁结合力:血清铁6.8 umol/L↓,不饱和铁结合力64.2 umol/L↑;可溶性转铁蛋白28.62 nmol/L↑;抗核抗体(+),抗核糖体P 蛋白抗体/抗Sm 抗体阳性,抗组蛋白抗体阳性,免疫球蛋白E 430 kU/L↑;抗心磷脂抗体、狼疮抗凝物、抗O 类风湿全套均阴性。
综合上述症状、体检以及实验室等检查结果,患者首诊诊断明确:STEMI(下壁),心功能Killip Ⅲ级;妊娠高血压;孕35 周+4 天待产;中度贫血(缺铁性贫血);低蛋白血症。
急性心肌梗死罪犯血管部位判断:因患者不能长时间平卧,未能完成冠状动脉CT 血管成像(computer tomography angiography,CTA)检查。根据主动脉CTA 影像可判断冠状动脉情况:左冠状动脉近端膨大,直径9.8 mm,左前降支近中段血管扩张伴局部钙化斑块,未能分析到右冠状动脉及回旋支血管情况。与床旁超声心动图报告一致:左冠状动脉瘤样扩张,内径约1.0 cm,内似可见低回声团;左冠状动脉扩张不排除血栓形成。结合患者心肌损伤标志物显著增高,心电图II、III、aVF 导联明显抬高,且III 导联抬高幅度大于II 导联,判断罪犯血管来自于右冠状动脉(图1,图2)。
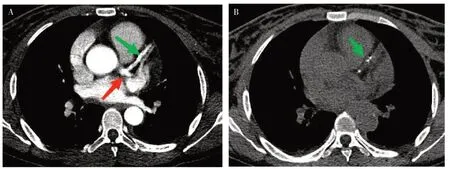
图2 主动脉CTA的冠脉影像分析Figure 2. Coronary imaging analysis of aortic CTA
1.2 诊疗经过
入院后主要排查患者急性冠状动脉事件是否因主动脉夹层导致,因为主动脉夹层所致AMI 的处理有可能需心血管外科紧急手术干预。该病例的首要任务为排除主动脉夹层后内膜飘浮下垂物遮盖右冠状动脉窦口导致AMI。Stanford A 型夹层累及患者升主动脉,主动脉根部夹层血肿向右后侧扩展,也容易累及右冠状动脉口部,或因为血肿压迫其近端导致血栓形成甚至闭塞,梗死多为下壁或后壁部位,且常合并主动脉瓣膜关闭不全临床表现[4]。患者虽患妊娠高血压,但双侧肢体收缩压相差不大,无双上肢血压不对称情况;且血压通过硝苯地平降压后容易达标。心脏听诊无主动脉瓣区舒张期吹风样杂音。主动脉CTA 显像可见主动脉窦部增宽,左室下壁及部分后间隔运动异常(图2),因此排除了主动脉夹层诊断。
患者面临的主要治疗问题包括:抗栓药物、急诊冠脉造影甚或急诊经皮冠脉介入术(percutaneous coronary intervention,PCI)、剖宫产时机的选择等。
根据患者冠脉血管炎症表现,以及实验室检查结果,风湿免疫科会诊后认为,患者可以补充诊断系统性红斑狼疮(systemic lupus erythematosus,SLE)。治疗方案主要考虑急性冠脉事件会危急患者及胎儿生命,倾向于选择积极抗栓药物方案治疗AMI 血栓。依据如下:患者胸痛发病时间超过12 h,已超过急诊PCI 时间窗,不考虑急诊PCI,且病情不适合溶栓治疗;急诊PCI术中肝素化对高龄产妇所致出血风险增大[5],若植入支架则需要双重抗血小板治疗,如阿司匹林联合氯吡格雷,其中氯吡格雷可通过胎盘影响胎儿安全和后续分娩治疗。分析病情后认为,患者即便为下壁AMI 但尚未影响血流动力学,罪犯血管影响程度与范围有限。已排除自发性夹层、动脉粥样硬化斑块破裂等病因,针对患者SLE 采用羟氯喹进行病因干预,为促进胎儿肺发育成熟启用小剂量激素,因在AMI 急性期暂不予以大剂量激素治疗。
妊娠高血压降压方案:针对妊娠高血压选择尼卡地平针剂控制血压、艾司洛尔针剂控制心率。抗栓方案:抗栓无明确禁忌证,选用低分子肝素抗凝联合阿司匹林抗血小板治疗[6]。
基于上述方案患者第一阶段以药物治疗为主,辅助其度过AMI 缺血坏死水肿阶段,防治可能出现的并发症如恶性心律失常、急性心力衰竭,甚至心脏破裂、乳头肌功能不全、乳头肌断裂风险等。于心血管重症监护病房严密监控血压、心率、心功能及胎儿健康状况。多学科团队联动,包括产科、儿科、麻醉科、手术室等相关科室,若患者病情演变加重,出现急性心衰或血流动力学不稳定,随时可终止妊娠,建立必要时一键启动急诊分娩手术方案。
经过上述对妊娠高血压合并AMI 患者的综合管理,患者于AMI 病程第7 天时,可平卧位,无胸痛无气促,无腹痛;生命体征平稳,实验室指标含脑钠肽、D-二聚体、血常规WBC 计数等指标正常,心肌损伤标志物恢复至正常;心电图ST段恢复正常,术前评估达到剖宫产指征。于病程第7 天腰硬联合麻醉剖宫产下一健康女婴。术后续用低分子肝素针3 d,术后第3 天恢复阿司匹林片100 mg,qd。术后第7 天以“妊娠合并心脏病、STEMI(下壁)、重度先兆子痫、低蛋白血症、经剖宫产术分娩、孕2 产1 孕36 周+4 天剖宫产一活女婴,头位,单胎活产,SLE,中度贫血”出院。随访情况汇报:术后1 月冠脉CTA 显示,左右冠脉血管正常,未见瘤样扩张(图3)。分析急性期冠脉瘤样变化可能与血栓形成或局部血流动力学改变有一定关联。现患者于风湿免疫科长期随访诊治SLE,病情稳定。
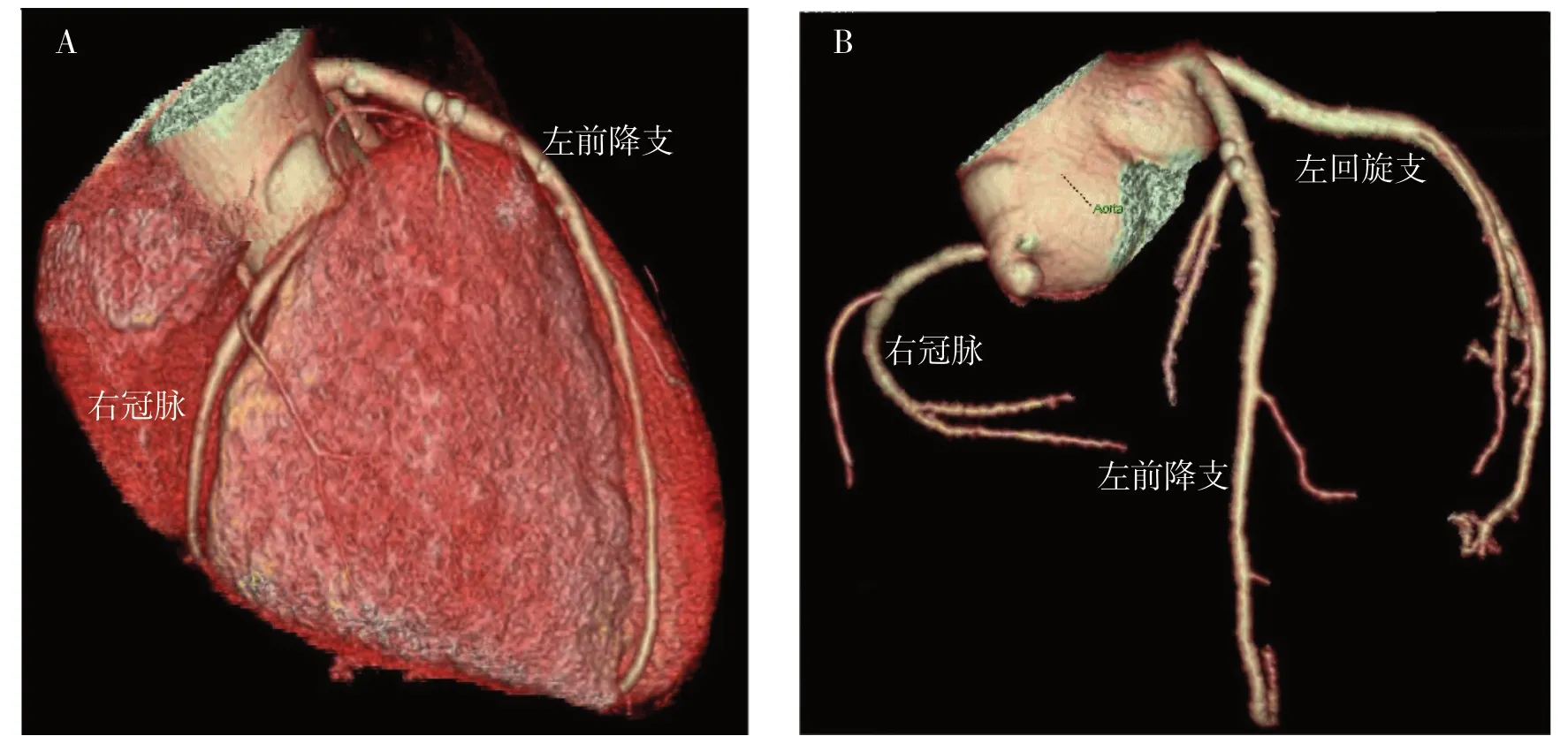
图3 出院1月后随访冠脉CTA结果Figure 3. Results of coronary CTA following up one month after discharge
2 讨论
妊娠期发生AMI 中由冠状动脉粥样硬化所致者占比27%~43%,冠状动脉正常者占29%。本例患者妊娠剖宫产术后1 月复查冠脉CTA,证实冠状动脉正常,提示急性阶段冠脉血栓并非动脉粥样硬化病变所致。病因可见于原位血栓、左侧瓣膜病变、卵圆孔未闭、房间隔缺损情况下冠状动脉的反常栓塞[7]。本例患者血栓事件与SLE 所致血管炎以及妊娠高血压密切相关。首先,SLE基本病理改变为免疫介导的坏死性血管炎:抗原抗体复合物沉积在血管壁,激活补体引起血管壁炎症,血管内皮损伤,血小板黏附,激活凝血系统形成血栓[8]。其次,妊娠高血压增加的血容量会对血管造成额外的压力,增加冠状动脉自发性夹层和斑块破裂血栓形成的风险[9]。因此,妊娠期间应积极控制血压,禁用如血管紧张素转化酶抑制剂、血管紧张素受体阻滞剂和他汀类药物。
妊娠合并AMI的风险比未孕女性高出3~4倍,AMI的治疗方式和药物使用需要考虑母婴安全性。目前在本领域尚无相关专家共识或指南进行指导。对于伴有动脉粥样硬化的STEMI 患者,如果在急诊PCI 时间窗内,有专家建议应及时进行急诊PCI[10]。在整个孕期内,PCI 术后可安全使用低剂量阿司匹林,但是氯吡格雷需谨慎使用。禁用其他抗血小板药如替格瑞洛[9]。对于情况稳定的低危STEMI 患者,可选择药物保守治疗。
对于剖宫产时机,现行指南中对于妊娠39~40 周的心血管病女性患者,若无自然分娩迹象,推荐择期剖宫产,一般在AMI 后尽可能延迟2~3 周分娩[11],以避免血流动力学快速变化和分娩相关的心脏压力增大。本病例在病程第7 天血流动力学已稳定,AMI 后分娩计划由多学科团队以患者为中心进行决策,产科、心血管内科、介入专家以及麻醉师等充分评估后在第7 天顺利剖宫产。
冠状动脉瘤样扩张(coronary artery ectasia,CAE)病理性改变及局部血流动力学异常使其易发生血栓,导致心肌梗死,可能由于内膜细胞受损导致冠状动脉血管痉挛。本例患者住院期间CTA 影像观察到的左前降支处瘤样扩张,推测为血管炎引发血栓事件或合并血管痉挛的表现[11]。出院后随访,冠脉CTA 显示血管光滑平整,未见瘤样扩张。患者经积极充分抗栓治疗后虽然ST段恢复正常水平,但是心电图遗留病理性Q 波,与急性期监测到左冠脉瘤样扩张、右冠脉血栓事件导致血管闭塞有关,支持SLE 诊断,且患者按照SLE 治疗随访2 年病情稳定。
在妊娠合并STEMI 用药的安全性上,普通肝素虽然不透过胎盘,不会导致婴儿出血和婴儿畸形,但抗凝药容易导致子宫胎盘交界处出血。低分子肝素与普通肝素相似,是妊娠合并STEMI 首选抗栓药物,其使用方便且效果可预测[12]。若分娩过程中需逆转肝素化可食用硫酸鱼精蛋白。在对肝素有严重过敏反应或肝素诱导的血小板减少症情况下,磺达肝癸钠可作为替代药物使用。
研究报道小剂量阿司匹林(80~150 mg/d)可用于妊娠期心血管疾病的治疗。目前低剂量阿司匹林用于治疗STEMI 的获益大于风险。双重抗血小板治疗、抗凝治疗可能会增加母婴并发症的风险[13]。氯吡格雷相关临床试验中均排除了妊娠患者,但是也有个案报道妊娠期使用了氯吡格雷后,产妇发生血小板减少症、胎儿宫内死亡、出血事件等不良反应,但报道并未指出上述不良反应确系氯吡格雷所致副反应。
综上所述,本病例虽为妊娠高血压且合并STEMI,入院时病情危重,但在严密监护下经过控制血压及积极抗栓治疗(低分子肝素联合阿司匹林)后,其血流动力学状况趋于稳定,故未进行侵入性干预,避免了因急诊PCI 可能出现的出血等并发症风险,且最终获得满意临床效果。本病例缺乏广泛性,但在心血管疾病作为孕产妇死亡的主要原因背景下,对于高危孕产妇,多学科团队对于孕期和产后预防母婴发病及死亡至关重要[14-15],应早期参与对妊娠相关母婴风险的全面评估。有AMI 病史的孕妇分娩时不应单独考虑心脏适应证,而应以产科适应证为主指导治疗[16]。Lameijer 等对妊娠和产褥期AMI 病例进行的回顾分析显示,总体剖宫产率为56%,如妊娠期间发生AMI,则剖宫产率为62%[17]。妊娠高血压合并AMI 诊治需要多学科紧密协作[18-20],解决环环相扣的临床问题,以保护孕产妇和胎儿安全。

