双脱甲氧基姜黄素结晶热力学及结晶过程研究
贺海波 彭静维 范丽鹏 齐立军 高伟 武耐英

摘要:采用动态法测定了278.15~323.15 K范围内双脱甲氧基姜黄素晶体在不同浓度乙醇中的溶解度,并用修正的Apelblat方程对溶解度数据进行拟合。使用Van't Hoff方程计算双脱甲氧基姜黄素晶体在不同浓度乙醇中溶解吉布斯自由能ΔG、溶解焓ΔH和溶解熵ΔS,并在90%乙醇中进行了降温结晶实验。结果表明,双脱甲氧基姜黃素在不同浓度乙醇中的溶解度随温度的升高而明显增加,修正的Apelblat方程拟合效果良好。使用90%乙醇作为溶剂的降温结晶得到的产品纯度在92%左右,收率大于70%。
关键词:双脱甲氧基姜黄素;溶解度;热力学;降温结晶
中图分类号:TS201.7 文献标志码:A 文章编号:1000-9973(2023)12-0176-04
Investigation on Crystallization Thermodynamics and
Crystallization Process of Bisdemethoxycurcumin
HE Hai-bo1, PENG Jing-wei2, FAN Li-peng2, QI Li-jun2,3,
GAO Wei2,3, WU Nai-ying1*
(1.School of Materials Science and Engineering, Hebei University of Engineering, Handan 056038,
China; 2.Chenguang Biotech Group Co., Ltd., Handan 057250, China; 3.Key Laboratory of
Plant Resources Comprehensive Utilization in Hebei Province, Handan 057250, China)
Abstract: The solubility of bisdemethoxycurcumin crystals in different concentrations of ethanol at 278.15~323.15 K is determined by dynamic method, and the modified Apelblat equation is used to fit the solubility data. The solution Gibbs free energy ΔG, solution enthalpy ΔH and solution entropy ΔS of bisdemethoxycurcumin crystals in different concentrations of ethanol are calculated using Van't Hoff equation, and the cooling crystallization experiment is carried out in 90% ethanol. The results show that the solubility of bisdemethoxycurcumin in different concentrations of ethanol increases significantly with the increase of temperature. The modified Apelblat equation fits well. The purity of the product obtained by cooling crystallization with 90% ethanol as the solvent is about 92%, and the yield is more than 70%.
Key words: bisdemethoxycurcumin; solubility; thermodynamics; cooling crystallization
姜黄素类化合物是从姜黄根茎中提取到的一种天然色素,目前姜黄素类化合物是世界上销量最高的天然食用色素之一。姜黄素类化合物可以作为食品添加剂,除此之外,研究发现姜黄素类化合物在抗菌、抗肿瘤、抗炎、抗氧化、降血脂、护肝等方面均具有独特的生理活性[1-6]。鉴于其明确的功效和政策许可,以姜黄素为主要原料或配料的保健产品、食品、化妆品等市场均有较大发展空间[7]。
姜黄素类化合物主要有效成分为姜黄素、脱甲氧基姜黄素、双脱甲氧基姜黄素,分子结构见图1。
到目前为止,很多研究都集中在姜黄素的研究上。尽管姜黄素能促进人体健康,但其稳定性差,在水中的溶解度低,生物利用度差,在光照和氧化条件下易降解[8]。因此,其他类姜黄素物质成为学术界和工业界的研究热点。有研究者指出,其他类姜黄素具有比姜黄素更高的生物活性,比如,它们对姜黄素的抗炎特性有协同作用。双脱甲氧基姜黄素是姜黄素的双去甲氧基衍生物,具有比姜黄素更好的稳定性、抗氧化和抗肿瘤活性[9-10]。但由于难以获得质量较大、纯度较高的双脱甲氧基姜黄素,因此其理化性质的研究较少。
前人对姜黄素类化合物的纯化分离研究主要是利用色谱手段分离姜黄素类化合物,例如,柱色谱法[11-12]、半制备型高效液相色谱法[13]、高速逆流色谱法[14]、制备型超临界流体色谱法[15]和结晶法[16]。其中,色谱类方法流动相消耗溶剂量大,固定相可重复利用率低,处理量有限。结晶法是化工行业生产中最重要的分离纯化技术之一,具有操作能耗低、设备要求简单等优点。因此,本文选择结晶法用于分离纯化。
本文测定了双脱甲氧基姜黄素在不同浓度乙醇中的溶解度,并对实验数据进行拟合关联。此外,确定了结晶过程中的热力学性质,并进行结晶过程研究。以低含量姜黄素作为原料,通过结晶操作提升晶体的纯度,得到了较高纯度的双脱甲氧基姜黄素晶体。本研究将为双脱甲氧基姜黄素工业结晶生产提供指导意义。
1 材料和方法
1.1 实验材料和仪器
低含量姜黄素(纯度67.04%):晨光生物科技集团股份有限公司;无水乙醇(分析纯):天津市博华通化工产品销售中心;双脱甲氧基姜黄素(纯度>98%):上海阿拉丁生化科技股份有限公司;纯水:实验室自制。
电子分析天平(精度为 0.000 01 g) 岛津菲律宾工厂;50 mL结晶器、250 mL结晶器 郑州市金水区欣瑞玻璃器皿经营部;酒精计 武强县亿达仪表厂;LCD数显加热型圆盘磁力搅拌器 大龙兴创实验仪器(北京)有限公司;AM110W-O电动恒速搅拌机 上海昂尼仪器仪表有限公司;陶瓷布氏漏斗 上海垒固仪器有限公司;循环水式多用真空泵 郑州长城科工贸有限公司;CF41型制冷循环器 上海科兴仪器有限公司;Waters e2695 HPLC高效液相色谱仪 沃特世科技(上海)有限公司;偏光显微镜 上海普丹光学仪器有限公司。
1.2 溶解度测定方法
利用动态法[17]测定双脱甲氧基姜黄素在不同濃度乙醇中的溶解度,温度范围控制在278.15~323.15 K,加入一定量的溶剂至50 mL结晶器中,设置搅拌速率为200 r/min,温度以6 K/h升高,缓慢加入少量溶质,待溶质搅拌溶解后,记录此时加入溶质的量,即得到此温度下双脱甲氧基姜黄素产品的溶解度,用mg/mL表示。
1.3 溶解度模型拟合
本文使用修正的Apelblat方程对双脱甲氧基姜黄素溶解度数据进行拟合,Apelblat方程常用来拟合溶解度随温度升高的变化,其方程所需参数少,简单方便。修正的Apelblat方程表达式为:
lnx=A+BT+ClnT。
式中:x为双脱甲氧基姜黄素晶体的溶解度(摩尔分数);A、B、C为模型参数;T为热力学温度,K。
1.4 热力学性质计算
溶解热力学性质分析使用Van't Hoff方程进行计算,得到溶解热力学数据:溶解吉布斯自由能ΔG、溶解焓ΔH和溶解熵ΔS,Van't Hoff方程如下所示:
lnx=-ΔHRT+ΔSR。
式中:x为双脱甲氧基姜黄素晶体的溶解度(摩尔分数);R为气体常数,8.314 J/(mol·K);T为热力学温度,K。
由此计算得到ΔH、ΔS,再由如下公式求得ΔG。
ΔG=ΔH-TΔS。
1.5 溶解度数据拟合
溶解度拟合结果使用相对误差(RD)和平均相对误差(ARD)评价,其相对误差和平均相对误差公式如下所示:
RD=|xexp-xcal|xexp。
ARD=1N∑ii=1|xexp,i-xcal,i|xexp,i。
式中:xexp为实验溶解度(摩尔分数);xcal为计算溶解度(摩尔分数);N为实验点的总数;i为每个实验点。
1.6 结晶条件实验
使用低含量姜黄素,确定选用90%乙醇进行结晶条件实验,以料液比、温度、时间为条件,进行结晶提纯实验,以提升纯度和收率为导向,确定合适的结晶操作条件。具体操作步骤:将原料加入90%乙醇中75 ℃高温溶解,搅拌1 h保证溶解完全,之后以一定降温速率进行降温结晶,过滤烘干得到产品,称取产品的质量,后续进行产品含量的测定。
1.7 产品含量检测
本文使用高效液相色谱法检测产品的纯度。产品含量的测定依据文献[18-19]修改后的HPLC法(Waters e2695 HPLC)进行测定。色谱条件:系统配备C18柱(250 mm×4.6 mm,5 μm);色谱柱温度为40 ℃;流动相为乙腈∶0.5%冰醋酸(45∶55);检测波长为430 nm;进样量为5 μL;保留时间为18 min。
2 数据结果与讨论
2.1 溶解度测定结果
双脱甲氧基姜黄素在不同温度、不同浓度乙醇中的溶解度见图2。
由图2可知,随着温度的升高,双脱甲氧基姜黄素在90%乙醇、80%乙醇、70%乙醇中的溶解度均不断增加。观察溶解度趋势可直观发现其在高温时溶解度很大,低温时溶解度很小,在90%乙醇中的结果最明显,且不存在拐点。
2.2 溶解度数据拟合
对实验溶解度数据使用修正的Apelblat方程拟合关联,得到模型参数、模型计算值、相对误差(RD)、平均相对误差(ARD),见表1。
由表2可知,对双脱甲氧基姜黄素在不同浓度乙醇中的溶解度进行拟合,修正的Apelblat方程拟合效果良好,拟合后的R2分别为0.999 08,0.972 08,0.989 75,表明修正的Apelblat方程能较好地关联双脱甲氧基姜黄素在不同浓度乙醇中的溶解度。
修正的Apelblat方程关联曲线见图3。
2.3 结晶热力学性质
对结晶热力学性质进行研究,可由Van't Hoff方程求得双脱甲氧基姜黄素的热力学参数:溶解吉布斯自由能ΔG、溶解焓ΔH和溶解熵ΔS,见表3。
由表3可知,ΔH>0,全为正值,表明双脱甲氧基姜黄素的溶解过程是一个吸热过程;ΔS>0,全为正值,表明双脱甲氧基姜黄素的溶解过程是一个熵增过程;ΔG>0,全为正值,表明双脱甲氧基姜黄素的溶解过程是非自发过程。
2.4 结晶过程研究
双脱甲氧基姜黄素在90%乙醇中的溶解度随温度升高的变化较大,在278.15~323.15 K范围内双脱甲氧基姜黄素在90%乙醇中的溶解度从0.96 mg/mL增加到65.15 mg/mL,变化较大,因此对原料进行降温结晶获得相应晶体更合适。通过改变结晶温度、结晶时间、料液比以提升结晶产品的纯度和收率。
2.4.1 温度对晶体纯度和收率的影响
控制料液比为1∶5、结晶时间为24 h,考察结晶温度分别为15,10,5,0 ℃时对双脱甲氧基姜黄素纯度和收率的影响,见表4。
由表4可知,当结晶温度逐渐降低时,产品的纯度呈下降趋势,产品的收率逐渐增加,在保证纯度高于90%和收率大于70%的同时,考虑成本效益问题,结晶温度控制在5 ℃更能节约成本。
2.4.2 时间对晶体纯度和收率的影响
控制料液比为1∶5、结晶温度为5 ℃,考察结晶时间分别为9,24,29,40 h时对双脱甲氧基姜黄素纯度和收率的影响,见表5。
由表5可知,随着结晶时间的增加,收率逐渐增大,在趋于29~40 h时收率增长趋势趋于平缓,因此结晶时间控制在29 h。
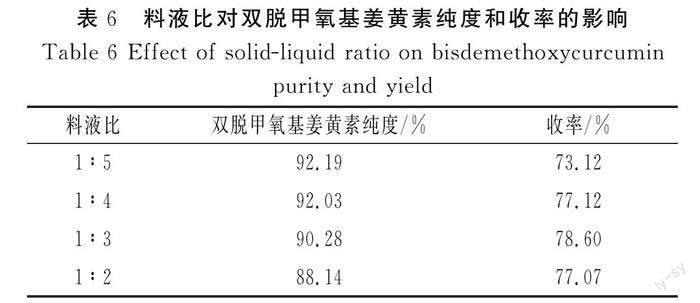
2.4.3 料液比对晶体纯度和收率的影响
控制结晶温度为5 ℃、结晶时间为29 h,考察料液比分别为1∶5、1∶4、1∶3、1∶2时对双脱甲氧基姜黄素纯度和收率的影响,见表6。
由表6可知,料液比由1∶5减小到1∶4时,纯度变化无明显差异,降低料液比使收率提高。料液比降低至1∶3、1∶2时,结晶得到的产品纯度降低,其原因为结晶溶剂用量过少,除杂能力下降,从而使得晶体纯度下降,因此确定料液比为1∶4。
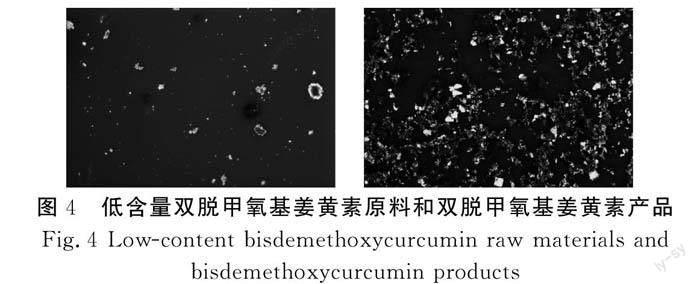
通过偏光显微镜观察原料和产品,由图4可以看出原料中姜黃素主要以非晶体形式存在,产品中双脱甲氧基姜黄素主要以晶体形式存在,通过降温结晶操作提升了产品的纯度,也极大改变了双脱甲氧基姜黄素晶体。
采用单步降温结晶方式纯化后,双脱甲氧基姜黄素纯度由67.04%提升至90%以上,收率大于70%,此法操作简单,研究结果可为姜黄素的工业生产提供重要的指导意义。
3 结论
采用动态法测定了双脱甲氧基姜黄素在90%、80%、70%乙醇中的溶解度,结果表明,双脱甲氧基姜黄素溶解度随温度和乙醇浓度的升高而增加,双脱甲氧基姜黄素的溶解过程为吸热非自发过程。
采用Apelblat模型对实验数据进行拟合,得到溶解度实验数据和计算值相对误差较小,拟合效果良好。
确定了以低含量姜黄素为原料获取高纯度姜黄素的降温结晶方式,确定了工艺参数,对双脱甲氧基姜黄素结晶工艺开发及工业生产提供了可行的指导。
参考文献:
[1]羊青,王茂媛,晏小霞,等.正交实验法优化姜黄油及姜黄素提取工艺[J].中国调味品,2018,43(10):81-84.
[2]HUANG L L, ZHANG J, SONG T Z, et al. Antifungal curcumin promotes chitin accumulation associated with decreased virulence of Sporothrix schenckii[J].International Immunopharmacology,2016,34:263-270.
[3]MING T Q, TAO Q, TANG S, et al. Curcumin: an epigenetic regulator and its application in cancer[J].Biomedicine & Pharmacotherapy,2022,156:113956.
[4]MEGHANA K, SANJEEV G, RAMESH B. Curcumin prevents streptozotocin-induced islet damage by scavenging free radicals: a prophylactic and protective role[J].European Journal of Pharmacology,2007,577(1):183-191.
[5]MUSAZADEH V, ROSHANRAVAN N, MOHAMMADIZADEH M, et al. Curcumin as a novel approach in improving lipid profile: an umbrella meta-analysis[J].Nutrition, Metabolism and Cardiovascular Diseases,2022,32(11):2493-2504.
[6]MOGHADAMTOUSI S Z, KADIR H A, HASSANDARVISH P, et al. A review on antibacterial, antiviral, and antifungal activity of curcumin[J].BioMed Research International,2014,2014:186864.
[7]代德财,闫浩,徐雪峰.姜黄素的提取工艺及其生物活性的研究[J].中国调味品,2020,45(8):159-161,171.
[8]HEFFERNAN C, UKRAINCZYK M, GAMIDI R K, et al. Extraction and purification of curcuminoids from crude curcumin by a combination of crystallization and chromatography[J].Organic Process Research & Development,2017,21(6):821-826.
[9]LIU Y L, LIU M, YAN H, et al. Enhanced solubility of bisdemethoxycurcumin by interaction with Tween surfactants: spectroscopic and coarse-grained molecular dynamics simulation studies[J].Journal of Molecular Liquids,2021,323:115073.
[10]RAMEZANI M, HATAMIPOUR M, SAHEBKAR A. Promising anti-tumor properties of bisdemethoxycurcumin: a naturally occurring curcumin analogue[J].Journal of Cellular Physiology,2018,233(2):880-887.
[11]REVATHY S, ELUMALAI S, BENNY M, et al. Isolation, purification and identification of curcuminoids from turmeric (Curcuma longa L.) by column chromatography[J].Journal of Experimental Sciences,2011,2(7):21-25.
[12]王明鉴,张凌,乔雪童,等.大孔树脂法纯化姜黄素的工艺优化[J].中国调味品,2015,40(5):39-45.
[13]MOLLAYI S, TAMHIDI S, HASHEMPOUR H, et al. Recycling preparative high performance liquid chromatography for the separation of curcumin from curcuminoids in Curcuma longa L.[J].Acta Chromatographica,2015,27(2):387-398.
[14]PAN Y, JU R H, CAO X L, et al. Optimization extraction and purification of biological activity curcumin from Curcuma longa L. by high-performance counter-current chromatography[J].Journal of Separation Science,2020,43(8):1586-1592.
[15]SONG W, QIAO X, LIANG W F, et al. Efficient separation of curcumin, demethoxycurcumin, and bisdemethoxycurcumin from turmeric using supercritical fluid chromatography:from analytical to preparative scale[J].Journal of Separation Science,2015,38(19):3450-3453.
[16]HOROSANSKAIA E, YUAN L, LORENZ H, et al. Purification of curcumin from ternary extract-similar mixtures of curcuminoids in a single crystallization step[J].Crystals,2020,10(3):206.
[17]赵鑫华,陈丽珍,王建龙,等.FOX-7在DMSO-EAC混合体系中的结晶热力学[J].含能材料,2020,28(9):826-833.
[18]赵欣,袁丹,王启隆,等.姜黄提取物中姜黄素类成分定量分析法研究[J].药物分析杂志,2005,25(6):643-647.
[19]劉东锋.植物提取物有效成分检测手册[M].南京:南京大学出版社,2010:273-277.
收稿日期:2023-06-19
基金项目:邯郸市科学技术研究与发展计划项目(21422012320,22313014014)
作者简介:贺海波(1998-),男,硕士,研究方向:天然提取物提取工艺。
*通信作者:武耐英(1980-),女,教授,博士,研究方向:污染物分析检测及天然提取物提取工艺。

