清营颗粒对大鼠的亚慢性毒性评价*
张瑜,刘月月,杨鹏,李克鑫,殷斌,赵增成,林树乾
(1.山东省农业科学院家禽研究所,山东 济南 250100;2.动物保健品山东省工程研究中心,山东 济南 250100;3.山东森康三峰生物有限公司,山东 济南 250023;4.山东鑫谷健康产业有限公司,山东 滨州 256600)
清营汤出自清代著名温病学家吴鞠通的《温病条辨》[1],该方在人医临床中应用广泛[2-9],在宠物临床中也有报道[10],主要功效为清营透热,养阴活血。方中犀角(现用水牛角代之)可入营分,清解营分热毒,为君药;热灼营阴,生地黄、麦冬、玄参共用既可清热养阴生津,又可助君药清营凉血解毒,共为臣药;银花、竹叶、连翘清热解毒、轻清透泄,清解转出之气热,因势利导,使营分热邪有外达之机,是“透热转气”的重要体现;黄连清心泻热解毒,丹参凉血散瘀,防止血与热结,同为佐药。诸药合用,清营养阴,使营分之邪热转出气分而解,为治疗营分证之主方[11]。据现代药效学及临床应用研究[12]表明,清营汤具有明显的解热、抗炎、免疫调节、抗氧化等作用,在一定程度上可改善血液流变、心肌损害。在兽医临床方面,研究发现清营口服液对鸡的大肠杆菌病[13]和流感病毒病[14]均具有较好的疗效。为了更好地开发清营汤,本试验将其改为颗粒剂,选用SD大鼠为研究对象,评估较长期摄入清营颗粒对大鼠的亚慢性毒性作用,为新药研发提供实验依据。
1 材料与方法
1.1 受试物
受试物清营颗粒,批号20220301,棕褐色颗粒,由山东德州神牛药业有限公司提供,每1 g 产品含原生药品1 g。
1.2 试验动物
SPF 级5~6 周龄SD 大鼠80 只(雌雄各半),雄性大鼠体重为110.2~129.2 g,雌性大鼠体重为96.6~128.3 g,均由三峡大学实验动物中心提供 [生产许可证号为SCXK(鄂)2022-0012]。
1.3 主要试剂
兽用血细胞分析用稀释液、LH 溶血剂、Diff溶血剂及肌酐(Crea)、葡萄糖(Glu)、丙氨酸氨基转移酶(ALT)、天门冬氨酸氨基转移酶(AST)、白蛋白(ALB)、甘油三酯(TG)、总胆固醇(TCHO)、尿素(Urea)、总蛋白(TP)检测试剂盒均购自深圳迈瑞生物医疗电子股份有限公司。
1.4 主要仪器
双扉脉动真空蒸汽灭菌器(YMQ 型)购自连云港佑源医药设备制造有限公司。电子天平(SQP型)购自赛多利斯科学仪器(北京)有限公司。全自动生化分析仪(BS-240 型)购自深圳迈瑞生物医疗电子股份有限公司。组织脱水机(TP1020型)、组织包埋机(EG1105A 型)、石蜡切片机(RM2235 型)及染封一体机(ST5010/5020 型)均购自德国徕卡公司。正置显微镜(DS-Fi 型)购自尼康仪器(上海)有限公司。
1.5 试验设计
将80 只5~6 周龄SPF 级SD 大鼠随机分为4组,每组20 只(雌雄各半)。4 组为空白对照组、低剂量组、中剂量组、高剂量组,分别灌服0、5、10、20 g/kg 体重的清营颗粒(按原生药材计),连续灌服30 d。试验期间每天观察大鼠的临床表现,每6 天称量一次体重,并计算采食量和饮水量。试验结束后,每组选取10 只大鼠(雌雄各半)收集血液和组织样本用于后续分析。
1.6 饲养管理
饲养环境要求达到SPF 级别,饮水、饲料符合国家标准(GB 14925、GB 5749、GB 14924.1、GB 14924.2、GB 14924.3)。大鼠饲养于聚丙烯塑料盒中,规格为423 mm×269 mm×192 mm,每笼饲养同组同性别3 只大鼠,温度控制在20.0~26.0 ℃,相对湿度控制在40.0%~70.0% ,每日光照12 h,换气频率15 次/h,每周更换2 次垫料和笼具,试验期间大鼠自由采食、饮水及活动。
1.7 检测指标
1.7.1 临床观察 观察频率:染毒前1 次,染毒后每天1 次,直至试验结束;观察例数:染毒前全部大鼠,染毒后所有存活大鼠;观察方法:每天观察记录大鼠的皮毛、眼睛和黏膜、分泌物、排泄物、呼吸、循环、自主和中枢神经系统、自主活动(如流泪、竖毛反应、瞳孔大小、异常呼吸)和行为的改变(如步态、姿势、对触摸的反应、反常行为等),注意有无震颤、惊厥、流涎、腹泻、昏睡和昏迷症状。记录局部和全身反应。
1.7.2 生长性能测定 染毒期间,每2 d 一次测定所有存活大鼠的体重,每6 d 一次测定采食量和饮水量。
1.7.3 血液指标的测定 试验结束时,每组选取10 只大鼠(雌雄各半),禁食12 h 后腹腔注射10 %水合氯醛麻醉,腹主动脉采血获得全血和血清样品。血液学指标包括Hg、Ec、Lc、 NL、AL、BL、LM、ML 的数量;血清生化指标包括ALT、AST、Urea、Cr、Glu、ALB、TP、TCH 和TG。
1.7.4 病理检查 大体解剖:采血结束后进行剖检,称量主要脏器(包括肝、肾、脾、胃肠、睾丸、肺、心、卵巢、子宫等)重量,计算各脏器的相对重量(脏器重/体重)。对对照组及高剂量组大鼠主要脏器进行组织病理学检查,若有病变则再对较低剂量组大鼠的相应器官进行检查,其中肝、肾、脾、胃肠、睾丸及卵巢的组织病理学检查为必测项目。
1.8 数据分析
应用SPSS 18.0 统计分析软件对数据进行单因素方差分析(One-way ANOVA),各试验参数在方差齐时,用LSD 检验作多重比较,方差不齐时,用Dunnett’s 检验作多重比较,结果以“平均值±标准差”表示,P<0.05 为差异显著。
2 结果与分析
2.1 临床观察
试验期间各组大鼠无死亡,精神状态良好,采食正常,中、高剂量组个别雄性大鼠偶见大便细软,其他大鼠大小便良好,未见明显异常的临床表现。
2.2 生长性能
2.2.1 周体重和增重率 图1 为雄性和雌性大鼠周平均体重。由图1 可知,各组雄性大鼠体重均大于雌性大鼠,符合大鼠正常生长发育规律。
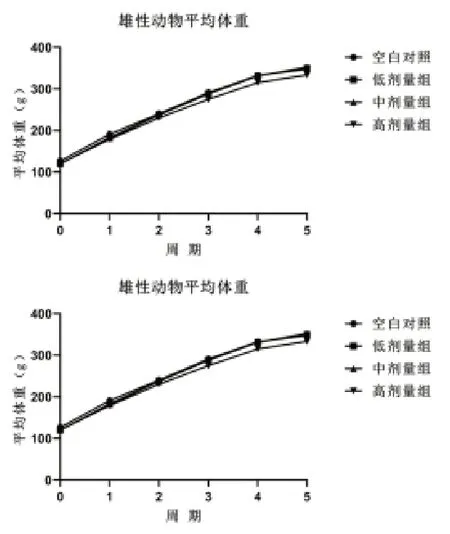
图1 大鼠周平均体重
表1 为大鼠周增重率。由表1 可知,各处理组间雄性大鼠周增重率均无显著性差异。而与空白组相比,雌性大鼠中剂量组第3 周增重率极显著提高(P<0.01);高剂量组雌性大鼠第2 周增重率显著降低(P<0.05),第3 周增重率极显著升高(P<0.01)。表明不同剂量的清营颗粒对雄性大鼠的生长无明显影响,20 g/kg 体重剂量对雌性大鼠个别周期的生长有影响,但无明显规律性。
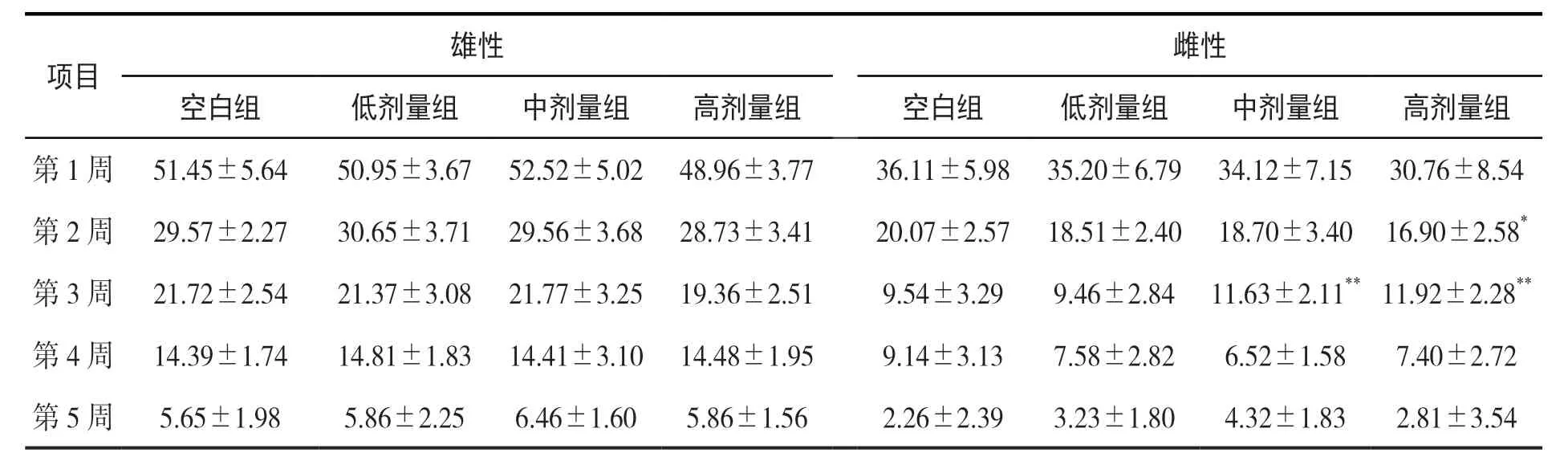
表1 大鼠周增重率 单位:%
2.2.2 采食量和增重耗料比 大鼠各周平均采食量的结果如表2 所示。与空白组相比,中剂量组雄性大鼠第2、3、4 周采食量显著降低(P<0.05),高剂量组雄性大鼠第1~5 周采食量均显著降低(P<0.05),中剂量组和高剂量组雌性大鼠第1~5周采食量显著降低(P<0.05)。

表2 大鼠各周平均采食量 单位:%
大鼠各周增重耗料比的结果如表3 所示。与空白组相比,高剂量组雄性大鼠第2、4 周增重耗料极显著升高(P<0.01),高剂量组雌性大鼠第2、3 周增重耗料极显著升高(P<0.01),而中、低剂量的清营颗粒对大鼠采食量及增重耗料比未产生明显影响。
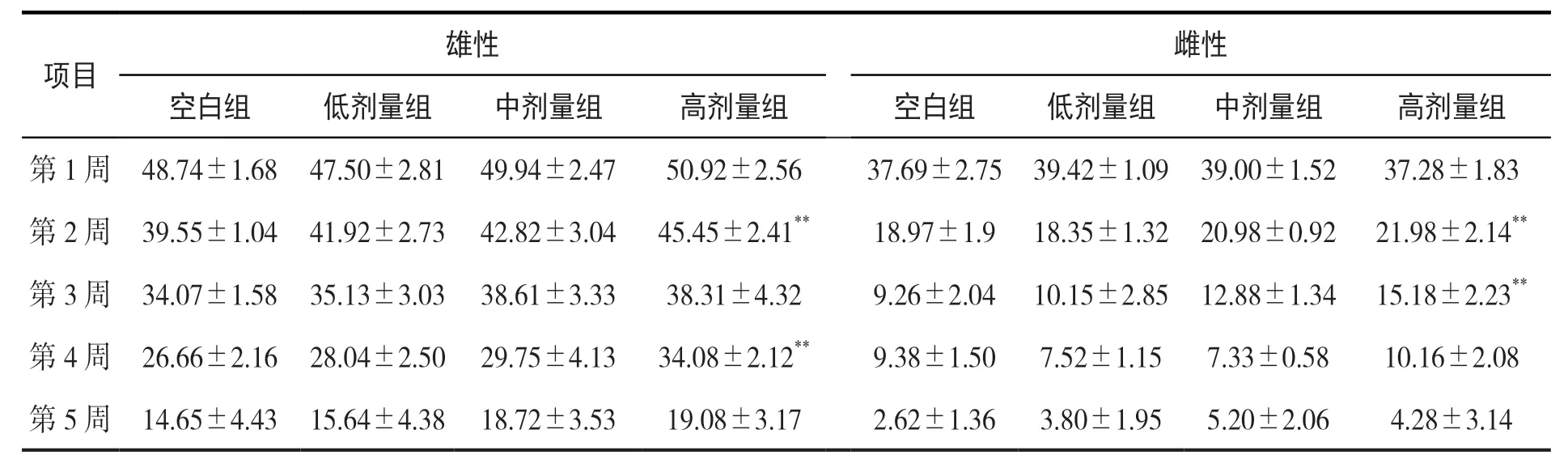
表3 大鼠各周增重耗料比 单位:%
2.2.3 饮水量 大鼠各周平均饮水量结果见表4。各处理组雄性及雌性大鼠间饮水量均无显著差异。
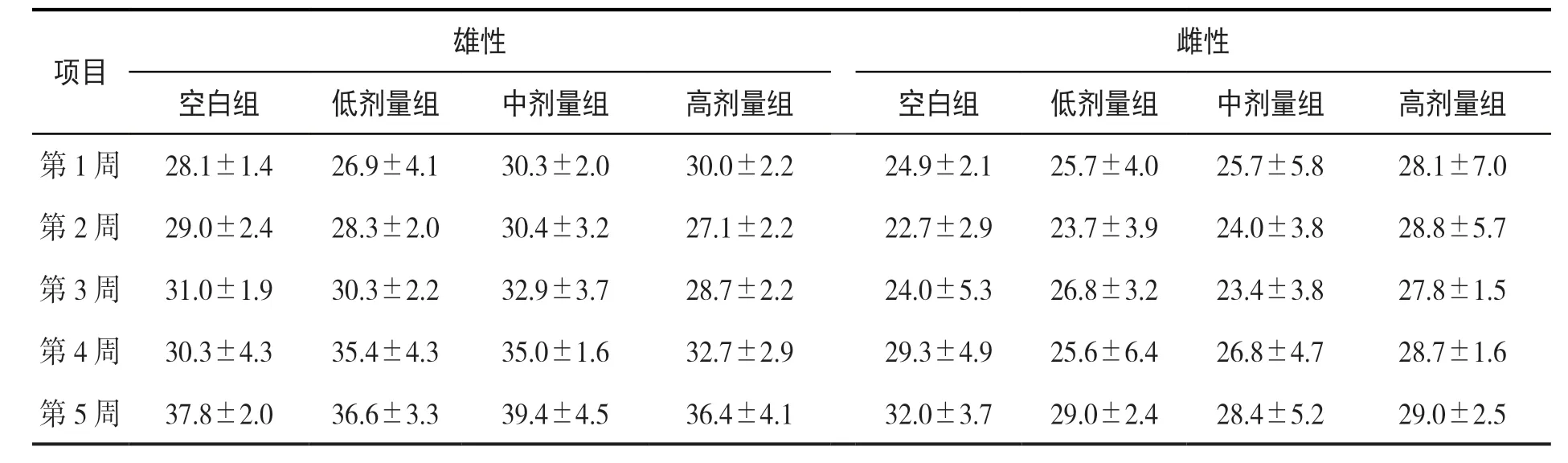
表4 大鼠各周平均饮水量 单位:mL
2.3 血液学检查结果
2.3.1 血常规检查结果 大鼠血常规各项指标检测结果如表5 所示。与空白组相比,低剂量组雄性大鼠各项指标差异不显著;中剂量组HGB、MCHC、MPV 显著降低(P<0.05);高剂量组MCHC、MPV 显著降低,PLT 显著升高(P<0.05),各处理组间雌性大鼠的各项指标差异不显著。
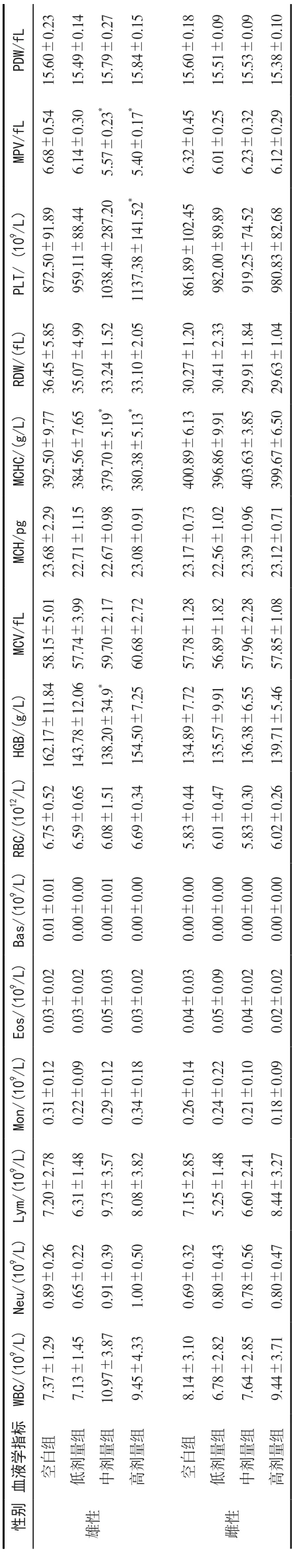
表5 大鼠血液学检测结果
2.3.2 血液生化检查结果 大鼠血清生化各项指标检测结果如表6 所示。与空白对照组相比,雄性大鼠低剂量组各指标差异不显著;中剂量组Glu偏低,AST 偏高,差异显著(P<0.05);高剂量组Glu、TG 偏低,差异显著(P<0.05),各处理组间雌性大鼠的各项指标差异不显著。
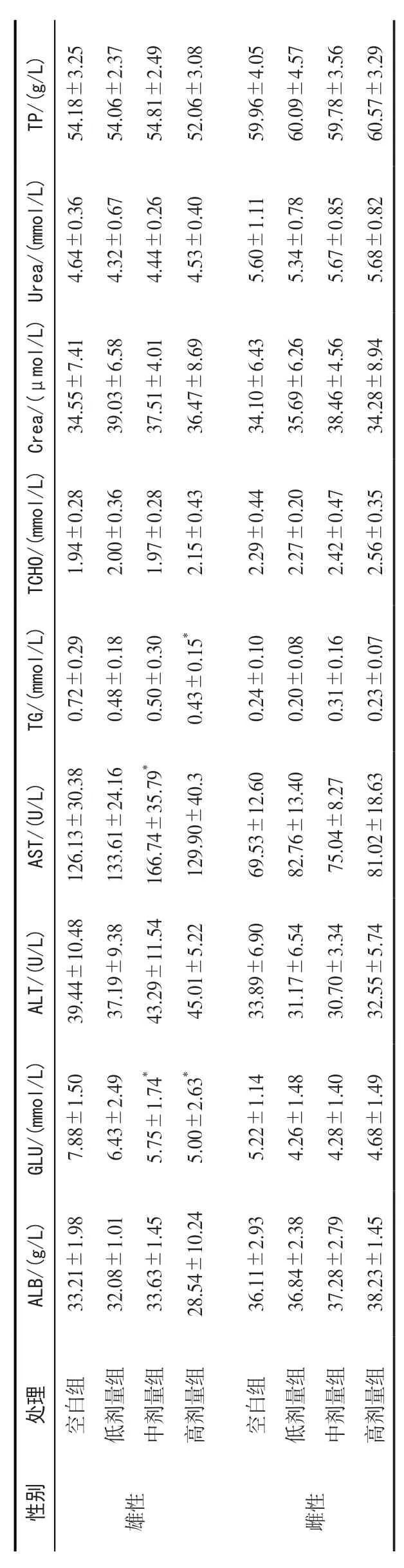
表6 大鼠血清生化检测结果
由此可见,给予10、20 g/kg 体重剂量的清营颗粒对雄性大鼠的个别血液学及血清生化指标有影响,但是对雌性大鼠无影响。
2.4 器官指数
大鼠各器官指数结果如表7 所示。与空白对照组相比,低、中剂量组雄性和雌性大鼠各器官指数均差异不显著,高剂量组胃器官指数显著升高(P<0.05);高剂量雌性大鼠心脏器官指数偏高,差异显著(P<0.05)。表明给予20 g/kg 体重的清营颗粒对大鼠的个别器官指数有一定影响。
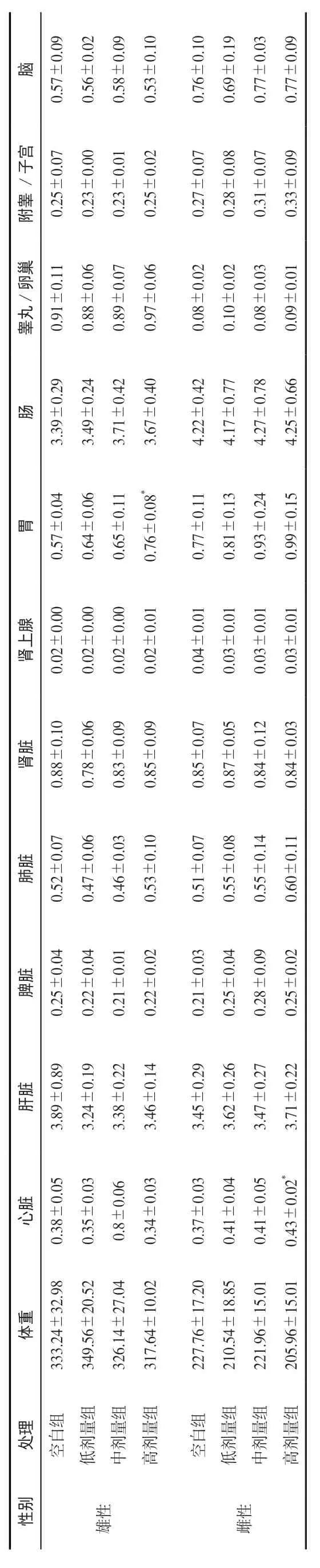
表7 大 鼠器官 指数 单位:g/100g
2.5 组织病理学检查
2.5.1 大体剖检 剖检显示,各处理组大鼠外观无明显病变,呼吸系统、消化系统、泌尿生殖系统、神经系统等无明显异常,主要脏器如肺脏、心脏、肝脏、脾脏、肾脏、肾上腺、胃肠、脑、卵巢、子宫或睾丸、附睾等未见肉眼可观明显病变。
2.5.2 组织病理学结果 组织病理学结果见图2。对于雄性和雌性大鼠:各组肝组织结构基本正常,肝索排列紧密,肝细胞胞核清晰,未见坏死及炎症细胞;汇管区和中央静脉区结构正常。各组脾组织结构正常,未见明显病理改变,脾小结结构正常,红白髓界限清晰,未见细胞坏死。各组肾组织肾小球结构正常,肾小管排列紧密,组织形态结构正常,未见明显病理改变。各组睾丸组织形态结构正常,未见明显病理改变,精原细胞和各级精母细胞梯次排列,细胞形态规则,管腔内可见大量精细胞。各组胃组织结构基本正常,未见明显病理改变,黏膜上皮细胞完整,黏膜层内胃底腺排列整齐,主细胞、壁细胞间杂排列,未见炎症细胞。各组肠组织结构正常,视野内黏膜层上皮细胞排列整齐紧密,未见脱落;黏膜层结构完整,黏膜下层未见水肿或炎症。表明给予5、10、20 g/ kg 体重的清营颗粒不会引起大鼠重要组织器官的明显病变。
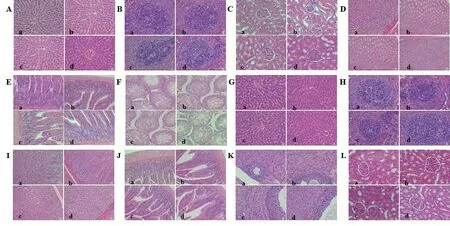
图2 组织病理学结果
3 小结
综上所述,5 g/kg 体重的清营颗粒未对大鼠表现明显的毒性作用,10、20 g/ kg 体重的清营颗粒对大鼠的采食量及雄性大鼠个别血液指标有一定的影响,20 g/kg 体重的清营颗粒对大鼠个别器官指数有影响,但均未引起大鼠重要器官的组织病理学显著变化。因此,清营颗粒的无作用剂量(NOEL)为5 g/kg 体重。

