硼替佐米、地塞米松联合来那度胺方案与硼替佐米、地塞米松联合环磷酰胺方案治疗多发性骨髓瘤的疗效及安全性观察
谌廷妹

【摘要】目的 观察硼替佐米、地塞米松联合来那度胺(VRD)方案與硼替佐米、地塞米松联合环磷酰胺(VCD)方案对多发性骨髓瘤患者的治疗效果及安全性,为临床提供参考。方法 回顾性分析盐城市第一人民医院2020年1月至2022年12月收治的60例多发性骨髓瘤患者的临床资料,根据治疗方案不同分为VRD组和VCD组,每组30例。比较两组患者治疗效果、各项生化指标水平、T淋巴细胞亚群水平及不良反应发生情况。结果 VRD组患者的整体疗效优于VCD组,且总缓解率高于VCD组(P<0.05)。两组患者治疗后血清M蛋白、骨髓中浆细胞比例及β2-微球蛋白水平低于治疗前,血红蛋白水平高于治疗前,且VRD组血清M蛋白、骨髓中浆细胞比例及β2-微球蛋白水平低于VCD组,血红蛋白水平高于VCD组(P<0.05)。两组患者治疗后CD4+T淋巴细胞百分比、CD4+/CD8+比值高于治疗前,CD8+T淋巴细胞百分比低于治疗前,且VRD组CD4+T淋巴细胞百分比、CD4+/CD8+比值高于VCD组,CD8+T淋巴细胞百分比低于VCD组(P<0.05)。两组患者不良反应发生率比较,差异无统计学意义(P>0.05)。结论 VRD方案治疗多发性骨髓瘤效果显著,能够明显优化机体生化指标,改善免疫功能,且安全性良好。
【关键词】硼替佐米;地塞米松;来那度胺;环磷酰胺;多发性骨髓瘤;血清M蛋白;血红蛋白
【中图分类号】R733.3 【文献标识码】A 【文章编号】2096-2665.2023.21.0001.04
DOI:10.3969/j.issn.2096-2665.2023.21.001
Efficacy and safety of bortezomib, dexamethasone combined with lenalidomide schemes and bortezomib, dexamethasone combined with cyclophosphamide schemes in the treatment of multiple myeloma
CHEN Tingmei
(Department of Hematopathology, Yancheng No.1 Peoples Hospital, Yancheng 224000, Jiangsu, China)
【Abstract】Objective To observe the therapeutic effect and safety of bortezomib, dexamethasone combined with lenalidomide (VRD) schemes and bortezomib, dexamethasone combined with cyclophosphamide (VCD) schemes in multiple myeloma patients, so as to provide reference for clinical practice. Methods The clinical data of 60 patients with multiple myeloma admitted to Yancheng No.1 Peoples Hospital from January 2020 to December 2022 were retrospectively analyzed. According to different treatment schemes, they were divided into VRD group and VCD group, with 30 cases in each group. The treatment efficacy, levels of various biochemical indicators, levels of T lymphocyte subpopulations, and incidence of adverse reactions were compared between the two groups. Results The overall curative effect of VRD group was better than that of VCD group, and the overall remission rate was higher than that of VCD group (P<0.05). After treatment, serum M protein, plasma cell ratio in bone marrow and β2-microglobulin levels of patients in two groups were lower than those before treatment, the hemoglobin levels was higher than that before treatment, and the serum M protein, plasma cell ratio in bone marrow and β2-microglobulin levels in the VRD group were lower than those in the VCD group, while hemoglobin levels were higher than the VCD group (P<0.05). After treatment, the percentage of CD4+T lymphocytes and the ratio of CD4+/CD8+ of patients in two groups were higher than those before treatment, while the percentage of CD8+T lymphocytes was lower than before treatment, and the percentage of CD4+T lymphocytes and the ratio of CD4+/CD8+ in the VRD group were higher than those in the VCD group, and the percentage of CD8+T lymphocytes was lower than that in the VCD group (P<0.05). There was no significant difference in the incidence of adverse reactions between the two groups (P>0.05). Conclusion VRD schemes has a significant effect in the treatment of multiple myeloma, which can significantly optimize the biochemical indicators of the body, improve immune function, and has good safety.
【Keywords】 Bortezomib; Dexamethasone; Lenalidomide; Cyclophosphamide; Multiple myeloma; Serum M protein; Hemoglobin
多发性骨髓瘤是由浆细胞异常增殖导致的恶性肿瘤,其特征是浆细胞异常增殖产生单克隆免疫球蛋白,从而导致组织损伤。多发性骨髓瘤的主要临床表现包括贫血、骨质破坏、肾功能障碍或复发性感染等[1]。多发性骨髓瘤多见于老年人,且大多数在70岁以上,随着人口老龄化的逐年加剧,多发性骨髓瘤发病率呈增长趋势[2]。目前临床对该病的治疗分为初始诱导治疗、巩固治疗和维持治疗[3]。目前初始治疗的首选方案是含硼替佐米的三药联合方案。其中以硼替佐米、来那度胺联合地塞米松(VRD)治疗方案与硼替佐米、环磷酰胺联合地塞米松(VCD)治疗方案较为常用。本研究旨在观察VRD与VCD两种治疗方案对多发性骨髓瘤的效果及安全性,现报道如下。
1 资料与方法
1.1 一般资料 回顾性分析盐城市第一人民医院2020年1月至2022年12月收治的60例多发性骨髓瘤患者的临床资料,根据治疗方案不同分为VRD组和VCD组,每组30例。VRD组患者中男性13例,女性17例;年龄45~81岁,平均年龄(60.46±12.94)岁;BMI 20~28 kg/m2,平均BMI (23.33±1.05)kg/m2。VCD组患者中男性15例,女性15例;年龄46~80岁,平均年龄(60.12±12.42)岁;BMI 21~29 kg/m2,平均BMI (23.91±1.22)kg/m2。两组患者一般资料比较,差异无统计学意义(P>0.05),组间具有可比性。本研究經盐城市第一人民医院医学伦理委员会批准。纳入标准:①符合多发性骨髓瘤的诊断标准[4];②预计生存期>6个月。排除标准:①合并其他恶性肿瘤者;②对本研究药物过敏者;③合并其他慢性肾脏疾病者。
1.2 治疗方法 VRD组患者在每个化疗疗程的第1、4、8、11天给予硼替佐米(南京正大天晴制药有限公司,国药准字H20183401,规格:3.5 mg/瓶)1.3 mg/m2进行皮下注射,1次/d;第1、2、4、5、8、9、11、12天给予地塞米松(辰欣药业股份有限公司,国药准字H37021969,规格:1 mL∶5 mg)20 mg+5%葡萄糖注射液100 mL进行静脉滴注,1次/d;第1~14天口服来那度胺(正大天晴药业集团南京顺欣制药有限公司,国药准字H20193006,规格:25 mg/粒)25 mg/次,1次/d。VCD组患者硼替佐米、地塞米松用法用量与VRD组相同,于每个化疗疗程的第1、8、15天给予注射用环磷酰胺[江苏恒瑞医药股份有限公司,国药准字H32020857,规格:0.2 g(按C7H15Cl2N2O2P计)]400 mg/m2+0.9%氯化钠注射液100 mL进行静脉滴注,1次/d。21 d为1个疗程,两组患者均持续治疗4个疗程。
1.3 观察指标 ①比较两组患者治疗效果。完全缓解:血清M蛋白水平较治疗前减少≥90%,患者贫血、骨痛症状消失;部分缓解:50%≤血清M蛋白水平较治疗前减少<90%,患者贫血、骨痛症状有所改善;进步:25%≤血清中M蛋白水平较治疗前减少<50%,患者贫血、骨痛症状有所改善;无效:血清M蛋白水平较治疗前减少<25%,患者贫血、骨痛症状无改善或甚至加重[5]。总缓解率=(完全缓解+部分缓解+进步)例数/总例数×100%。②比较两组患者各项生化指标水平。采集两组患者治疗前后晨起空腹肘静脉血5 mL,采用离心机(湖南湘仪实验室仪器开发有限公司,型号:L600-A)以3 000 r/min进行离心5 min,采用免疫固定电泳法测定血清M蛋白水平,采用骨髓涂片法检测骨髓中浆细胞比例,采用免疫比浊法检测β2-微球蛋白水平。采集两组患者治疗前后的晨起空腹肘静脉血3 mL,采用血液细胞分析仪(深圳迈瑞生物医疗电子股份有限公司,型号:BC-11)测定血红蛋白。③比较两组患者T淋巴细胞亚群水平。取血清方式同②,采用流式细胞仪(美国BD公司,型号:BD FACSCanto Ⅱ)测定CD4+T淋巴细胞百分比、CD8+T淋巴细胞百分比,计算CD4+/CD8+比值。④比较两组患者不良反应发生情况。不良反应包括恶心呕吐、疲劳乏力及腹胀。不良反应发生率=各项不良反应发生例数之和/总例数×100%。
1.4 统计学分析 采用SPSS 22.0统计学软件处理数据。计数资料以[例(%)]表示,组间比较采用χ2检验,等级资料比较采用秩和检验。计量资料以(x)表示,组间比较采用独立样本t检验,组内比较采用配对样本t检验。以P<0.05为差异有统计学意义。
2 结果
2.1 两组患者治疗效果比较 VRD组患者的整体疗效优于VCD组,且总缓解率高于VCD组,差异有统计学意义(P<0.05),见表1。
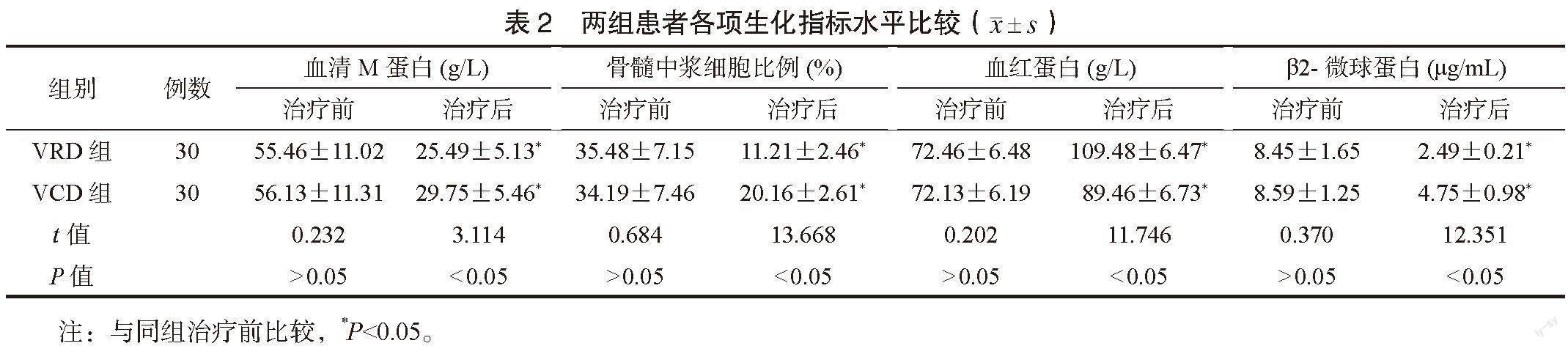
2.2 两组患者各项生化指标水平比较 两组患者治疗前血清M蛋白、骨髓中浆细胞比例、血红蛋白及β2-微球蛋白水平比较,差异无统计学意义(P>0.05);两组患者治疗后血清M蛋白、骨髓中浆细胞比例及β2-微球蛋白水平低于治疗前,血红蛋白水平高于治疗前,且VRD组血清M蛋白、骨髓中浆细胞比例及β2-微球蛋白水平低于VCD组,血红蛋白水平高于VCD组,差异有统计学意义(P<0.05),见表2。
2.3 两组患者T淋巴细胞亚群水平比较 两组患者治疗前CD4+T淋巴细胞百分比、CD8+T淋巴细胞百分比、CD4+/CD8+比值比较,差异无统计学意义(P>0.05);两组患者治疗后CD4+T淋巴细胞百分比、CD4+/CD8+比值高于治疗前,CD8+T淋巴细胞百分比低于治疗前,且VRD组CD4+T淋巴细胞百分比、CD4+/CD8+比值高于VCD组,CD8+T淋巴细胞百分比低于VCD组,差异有统计学意义(P<0.05),见表3。
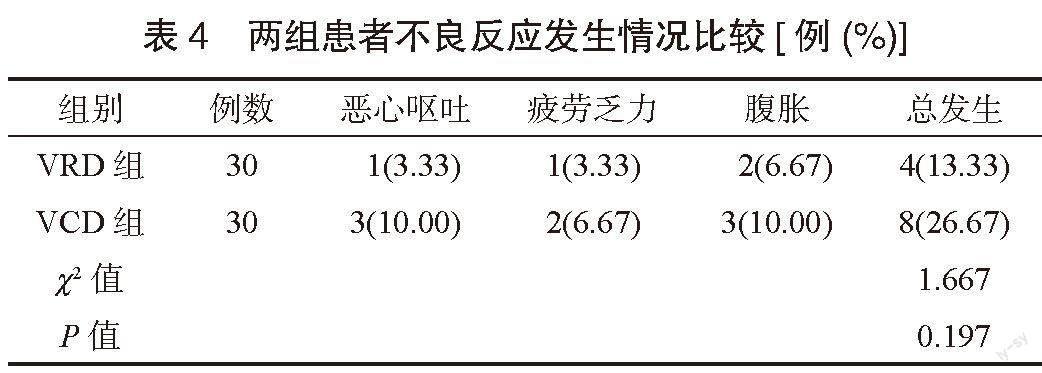
2.4 两组患者不良反应发生情况比较 两组患者不良反应发生率比较,差异无统计学意义(P>0.05),见表4。
3 讨论
多发性骨髓瘤是一种由浆细胞异常增殖所致的恶性肿瘤,调查显示,其发病与性别、年龄有关,职业环境、生活方式、自身免疫性疾病等也可能在该病的发病中起到一定作用[6-7]。目前临床治疗该病的方法多为造血干细胞移植,但由于移植对患者身体条件有一定要求,且多发性骨髓患者多以老年人为主,接受造血干细胞移植治疗的风险较高[8],因此,越来越多的学者致力于寻找一种既能提高患者耐受性,又能延长患者生存期的方案。
本研究结果显示,VRD组患者的整体疗效优于VCD组,且总缓解率高于VCD组,这表明VRD方案治疗多发性骨髓瘤患者效果显著。临床研究显示,硼替佐米能够抑制蛋白酶功能、诱导细胞凋亡且能够抑制血管生成,杀伤骨髓瘤细胞,硼替佐米可作用于骨髓微环境,抑制骨髓瘤细胞黏附,调节各种细胞因子的产生[9]。地塞米松属于肾上腺皮质激素类药物,可溶解淋巴细胞并抑制细胞有丝分裂[10]。来那度胺具有抗肿瘤、免疫调节等多种作用,可抑制前炎症因子的分泌[11]。因此,VRD方案可通过抗血管生成、改善骨髓微环境、促进肿瘤细胞凋亡等多种途径提高治疗多发性骨髓瘤的效果。
本研究结果显示,治疗后VRD组患者血清M蛋白、骨髓中浆细胞比例及β2-微球蛋白水平低于VCD组,血红蛋白水平高于VCD组,这表明VRD方案能够有效提高临床疗效,调节患者生化指标水平。当浆细胞异常增殖时,机体内会分泌血清肿瘤标记物——M蛋白,因此,M蛋白水平可作为诊断多发性骨髓瘤的依据[12]。VRD方案中的来那度胺可通过多靶点作用于骨髓瘤细胞的微环境,抑制血管生长、骨髓细胞增殖并诱导异常细胞分解,且能够恢复骨髓造血功能,发挥直接抗肿瘤、免疫功能调节等多重作用,且不同药物之间无交叉耐药性,可以获得更显著的治疗效果[13]。本研究结果表明,治疗后VRD组患者CD4+T淋巴细胞百分比、CD4+/CD8+比值高于VCD组,CD8+T淋巴细胞百分比低于VCD组,这说明VRD方案可有效改善患者免疫功能,可能与来那度胺调节机体内免疫抑制的微环境,从而降低肿瘤负荷,改善机体免疫功能有关[14]。且本研究结果显示,两组患者不良反应发生率比较,差异無统计学意义,这表明VRD方案不会增加患者不良反应,安全性良好。
综上所述,VRD方案用于多发性骨髓瘤治疗效果显著,能够明显优化机体生化指标,改善免疫功能,且安全性良好。
参考文献
闫慧.多发性骨髓瘤化疗患者症状群现状及其影响因素分析[D].唐山:华北理工大学, 2021.
况小红,童浩,代明辉,等.全球多发性骨髓瘤发病和死亡现状及其与人类发展指数的关系[J].现代肿瘤医学, 2021, 29(2): 302-306.
陈凯.多发性骨髓瘤诊断与治疗的研究进展[J].大医生, 2019, 4(7): 149-150.
中国医师协会血液科医师分会,中华医学会血液学分会,中国多发性骨髓瘤工作组.中国多发性骨髓瘤诊治指南(2011年修订)[J].中华内科杂志, 2011, 50(10): 892-896.
中华医学会血液学分会.多发性骨髓瘤骨病诊治指南[J].中华血液学杂志, 2011, 32(10): 721-723.
黄勃,吴春叶,王晓桃.多发性骨髓瘤治疗新进展[J].医学综述, 2019, 25(8): 1511-1516.
王得印,郝云良,肖萌,等.多发性骨髓瘤流行病学及病因分析[J].国际流行病学传染病学杂志, 2018, 45(4): 277-280.
李静静,柴晔.多发性骨髓瘤移植后的维持治疗进展[J].西北国防医学杂志, 2018, 39(3): 204-207.
李星,石昊.多发性骨髓瘤应用硼替佐米为主化疗方案的临床疗效观察[J].山西医药杂志, 2020, 49(19): 2593-2595.
雷丽华,何东,林娟,等.硼替佐米联合地塞米松治疗多发性骨髓瘤对患者骨代谢及免疫功能的影响[J].实用癌症杂志, 2020, 35(6): 917-920.
郭秋霞,王吉刚,刘彦琴,等.来那度胺对多发性骨髓瘤患者自体移植造血干细胞采集影响[J].临床军医杂志, 2021, 49(1): 37-39, 43.
张柳芸,向云会,李艳英,等.M蛋白在多发性骨髓瘤与淋巴瘤中的临床作用[J].中国实验血液学杂志, 2022, 30(4): 1281-1285.
许晗,王梦莹,姜骁娜,等.硼替佐米联合来那度胺和地塞米松治疗新诊断多发性骨髓瘤疗效及安全性分析[J].临床血液学杂志, 2022, 35(1): 46-51, 57.
王飞,罗达似,夏天,等.来那度胺联合硼替佐米治疗多发性骨髓瘤的疗效及免疫相关细胞因子含量的影响[J].华夏医学, 2019, 32(4): 20-23.

