焦炉煤气典型组分热重整反应平衡常数分析
董 靖
(上海电气集团国控环球工程有限公司,山西 太原 030001)
0 引言
焦炉煤气传统直排或燃烧的解决方案,在导致资源损耗的同时,还会引发环境污染[1],焦炉煤气主要成分是CH4,将其重整转化为合成气是一条有效的资源化路线[2-3]。焦炉煤气热重整涉及多种化学物质,是非常复杂的反应过程。为实现焦炉煤气的非催化热重整,需要在荒煤气中喷入纯氧作为反应物料,提高反应温度。焦炉煤气中存在28%左右的水蒸气和3%左右的CO2,焦炉煤气重整反应本质是甲烷、小分子脂肪烃、苯类、酚类、萘、蒽类稠环芳烃、焦油类重质烃等多种组分与O2、水蒸气、CO2的高温化学反应[4-5],气体产物组成取决于各反应的热力学平衡结果。本文研究工作针对上述反应,选取相应的典型代表组分,进行相关化学反应的热力学平衡常数分析[6],推断有机烃的转化率和合成气组成。
1 典型组分重整反应平衡常数分析
焦炉煤气中含28%左右的水蒸气,在加氧提温过程中,H2等可燃组分与O2反应生成水蒸气。根据反应物和产物的热力学参数,分别计算水蒸气气氛、O2/水蒸气气氛中,各类有机烃的反应吉布斯自由能和反应平衡常数[6-7]。
1.1 甲烷重整
从表1 可以看出,反应温度高于973 K,反应吉布斯自由能小于0 kJ,甲烷水蒸气重整反应可以自发进行,反应向产物H2、CO 方向移动。当反应温度达到1 473 K,甲烷转化率达到99%以上。反应系统中O2存在条件下,既使反应温度在773 K,反应的吉布斯自由能达到-320 kJ/mol,平衡常数达到4.395 E+021。可见,O2的存在可以极大地推动反应向产物(H2、CO)方向移动,促进甲烷的分解和转化,1 000 ℃以上,甲烷几乎完全转化。
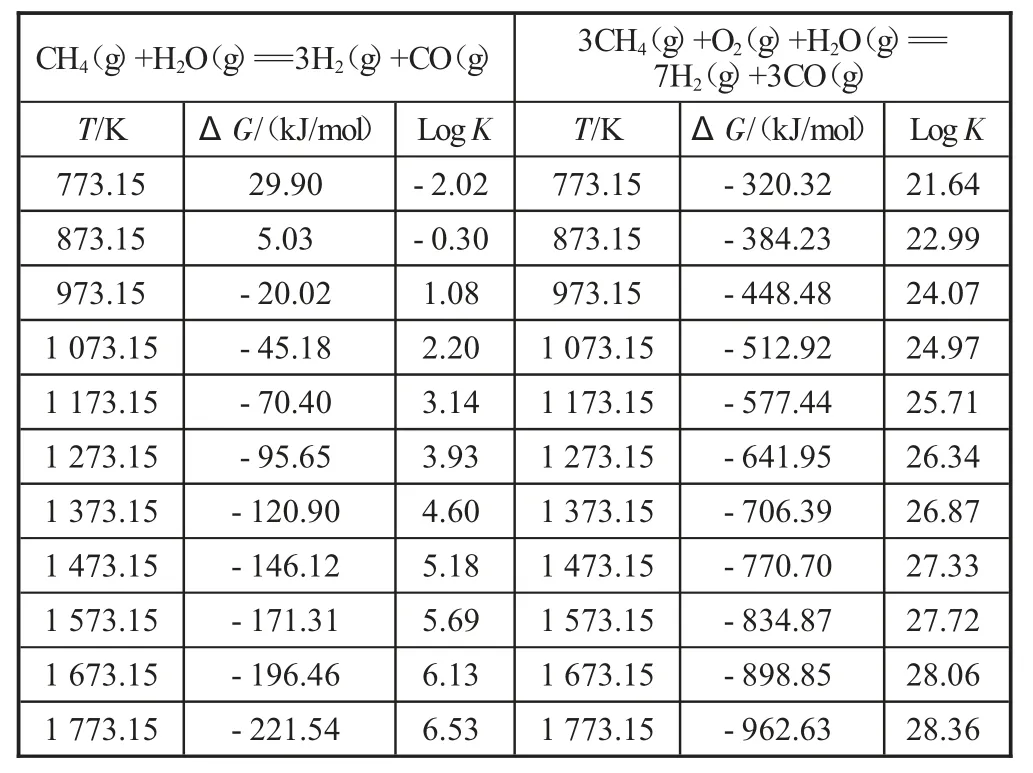
表1 甲烷重整反应热力学参数和平衡常数分析
1.2 小分子烯烃重整
从表2 可以看出,既使反应温度低于773 K,乙烯与水蒸气反应的吉布斯自由能依然小于0 kJ,乙烯的水蒸气重整反应可以自发进行,反应向产物H2和CO方向移动。当反应温度达到1 573 K,乙烯转化率达到99.99%以上,乙烯体积分数仅为10-9级。O2存在条件下,反应更易于向合成气产物方向进行,即使在较低的温度(773 K)下,乙烯小分子也几乎完全转化。
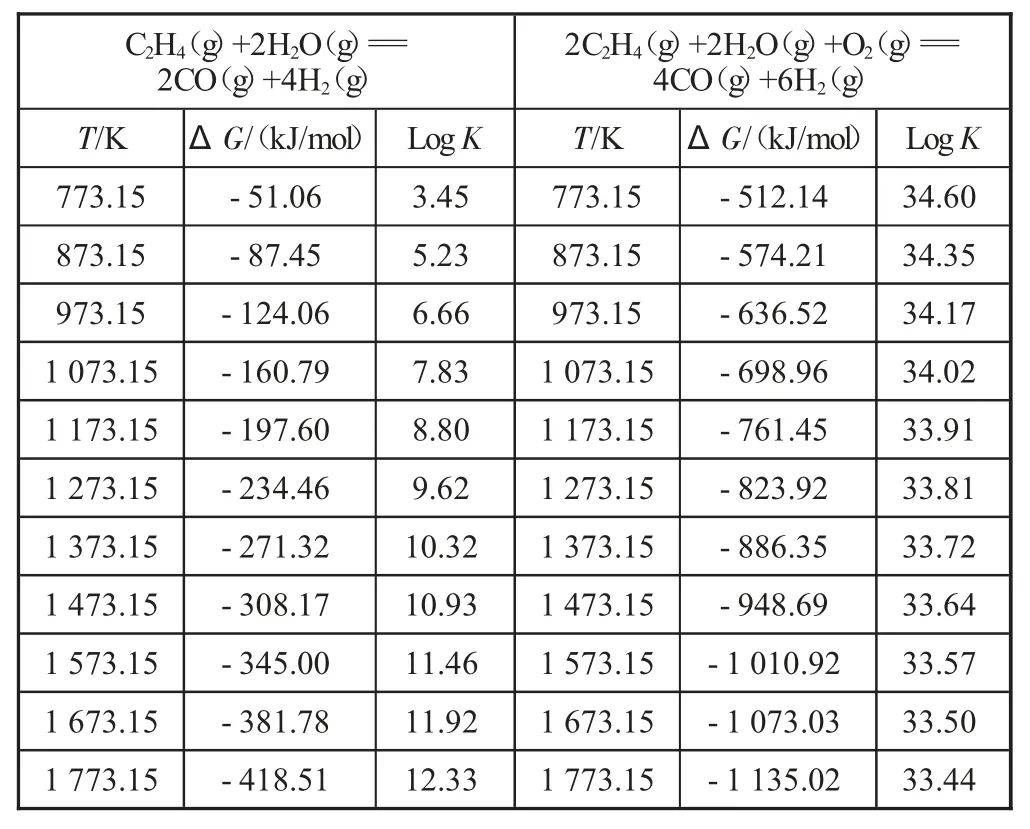
表2 小分子烃类(乙烯)重整反应热力学参数和平衡常数分析
1.3 芳烃重整
从表3 可以看出,苯类芳烃的水蒸气重整反应比较容易进行。当反应温度为773 K,反应吉布斯自由能-65.68 kJ/mol,反应平衡常数较大。随着温度的升高,反应吉布斯自由能快速减小,平衡常数显著增大。当反应温度1 273 K,反应吉布斯自由能-592.9 kJ/mol,反应的平衡常数达2.122 E+024,苯类芳烃几乎完全转化。系统中有O2条件下,随着反应温度的升高,反应平衡常数有所减小,但在1 273 K,反应吉布斯自由能-1 302.9 kJ/mol,反应平衡常数达2.880 E+053,苯类芳烃几乎完全转化。由此可见,O2可以极大地推动反应向合成气产物(H2和CO)方向移动,促进苯类芳烃的分解和转化。
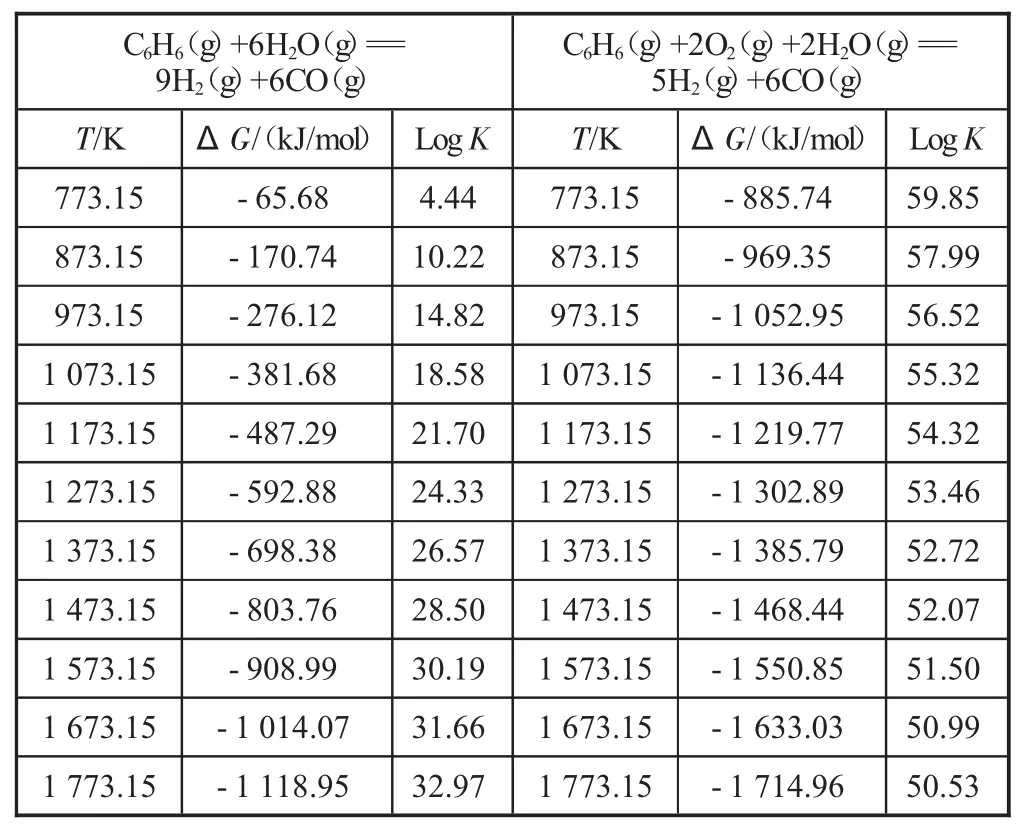
表3 芳烃类(苯)重整反应热力学参数和平衡常数分析
1.4 酚类重整
从表4 可以看出,酚类芳烃的水蒸气重整反应比苯类有机物更容易进行。当反应温度773 K,反应吉布斯自由能-100.2 kJ/mol,反应的平衡常数较大。随温度的升高,反应吉布斯自由能有所减小,平衡常数显著增大。当反应温度1 273 K,反应吉布斯自由能-225.2 kJ/mol,反应平衡常数达6.934E+031,酚类芳烃几乎完全转化。反应系统中有O2存在条件下,随着反应温度升高,反应平衡常数减小,但反应温度在1 273 K,反应吉布斯自由能-380.1 kJ/mol,反应平衡常数达到5.438E+053,酚类芳烃几乎完全转化。由此可见,O2的存在可以极大地推动反应向合成气产物(H2和CO)方向移动,促进酚类芳烃的分解和转化。
1.5 多环芳烃重整
从表5 可以看出,萘的水蒸气重整反应比苯类有机物更容易进行。当反应温度为773 K,反应吉布斯自由能为-105.8 kJ/mol,反应平衡常数较大。随着温度的升高,反应吉布斯自由能有所减小,平衡常数显著增大。当反应温度为1 273 K,反应吉布斯自由能为-968.1 kJ/mol,反应的平衡常数达到5.267E+039,萘类芳烃几乎完全转化。反应系统中有O2存在条件下,尽管随着反应温度升高,反应的平衡常数有所减小,但在反应温度1273K,反应吉布斯自由能-2 033.1 kJ/mol,反应平衡常数达到2.634E+083,酚类芳烃几乎完全转化。由此可见,O2的存在可以极大地推动反应向合成气产物(H2和CO)方向移动,促进萘类稠环芳烃的分解和转化。
1.6 重质烃重整
从表6 可以看出,重质烃的水蒸气重整反应比苯、酚、萘类有机物更容易进行。当反应温度为773 K,反应吉布斯自由能为-634.7 kJ/mol,反应平衡常数较大。随着温度的升高,反应吉布斯自由能减小,反应平衡常数迅速增大。当反应温度为1 273 K,反应吉布斯自由能为-2 974.6 kJ/mol,反应平衡常数达1.124E+122,重质烃类物质完全转化。系统中有O2存在条件下,随反应温度升高,反应平衡常数有所减小,但反应温度在1 273 K,反应吉布斯自由能为-5 459.627 kJ/mol,反应的平衡常数达到1.036E+224,重质烃几乎完全转化。由此可见,O2的存在可以极大地推动反应向合成气产物(H2和CO)方向移动,促进重质烃类物质的分解和转化。
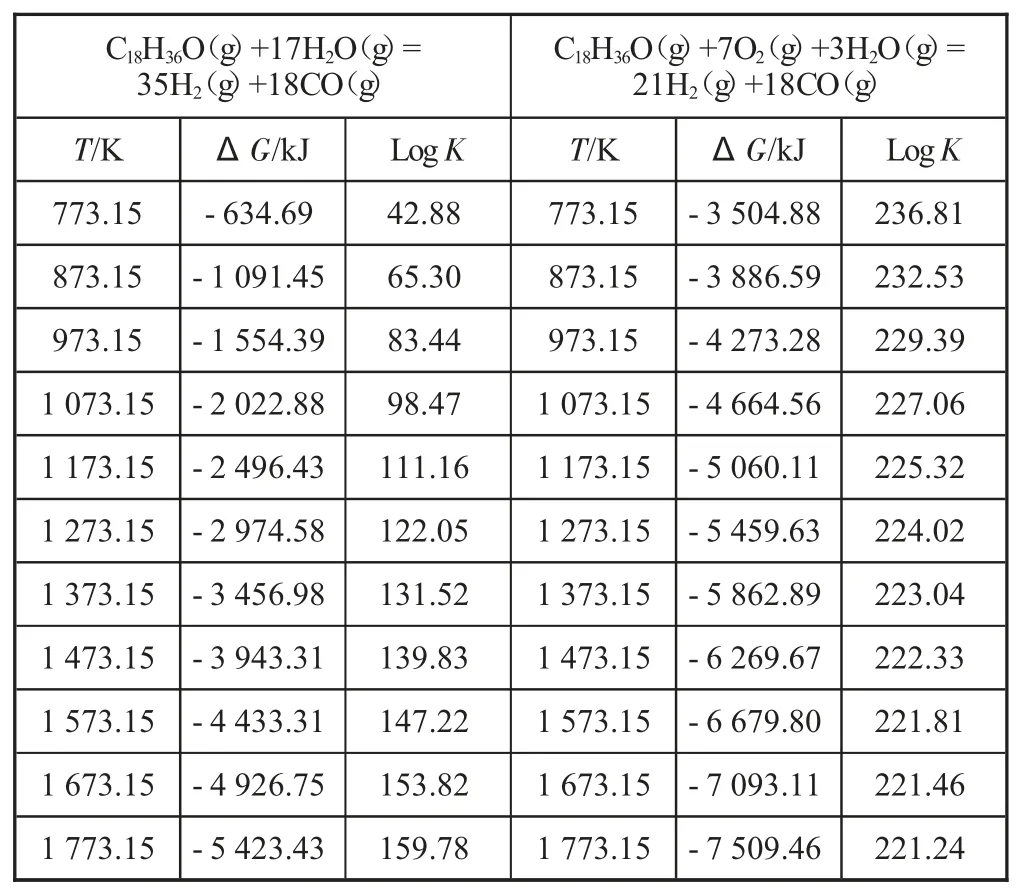
表6 重质烃重整反应热力学参数和平衡常数分析
2 结论及分析
1)焦炉煤气中CH4含量高,与大分子有机烃类相比,CH4重整反应的平衡常数较小,只有提高温度至1 200 ℃以上,才能保证甲烷转化。提高甲烷的转化率,减小合成气中甲烷浓度,是焦炉煤气重整技术成功的关键。
2)对于各种有机烃,大分子烃类物质更易与水蒸气发生重整反应,生成H2和CO。小分子烃类、芳烃类、多环芳烃、重质烃的水蒸气重整反应平衡常数均远高于甲烷。在O2和水蒸气混合气氛中,反应温度达到1 000 ℃以上,上述有机烃类几乎完全转化。
3)O2的加入提高了反应温度和反应速率,推动热力学平衡向合成气产物方向移动,增大有机烃类重整反应的化学平衡常数,提升其转化率。
4)根据热力学平衡常数,在焦炉煤气热重整反应体系中,只要维持一定的温度和水蒸气浓度,荒煤气中的有机组成可以完全转化为合成气,化学反应热力学并不是重整反应的限制因素。提升重整反应速度,突破反应动力学的限制是进行工艺技术开发的关键。

