基于化学学科理解视角,建构判断“基元反应”的思维模型
董拥军
(江苏省南京师范大学附属扬子中学)
关于“基元反应”,《普通高中化学课程标准》(2017年版2020年修订)(以下简称新课标)的要求如下:知道化学反应是有历程的,认识基元反应活化能对化学反应速率的影响。在人教版(2019年版)选择性必修1《化学反应原理》中“基元反应”相关叙述如下:




基元反应发生的先决条件是反应物的分子必须发生碰撞。
无论是新课标还是新人教版教材,都没有对“基元反应”准确地下定义,这就给教师的教和学生的学带来了一定的困惑,在确定一个总反应到底有多少个基元反应时就会产生不同的看法。
1.关于一道与“基元反应”相关题目的争论
1.1 原题呈现

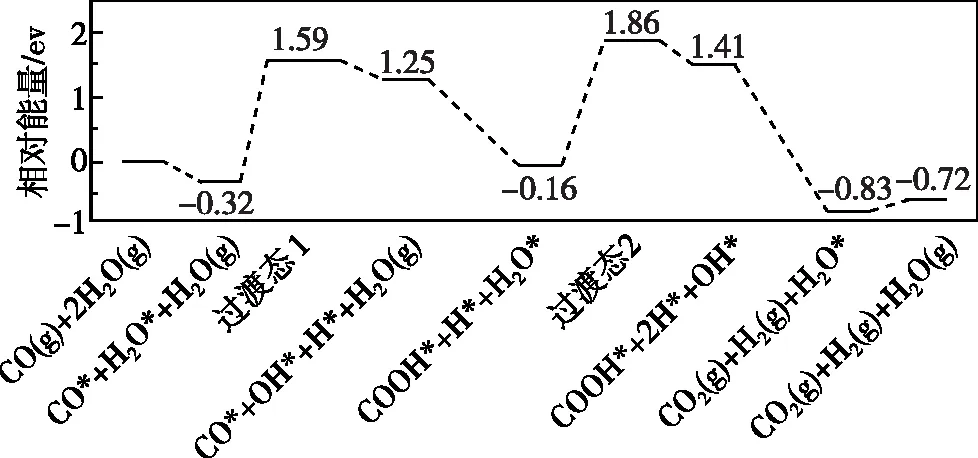
图1
下列说法正确的是
( )
A.该历程共包括8个基元反应
B.CO(g)和H2O(g)被吸附在催化剂表面时吸收能量

D.放热最多的步骤只有极性键的断裂与形成
1.2 试题来源
本试题来源于2019年全国Ⅰ卷,28题节选:

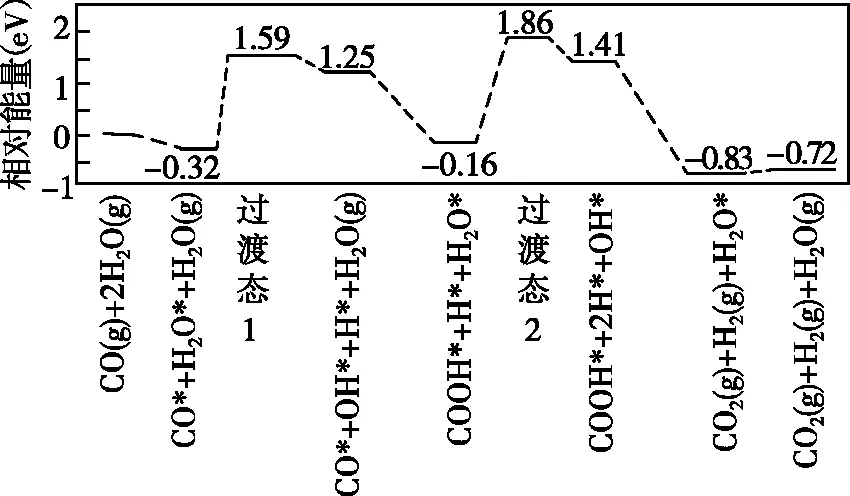
图2

图3 基元过程分类图

图4 基元反应作为化学反应的基本属性

图5 确定基元反应的基本方法
可知水煤气变换的ΔH________(填“大于” “等于”或“小于”)0,该历程中最大能垒(活化能)E正=________eV,写出该步骤的化学方程式:______________________________。
1.3 争论的焦点
争论的焦点在于:本反应历程中共有几个基元反应?
本反应的历程可表示为如下过程:






主要的观点有:
(1)有8个基元反应。有老师认为,图中共有8条虚线,代表着有9种不同状态间的转化,每一条虚线代表一次转化,为一个基元反应,共转化了8次,则共有8个基元反应。
(2)有6个基元反应。有老师认为,图中虽然有8条虚线,但并不代表9种不同状态间的转化,其中的过渡态表示旧化学键将断未断、新化学键将成未成,不能代表有新物质生成。过渡态前后不同状态间的一次转化为一个基元反应,过渡态代表物质转化所需要跨过的能量峰值,标志着该基元反应的活化能。
(3)有4个基元反应。有老师认为,过渡态前后不同状态间的一次转化只能算作一个基元反应,而且反应物分子在催化剂上的吸附和生成物分子在催化剂上的解吸都不能算作基元反应,所以本反应的基元反应只有4个。
(4)只有2个基元反应。有老师认为,基元反应就是反应物和产物之间只有一个能量峰值的化学变化过程,本反应中只有两个能量峰值,所以基元反应只有2个。
基于上述的争论,有必要在化学学科本原上厘清“基元反应”的定义,只有在基于化学学科理解的基础上,把握“基元反应”的内涵和外延,才能对一个总反应包含“基元反应”的个数作出准确的判断。
2.基元反应的定义和判断方法
2.1 基元反应的定义
如果一个化学反应,反应物分子在碰撞过程中相互作用直接转化为生成物分子,这种化学反应称为基元反应,反之就是非基元反应,也称为总包反应,简称总反应。一个复杂反应要经过若干基元反应才能完成,这些基元反应代表了反应所经过的途径,动力学上称为反应机理或反应历程。活化能有基元反应活化能和总反应表观活化能之分。活化能仅对基元反应有明确的物理意义,即活化分子的平均能量与全部反应物分子平均能量之差;而在复杂反应中,它只是各基元反应活化能的综合表现,是反应速率的温度系数,这时的活化能称为该总包反应的表观活化能。
江苏南通崔恒祥老师认为:所谓基元反应是指反应物粒子(原子、离子、分子、自由基等)在碰撞过程中相互作用直接转变为新产物的反应。
西安交通大学王明德教授认为:基元过程是只被一个能峰隔开的两个相邻的有一定稳定性的状态之间的变化。能峰可高可低,最低时为0。可以把所有能一步完成的简单变化过程称为基元过程,基元过程既可以是发生化学变化的基元反应,也可以是简单的物理变化。将有新物质生成的基元过程视为基元反应,即它们都涉及化学键的重组。基元反应就是反应物和产物之间只有一个能峰的化学变化过程。
2.2 确定基元反应的方法
上海大学吴俊明教授认为基元反应没有任何中间产物,这是判定基元反应的准则。反应机理又称反应历程,包括某一化学反应过程中所经历的全部基元反应和按照一定规律组合这些基元反应来描述复杂反应的过程,以及体现总反应与基元反应内在联系的复杂组合。反应机理(反应历程)应尽可能详细地描述反应物向生成物每一步转化的过程,包括过渡态的形成、键的断裂和形成,以及各基元反应的相对速率大小等。基于微观视角分析,反应物分子一般总是要经过若干简单反应步骤,才最终转化为产物分子。而每一个简单的反应步骤,就是一个基元反应。

从以上论述可知,基元反应作为一种化学反应,一定也遵循作为化学反应的基本要求。在宏观上,基元反应遵循着有新物质生成的规律;在微观上,基元反应遵循着有旧键断裂或有新键形成的规律。
宏观上有新物质生成、微观上有旧键断裂或有新键形成的反应一定是化学反应但并不一定是基元反应,所以我们要确定一个过程是否是基元反应,首先确定这个过程是否是化学反应。一个过程是化学反应是判断这个过程是否是基元反应的必要条件。
作为基元反应还有一些重要特征,比如“能一步完成的简单化学变化” “只有一个能峰的化学变化”等。但事实上并不是所有的基元反应都有能峰,正如图2反应的过程d和过程g:


从图2的能量变化可以看出,过程d和过程g都没有能峰,在变化过程中向外释放能量,体系能量降低。

首先,排队网理论就成功地运用在网络建模中。排队网络的特点是运用概率和统计的方法对DEDS进行建模,一般是先对网络特性作基本的假设,然后采用基于状态稳态概率分布的平均性能分析方法,用以导出表征系统性能的解析表达式。它的优点是能够很好地描述具有成熟的随机过程和概率论的理论基础和常规类型的排队系统。
过程g同样如此,发生了形成新化学键和分子在催化剂上的解吸,从宏观上看有新物质生成,从微观上看有新键形成,又是能一步完成的简单化学变化,也属于基元反应。
如上所述,“能一步完成的简单化学变化”是判断一个化学反应是否属于基元反应的充要条件,而“只有一个能峰的化学变化”是判断一个化学反应是否属于基元反应的充分条件而非必要条件。即若一个化学反应只有一个能峰,则该化学反应必定是基元反应。若一个化学反应有几个能峰,则该反应一定不是基元反应。但基元反应有可能只表现为能量降低,不出现能峰。
3.建构判断“基元反应”的思维模型
判断一个过程是否是“基元反应”首先要判断该过程是否是化学反应,即在宏观上是否有新物质生成,或在微观上是否有旧键断裂或新键形成。若该过程是化学变化,再看是不是能一步完成的简单变化,若是则就是“基元反应”。判断“基元反应”的思维模型如图6所示。

图6 判断“基元反应”的思维模型

图7 吸附与解吸过程
4.判断“基元反应”需要注意的几个地方
4.1 并不是所有的基元过程都是基元反应

在固体对气体的吸附方面,Langmuir单层吸附理论的基本假设包括:固体表面均匀一致;它的每一个吸附活性中心只能吸附一个分子;吸附是单层的;被吸附分子彼此之间无相互作用;吸附与解吸同时进行,平衡时吸附速率与解吸速率相等。吸附与解吸过程可以用化学反应方程式的形式表示如下:
此处并未对吸附属于物理吸附和化学吸附加以区分,若依质量作用定律的形式同样可以分别给出吸附过程和解吸过程的速率表达式。这是因为硬球碰撞理论的结果——质量作用定律不仅适用于化学变化,也适用于物理变化。
正如放热过程和放热反应一样,放热过程或过程放热包含了放热反应和变化过程中放出热量的物理变化。放热反应属于放热过程,但只有属于化学反应的放热过程才是放热反应。同理,只有属于化学反应的基元过程才是基元反应。

4.2 一个基元反应可能包含过渡态,也有可能不包含
山西张建东老师认为每经历一个过渡态,就发生一个基元反应。复杂的化学反应进行时一般都会经过一系列连续的基元过程,其主要特点之一是在化学反应过程中会生成能继续发生变化的中间产物。所谓中间物质就是指在反应中生成的,而当反应时间趋向无限长后,其浓度会趋近于零的任何物质。中间产物会在化学反应过程中生成,又会在继续反应中消失,以致在最终反应生成物中并不存在。
但过渡态与中间产物不同,过渡态理论认为任何化学反应都不是只通过简单碰撞就形成产物,而是经过一个以一定构型存在的过渡态。过渡态理论认为两个具有足够能量的反应物分子在相互接近时,价键要重组,能量要重新分配,因此要通过一个过渡状态。在过渡态中,从微观上分析,过渡态是由反应物到产物的中间状态,是指旧的化学键将断未断,新的化学键将成未成,但旧的化学键已经减弱,新的化学键也已部分形成。但与中间产物不同,这种过渡状态中的活化络合物仅能存在于瞬时,会不可避免地分解为产物。而一个过渡态的存在,意味着这个过渡态前后两种状态经过过渡态而发生了基元反应。在一个基元反应中,过渡态在反应历程能量图中位于能量最高处。

综上所述:原题的反应历程中共有4个基元反应,它们分别是:





5.值得继续探讨的一个问题




